Статьи по апластической анемии
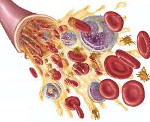

Апластическая анемия – угнетение функции кроветворения красного костного мозга (эритроцитопоэза, лейкопоэза и тромбоцитопоэза), приводящее к пангемоцитопении. К основным клиническим проявлениям гематологического синдрома принадлежат головокружение, слабость, обмороки, одышка, покалывание в груди, кожные геморрагии, кровотечения, склонность к развитию инфекционно-воспалительных и гнойных процессов. Заболевание диагностируется на основании характерных изменений гемограммы, миелограммы и гистологического исследования трепанобиоптата. Лечение патологии включает проведение гемотрансфузий, иммуносупрессивной терапии, миелотрансплантации.
Общие сведения
Апластическая (гипопластическая) анемия – тяжелое расстройство гемопоэза (чаще всех его звеньев), сопровождающееся развитием анемического, геморрагического синдромов и инфекционных осложнений. Развивается в среднем у 2 человек на 1 млн. населения в год. Приблизительно с одинаковой частотой патология поражает мужчин и женщин. Возрастные пики заболеваемости приходятся на возраст 10–25 и старше 50 лет. При данной патологии в костном мозге чаще нарушается образование всех трех типов клеточных элементов крови (эритроцитов, лейкоцитов и тромбоцитов), иногда – только одних эритроцитов; в зависимости от этого различают истинную и парциальную апластическую анемию. В гематологии данный вид анемии относится к числу потенциально фатальных заболеваний, приводящих к гибели 2/3 заболевших.

Апластическая анемия
Причины
По происхождению апластическая анемия может быть врожденной (связанной с хромосомными аберрациями) и приобретенной (развившейся в течение жизни). Принято считать, что угнетение миелопоэза связано с появлением в красном костном мозге и крови цитотоксических T-лимфоцитов, производящих фактор некроза опухолей и γ-интерферон, которые в свою очередь подавляют ростки кроветворения. Запускать этот механизм могут различные внешнесредовые (химические соединения, физические явления, лекарственные вещества), а также эндогенные факторы (вирусы, аутоиммунные реакции). К числу наиболее значимых причин относят:
- Прием миелотоксических препаратов. Достоверно установлена связь анемии с приемом некоторых противоопухолевых, противосудорожных, антибактериальных, антитиреоидных, противомалярийных препаратов, транквилизаторов, препаратов золота и др., обладающих потенциальным миелотоксическим эффектом. Лекарственные вещества могут вызывать как прямое повреждение стволовых кроветворных клеток, так и опосредованное – через аутоиммунные реакции. Анемии, связанные с таким механизмом развития, называются лекарственными.
- Контакт с химическими и физическими агентами. Супрессию костного мозга может вызывать взаимодействие с органическими растворителями, соединениями мышьяка, бензольными соединениями, пестицидами, облучение всего тела. В некоторых случаях недостаточность гемопоэза является временной и обратимой – главными факторами здесь являются концентрация/доза вещества и время контакта. супрессию костного мозга.
- Вирусные инфекции. Из вирусных агентов наибольшее значение уделяется возбудителям гепатитов В, С и D. В этом случае гипопластическая анемия обычно развивается в течение полугода после перенесенного вирусного гепатита. При изучении патогенеза было замечено, что репликация вируса происходит в мононуклеарах крови и костного мозга, а также в иммунных клетках. Предполагается, что подавление миелопоэза в этом случае является своеобразным иммунным ответом, возникающим против клеток, несущих на своей поверхности вирусные антигены. Такой вид анемии выделяется в отдельную форму – постгепатитную. Среди других вирусных инфекций называются ЦМВ, инфекционный мононуклеоз, грипп.
Также описаны случаи панцитопении, вызванные инфицированием туберкулезом, интоксикацией, лучевой болезнью, лимфопролиферативными заболеваниями (тимомой, лимфомой, хроническим лимфобластным лейкозом), беременностью. Почти в половине наблюдений причину анемии выявить не удается – такие случаи относят к идиопатической форме.
Патогенез
В основе апластической анемии может лежать либо первичное повреждение гемопоэтических стволовых клеток, либо нарушение их эффективной дифференцировки. При наследственных анемиях недостаточность гемопоэза опосредована кариотипическими аберрациями, приводящими к нарушению репарации ДНК и невозможности репликации стволовых клеток костного мозга. В случае приобретенной анемии под влиянием этиофакторов наблюдается активация Т-клеток, которые начинают продуцировать цитокины (интерферон-гамма, ФНО), поражающие клетки-предшественники гемопоэза. В стволовых клетках костного мозга повышается экспрессия генов, отвечающих за апоптоз и активизацию клеточной гибели. Основные клинические проявления обусловлены пангемоцитопенией – снижением в составе крови всех ее форменных элементов (эритроцитов, лейкоцитов, тромбоцитов).
Классификация
Кроме различных этиологических вариантов (лекарственного, постгепатитного, идиопатического), различают острую (до 1 мес. течения), подострую (от 1 до 6 мес.) и хроническую (более 6 мес.) форму заболевания. Анемию, протекающую с избирательным угнетением эритропоэза, называют парциальной красноклеточной аплазией. На основании выраженности тромбо- и гранулоцитопении данная форма анемии подразделяется на 3 степени тяжести:
- очень тяжелую (тромбоцитов менее 20,0х109/л; гранулоцитов менее 0,2х109/л)
- тяжелую (тромбоцитов менее 20,0х109/л; гранулоцитов менее 0,5х109/л), по данным трепанобиопсии – низкая клеточность костного мозга (менее 30% от нормы)
- умеренную (тромбоцитов более 20,0х109/л; гранулоцитов более 0,5х109/л)
Симптомы апластической анемии
Поражение трех гемопоэтических ростков (эритро-, тромбоцито- и лейкопоэза) обусловливает развитие анемического и геморрагического синдромов, инфекционных осложнений. Дебют апластической анемии обычно происходит остро. Анемический синдром сопровождается общей слабостью и утомляемостью, бледностью кожи и видимых слизистых, шумом в ушах, головокружением, покалыванием в груди, одышкой при нагрузке.
Основным проявлением тромбоцитопении выступает геморрагический синдром. Больные отмечают появление петехий и экхимозов на коже, повышенную кровоточивость десен, спонтанные носовые кровотечения, меноррагии. Возможно возникновение гематурии, маточных и желудочно-кишечных кровотечений. Следствием лейкопении и агранулоцитоза служит частое развитие инфекционных процессов – стоматитов, пневмоний, инфекций кожи и мочевыводящих путей. Для апластической анемий нехарактерны похудание, лимфаденопатия, гепато- и спленомегалия – при этих признаках следует искать другую причину пангемоцитопении.
Врожденная апластическая анемия (синдром Фанкони) обычно развивается у детей в возрасте до 10 лет и кроме аплазии костного мозга характеризуется другими нарушениями: микроцефалией, гипоплазией почек, низкорослостью, аномалиями развития верхних конечностей (гипоплазией первой пястной и лучевой кости), гипоспадией, гиперпигментацией кожи, крайней степенью тугоухости и др. При наследственной анемии Эстрена-Дамешека отмечается тотальное поражение кроветворения и панцитопения при отсутствии врожденных аномалий развития. Для анемии Даймонда-Блекфена или парциальной красноклеточной аплазии характерно только снижение количества эритроцитов.

Экхимозы на коже при апластической анемии
Осложнения
Летальный исход может быть обусловлен кровоизлияниями во внутренние органы, массивными кровотечениями, инфекционными осложнениями, анемической комой. Наиболее грозное из геморрагических осложнений – кровоизлияние в головной мозг (геморрагический инсульт). Больные склонны к частым и тяжело протекающим вирусным и бактериальным инфекциям респираторного тракта. Значительное или стремительное снижение уровня красных кровяных телец может привести к анемической коме. При молниеносной форме крайне быстро развиваются тяжелейшая анемия, иммунодефицит, коагулопатии, имеющие фатальные последствия.
Диагностика
Оценка гематологического статуса включает внимательный клинический осмотр и проведение тщательной лабораторной диагностики. При физикальном обследовании выявляется выраженная бледность или желтушность кожи, артериальная гипотония, тахикардия. Основу диагностического алгоритма составляет проведение общего и биохимического анализа крови, стернальной пункции, трепанобиопсии:
- Исследования крови. Для гемограммы при гипопластической анемии типичны эритро-, лейкоцито- и тромбоцитопения, нейтропения и относительный лимфоцитоз. Оценка биохимических показателей (печеночных проб, нефрологического комплекса, сывороточного железа, билирубина) информативна для исключения других анемий.
- Исследование пунктата костного мозга. В миелограмме обнаруживается уменьшение количества миелокариоцитов и мегакариоцитов, снижение клеточности. В трепанобиоптате определяется замещение красного костного мозга жировым (желтым).
В рамках диагностического поиска апластическую анемию необходимо дифференцировать с мегабластными (В12-дефицитными, фолиеводефицитными) анемиями, идиопатической тромбоцитопенической пурпурой, пароксизмальной ночной гемоглобинурией, острым лейкозом.

Миелограмма: слева – апластическая анемия, справа – нормальный костный мозг
Лечение апластической анемии
Больные с апластической анемией госпитализируются в специализированные отделения. Им обеспечиваются полная изоляция и асептические условия для предупреждения возможных инфекционных осложнений. Проведение эффективного лечения является сложной проблемой практической гематологии. В зависимости от уровня цитопении используются следующие лечебные подходы:
- Иммуносупрессиная терапия. При умеренной цитопении назначается фармакотерапия, включающая комбинацию антитимоцитарного иммуноглобулина и циклоспорина А. Поддерживающая терапия проводится анаболическими стероидами или их сочетанием с циклоспоринами.
- Гемотрансфузии. В комплексе с курсом иммуносупрессивной терапии при низких показателях красной крови показано проведение заместительной гемотрансфузионной терапии (переливание тромбоцитов и эритроцитарной массы), плазмафереза. Данная мера не оказывает воздействия на патогенетическое звено заболевания, но позволяет восполнить дефицит кровяных телец, не вырабатываемых костным мозгом.
- Трансплантация КМ и СК. Наиболее благоприятные прогнозы на долгосрочную выживаемость оказывает выполнение аллогенной трансплантации костного мозга. Однако ввиду сложности подбора иммунологически совместимого донора процедура используется ограниченно. В качестве экспериментальных подходов рассматриваются аутологичные трансплантации, пересадка стволовых клеток периферической крови. Больным с нетяжелой формой анемии может быть показано проведение спленэктомии, эндоваскулярной окклюзии селезеночной артерии.
Прогноз и профилактика
Прогноз определяется этиологической формой, тяжестью и остротой течения анемии. Критериями неблагоприятного исхода служат быстрое прогрессирование заболевания, тяжелый геморрагический синдром и инфекционные осложнения. После трансплантации костного мозга ремиссии удается достичь у 75–90% пациентов. Первичная профилактика данной разновидности анемии предполагает исключение влияния неблагоприятных внешнесредовых факторов, необоснованного применения лекарственных препаратов, предупреждение инфекционной заболеваемости и др. Пациентам с уже развившимся заболеванием требуется диспансерное наблюдение гематолога, систематическое обследование и длительная поддерживающая терапия.
Источник
Апластическая анемия — это заболевание крови, форма анемии, при которой в костном мозге недостаточно тромбоцитов (эритроцитов), эритроцитов и лейкоцитов. Это редкое заболевание, которое может возникнуть в любом возрасте. Болезнь может развиваться медленно или быстро.
Что такое апластическая анемия
Апластическая анемия — это патологическое состояние организма, при котором костный мозг перестает вырабатывать все три типа клеток крови: красные кровяные тельца (эритроциты), белые кровяные тельца (лейкоциты) и тромбоциты (тромбоциты). Это происходит, когда по какой-то причине в костном мозге уменьшается количество стволовых клеток, из которых развиваются все клетки крови.
Точнее сказать — это синдром недостаточности костного мозга, характеризующийся снижением количества эритроцитов, лейкоцитов, тромбоцитов в крови и гипоплазией костного мозга с менее чем 30% гематопоэтических клеток.
Что такое апластическая анемия
Апластическая анемия подразделяется на первичную и вторичную.
- Первичная — анемия Фанкони, врожденный склероз и семейная апластическая анемия.
- Вторичная — анемия, вызванная химическими веществами, лекарствами, вирусами.
Распространенность
Апластическая анемия — относительно редкое заболевание: заболеваемость составляет 5-10 случаев на миллион людей в год.
Симптомы апластической анемии
Больные жалуются на нарастающую слабость, утомляемость, нехватку воздуха. Возможно кровотечение, быстрее возникают синяки. У пациентов с анапластической анемией более частые инфекции, высокая температура с ознобом — серьезное состояние, требующее безотлагательного медицинского обследования и лечения.
Часто встречающиеся симптомы:
- общая слабость;
- быстрая утомляемость;
- одышка в покое и во время упражнений;
- частое сердцебиение;
- аритмичное сердцебиение;
- бледная кожа;
- кровотечение из ран;
- синяки на коже;
- кровотечение из носа;
- десневое кровотечение;
- общие инфекции;
- высокая температура;
- головная боль.
Высокая температура
Кровотечение из носа
Этиология. Причины развития апластической анемии
Апластическая анемия возникает при повреждении костного мозга, который производит стволовые клетки крови. Производство клеток может замедляться, они могут полностью разрушаться или производиться в деформированном, дисфункциональном виде. В 65% случаях причина заболевания неясна.
Врожденные патологии. Врожденная апластическая анемия встречается редко. Наиболее частой формой врожденного заболевания является синдром Фанкони: пациенты с низким ростом, измененной пигментацией кожи, различными проблемами с почками. Генетическое тестирование в этом случае выявляет хромосомные аберрации.
Лекарства и токсины. Наиболее частой известной причиной апластической анемии является воздействие лекарств и токсинов окружающей среды.
Причина апластической анемии – воздействие лекарств
Недостаточность костного мозга, наряду с апластической анемией, часто вызвана токсинами — органическими химикатами (бензолом, толуолом, инсектицидами, нефтяными дистиллятами).
Что касается лекарств, апластическая анемия вызывается:
- антибиотиком хлорамфениколом;
- пеницилламином — используется для лечения заболеваний суставов;
- карбамазепином и фенитоином — используется для лечения эпилепсии;
- ацетазоламидом — диуретик;
- цитотоксическими препаратами, используемыми для лечения рака.
Встречаются случаи апластической анемии, развивающиеся на фоне вирусных инфекций — парвовирус B19, вирусы гепатита B и C, вирусы Эпштейна-Бар (EBV), цитомегаловирусы (CMV). Очень редко апластическая анемия возникает при беременности.
Цитотоксические препараты подавляют и убивают клетки костного мозга, но костный мозг восстанавливается довольно быстро, после прекращения их приема. Угнетает костный мозг и лучевая терапия. Иногда химиотерапией намеренно разрушают костный мозг при подготовке к трансплантации.
Течение болезни
Заболевание может развиваться очень медленно, а может возникать очень внезапно. Обычно апластическая анемия развивается незаметно и подозревается при возникновении комплекса различных симптомов. В некоторых случаях, например, при лечении рака, апластическая анемия довольно распространена и считается осложнением, в других случаях диагноз может быть отложен.
У пациента отсутствуют все клетки крови, что вызывает множество сопутствующих симптомов.
- Недостаток эритроцитов характеризуется одышкой, слабостью, утомляемостью, бледностью, головной болью, шумом в ушах.
- Недостаток тромбоцитов приводит к длительному кровотечению во время травмы или менструации, появлению синяков даже от малейших травм, покраснению глаз, спонтанному кровотечению из носа и десен.
- Отсутствие лейкоцитов характерно для частых инфекций, более трудно заживающих ран, лихорадки, иногда с ознобом.
Шум в ушах
Диагностика апластической анемии
Диагноз ставится на основании физического обследования — увеличение печени, возможные аномалии развития, изменение пигментации, быстрый рост, высокое небо, клинических симптомов, лабораторных тестов.
Важные клинические симптомы включают слабость, одышку (указывающую на возможное уменьшение количества эритроцитов), лихорадку, озноб, боль в горле (указывающую на возможную инфекцию из-за уменьшения лейкоцитов), кровотечения или синяки в различных частях тела, петехии (небольшие кровотечения) в слизистой оболочке рта (из-за уменьшения тромбоцитов). Пациент может быть бледным и иметь язвы во рту.
При осмотре глазного дна часто наблюдаются кровоизлияния в сетчатку.
При обследовании важно определить показатели крови, оценить степень истощения костного мозга и, если возможно, найти причину.
Анализ крови:
- Выявляется уменьшение количества всех клеток крови (эритроцитов (эритроцитопения), лейкоцитов (лейкоцитопения), тромбоцитов (тромбоцитопения)) – тогда состояние называется панцитопенией.
- Уменьшение количества нейтрофилов указывает на тяжесть апластической анемии: 0,5 х 10 9/ л показывают тяжелую и 0,2 х 10 9 / л – очень тяжелую апластическую анемию.
В случае заметного уменьшения количества кровяных телец требуется срочная консультация гематолога. Чтобы поставить диагноз, он выполняет аспирацию костного мозга или биопсию трепана, при которой из костного мозга берется небольшое количество клеток для более точного исследования. Это исследование помогает отличить апластическую анемию от других заболеваний крови.
Анализ крови
Биопсия трепан
Также проводится УЗИ внутренних органов. При необходимости цитогенетические исследования.
Лечение
Если возможно, следует устранить причину недостаточности костного мозга и апластической анемии. Иногда функция костного мозга восстанавливается, когда причина легкая, при только симптоматическом лечении легкой апластической анемии. Если количество клеток не очень велико, достаточно наладить питьевой режим и перейти на специальную диету.
Тяжелые и очень тяжелые формы апластической анемии представляют собой опасные для жизни состояния, требующие срочного и серьезного лечения. При температуре выше 38 o C в течение более двух часов пациента госпитализируют и лечат антибиотиками.
Лечение апластической анемии антибиотиками
Может потребоваться дополнительная инфузия тромбоцитов, когда риск кровотечения становится высоким — количество тромбоцитов падает ниже 10 x 10 9/ л. Инфузия эритроцитов назначается при тяжелых симптомах анемии.
Трансплантация костного мозга является методом выбора для лечения пациентов с тяжелой и очень тяжелой апластической анемией в возрасте до 50 лет. Пациенты старше 50 лет получают иммуносупрессивную терапию антитимоцитарным глобулином и циклоспорином.
В случае разрушения костного мозга из-за аутоиммунного процесса и невозможности трансплантации нельзя использовать иммунодепрессанты — циклоспорин, антитимоцитарный глобулин, метилпреднизолон, подавляющие атаку организма на костный мозг. Назначаются стимуляторы костного мозга — филрастин, колониестимулирующий фактор, эритропоэтин, др. Это препараты, стимулирующие костный мозг производить более специфические клетки. Лечение этими препаратами часто сочетается с иммуносупрессивной терапией.
В профилактических целях могут быть назначены антибиотики для предотвращения инфекций, поскольку сопротивляемость организма резко снижается.
В случае апластической анемии, вызванной лучевой терапией или химиотерапией для лечения рака, функция костного мозга восстанавливается после прекращения лечения.
Беременным женщинам делают переливание крови, и функция костного мозга также восстанавливается после родов, но если этого не происходит, лечение жизненно необходимо.
Осложнения
При тяжелой и очень тяжелой апластической анемии восприимчивость к различным инфекциям значительно увеличивается, и из-за низкого количества тромбоцитов возможно кровотечение. После трансплантации может возникнуть такая реакция отторжения, как сыпь, диарея, проблемы с печенью. Высокие дозы циклоспорина могут повышать артериальное давление, что приводит к почечной недостаточности.
Поделиться ссылкой:
Источник
