Транспорт кислорода при анемии

Транспорт кислорода и углекислого газа кровью, формы анемии
Транспорт О2 с помощью гемоглобина
Красный пигмент гемоглобин (Нb) состоит из белковой части (глобина) и собственно пигмента (гема). Молекулы составляют четыре белковые субъединицы, каждая из которых присоединяет гем-группу с двухвалентным атомом железа, находящимся в ее центре. В легких каждый атом железа присоединяет одну молекулу кислорода. Кислород переносится в ткани, где он отделяется. Присоединение О2 называется оксигенацией (насыщением кислородом), а его отсоединение – дезоксигенацией.
Транспорт СО2

Около 10% углекислого газа (СО2), конечного продукта окислительного метаболизма в клетках тканей, переносится кровью физически растворенным п 90% — в химически связанной форме. Большая часть углекислого газа сначала диффундирует из клеток тканей в плазму, а оттуда в эритроциты. Там молекулы СО2 химически связываются и превращаются с помощью ферментов в намного более растворимые бикарбонат-ионы (НСО3-), которые переносятся в плазме крови. Образование СO2 из НСО3- значительно ускоряется с помощью фермента карбоангидразы, присутствующего в эритроцитах.
Большая часть (около 50-60%) образованных бикарбонат-ионов поступает из эритроцитов обратно в плазму в обмен на хлорид-ионы. Они переносятся в легкие и выделяются в процессе выдоха после превращения в СO2. Оба процесса — образование НСО3- и освобождение СO2, соответственно связаны с оксигенацией и дезоксигенацией гемоглобина. Дезоксигемоглобин — заметно более сильное основание, чем оксигемоглобин, и может присоединить больше ионов Н+ (буферная функция гемоглобина), таким образом способствуя образованию НСО3- в капиллярах тканей. В капиллярах легких НСО3- опять проходит из плазмы крови в эритроциты, соединяется с Н+-ионами и превращается опять в СO2. Этот процесс подтверждается тем фактом, что окисленная кровь выделяет больше протонов Н+. Намного меньшая доля СО2 (около 5-10%) связана непосредственно с гемоглобином и переносится как карбаминогемоглобин.
Гемоглобин и угарный газ
Оксид углерода (угарный газ, СО) является бесцветным газом без запаха, который образуется во время неполного сгорания и, как кислород, может обратимо связываться с гемоглобином. Однако сродство угарного газа к гемоглобину заметно больше, чем у кислорода. Таким образом, даже когда содержание СО во вдыхаемом воздухе составляет 0,3%, 80% гемоглобина связывается с угарным газом (НbСО). Так как угарный газ в 200-300 раз медленней, чем кислород, освобождается от связи с гемоглобином, его токсическое действие определяется тем, что гемоглобин больше не может переносить кислород. У тяжелых курильщиков, например, 5-10% гемоглобина присутствует как НbСО, в то время как при его содержании в 20% появляются симптомы острого отравления (головная боль, головокружение, тошнота), а 65% могут быть смертельным.
Содержание гемоглобина в крови (Нb)
Часто для оценки гемопоэза или для распознавания различных форм анемии определяют среднее содержание гемоглобина в эритроците (СГЭ). Оно вычисляется по формуле:
СГЭ = (содержание гемоглобина (г/100 мл крови) / количество эритроцитов (10ˉ6г/мкл))*10
Значение среднего содержания гемоглобина в эритроците лежит между 38 и 36 пикограммами (пг) (1 пг = 10ˉ¹² г). Эритроциты с нормальным СГЭ называются нормохромными (ортохромными). Если СГЭ низкое (например, из-за постоянной потери крови или дефицита железа), эритроциты называются гипохромными; если СГЭ высокое (например, при пернициозной анемии благодаря дефициту витамина В12), они называются гиперхромными.
Формы анемии
Анемия определяется как дефицит (снижение количества) эритроцитов или сниженное содержание гемоглобина в крови. Диагноз анемии обычно ставится по содержанию гемоглобина, нижняя граница нормы достигает 140 г/л у мужчин и 120 г/л у женщин. Почти при всех формах анемии надежным симптомом заболевания является бледный цвет кожи и слизистых оболочек. Часто во время физических нагрузок заметно увеличивается сердечный ритм (увеличивая скорость кровообращения), а уменьшение кислорода в тканях приводит к одышке. Кроме того, встречается головокружение и легкая утомляемость.
Кроме железодефицитной анемии и хронической потери крови, например, из-за кровоточащих язв или опухолей в желудочно-кишечном тракте (гипохромные анемии), анемия может возникать при дефиците витамина В12. фолиевой кислоты или эритропоэтина. Витамин В12 и фолиевая кислота участвуют в синтезе ДНК в незрелых клетках костного мозга и, таким образом, заметно влияют на деление и созревание эритроцитов (эритропоэз). При их нехватке образуется меньше эритроцитов, но они заметно увеличены из-за повышенного содержания гемоглобина (макроциты (мегалоциты), предшественники: мегалобласты), поэтому содержание гемоглобина в крови практически не изменяется (гиперхромная, мегалобластическая, макроцитарная анемия).
Дефицит витамина В12 нередко возникает из-за нарушения всасывания витамина в кишечнике, реже — вследствие недостаточного приема с пищей. Эта так называемая пернициозная анемия наиболее часто является результатом хронического воспаления в слизистой кишечника с уменьшением образования желудочного сока.
Витамин В12 всасывается в кишечнике только в связанном виде с фактором, находящимся в желудочном соке «внутренним фактором (Кастла)», который защищает его от разрушения пищеварительным соком в желудке. Так как печень может запасать большое количество витамина В12, то перед тем, как ухудшение всасывания в кишечнике повлияет на образование эритроцитов, может пройти 2-5 лет. Как и в случае дефицита витамина В12, дефицит фолиевой кислоты, другого витамина группы В, приводит к нарушению эритропоэза в костном мозге.
Есть две другие причины анемии. Одна из них — разрушение костного мозга (аплазия костного мозга) радиоактивным излучением (например, после аварии на атомной электростанции) или в результате токсичных реакций на лекарства (например, цитостатики) (апластическая анемия). Другая причина — это уменьшение продолжительности жизни эритроцитов в результате их разрушения или увеличенного распада (гемолитическая анемия). При сильной форме гемолитической анемии (например, следующей за неудачным переливанием крови), кроме бледности может наблюдаться изменение цвета кожи и слизистых оболочек на желтоватый. Эта желтуха (гемолитическая желтуха) вызвана увеличивающимся разрушением гемоглобина до билирубина (желтого желчного пигмента) в печени. Последнее приводит к увеличению уровня билирубина в плазме и его отложению в тканях.
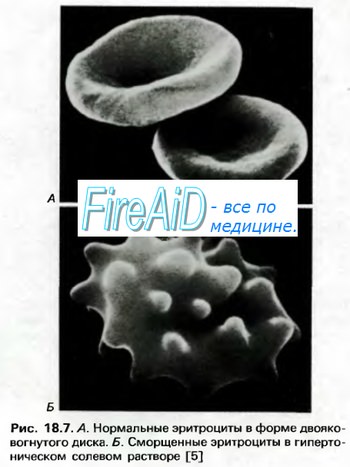
Примером анемии, возникающей в результате наследственного нарушения синтеза гемоглобина, клинически проявляющейся как гемолитическая, служит серповидноклеточная анемия. При этой болезни, которая практически встречается только у представителей негроидных популяций, имеется молекулярное нарушение, приводящее к замене нормального гемоглобина на другую форму гемоглобина (HbS). В HbS аминокислота валин заменена на глутаминовую кислоту. Эритроцит, содержащий такой неправильный гемоглобин, в дезоксигенированном состоянии принимает форму серпа. Серповидные эритроциты более жесткие и плохо проходят через капилляры.
Наследственное нарушение у гомозигот (доля HbS в суммарном гемоглобине 70-99%) приводит к закупорке небольших сосудов и, таким образом, к постоянному повреждению органов. Пораженные этой болезнью люди обычно достигают зрелости только при интенсивном лечении (например, частичной замене крови, приеме анальгетиков, избегании гипоксии (кислородного голодания) и иногда — пересадке костного мозга). В некоторых регионах тропической Африки с высоким процентом малярии 40% популяции являются гетерозиготными носителями данного гена (когда содержание HbS менее 50%), у них таких симптомов не обнаруживается. Измененный ген обусловливает устойчивость к малярийной инфекции (селективное преимущество).
Регуляция образования эритроцитов
Образование эритроцитов регулируется гормоном почек эритропоэтином. Организм обладает простой, но очень эффективной системой регуляции для поддержания содержания кислорода и вместе с тем количества эритроцитов относительно постоянным. Если содержание кислорода в крови падает ниже определенного уровня, например, после большой потери крови или во время пребывания на больших высотах, постоянно стимулируется образование эритропоэтина. В результате усиливается образование эритроцитов в костном мозге, что увеличивает способность крови к переносу кислорода. Когда дефицит кислорода преодолевается увеличением числа эритроцитов, образование эритропоэтина опять уменьшается. Пациенты, нуждающиеся в диализе (искусственном очищении крови от продуктов обмена веществ), с нарушением функционирования почек (например, с хронической почечной недостаточностью) часто испытывают явный дефицит эритропоэтина и поэтому почти всегда страдают от сопутствующей анемии.
Невероятные курсы массажа! СПб.
Источник
Оглавление темы “Вентиляция легких. Перфузия легких кровью.”:
1. Вентиляция легких. Вентиляция кровью легких. Физиологическое мертвое пространство. Альвеолярная вентиляция.
2. Перфузия легких кровью. Влияние гравитации на вентиляцию легких. Влияние гравитации на перфузию легких кровью.
3. Коэффициент вентиляционно-перфузионных отношений в легких. Газообмен в легких.
4. Состав альвеолярного воздуха. Газовый состав альвеолярного воздуха.
5. Напряжение газов в крови капилляров легких. Скорость диффузии кислорода и углекислого газа в легких. Уравнение Фика.
6. Транспорт газов кровью. Транспорт кислорода. Кислородная емкость гемоглобина.
7. Сродство гемоглобина к кислороду. Изменение сродства гемоглобина к кислороду. Эффект Бора.
8. Углекислый газ. Транспорт углекислого газа.
9. Роль эритроцитов в транспорте углекислого газа. Эффект Холдена..
10. Регуляция дыхания. Регуляция вентиляции легких.
Транспорт газов кровью. Транспорт кислорода. Кислородная емкость гемоглобина.
Кровообращение выполняет одну из важнейших функций переноса кислорода от легких к тканям, а углекислого газа — от тканей к легким. Потребление кислорода клетками тканей может изменяться в значительных пределах, например при переходе от состояния покоя к физической нагрузке и наоборот. В связи с этим кровь должна обладать большими резервами, необходимыми для увеличения ее способности переносить кислород от легких к тканям, а углекислый газ в обратном направлении.
Транспорт кислорода.
При 37 С растворимость 02 в жидкости составляет 0,225 мл • л-1 • кПа-1 (0,03 мл/л/мм рт. ст.). В условиях нормального парциального давления кислорода в альвеолярном воздухе, т. е. 13,3 кПа или 100 мм рт.ст., 1 л плазмы крови может переносить только 3 мл 02, что недостаточно для жизнедеятельности организма в целом. В покое в организме человека за минуту потребляется примерно 250 мл кислорода. Чтобы тканям получить такое количество кислорода в физически растворенном состоянии, сердце должно перекачивать за минуту огромное количество крови. В эволюции живых существ проблема транспорта кислорода была более эффективно решена за счет обратимой химической реакции с гемоглобином эритроцитов. Кислород переносится кровью от легких к тканям организма молекулами гемоглобина, которые содержатся в эритроцитах.
Гемоглобин способен захватывать кислород из альвеолярного воздуха (соединение называется ок-сигемоглобином) и освобождать необходимое количество кислорода в тканях. Особенностью химической реакции кислорода с гемоглобином является то, что количество связанного кислорода ограничено количеством молекул гемоглобина в эритроцитах крови. Молекула гемоглобина имеет 4 места связывания с кислородом, которые взаимодействуют таким образом, что зависимость между парциальным давлением кислорода и количеством переносимого кислорода с кровью имеет S-образную форму, которая носит название кривой насыщения или диссоциации оксигемоглобина (рис. 10.18). При парциальном давлении кислорода 10 мм рт. ст. насыщение гемоглобина кислородом составляет примерно 10 %, а при Р02 30 мм рт. ст. — 50—60 %. При дальнейшем увеличении парциального давления кислорода от 40 мм рт. ст. до 60 мм рт. ст. происходит уменьшение крутизны кривой диссоциации оксигемоглобина и процент его насыщения кислородом возрастает в диапазоне от 70—75 до 90 % соответственно. Затем кривая диссоциации оксигемоглобина начинает занимать практически горизонтальное положение, поскольку увеличение парциального давления кислорода с 60 до 80 мм рт. ст. вызывает прирост насыщения гемоглобина кислородом на 6 %. В диапазоне от 80 до 100 мм рт. ст. процент образования оксигемоглобина составляет порядка 2. В результате кривая диссоциации оксигемоглобина переходит в горизонтальную линию и процент насыщения гемоглобина кислородом достигает предела, т. е. 100. Насыщение гемоглобина кислородом под влиянием Р02 характеризует своеобразный молекулярный «аппетит» этого соединения к кислороду.
Значительная крутизна кривой насыщения гемоглобина кислородом в диапазоне парциального давления от 20 до 40 мм рт. ст. способствует тому, что в ткани организма значительное количество кислорода может диффундировать из крови в условиях фадиента его парциального давления между кровью и клетками тканей (не менее 20 мм рт. ст.). Незначительный процент насыщения гемоглобина кислородом в диапазоне его парциального давления от 80 до 100 мм рт. ст. способствует тому, что человек без риска снижения насыщения артериальной крови кислородом может перемещаться в диапазоне высот над уровнем моря до 2000 м.
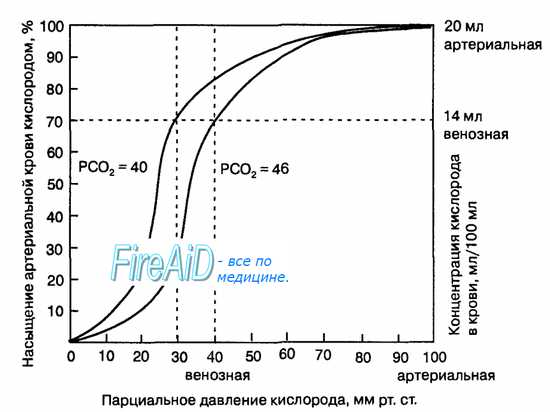
Рис. 10.18. Кривая диссоциации оксигемоглобина. Пределы колебания кривой при РС02 = 40 мм рт. ст. (артериальная кровь) и РС02 = 46 мм рт. ст. (венозная кровь) показывают изменение сродства гемоглобина к кислороду (эффект Ходена).
Общие запасы кислорода в организме обусловлены его количеством, находящимся в связанном состоянии с ионами Fe2+ в составе органических молекул гемоглобина эритроцитов и миоглобина мышечных клеток.
Один грамм гемоглобина связывает 1,34 мл 02. Поэтому в норме при концентрации гемоглобина 150 г/л каждые 100 мл крови могут переносить 20,0 мл 02.
Количество 02, которое может связаться с гемоглобином эритроцитов крови при насыщении 100 % его количества, называется кислородной емкостью гемоглобина. Другим показателем дыхательной функции крови является содержание 02 в крови (кислородная емкость крови), которое отражает его истинное количество, как связанного с гемоглобином, так и физически растворенного в плазме. Поскольку в норме артериальная кровь насыщена кислородом на 97 %, то в 100 мл артериальной крови содержится примерно 19,4 мл 02.
– Также рекомендуем “Сродство гемоглобина к кислороду. Изменение сродства гемоглобина к кислороду. Эффект Бора.”
Источник
Для выживания человек должен быть способен поглощать кислород из атмосферы и транспортировать его клеткам, где он используется в метаболизме. Некоторые клетки могут короткое время вырабатывать небольшое количество энергии без участия кислорода (анаэробный метаболизм). Другие органы (например, головной мозг) состоят из клеток, которые могут существовать только при наличии постоянного снабжения кислородом (аэробный метаболизм). Различные ткани имеют различную степень толерантности к аноксии (отсутствие кислорода). Мозг и сердце – наиболее уязвимые органы. Вначале недостаток кислорода поражает функцию органа, а с течением времени вызывает и необратимые морфологические изменения (в течение минут в случае с мозгом), когда восстановление функции невозможно.
Транспорт кислорода из воздуха тканям.
Кислород доставляется из воздуха, которым мы дышим, каждой клетке организма. В целом, газы перемещаются из области высокой концентрации (давления) в зону низкой концентрации (давления). Если в резервуаре имеется смесь газов, то давление каждого газа (парциальное давление) равняется давлению, при котором находился бы газ, будь он в резервуаре один.
Из атмосферы к альвеолам.
Воздух (атмосфера) вокруг нас имеет давление 760 мм Hg (1 атмосфера = 760 мм Hg = 101 кРа). Воздух содержит 21% кислорода, 78% азота и небольшое количество СО2, аргона и гелия. Давление, создаваемое двумя основными газами, смешанными вместе, равняется общему или атмосферному давлению. Давление кислорода (РО2) в сухом воздухе на уровне моря равняется 159 мм Hg (21/100 х 760 = 159). При вдохе воздух, продвигающийся по верхним дыхательным путям, нагревается и увлажняется. Влажность, формирующаяся парами воды, создает давление, которое при 37 градусах в трахее составляет 47 мм Hg. Беря в расчет давление водяных паров, РО2 в трахее при дыхании воздухом (760-47) х 21/100 = 150 мм Hg. При достижении альвеол РО2 падает до 100 мм Hg. Это происходит из-за того, что в альвеолах идет процесс постоянного поступления О2 извне (дыхание) и удаления его из организма легочными капиллярами.
Из альвеол в кровь.
Кровь, возвращающаяся к сердцу из тканей, имеет низкое РО2 (40 мм Hg). Она идет к легким по легочным артериям. Легочные артерии образуют легочные капилляры, окружающие альвеолы. Кислород диффундирует из альвеол – зоны высокого РАО2 (100 мм Hg) в капилляры – зону низкого РаО2 (40 мм Hg). После оксигенации кровь поступает по легочным венам в левые отделы сердца и далее в ткани организма. В «идеальном легком» РаО2 крови в легочных венах должно равняться РАО2 в альвеолах. Три фактора делают РО2 венозной крови ниже альвеолярного: нарушение вентиляционно/перфузионных (V/Q) отношений, шунт и медленная диффузия.
Нарушение вентиляционно/перфузионных отношений.
В «идеальном легком» все альвеолы получали бы одинаковую степень вентиляции и капилляризации с одинаковым током крови по ним.
Пораженные легкие могут иметь значительный дисбаланс между вентиляцией и кровотоком. Некоторые альвеолы сравнительно гипервентилируются, другие же «гиперперфузируются». Наиболее яркой формой этого нарушения является шунт, когда кровь протекает по альвеолам без газообмена (рисунок 1). Хорошо вентилируемые альвеолы (с высоким РО2 в капиллярной крови) не способны компенсировать газообмен при наличии большого числа невентилируемых альвеол с низким РО2 в капиллярах. Это происходит из-за того, что гемоглобин способен нести лимитированное количество кислорода (см. кривую диссоциации оксигемоглобина, рис. 2а). Легочная венозная кровь (смешанная кровь всех легочных капилляров) будет иметь меньшее РО2, чем в альвеолах. Даже нормальные легкие имеют некоторый вентиляционно/перфузионный дисбаланс; верхние зоны сравнительно лучше вентилируются, тогда как нижние – лучше перфузируются, но гиповентилируются.

Рис. 1. Отражена норма и два типа V/Q нарушений, таких как шунт и мертвое пространство.
Шунт имеет место, когда деоксигенированная венозная кровь, возвращающаяся от тканей проходит через невентилируемые альвеолы и поступает в легочные вены и большой круг кровообращения с неизмененным РО2 (40 мм Hg) (рисунок 1). Ателектазы (коллабированные альвеолы), уплотнение легкого, отек легких или обструкция дыхательных путей малого калибра (см. ниже) вызывают развитие шунта.
Диффузия.
Кислород диффундирует из альвеол в капилляры до момента выравнивания РО2 в капиллярах и альвеолах. Этот процесс завершается, когда кровь проходит одну треть пути по легочному капилляру. В интактных легких процесс диффузии происходит очень быстро и завершается даже при высоком сердечном выбросе (нагрузка), когда кровь находится меньшее время в контакте с альвеолами. Этого может не происходить в поврежденной капиллярной сети легких (легочные заболевания). Однако, легкие имеют широкий диапазон компенсации и проблемы, связанные с неадекватной диффузией газов – редкая причина гипоксии, за исключением случаев альвеолярного фиброза.
Для нивелирования негативных эффектов легочного шунта и вентиляционно/перфузионных нарушений на оксигенацию крови легочные сосуды обладают способностью к вазоконстрикции — таким образом снижается кровоток по плохо вентилируемым зонам. Это называется гипоксической легочной вазоконстрикцией, снижающей эффект шунта.
Транспорт кислорода кровью.
Кислород переносится кровью в двух формах. Большая часть связывается с гемоглобином (рисунок 2b), но также имеется очень небольшая доля кислорода, растворенного в плазме. Каждый грамм гемоглобина при полном насыщении способен переносить 1,31 мл кислорода. Таким образом, каждый литр крови с концентрацией гемоглобина 15 г/дл (150 г/л – пер.) может переносить около 200 мл кислорода при полном насыщении (РО2 >100 мм Hg). При этом РО2 всего 3 мл кислорода растворится в каждом литре плазмы.
Если РаО2 значительно повышено (при дыхании 100% кислородом), небольшое количество кислорода растворится в плазме (0,003 мл О2/100 мл крови/мм Hg РО2), но при этом гемоглобин при сатурации > 95% не способен продолжать связываться с кислородом. При рассмотрении адекватности доставки кислорода тканям следует иметь в виду три фактора: концентрация гемоглобина, сердечный выброс и оксигенация.
Кислородный каскад.
Кислород перемещается по градиенту из зоны более высокой концентрации в воздухе через дыхательные пути, смешиваясь с альвеолярным газом, далее поступает в артериальную кровь, капилляры и, наконец, в клетку. РО2 достигает минимального уровня (4-20 мм Hg) в митохондриях (структурное образование клетки, ответственное за продукцию энергии). Это снижение парциального давления кислорода от воздуха к митохондрии известно как кислородный каскад, каждая ступень которого может быть затронута патологическим процессом и вызывать гипоксию (рисунок 3).

Рис. 2а. Кривая диссоциации HbО2 при рН=7,4, РСО2= 40 ммHg и 37оС. Рис. 2b. Относительные доли О2, растворенного в плазме, и О2, связанного с Hb (концентрация Hb = 15г/100 мл крови).
Доставка кислорода.
Количество кислорода, доступного для организма за минуту, известно как доставка кислорода и равняется сердечному выбросу х содержание кислорода в артериальной крови (см. выше). Например, 5000 мл крови/мин х 200 мл О2/1000 мл крови = 1000 мл О2/мин. Доставка кислорода (млО2/мин) = сердечный выброс (л/мин) х концентрация Нb (г/л) х 1,30 (млО2/г Hb) х % сатурации.

Рис. 3. Кислородный каскад.
Эффекты гиповентиляции показаны тонким пунктиром, шунта — ширным.
Потребление кислорода.
Человеком в покое каждую минуту потребляет около 250 мл кислорода (потребление кислорода), то есть используется всего 25% кислорода артериальной крови. Гемоглобин в смешанной венозной крови насыщен примерно на 75% (95% — 25%).
Клеткам доставляется больше кислорода, чем они могут использовать. При высоком потреблении кислорода (например, при физической нагрузке) повышенная потребность компенсируется повышением сердечного выброса (см. формулу выше). Однако низкий сердечный выброс, низкое содержание гемоглобина (анемия) или низкая сатурация гемоглобина приведет к неадекватной доставке кислорода, если не произойдет компенсаторных изменений в одном из перечисленных звеньев. С другой стороны, если доставка кислорода падает на уровень потребления кислорода, ткани начинают экстрагировать большее его количество (сатурация смешанной венозной крови падает ниже 70%)(рис. 4 а-b). Снижение доставки ниже точки «с» на рисунке 4 не может быть компенсировано повышением экстракции кислорода и ведет к анаэробному метаболизму и лактат ацидозу.
Запасы кислорода.
Несмотря на огромную важность кислорода, его запасы в организме человека невелики и недостаточны для поддержания жизни более, чем несколько минут. При отсутствии дыхания запасы кислорода ограничены его наличием в легких и крови. Количество кислорода в рови зависит от объема циркулирующей крови и концентрации Hb. Количество в легких – от величины функциональной остаточной емкости (ФОЕ) и альвеолярной концентрации кислорода. ФОЕ это объем воздуха (около 3 литров у взрослых), который остается в легких в конце выдоха, когда эластические силы легких находятся в равновесии с диафрагмой и расслабленной грудной клеткой. При дыхании общий запас кислорода (кислород крови и легких) невелик и так как в основном он связан с гемоглобином (см. рис. 5), только небольшая его часть высвобождается при отсутствии недопустимого падения РО2 (когда насыщение — сатурация гемоглобина 50% и РО2 снижено до 26 мм Hg). Дыхание 100% кислородом приводит к значительному увеличению запасов кислорода в организме, так как ФОЕ заполнена кислородом. Основной компонент запаса теперь находится в легких и 80% его может быть использовано без опасности критического снижения сатурации гемоглобина (РАО2 остается около 100 ммHg). Это объясняет эффективность преоксигенации (см. ниже).
Транспорт кислорода – эффекты анестезии.
Гиповентиляция может возникать во время анестезии вследствие обструкции дыхательных путей, действия ингаляционных анестетиков, опиоидов и гипнотиков. С другой стороны, при анестезии кетамином и эфиром (менее 1 МАК) наблюдается менее выраженная депрессия дыхания, чем при использовании других анестетиков. Альвеолярное РО2 сбалансировано поступлением кислорода при дыхании и его потреблением в метаболических процессах организма. Гиповентиляция и сниженная вдыхаемая концентрация кислорода приведет к падению альвеолярного РАО2. Повышенное потребление кислорода при растущих метаболических потребностях, например, при послеоперационном ознобе или злокачественной гипертермии также приводит к снижению РaО2.
При падении РаО2 ниже 60 мм Hg хеморецепторы каротидного синуса и дуги аорты вызывают гипервентиляцию и повышение сердечного выброса через стимуляцию симпатической нервной системы. Эту нормальную протективную реакцию на гипоксию подавляют анестетики в интра- и послеоперационном периоде.
После индукции в наркоз наблюдается быстрое снижение ФОЕ, приводящее с закрытию мелких бронхиол, особенно в зависимых частях легких, которые спадаются и находятся в закрытом состоянии втечение всего респираторного цикла. Некоторые альвеолы при этом не вентилируются и возникает шунт.
Нарастают V/Q нарушения, что приводит к снижению сатурации крови в легочных венах ниже, чем в капиллярах вентилируемых альвеол. Ситуация усугубляется во время индукции в наркоз, когда примесь неоксигенированной крови может составлять не 1%, а 10%. За исключением пациентов с сохраненным спонтанным дыханием на фоне анестезии кетамином подобная картина возникает вне зависимости от использованного анестетика и от того, вводились ли пациенту миорелаксанты. Это следует рассматривать как неизбежный побочный эффект анестезии. Ингаляционные анестетики подавляют легочную гипоксическую вазоконстрикцию и кровоток по невентилируемым альвеолам не снижается. Многие анестетики снижают сердечный выброс и соответственно доставку кислорода. При анестезии на 15% падает уровень метаболизма и, следовательно, потребность в кислороде. Искусственная вентиляция снижает потребности в кислороде на 6% вследствие отсутствия работы дыхательной мускулатуры. Анестетики не влияют на кислородотранспортные свойства гемоглобина.

Рис. 4. На рисунке горизонтальной линией показан лимит, до которого снижение доставки О2 не вызовет снижение его потребления (оксигенация, не зависимая от доставки) (А-В). Ниже указанного критического значения доставки О2 потребление становится зависимым от доставки и возникают признаки гипоксии. Положение точки С зависит от значения максимально возможной экстракции кислорода.
Практическое использование кислорода.
Концентрация вдыхаемого кислорода.
Эффективность оксигенации во время анестезии снижается вследствие гиповентиляции и легочного шунта. Эффективной мерой борьбы с гипоксией является поддержание фракции вдыхаемого кислорода 25-30% для поддержания нормального РаО2 (рисунок 6). При росте легочного шунта для поддержания нормального РаО2следует повышать фракцию вдыхаемого кислорода, но приходится отметить, что при значениях легочного шунта более 30% эта мера перестает быть эффективной (рисунок 7). Во время поддержания анестезии фракция вдыхаемого кислорода должна всегда при имеющейся возможности равняться или превышать 30% для компенсации гиповентиляции и легочного шунта, сопровождающих анестезию. Дополнительная оксигенация должна использоваться у пациентов с риском развития нарушений транспорта кислорода (анемия или сниженный сердечный выброс) или повышенным потреблением кислорода (лихорадка).
Рис. 5. Основные запасы кислорода в организме
| При дыхании воздухом | При дыхании 100 О2 | |
| В легких (ФОЕ) | 450 мл | 3000 мл |
| В крови | 850 мл | 950 мл |
| Растворенного или связанного в тканях | 250 мл | 300 мл |
| Всего | 1550 мл | 4250 мл |
Преоксигенация.
Небольшой объем кислорода, содержащийся в ФОЕ при дыхании воздухом, объясняет быстрое падение сатурации кислородом крови во время апноэ (например, после индукции в наркоз, при ларингоспазме или обструкции верхних дыхательных путей). Преоксигенация это дыхание 100% кислородом втечение трех минут через плотно прижатую к лицу маску, соединенную с дыхательным контуром наркозного аппарата. Это время необходимо для вытеснения азота из ФОЕ кислородом в условиях нормовентиляции. Во время анестезии наблюдается снижение ФОЕ, таким образом преоксигенация необходима для создания дополнительного запаса кислорода на период апное, который возникает при индукции в наркоз или трудной интубации.
У пациентов с низкой ФОЕ (новорожденные, беременные, полные) или низким содержанием гемоглобина и, следовательно, небольшим запасом кислорода быстро наступает гипоксия, поэтому преоксигенация у них особенно важна.

Рис. 6. Влияние возрастающего FiO2 (от 21% до 30% — тонкая линия) на РАО2 (толстая линия) при постоянном потреблении кислорода 200 мл/мин. Стрелкой показано влияние растущего FiO2 на РО2 у пациента с альвеолярной вентиляцией 1,5 л/мин.
Аноксические смеси газов.
Если по ошибке пациенту дана 100% закись азота, падение альвеолярного РО2 наступит быстрее, чем при апноэ. Снижение альвеолярного РО2 до критических значений произойдет менее, чем за 10 секунд. Это происходит потому, что кислород в легких и крови быстро вымывается при каждом вдохе, не содержащем кислород. Снижение РО2 произойдет быстрее, чем если бы он только использовался на покрытие метаболических потребностей организма (250 мл/мин).
Неотложная помощь.
При лечении неотложных состояний, связанных с гипоксией во время анестезии, первое, что требуется сделать еще до определения ее причины – дать 100% кислород. Это один важных этапов терапии острых нарушений кардиореспираторных функций.
Диффузионная гипоксия.
Закись азота в 45 раз лучше растворяется в крови, чем азот. При прекращении подачи закиси азота в конце анестезии, закись азоте втечение 2-3 минут в больших количествах продолжает диффундировать в альвеолы из крови. Если пациент дышит воздухом, присутствие в газовой смеси закиси азота и азота снижает PO2. Это явление вызывает диффузионную гипоксию, которая может быть устранена вдыханием 100% кислорода втечение 2-3 минут после прекращение подачи закиси азота.
Послеоперационное использование кислорода.
Причины повышенной примеси неоксигенированной венозной крови (нарушения V/Q отношений, шунт, обструкция дыхательных путей) сохраняются в послеоперационном периоде втечение нескольких дней после большинства оперативных вмешательств. Послеоперационная гиповентиляция — частое следствие остаточного действия наркоза, анальгезии опиоидами, боли или обструкции дыхательных путей. Озноб в раннем послеоперационном периоде повышает потребление кислорода, поэтому всем пациентам, находящимся без сознания и пациентам с ознобом, гиповентиляцией и с риском развития сердечно-сосудистых нарушений (например, с ИБС) необходима оксигенотерапия.

Рис. 7. Взаимосвязь концентрации вдыхаемого кислорода (FiO2) на РаО2 при наличии различного уровня легочного шунта. Можно отметить, что при уровне шунта более 50% от сердечного выброса повышение FiO2 не способно поддерживать РаО2 на нормальном уровне.
В послеоперационном периоде, в палате часты случаи обструкции дыхательных путей, приводящие к критическому снижению сатурации вследствие перечисленных выше факторов. Причиной нарушений могут быть опиоиды и изменение структуры сна, возникающие на вторую и третью ночи после операции. Известно, что после больших операций риск развития гипоксемии в послеоперационном периоде возрастает. Все пациентам следует назначить кислород, так как легкий цианоз не всегда легко распознать, особенно у пациентов с анемией. Особенно важно назначать его втечение всей первой ночи у пациентов особого риска (ИБС). Следует также проводить адекватное обезболивание, так как у пациентов с выраженным болевым синдромом после абдоминальных или торакальных операций наблюдается поверхностное дыхание. При использовании опиоидных анальгетиков следует предвидеть гиповентиляцию и проводить оксигенотерапию.
Проблемы, связанные с применением кислорода.
Предполагалось, что использование высоких концентраций кислорода (90-100%) у пациентов втечение длительного периода (несколько дней) может вызвать повреждение легких. Доказательств этому суждению нет и оно не до?
