Уровень гемоглобина при пороках сердцах
Анемия при пороке сердца. Гипохромная анемия при цианотических пороках сердцаПри врожденных пороках сердца, особенно «синего» типа, чаще наблюдается одна из форм экзогенной анемии — алиментарная гипохромная железодефицитная. Эта форма характеризуется не столько снижением количества эритроцитов, сколько уменьшением общего количества гемоглобина, а также содержания и концентрации гемоглобина в эритроцитах. Поэтому ведущим симптомом ее являются уменьшение объема эритроцитов (микроцитов) и снижение цветного показателя. Гипохромная анемия у детей с цианозом носит своеобразный характер. Она развивается несмотря на растущее количество эритроцитов и характеризуется относительно низким или нормальным количеством гемоглобина и значительным снижением цветного показателя (до 0,6—0,4). В связи с этим К. Ф. Ширяева называет анемию у таких детей «релятивной». В развитии анемии у детей раннего возраста без врожденного порока сердца играют роль следующие факторы: недостаточное гемоглобинообразование вследствие недостаточного поступления железа с пищей, развивающееся к 5—6 месяцам (к этому времени истощаются запасы железа, отложенные к моменту рождения в печени); физиологически низкое содержание соляной кислоты в желудочном соке, в результате чего железо, принятое с пищей, не всасывается; сопутствующие рахит и гипотрофия; повторные простудные заболевания. Кроме того, по мнению Rossi с соавторами, имеют значение также кровопотери и конституциональные факторы. У детей, страдающих врожденными пороками сердца «синего» типа, кроме перечисленных выше факторов, отмечается хроническая гипоксия, вызывающая патологическую реакцию организма — развитие полицитемии. Однако в связи с дистрофией и нарушенным балансом эндогенного железа в организме костный мозг продуцирует большое количество эритроцитов, бедных гемоглобином и с уменьшенным средним диаметром (Rossi с соавт., 1961; К. Ф. Ширяева, 1962).
Изучая гемопоэз у детей раннего возраста с врожденными пороками сердца, С. Т.. Цыганкова, В. И. Францев и М. Н. Кириченко (1963), установили, что он не адекватен степени гипоксии. К этому же выводу приходит К. Ф. Ширяева (1965). Частота гипохромной анемии у больных врожденными пороками сердца в возрасте до 3 лет, по данным Е. Ф. Ширяевой (1962), достигает 50%, по данным Rossi с соавторами (1961), — 9,2%. Мы наблюдали 183 детей врожденными пороками сердца «синего» типа в возрасте до 3 лет, из них гипо-хромная анемия была отмечена у 64 (35%). До 1 года было 26 детей, из них гипохромная анемия наблюдалась у 7, в возрасте 1—2 года соответственно 61 и 31, в возрасте 2—3 лет — 96 и 26. Гипохромная анемия развивается у детей в первые месяцы жизни. Так, Б. А. Константинов, М. И. Чернова и Г. И. Алексеев (1966) указывают, что она достигает максимума к 3 месяцам, причем количество эритроцитов не превышает 4 000 000, гемоглобина 100 ед., к 8— 12 месяцам анемия уменьшается и нарастает полицитемия. Rossi с соавторами, напротив, наблюдали анемию у детей до 18 месяцев, К. Ф. Ширяева — до 2 лет. Мы обнаружили гипохромную анемию даже у детей 3 лет. У детей с гипохромной анемией, несмотря на гипоксию, цианоз отсутствует или незначителен; кожные покровы серо-бледного цвета; выражены явления гипотрофии, рахита; отмечается значительное увеличение печени; нарастают явления сердечной недостаточности: одышка, тахикардия, увеличение сердца. Как известно, причиной цианоза считается повышение количества редуцированного гемоглобина до 5 г на 100 мл крови (Литтман и Фоно, 1954). – Также рекомендуем “Синюшно-одышечные приступы при тетраде Фалло. Тромбоцитопении при пороке сердца” Оглавление темы “Болезни сопровождающие пороки сердца”: |
В последнее время все больше внимания исследователей привлекают вопросы, связанные с изучением общего гемоглобина, свободного гемоглобина и мышечного гемоглобина — миоглобина. В литературе нет единого мнения о количестве гемоглобина плазмы крови в норме (И. А. Кассирский, Г. А. Алексеев, А. М. Чарный, Ю. И. Лорне, И. Тодоров, Г. В. Дервиз), также малочисленны сведения о изменении количества миоглобина при патологии, в частности, при врожденных пороках сердца «бледного» и «синего» типа.
Содержание общего гемоглобина и свободного гемоглобина периферической крови определялось: у 30 доноров в возрасте от 20 до 49 лет; у 73 больных с врожденными пороками «бледного» типа в возрасте от 2 лет до 47; у 55 больных с врожденными пороками «синего» типа в возрасте от 1 года 7 мес. до 23 лет. Кроме того, у 40 больных с пороками сердца «бледного» типа и у 47 больных с врожденными пороками «синего» типа определен был миоглобин. Общий гемоглобин определен путем перевода в оксигемоглобин, гемоглобин плазмы крови и миоглобин (бензидиновым методом ФЭК-М) по калибровочной кривой, для построения которой использовалась кровь с точно определенным количеством гемоглобина.
Содержание миоглобина определялось в межреберной мышце, биопсия производилась во время операции. Количество миоглобина выражалось в граммах на 100,0 г сухой ткани. Полученные данные обработаны методом вариационной статистики.
Изучение общего и свободного гемоглобина у здоровых людей показало, что количество общего гемоглобина в периферической крови составляет 14,2±0,2 г% ( о =1,18), свободного гемоглобина 3,1 ±0,05 мг% (а =0,26), у больных с дефектом межпредсердной перегородки содержание общего гемоглобина 12,5+0,15 г% (с =1,04), а гемоглобина плазмы крови 3,1 ±0,05 мг% (а =0,35), миоглобина 2,3+0,05 г (а ±0,23).

Проведенное исследование гемоглобина у больных с дефектом межжелудочковой перегородки показало, что общий гемоглобин у них составляет 13,0±0,01 г% ( а =0,018), свободный гемоглобин 3,3±0,008 мг% (О:=0,88), миоглобнн 2,7±0,5 г (а=0,20).
По содержанию общего гемоглобина больные с врожденными пороками сердца «синего» типа были разделены на 2 группы: от 12,3 г% до 17,0 г%—26 больных и от 17,0 г% и выше— 29 больных.
В первый группе больных общий гемоглобин 14,0±0,3 г% (а = 1,7), свободный гемоглобин 5,3±0,20 мг% (а =1,4), миоглобнн 2,7Э±0,4 г (о=0,2).
Исследуемые показатели у больных второй группы следующие: общий гемоглобин — 20,0±0,6 г% ( о =0,11), свободный гемоглобин 12,5 + 0,18 мг% (о =1,0), миоглобнн 5,0±0,14 г (а=0,80).
Изучение вариационного распределения содержания общего гемоглобина, свободного гемоглобина и миоглобина показало, что в пределах М—±2о укладываются 96% исследований.
Таким образом, проведенное исследование показало, что содержание общего гемоглобина и гемоглобина плазмы крови одинаково у здоровых людей, у больных с дефектами перегородок сердца и у больных тетрадой Фалло со слабо выраженной гипоксемией.
У больных тетрадой Фалло с резко выраженной гипоксемией увеличено содержание общего гемоглобина в 1,5 раза, гемоглобина плазмы крови в 3,5 раза и миоглобина в 2 раза, что свидетельствует о крайнем напряжении эритропоэза компенсирующим гипоксемию.
– Читать далее “Тканевое дыхание при ВПС. Влияние легочной гипертензии на тканевое дыхание”
Оглавление темы “Компенсаторные изменения в организме при пороке сердца”:
1. Содержание гемоглобина при ВПС. Миоглобин у больных с ВПС
2. Тканевое дыхание при ВПС. Влияние легочной гипертензии на тканевое дыхание
3. Буферные системы при пороке сердца. Резервы газового состава крови при ВПС
4. Железо, медь, цинк при пороке сердца. Значение железа в приспособлении организма к операции
5. Гепаторенальная система при врожденных пороках сердца. Печень, почки при ВПС
6. Легочное сосудистое русло при ВПС у детей до 3-х лет. Морфология легочных сосудов при врожденном пороке сердца
7. Степень гипертрофии миокарда при ВПС. Оценка гипертрофии миокарда у детей с пороком сердца
8. Симпато-адреналовая система при пороке сердца. Уровень адреналина после операции на сердце
9. Компенсация при тетраде Фалло. Гипертрофия правого желудочка при тетраде Фалло
10. Минутный объем кровообращения при тетраде Фалло. Адаптация к артериальной гипоксемии при тетраде Фалло
Сердечно-сосудистые заболевания считаются основной причиной смерти у россиян. По статистике 46% людей умирают именно из-за болезней сердца.
Первые симптомы сердечных патологий знают многие. А вот как самостоятельно проверить здоровье сердца и понять, что у вас нет проблем?
Фото взято из свободного доступа в Яндексе
1. У вас нормальное артериальное и пульсовое давление
Повышенное артериальное давление относится к основному фактору риска развития сердечно-сосудистых заболеваний. Риск инфаркта у людей с артериальной гипертонией повышается в 4 раза, а инсульта в 7 раз.
Постоянная артериальная гипертензия, плохо поддающаяся лечению, может наблюдаться при:
· выраженном атеросклерозе;
· приобретенных пороках сердца;
· заболеваниях почек;
· сердечной недостаточности;
· тяжелых эндокринных нарушениях (гиперфункция щитовидной железы или надпочечников, сахарный диабет).
Резкое снижение давления, в сочетании с повышением температуры тела, нарушением сердечного ритма и одышкой может наблюдаться при миокардите (воспалении сердечной мышцы).
Кроме оценки самого артериального давления важно рассчитывать показатель пульсового давления – разницы между верхним (систолическим) и нижним (диастолическим) давлением.
В норме, пульсовое давление составляет 30-50 мм рт. ст. Большое пульсовое давление (когда повышается систолическое давление, а диастолическое снижается) может наблюдаться у людей с аортальной недостаточностью.
Как проверить свое давление? Смотрите таблицу нормального артериального давления по возрасту.
нормы давления по возрасту
2. У вас нет пульсации брюшной аорты ниже пупка
Пульсация брюшной аорты выше пупка может наблюдаться в норме у худых людей или при слабых мышцах живота.
Видимая пульсация ниже пупка (особенно справа) может свидетельствовать о развитии аневризмы брюшной аорты.
3. У вас нормальный пульс
Нормальным пульсом считается показатель от 60 до 90 ударов в минуту. У мужчин обычно пульс реже, чем у женщин.
Нормальный пульс:
· одинаков на обеих руках;
· одинаков на шее и на руках;
· равномерный – без перебоев и неожиданных скачков или замираний;
· равномерный – толчки одинаковой силы и частоты.
4. У вас нет пульсации шейных вен
Не путать с пульсацией сонных артерий, которая может наблюдаться в норме.
фото взято из свободного доступа в Яндексе
Пульсация вен характерна для сердечной недостаточности.
5. У вас нет патологических пульсаций
К патологической пульсации относится:
· пульсация зрачков (зрачки ритмично пульсируют в такт сердцебиению);
· капиллярная пульсация (пульсация белого пятнышка, которое появляется при нажатии на губу или ногтевую пластину).
Патологическая пульсация характерна для аортальной недостаточности.
6. У вас нет отеков шеи и голеней
Для сердечной недостаточности характерны плотные отеки шеи и голеней. Отеки голени появляются ближе к вечеру.
7. Вас не беспокоят боли за грудиной
При заболеваниях сердца отмечаются:
· острые боли слева, отдающие в нижнюю челюсть, лопатку, руку;
· тупые боли за грудиной, сопровождающиеся невозможностью сделать вдох;
· боли после физической нагрузки.
8. Вы не страдаете одышкой и адекватно переносите физические нагрузки
Вы можете присесть 15-20 раз без резкого повышения пульса или подняться на 4-5 этаж без одышки? Тогда у вас вряд ли есть проблемы с сердцем. А вот если вы заметили, что стали хуже переносить привычную нагрузку, стоит обратиться к кардиологу.
Картинка взята из свободного доступа в Яндексе
9. У вас нет варикоза и сосудистых звездочек
Венозная недостаточность увеличивает риск развития тромбоза, что в свою очередь может привести к инсульту или инфаркту. При лечении варикоза этот риск сводится к минимуму.
10. Вы не страдаете частыми головными болями и постоянными головокружениями
Нарушения сердечного ритма, высокое или низкое давление, сердечная недостаточность и другие проблемы с сердечно-сосудистой системой могут приводить к:
· постоянным головным болям и мигреням;
· головокружениям;
· появлению шума в ушах;
· частым обморокам;
· постоянной слабости.
11. У вас нет ночного апноэ
Ночные остановки дыхания часто могут свидетельствовать о заболеваниях сердца. Как проявляются ночные апноэ:
· человек часто просыпается ночью без видимой причины;
· сильный храп резко прерывается, а затем, человек делает судорожный вздох и снова начинает храпеть.
Короткие ночные апноэ могут быть вариантом физиологической нормы, однако провериться у кардиолога все равно не будет лишним.
12. У вас нет цианоза губ и носогубного треугольника
Многие пороки сердца, ишемическая болезнь сердца и сердечная недостаточность сопровождаются появлением цианоза (синеватый или синевато-фиолетовый оттенок) губ и носогубного треугольника.
Цианоз часто сочетается с общей бледностью кожи.
13. У вас нет лишнего веса
Избыточная масса тела сопровождается развитием:
· метаболического синдрома (приводит к развитию инсулинорезистентности в тканях и формированию сахарного диабета 2 типа);
· артериальной гипертензии, плохо поддающейся лечению;
· атеросклероза;
· гипертриглицеридемии (увеличивается вязкость крови и начинают формироваться микротромбы в сосудах).
Все это увеличивает риск развития сердечной недостаточности, стенокардии, ишемической болезни сердца, тромбоза, инфаркта и инсульта.
14. У вас хорошие анализы крови и ЭКГ
При отсутствии изменений на ЭКГ риск наличия заболеваний сердца минимальный.
Также в пользу здоровья сердечно-сосудистой системы могут свидетельствовать нормальные результаты анализа крови.
фото взято из свободного доступа в Яндексе
Нормальный уровень показателей:
· гемоглобина – говорит об отсутствии анемий;
· тромбоцитов – минимальный риск развития кровотечений или тромбов;
· СОЭ и лейкоциты – отсутствуют воспалительные процессы;
· триглицериды, липопротеиды и холестерин – минимальный риск развития атеросклероза и тромбоза.
Лучшие способы снижения риска развития сердечно-сосудистых заболеваний
Развитие сердечно-сосудистых заболеваний напрямую зависит от образа жизни. Свести к минимуму риск развития опасных заболеваний можно, соблюдая простые правила:
1. Не курить (отказ от курения является основой профилактики заболевания сердца и сосудов).
2. Не злоупотреблять спиртными напитками (речь идет о систематическом употреблении спиртных напитков, поскольку статистической разницы по заболеваниям сердца и сосудов у людей, периодически употребляющих умеренное количество спиртного и вообще не пьющих – нет).
3. Вести активный образ жизни (умеренные физические нагрузки – это лучший способ профилактики сердечно-сосудистых заболеваний, сахарного диабета, старческой деменции и онкологических заболеваний).
4. Употреблять больше свежих фруктов и овощей.
5. Не есть много мяса.
6. Отказаться от злоупотребления жирной и жареной пищей, солью, сладкими газировками.
7. Полноценно высыпаться и стараться меньше нервничать (стресс является основным пусковым механизмом в развитии инфаркта и инсульта).
Статья посвящена проблеме приобретенной механической гемолитической анемии, вызванной дисфункцией имплантированных сердечных клапанов. Показано, что в современных условиях наиболее часто выраженные признаки гемолиза наблюдаются при дисфункции протеза, например, вследствие образования параклапанной фистулы. Представлены клинические случаи.
В настоящее время благодаря современным возможностям сердечно-сосудистой хирургии операция протезирования клапанов сердца стала повседневной в работе специализированных кардиохирургических центров. В мире живут десятки тысяч пациентов с имплантированными сердечными протезами. В условиях хирургической коррекции клапанов становится актуальной проблема послеоперационной анемии, которая может носить различный характер. Вероятность развития у такого рода больных приобретенной механической гемолитической анемии во многом определяет течение послеоперационного периода. Большое значение в достижении хороших отдаленных результатов приобретают квалифицированный контроль и лечение этих пациентов у врача поликлиники по месту жительства [1].
Данные о воздействии протезов на эритроциты и на возникновение гемолиза противоречивы. По данным некоторых исследователей, гемолиз бывает клинически невыраженным, в других работах имеются указания на значительные клинические проявления гемолиза [1–4]. Степень клинических проявлений гемолиза зависит как от состояния самих эритроцитов, так и от механических свойств протезов [5, 6]. Несомненно, играют роль не только обработка протеза и материал, из которого он сделан, но и гемодинамические условия: скорость кровотока в области протеза, образование завихрений.
В связи с улучшением методологии оперативных вмешательств, а также с модернизацией искусственных клапанов сердца (ИКС) сердечно-сосудистый риск при операциях на сердце в течение последних десятилетий существенно снизился во всех возрастных группах. В 1960–1970-е гг. после введения в практику протезирования клапанов сердца гемолитическая анемия развивалась у 5–15% прооперированных пациентов, особенно после имплантирования механических шаровых протезов [2, 5]. Использование протезов нового поколения снизило частоту гемолитической анемии до 1% [2, 6]. Современные искусственные клапаны сердца разработаны на основе клинических данных использования нескольких поколений протезов. Они изготовлены из новейших материалов и имеют уникальную конструкцию [7, 8]. Однако компенсированный гемолиз может возникнуть при любом типе протеза. Наиболее часто выраженные признаки гемолиза наблюдаются при нарушении функции протеза, например, вследствие образования параклапанной фистулы. Разрушение эритроцитов с развитием гемолиза связано с нарушением кровотока через дефектный протез и увеличением повреждения эритроцитов его створками [3, 7]. Клинически гемолиз может проявляться симптомами сердечной недостаточности и анемии. Наблюдаются бледность кожных покровов, желтуха, моча может приобретать коричневый или черный цвет. Содержание билирубина повышено, особенно непрямая фракция, могут быть ретикулоцитоз, повышение активности лактатдегидрогеназы (ЛДГ) и уровня свободного гемоглобина в плазме крови. Синдром механического гемолиза подтверждается обнаружением в мазке крови больного фрагментов (обломков) эритроцитов (Fragmentes Red Cell (FRC)) или шистоцитов (син. — шизоциты). Наблюдаются анизопойкилоцитоз (изменение формы и размеров эритроцитов), полихромазия (способность окрашиваться как основными, так и кислыми красителями). При длительно протекающем гемолизе развивается дефицит железа.
В отечественной и зарубежной литературе описано очень мало случаев макроангиопатической гемолитической анемии, связанной с механическим повреждением эритроцитов у пациентов с ИКС. Мы приводим собственные наблюдения о гемолизе, вызванном дисфункцией механического двустворчатого протеза МедИнж (ЗАО НПП «МедИнж», Россия).
Пациентка, 65 лет.
Диагноз: сочетанный приобретенный порок митрального, аортального и трикуспидального клапанов. Проведено протезирование аортального (МедИнж 23) и митрального (МедИнж 29) клапанов, аннулопластика трикуспидального клапана по Де Вега-2.
До оперативного вмешательства у пациентки показатели красной крови не выходили за пределы соответствующих референтных интервалов: эритроциты — 4,16×1012/л; гемоглобин — 124 г/л; гематокрит — 36%; средний объем эритроцитов — 86,6 фл; среднее содержание гемоглобина в эритроците — 29,8 пг; средняя концентрация гемоглобина в эритроците — 344 г/л; ширина распределения эритроцитов по объему — 13,7%. На 10-е сут после операции у нее наблюдалась нормохромная анемия: эритроциты — 2,74×1012/л; гемоглобин — 83,2 г/л; гематокрит — 23,7%; средний объем эритроцитов — 86,7 фл; среднее содержание гемоглобина в эритроците — 30,4 пг; средняя концентрация гемоглобина в эритроците — 351 г/л; ширина распределения эритроцитов по объему — 16,1%. Через 1 мес. признаки анемии сохранялись: эритроциты — 2,54×1012/л; гемоглобин — 80,2 г/л; гематокрит — 23%; средний объем эритроцитов — 82,3 фл; среднее содержание гемоглобина в эритроците — 27,4 пг; средняя концентрация гемоглобина в эритроците — 351 г/л; ширина распределения эритроцитов по объему — 17,1%. На фоне приема сульфата железа и аскорбиновой кислоты 200 мг/сут эффекта не наблюдалось.
Пациентку беспокоили одышка при минимальной физической нагрузке, в положении лежа, отеки, повышенная утомляемость. Через 6 мес. после операции в связи с сохранением жалоб, признаков анемии (гемоглобин — 70–80 г/л) находилась на лечении в терапевтическом отделении. У пациентки был повышен уровень непрямого билирубина (40,4 мкмоль/л), проба Кумбса отрицательная, отмечалось периодическое выделение мочи черного цвета. Эффекта от преднизолона не было. Была обследована у гематолога, диагностирована приобретенная гемолитическая анемия, обусловленная механическим повреждением эритроцитов протезированными клапанами сердца. Направлена в кардиохирургический стационар для решения вопроса о повторном оперативном вмешательстве.
При поступлении в стационар состояние тяжелое. Кожные покровы бледные, желтушные. Живот увеличен за счет асцита. Пастозность стоп, лодыжек. Тоны сердца приглушены, аритмичные. Мелодия протеза четкая, систолический шум во всех точках. На эхокардиографии: в проекции аортального клапана протез без признаков дисфункции; в проекции митрального клапана диагностирована трансклапанная регургитация 1–2 степени, по задней части протеза — параклапанная фистула 2 степени. Показатели красной крови: эритроциты — 2,76×1012/л; гемоглобин — 90 г/л; гематокрит — 26,3%; средний объем эритроцитов — 95,6 фл; среднее содержание гемоглобина в эритроците — 32,2 пг; средняя концентрация гемоглобина в эритроците — 342 г/л; ширина распределения эритроцитов по объему — 24,3%, при микроскопии окрашенного мазка — полихромазия, шистоциты (2,0%) (рис. 1), ретикулоциты — 2,5%. Билирубин общий — 98,5 мкмоль/л, билирубин непрямой — 50,4 мкмоль/л, свободный гемоглобин — 0,6 г/л.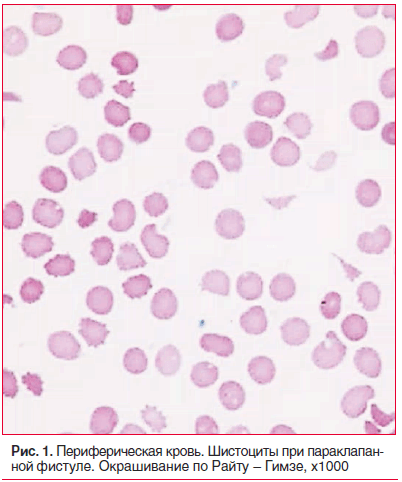
К сожалению, ввиду наличия у пациентки аортального протеза эндоваскулярное закрытие параклапанной фистулы митрального протеза было технически невыполнимо. В настоящее время пациентка наблюдается у кардиолога и гематолога по месту жительства. При снижении гемоглобина ниже 60 г/л ей проводятся трансфузии эритроцитосодержащих компонентов крови.
Пациентка, 60 лет. Диагноз: приобретенный порок митрального и трикуспидального клапанов. Проведены протезирование митрального (МедИнж 29) клапана, аннулопластика трикуспидального клапана по Де Вега.
Через 1 год после оперативного вмешательства у пациентки наблюдалось ухудшение состояния: одышка при минимальной физической нагрузке, отеки на ногах, последние 6 мес. — желтушность склер. В анализах, выполненных по месту жительства, — билирубин до 134 мкмоль/л. По данным чреспищеводной эхокардиографии в проекции митрального клапана — параклапанная фистула 1 степени.
Пациентка была госпитализирована в кардиохирургический стационар для устранения дефекта. При поступлении: билирубин — 110 мкмоль/л, непрямой билирубин — 22,7 мкмоль/л, свободный гемоглобин — 0,3 г/л. Наблюдалась гипохромная анемия: эритроциты — 4,6×1012/л; гемоглобин — 100 г/л; гематокрит — 36%; средний объем эритроцитов — 73,9 фл; среднее содержание гемоглобина в эритроците — 21,7 пг; средняя концентрация гемоглобина в эритроците — 291 г/л; ширина распределения эритроцитов по объему — 24,4%, шистоциты — 1,3%. Пациентке было проведено эндоваскулярное закрытие параклапанной фистулы окклюдером с положительной динамикой, с постепенным снижением уровня общего и непрямого билирубина, повышением уровня гемоглобина. При выписке гемоглобин — 128 г/л.
Таким образом, при подозрении на гемолиз у больных с ИКС всегда необходимо исключать механическую причину повреждения эритроцитов. Степень анемии в зависимости от степени и выраженности гемолиза может быть различной. Чаще всего анемия нормохромная, но при длительно протекающем гемолизе может носить гипохромный характер, с изменением морфологии красных клеток крови и присутствием шистоцитов либо только с присутствием шистоцитов как изолированным проявлением пойкилоцитоза. Рабочая группа Международного совета стандартизации в гематологии (МССГ (ICSH)) подготовила рекомендации для стандартизации, идентификации, подсчета и описания шистоцитов. Рекомендации определяют морфологическое описание шистоцитов, основанное на соответствующих критериях (в виде шлема; маленькие, неправильной треугольной формы, с наличием 2–3 углов; в форме полумесяца, с заостренными выступами, а также с отсутствием просветления в центре) [9–11]. В качестве полезного дополнения к микроскопу рекомендуется автоматизированный подсчет FRC. К сожалению, не все современные гематологические анализаторы демонстрируют сигналы тревоги («флаги»), сигнализирующие о наличии шистоцитов, а тем более проводят их подсчет. Да и специфичность автоматического метода очень низка (около 20%), требуется микроскопическое исследование для их подтверждения [9]. Поэтому общий анализ крови у пациентов с ИКС при подозрении на гемолиз необходимо дополнять микроскопией окрашенного мазка крови с описанием морфологии эритроцитов.
Выявленный шистоцитоз требует от врача-клинициста безотлагательных действий по установлению диагноза. При наличии клинической картины, лабораторных признаков гемолиза, нарастании в динамике процентного содержания шистоцитов диагноз механического разрушения эритроцитов становится очевидным. При подтверждении механической гемолитической анемии оправданным методом лечения является своевременное репротезирование клапанов сердца.