В гене одной из цепей гемоглобина
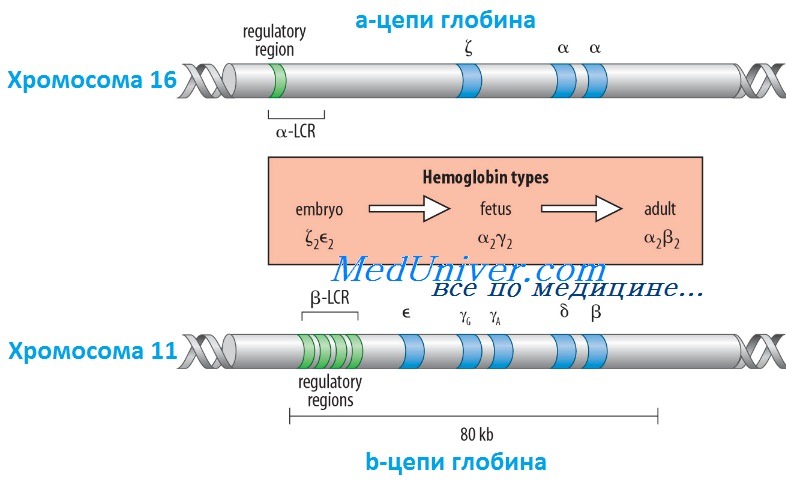
Гены гемоглобина человекаКроме НbА, у человека есть еще пять других нормальных гемоглобинов, которые имеют тетрамерные структуры, сравнимые с НbА и состоящие из двух а- или а-подобных цепей и двух не-b-цепей. Гены а- и а-подобных цепей расположены тандемно в хромосоме 16, а для b- и b-подобных — в хромосоме 11. В каждой копии хромосомы 16 есть два идентичных гена а-глобина, названные а1 и а2. В пределах комплекса генов b-глобина существует тесная гомология между разными генами. Например, b- и q-глобины отличаются только 10 из 146 аминокислот. Все гены глобина, несомненно, возникли из общего гена-предшественнника. Изменение экспрессии различных генов глобина в ходе развития иногда называют переключением глобинов. Это классический пример упорядоченного регулирования экспрессии генов в ходе развития. Гены в а- и b-группах размещаются в одной и той же транскрипционной ориентации и, что замечательно, гены внутри каждой группы расположены в той же последовательности, в которой они экспрессируются в процессе развития. Существует эквимолярное соответствие синтеза а- и b-подобных цепей глобина. Интересно, что переключение синтеза глобинов по времени сопровождается изменениями в основном месте эритропоэза. Эмбриональный синтез глобина происходит в желточном мешке с 3 по 8 нед гестации, но приблизительно около 5 нед гестации основное место кроветворения начинает перемещаться из желточного мешка в печень плода. HbF (а2у2) — преобладающий гемоглобин в внутриутробном периоде — составляет приблизительно 70% общего гемоглобина при рождении, но во взрослой жизни HbF составляет менее 1% общего гемоглобина. Хотя b-цепи могут обнаруживаться на ранних сроках гестации, их синтез становится значимым только ближе к сроку родов; к 3-месячному возрасту почти весь гемоглобин становится гемоглобином взрослого типа — HbА. Синтез 8-цепи также продолжается после рождения, но НbА2 (а2q2) никогда не составляет более примерно 2% гемоглобина взрослых. К несчастью, небольших количеств q-глобина (и, следовательно, HbA2) и у-глобина (и, следовательно, HbF), обнаруживаемых в норме в крови взрослого человека, недостаточно для компенсации сниженного количества b-глобина (и, следовательно, НbА), образующегося при болезнях типа b-талассемии. Следовательно, знание механизмов, регулирующих производство цепей глобина, потенциально имеет терапевтическое значение. Обнаружено множество факторов транскрипции, управляющих экспрессией генов глобина, что дает надежду на разработку лечения, направленного на увеличение синтеза q- и у-глобинов.
Регулирование экспрессии генов b-глобина: управляющий регион локусаКак и во многих других областях медицинской генетики, изучение механизмов, регулирующих экспрессию генов глобина, дало понимание как нормальных, так и патологических биологических процессов. Экспрессия гена b-глобина, как оказалось, только частично контролируется промотором и двумя энхансерами в фланговой ДНК, расположенной непосредственно рядом с геном. Необходимость дополнительных регулятор-ных элементов была заподозрена после идентификации уникальной группы пациентов, не имевших экспрессии ни одного гена в группе b-глобина, даже если сами гены (включая их индивидуальные регуляторные элементы) были неповрежденными. Оказалось, что такие пациенты имеют большие делеции выше комплекса b-глобина, удаляющие область приблизительно в 20 килобаз, названную локус-контролирующей областью (LCR, от англ. locus control region), которая начинается приблизительно в 6 килобазах выше гена е-глобина. Развивающаяся при этом болезнь, еу5р-талассемия, описана ниже. Данные пациенты показали, что LCR необходим для экспрессии всех генов в группе b-глобина в хромосоме 11. LCR определяется пятью сверхчувствительными к ДНКазе 1 участками, необходимыми для поддержки открытой конфигурации хроматина в данном локусе, что обеспечивает доступ факторам транскрипции к элементам, регулирующим экспрессию каждого гена в комплексе b-глобина. LCR вместе с ассоциированными связанными с ДНК белками, взаимодействует с генами локуса, формируя часть ядра, названную «транскрипционным узлом» (англ. active chromatin hub), в котором происходит экспрессия генов b-глобина. Последовательное переключение экспрессии генов, происходящее между пятью участниками комплекса гена b-глобина в ходе развития, вызвано последовательной ассоциацией транскрипционного узла с разными генами в группе, так как узел перемещается от 5′-конца комплекса (от экспрессирующегося в эмбриональном периоде гена e-глобина) через ген q до гена b-глобина у взрослых. Клиническое значение LCR разнообразно. Во-первых, пациенты с делециями LCR не экспрессируют гены группы b-глобина. Во-вторых, компоненты LCR, вероятно, окажутся существенными для генотерапии болезней группы b-глобина. В-третьих, знание молекулярных механизмов, лежащих в основе переключения глобинов, может сделать выполнимой, например, регуляцию экспрессии гена у-глобина у пациентов с b-талассемией (с мутациями в гене р-глобина), для стимуляции синтеза HbF (a2y2), — эффективного переносчика кислорода у взрослых с дефицитом НbА (а2b2). Для понимания патогенеза большинства гемоглобинопатий важны различия в дозе генов (четыре гена а-глобина и два гена b-глобина на диплоидный геном) и онтогенез а- и b-глобинов. Мутации в генах b-глобина более вероятно вызывают болезнь, чем мутации а-цепи, поскольку мутация единственного гена b-глобина влияет на 50% р-цепей, тогда как мутация одного гена а-цепи влияет только на 25% a-цепей. С другой стороны, мутации в гене b-глобина не имеют последствий во внутриутробном периоде, поскольку у-глобин является основным глобином до рождения, и к моменту родов HbF составляет три четверти общего гемоглобина. Поскольку а-цепи — единственный а-подобный компонент всех гемоглобинов, начиная с 6 нед после зачатия, мутации а-глобина вызывают тяжелую патологию как плода, так и послеродовой жизни. – Вернуться в содержание раздела “генетика” на нашем сайте Оглавление темы “Выявление генов болезни”:
|
Талассемия — это заболевание, из-за которого происходит нарушение синтеза гемоглобина. Название патологии дословно означает «анемия морского побережья». Заболевание наследуется по рецессивному типу, проявляется в результате генетических мутаций. Знания о том, что за болезнь талассемия, будут полезными при планировании семьи.
Этиология
Причиной талассемии являются точечные мутации или делеции в генах, кодирующих цепи гемоглобина. В результате это может привести к уменьшению синтеза или полному отсутствию одной из цепей в организме. Другая цепь образует неадекватные тетрамеры гемоглобина, что приводит к разрушению эритроцитов и гемолитической анемии.
Строение гемоглобина
Гемоглобин – белок содержащийся в эритроцитах, отвечающий за перенос кислорода к тканям и углекислого газа от них.
Гемоглобин (речь идёт о HbA) состоит из четырёх цепей: двух альфа-субъединиц и двух бета-субъединиц. Такой гемоглобин составляет 97% от общего содержания его в эритроцитах.
Оставшиеся 3% составляет гемоглобин HbA2, отличающийся по строению двух цепей: вместо бета-субъединиц у него дельта-субъединицы. HbA и HbA2 является вариантом нормы при их правильном соотношении.
Каждая из цепей гемоглобина связывается с его небелковой частью – гемом.
Так вот при талассемии нарушается синтез одной из цепей гемоглобина: либо альфа, либо бета. По этому принципу имеется классификация талассемии на:
- альфа-талассемию;
- бета-талассемию.
По степени тяжести выделяют талассемию:
- лёгкой степени;
- средней степени;
- тяжёлой степени.
Разновидности гемоглобина
Существуют физиологические виды гемоглобина и патологические.
К гемоглобину, который может быть в норме у человека, относится:
- HbP – примитивный гемоглобин, встречается в эмбрионе между 7 — 12-й неделей жизни;
- HbF – фетальный гемоглобин, содержит две альфа и две гамма-цепи, появляется через 12 недель внутриутробного развития, у взрослых его содержание составляет менее 1%;
- HbA – гемоглобин взрослых, доля составляет 97%, содержит две альфа и две бета-цепи;
- HbA2 – гемоглобин взрослых, доля составляет 2%, содержит две альфа и две дельта-цепи,
- HbO2 – оксигемоглобин, образуется при связывании кислорода в лёгких;
- HbCO2 – карбогемоглобин, образуется при связывании углекислого газа в тканях.
К патологическим формам гемоглобина относятся:
- HbS – гемоглобин, определяемый при серповидноклеточной анемии;
- MetHb – метгемоглобин, содержит трёхвалентный ион железа, когда в норме оно двухвалентное. Такая форма образуется при употреблении сульфаниламидов, нитратов, дефиците витамина С. Метгемоглобин не способен связывать кислород, в результате чего возникает гипоксия тканей;
- HbCO – карбоксигемоглобин, образуется при наличии избытка угарного газа во вдыхаемом воздухе. В крови он присутствует в небольших концентрациях, но его уровень может повышаться в зависимости от характеристики вдыхаемого воздуха.
HbS – вид гемоглобина, возникающего при мутации бета-цепи (одна аминокислота заменяется на другую). Он образуется у людей с серповидноклеточной анемией. Эритроциты, содержащие такой гемоглобин, долго не живут и быстро разрушаются, что хорошо в местах обитания малярийного плазмодия. У лиц с серповидноклеточной анемией имеется устойчивость к этому паразиту.
Почему разрушаются эритроциты?
Патогенез талассемии достаточно изучен. Первичные изменения начинаются с нарушенного синтеза гемоглобина, а именно белковых цепочек вещества. Известно, что гемоглобин, входящий в состав 90% массы эритроцитов, — единственное вещество, способное связывать молекулы кислорода и разносить их из легочной ткани по всему организму.
Его структура состоит из пигмента (гема), включающего железо, и набора из двух пар белковых цепочек. Их называют по типичному расположению аминокислот альфа- и бета-цепями. При нарушенном синтезе одного из типов полипептидов накапливается другой вид.
В результате разрушаются все клетки эритроцитарного ряда (сами эритроциты и их предшественники), из них выходит гемоглобин. Малокровие (анемия) развивается по гипохромному типу. Это подтверждается низким цветовым показателем.
«Виновниками» разрушений являются гены, ответственные за построение белковой части гемоглобина. Их мутация нарушает способность составлять необходимый набор аминокислот в цепи. Причину изменений связывают с возбудителем малярии — плазмодием. Доказаны его мутирующие способности. Талассемия по территории распространенности совпадает с эпидемическими зонами малярии.
Основные четыре цепочки белков, связывающие гем и влияющие на эритроциты
Дети могут получить болезнь путем наследования от родителей в двух видах:
- гомозиготном — ген-мутант передается от обоих родителей;
- гетерозиготном — ген болезни передается только от матери или отца, носителем может быть один из родителей.
Соответственно, называются формы талассемии.
При гетерозиготном носительстве выделяют:
- «немой» ген (α-th2);
- «манифестный» ген (α-th1).
Частота встречаемости
Талассемия наследуется аутосомно-рецессивно. Это значит, что поражает одинаково и мальчиков, и девочек. Рецессивный характер говорит о том, что дети больные талассемией появляются в тех семьях, где мама и папа оба являются носителями мутаций. Хотя они могут даже не догадываться о своём носительстве, так как симптомы порой бывают незаметны.
В среднем частота встречаемости составляет 1 на 100 000 человек и может изменяться в зависимости от региона. Бета-талассемия встречается чаще, чем альфа.
Альфа-талассемия
Существует 4 участка гена, которые кодируют синтез альфа-цепи гемоглобина. При наличии генетического дефекта (мутации) в них возникает альфа-талассемия. Выделяют несколько форм альфа-талассемии.
Гомозиготная
При ней нарушается синтез альфа-субъединиц на всех четырёх участках гена. В результате образуется гемоглобин, состоящий полностью из бета-цепей. Ещё он носит название гемоглобин Барта. Такой гемоглобин обладает высоким сродством к кислороду. Это означает, что он с трудом отдаёт кислород тканям. В результате возникает недостаток этого газа, что приводит к развитию сердечной недостаточности, отёкам, водянке и, как следствие, внутриутробной гибели плода.
Н-гемоглобинопатия
Н-гемоглобинопатия – форма, при которой нарушается синтез альфа-цепи на трёх участках гена. В результате избытка бета-субъединиц образуется HbH. У него также имеется достаточно высокое сродство к кислороду, он не стабилен, легко окисляется.
Присутствие такого гемоглобина в эритроцитах изменяет мембрану эритроцитов, сопровождается развитием гемолитической анемии, то есть усиленным распадом красных кровяных клеток. Проявляется такая форма альфа-талассемии к 1 году жизни в виде гемолитической анемии. Отмечаются признаки анемического синдрома, увеличение селезёнки. В анализах крови повышенные значения ретикулоцитов, что указывает на повышенную регенераторную способность костного мозга восстанавливать разрушенные клетки. Эритроциты гипохромные и похожи на мишень.
Малая альфа-талассемия
Малая альфа-талассемия – форма, при которой нарушен синтез 1 или 2 альфа-цепей. При такой форме отсутствуют тяжёлые клинические проявления. В крови может отмечаться лёгкая степень анемии (микроцитарная, гипохромная).
Несмотря на то, что нарушены 1 или 2 гена, отвечающих за синтез альфа-субъединиц, это не приводит к таким серьёзным нарушениям как, например, при бета-талассемии.
Прогноз заболевания
Гемотрансфузия массы эритроцитов совместно с медикаментозным лечением обеспечивают улучшение качества жизни пациента. Несмотря на это, подобная терапия полностью диагноз не устраняет, потому как обладает поддерживающим предназначением. Жизнь людей, пораженных тяжелым видом талассемии, обычно не превышает более 7 лет при условии регулярного прохождения процедур гемотрансфузии. Болезненное деформирование внутренних органов отличается прогрессированием, что приносит ребенку страдания.
Бета-талассемия
Бета-талассемия возникает при нарушении синтеза бета-субъединиц. Вследствие мутаций образуется гемоглобин, в котором бета-цепи замещаются на альфа. В эритроцитах образуются альфа-тетрамеры. Ретикулоэндотелиальная система удаляет их из красных кровяных клеток, они повреждаются, и происходит гемолиз.
В результате мутаций в гене бета-цепи различают большую и малую бета-талассемии.
Малая бета талассемия
Малая (минорная) бета-талассемия – гетерозиготная форма, характеризующаяся лёгким течением.
В лабораторных анализах:
- в норме или повышено количество сидеробластов;
- гипохромная микроцитарная анемия;
- анизоцитоз – разные эритроциты по размеру;
- пойкилоцитоз – эритроциты разной формы;
- повышено количество ретикулоцитов;
- железо в норме;
- повышенные уровни непрямого билирубина.
У больных малой формой бета-талассемии отмечается повышение уровня HbA2 (до 6%, норма до 3%) и HbF (до7%, в норме – менее 1%).
Малую форму бета-талассемии зачастую путают с железодефицитной анемией, ошибочно лечат препаратами железа. Для дифференциальной диагностики этих двух состояний необходимо проводить оценку уровня железа в крови. При бета-талассемии оно будет в пределах нормы.
Большая талассемия
Большая талассемия (анемия Кули) – гомозиготная, считается тяжёлой прогрессирующей формой бета-талассемии. Как и другие формы талассемии, она проявляется бледностью кожи, увеличением размеров селезёнки. Они возникают к 1 году ребёнка. Особенностью анемии Кули являются изменения костей: выступающие скулы, узкие глазные щели, квадратный череп, плоская переносица. У таких детей физическое развитие на низком уровне.
В лабораторных анализах отмечается:
- повышенное содержание сидеробластов;
- низкие показатели MCV, МСН, МСНС, свидетельствующие о гипохромной микроцитарной анемии;
- анизоцитоз;
- пойкилоцитоз – в виде мишени, шизоциты;
- базофильная пунктация эритроцитов;
- увеличение осмотической резистентности эритроцитов;
- увеличение неконъюгированного билирубина;
- избыточное содержание железа, вплоть до отложения его в органах (гемосидероз).
Для большой бета-талассемии характерно увеличение содержания в крови фетального (HbF) гемоглобина до 70%, что подтверждается при проведении электрофореза.
Сидеробласты – их ещё по-другому называют эритробластами. Они содержат в цитоплазме негемоглобиновое железо в виде гемосидерина и ферритина.
Немного истории
Болезнь была впервые описана в 1925 году американскими врачами-педиатрами, которые при лечении эмигрантов из Италии выявили одинаковую клиническую картину у детей с тяжелым малокровием, увеличением печени и селезенки, изменениями костей.
Затем появились работы, описывающие более легкое течение болезни у взрослых пациентов. Термин «талассемия» предложили в 1936 году. Дословно он означает «болезнь морского побережья». Высказана мысль о связи патогенеза заболевания с нарушением синтеза глобиновых цепочек.
Общие клинические признаки талассемии
- Гемолитическая анемия приведёт к бледности, вялости и иногда даже к пожелтению кожного покрова.
- Живот будет увеличен за счёт спленомегалии (увлечение селезёнки).
- При некоторых формах талассемии отмечаются костные деформации.
- У детей, больных талассемией наблюдается задержка физического развития, обусловленная нехваткой кислорода для роста и развития тканей.
- Из-за повышенного всасывания железа в кишечнике и частых переливаний крови наблюдается повышение этого элемента в крови, он откладывается в органах и тканях (например, сердце, печень), нарушая их работу.
Возможные осложнения и прогноз
При тяжелой форме патологии в тканях накапливается гемосидерин. У больных развивается цирроз печени, диабет. Гемосидероз миокарда приводит к гибели пациента.
При гемоглобинозе Н проводят удаление селезенки. Из-за того, что больные склонны к развитию инфекционных осложнений, им необходимо проходить вакцинацию против пневмококковых инфекций.
Прогноз большинства разновидностей гомозиготной талассемии неблагоприятный. Больные умирают в младенческом либо молодом возрасте. При тяжелых формах патологии продолжительность жизни больного зависит от своевременной терапии и предупреждения гемосидероза.
При гетерозиготной форме талассемии качество жизни пациентов не страдает. Трансплантация костного мозга улучшает прогноз.
Диагностика талассемии
При диагностике талассемии нельзя ориентироваться только на одну лишь клинику, тем более, что она не всегда может быть, например, при лёгких формах. Поэтому для точной диагностики необходимо «заглянуть» внутрь организма и оценить процессы, происходящие в нём. В этом помогут лабораторные исследования крови.
На анемию укажут низкий уровень гемоглобина и эритроцитов крови. При микроскопическом исследовании мазка крови будет замечена форма красных кровяных клеток и содержание гемоглобина в них. То есть подтвердится микроцитарный гипохромный характер анемии.
Электрофорез гемоглобина позволит оценить, как изменился его фракционный состав (соотношение HbA, HbA2, HbF между собой).
Ультразвуковое исследование позволит увидеть увеличение размера селезёнки.
Рентгеновское исследование используется для изучения костных деформаций.
Пункция костного мозга позволит оценить процессы кроветворения и сделать заключение о выраженности процессов.
Главным исследованием, которое может подтвердить наличие талассемии, является молекулярно-генетический анализ. Выявленная мутация гена альфа или бета-цепей свидетельствует о талассемии.
Биохимическое исследование крови позволит определить ряд показателей, которые могут повышаться при талассемии, например, непрямой билирубин. Оценка метаболизма железа в организме позволит провести дифференциальную диагностику между железодефицитной анемией и талассемией.
Перед тем как приступить к лечению, необходимо провести генетическое исследование, чтобы определить тип мутации и дальнейший прогноз развития заболевания.
Профилактические меры
Для будущих мам, находящихся в положении, проводится полная дородовая диагностика, обследования генетического характера
Профилактика бета-талассемии основана на предотвращении зачатия и появления на свет больных детей. Выполняется это несложно посредством простого исследования крови и процесса скрининга. Носителей заболевания предостерегают об угрозе связи с партнерами, пораженными таким же диагнозом.
Для снижения опасности рождения больного ребенка у пары с талассемией берется кровь на исследования различного рода. Для будущих мам, находящихся в положении, проводится полная дородовая диагностика, обследования генетического характера. Исследования ДНК и тесты ворсинок позволяют с начала беременности выявить гемоглобинопатию.
Чтобы оградить своих детей от любых заболеваний будущей мамочке необходимо всегда следить за своим здоровьем, а в случае наличия бета-талассемии, важное значение будет играть тщательный подход к выбору партнера.
На сегодняшний день заболевание считается неизлечимым. Новорожденный с легким типом бета-талассемии может прожить полноценную жизнь без серьезных последствий. Однако гарантировать непосредственно такую форму недуга современные ученые возможности не имеют. В особенности задуматься о деторождении нужно парам с гомозиготной наследственностью.
Лечение талассемии
Талассемия – наследственное заболевание, поэтому существует только симптоматическая терапия.
Лечение талассемии будет зависеть от формы. При лёгких формах терапия не проводится. При необходимости проводят переливание крови. Пациентам в бета-талассемией необходимо следить за уровнем железа в крови, в случае его избытка им должны быть назначены железо-связывающие лекарственные средства.
Пациентам с тяжёлыми формами назначается переливание крови в комбинации с препаратами, выводящими железо из организма. Гемоглобин поддерживают на уровне 100 г/л.
Дефероксамин относится к тем препаратам, который способен образовывать комплексы с железом и выводить его с мочой. Самостоятельно ничего не принимайте, все лекарственные средства только по назначению врача.
Если облегчение симптомов после переливания крови не наступает, может быть проведена операция по удалению селезёнки.
Профилактика
Так как заболевание талассемия является генетически обусловленным, то первичная профилактика включает в себя дородовую диагностику. Если оба родителя болеют талассемией, необходимо провести исследование плода. Иногда врач рекомендует прерывание беременности.
При обследовании беременных применяют фетоскопию, амниоцентез (под контролем ультразвука). В дальнейшем проводят генетическое обследование плода.
Родителям, которые имеют родственников, страдающих талассемией, нужно обратиться перед планированием беременности к генетику. В случае необходимости назначают генетическое обследование.
