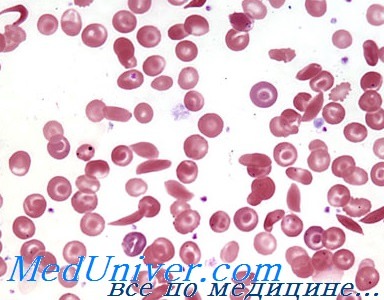
В крови при серповидноклеточной анемии
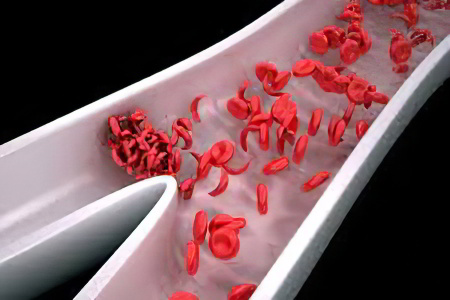
Серповидноклеточная анемия представляет собой болезнь системы кроветворения, которая передается по наследству. Патология характеризуется нарушением формирования цепей гемоглобина в эритроцитах.
По МКБ-10 серповидноклеточная анемия имеет код D57, а по МКБ-9 ей присвоен код 282.6.
Содержание:
- Серповидноклеточная анемия – что это?
- Причины развития серповидноклеточной анемии
- Механизм развития серповидноклеточной анемии
- Как проявляется серповидноклеточная анемия
- Как обнаружить серповидноклеточную анемию?
- Лечение серповидноклеточной анемии
- Профилактика и прогноз
Серповидноклеточная анемия – что это?
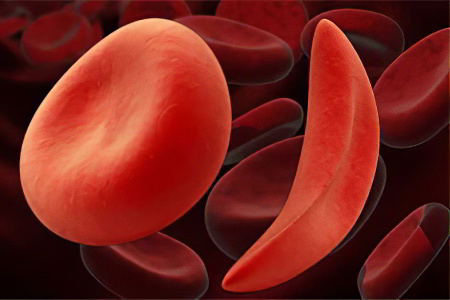
Серповидноклеточную анемию по праву считают сложнейшей формой болезни крови, передающейся по наследству. При этом вместо гемоглобина А в организме больного вырабатывается гемоглобин S.
Мутированный протеин имеет неправильное строение, что придает ему характеристики, которыми он обладать в норме не должен. Красные тельца крови, переносящие гемоглобин S изменяют свою форму двояковогнутого диска на форму серпа, удлиняясь в размерах. Такие эритроциты не отличаются особой устойчивостью и быстро разрушаются в сосудах.
Чаще всего патология встречается в Африке, страдают от не в равной степени как мужчины, так и женщины. Люди, с серповидноклеточной анемии (как с клиническими проявлениями болезни, так и со скрытым ее течением) не восприимчивы к малярии.
Причины развития серповидноклеточной анемии
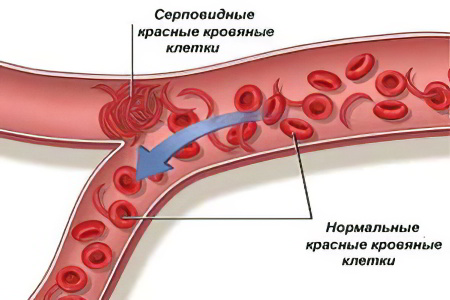
Причиной серповидноклеточной анемии является мутация в генах, которая передает по наследству. Страдает при этом ген НВВ, который отвечает за выработку гемоглобина. Как итог, в организме больного человека образуется протеин с неправильной позицией бета-цепи (глутаминовая кислота в этой цепочке замещается валином).
При этом гемоглобин продолжает вырабатываться, но его электрофизические свойства нарушаются. Если организм страдает от нехватки кислорода, то протеин изменяет свою структуру – он кристаллизуется и вытягивается в продолжительные цепи, то есть трансформируется в гемоглобин S (HbS). Эритроциты реагируют на такую деформацию изменением своей формы. Они тоже удлиняются, что приводит к истончению их стенки и разрушению.
Наследование серповидноклеточной анемии осуществляется по аутосомно-рецессивному типу. Чтобы патология дала о себе знать, измененный ген должен быть получен как от отца, так и от матери. Это так называемая гомозиготная форма, при которой в крови человека будут присутствовать молекулы гемоглобина S и никакие другие.
Если мутированный ген имеется только у одного из родителей, то наследование патологии тоже случится, но форма полиморфизма будет гетерозиготной. При этом сам ребенок страдать от анемии не будет, но станет бессимптомным носителем патологического гена. В его крови будет циркулировать гемоглобин А и гемоглобин S в разных пропорциях. Если человек здоров, то анемия никак себя не проявляет, так как гемоглобина А оказывается достаточно, чтобы перекрыть все нужды организма. При выраженном обезвоживании или при гипоксии анемия даст о себе знать. Человек, являющийся бессимптомным носителем мутированного гена НВВ, может передавать его своим детям по наследству.
Механизм развития серповидноклеточной анемии
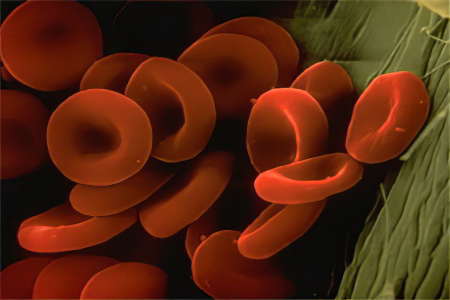
Эритроциты при серповидноклеточной анемии перестают выполнять свои функции. Их стенки становятся тонкими и хрупкими. Кроме того, красные кровяные тельца, переносящие гемоглобин S, не в состоянии транспортировать необходимое количество кислорода. Сами они не могут менять форму и проникать в мельчайшие капилляры.
Все эти патологические изменения в структуре эритроцитов и гемоглобина приводят к развитию следующих нарушений:
Продолжительность жизни эритроцитов сокращается. Они быстро и массово погибают в селезенке.
Видоизмененные эритроцит выпадают в осадок и скапливаются в капиллярах, перекрывая их просветы.
Дефицит эритроцитов приводит к их усиленному формированию в почках, а сам эритроцитарный росток костного мозга перерождается.
Как проявляется серповидноклеточная анемия

У человека симптомы серповидноклеточной анемии будут тем ярче выражены, чем слабее здоровье. Также на клинических проявлениях анемии сказывается возраст пациента, условия его жизни и наличие сопутствующих заболеваний. Принято различать несколько групп симптомов, среди которых:
Симптомы анемии, обусловленные ускоренным разрушением эритроцитов.
Симптомы анемии, обусловленные перекрытыми просветами сосудов.
Симптомы анемии, спровоцированные гемолитическим кризом.
Заболевание не дает о себе знать у детей младше 3 месяцев. Иногда впервые оно манифестирует в возрасте 6 месяцев.
Симптомы могут быть следующими:
Отеки в области кистей рук и в области стоп, их болезненность.
Слабость мышечного аппарата.
Изменение формы конечностей.
Отставание в физическом развитии в плане формирования моторики.
Сухость кожи, ее бледность.
При массивном разрушении эритроцитов кожные покровы становятся желтого цвета, что происходит из-за выделения билирубина из разрушенных эритроцитов в кровь.
Пока ребенок не достигнет возраста 5-6 лет, любые инфекции могут иметь у него тяжелое течение, что связано с патологическими изменениями в селезенки. Ее просветы закупориваются разрушенными эритроцитами, и орган не в состоянии нормально функционировать. Именно селезенка в организме человека призвана очищать кровь от инфекционных агентов, также в ней формируются лимфоциты. Поэтому практически любая инфекция может привести к развитию сепсиса. В этом плане родители должны проявлять особенную настороженность и при любых заболеваниях обращаться за врачебной помощью.
Чем старше становится ребенок, тем большую интенсивность у него набирают симптомы, обусловленные хроническим кислородным голоданием, среди которых:
Ребенок быстро устает.
У него регулярно кружится голова.
Появляется одышка.
Физическое, умственное и половое развитие задерживается.
Женщины с диагностированной серповидноклеточной анемией могут рожать детей, но беременность сопряжена с рядом осложнений.
Симптомы серповидноклеточной анемии у подростков и у взрослых пациентов:
Время от времени возникают болезненные ощущения в разных органах.
На коже часто образуются язвы.
Ухудшается зрение.
Может развиваться почечная недостаточность.
Структура костей изменяется.
Суставы начинают болеть, сильно отекают.
Чувствительность конечностей ухудшается, беспокоят парезы.
Гемолитический криз является опасным состоянием для человека. При серповидноклеточной анемии его могут спровоцировать обезвоживание, сильное переохлаждение организма, чрезмерные физические нагрузки, горная болезнь.
На развивающийся криз указывают следующие симптомы:
Снижение уровня гемоглобина до критических отметок.
Обморочные состояния.
Высокая температура тела.
Моча становится темного цвета.
Как обнаружить серповидноклеточную анемию?
Диагностика серповидноклеточной анемии начинается с опроса жалоб больного и сбора анамнеза. Симптомы, которые дает заболевание, характерны для многих патологий, поэтому требуется проведение лабораторных исследований.
К основным методам диагностики относят:
Забор крови на клинический анализ. При этом будет обнаружено снижение уровня эритроцитов и гемоглобина в крови до отметок менее 3,5-4,0*1012/л и 120 г/л, соответственно.
Биохимическое исследование крови позволяет диагностировать повышение уровня билирубина и свободного железа в крови.
К дополнительным диагностическим процедурам относят:
Выполнение исследования крови с применением метабисульфита натрия. При взаимодействии с этим веществом эритроциты высвобождают кислород, после чего можно визуализировать их серповидную форму.
Обработка крови буферными составами. В них HbS плохо растворяется.
Выполнение электрофореза гемоглобина, что дает возможность визуализировать видоизмененные эритроциты. Также этот метод позволяет отличить гетерозиготную мутацию от гомозиготной.
Иные методики обследования, которые могут потребоваться:
Ультразвуковое обследование печени и селезенки, а также прочих внутренних органов на предмет обнаружения в них патологических изменений.
Выполнение рентгена костей скелета и позвоночника.
Лечение серповидноклеточной анемии
Лечение серповидноклеточной анемии предполагает воздействие на симптомы болезни, а также призвано не допустить развития осложнений.
Поэтому при проведении терапии нужно ориентироваться на следующие принципы:
Восполнить нехватку эритроцитов и гемоглобина.
Снять болезненные ощущения.
Устранить из организма лишнее железо.
Устранить последствия гемолитического криза.
Чтобы привести в норму уровень эритроцитов и гемоглобина может потребоваться переливание эритроцитарной массы. Как вариант, пациенту вводят цитостатики (гидроксимочевина), которые позволяют повысить уровень гемоглобина в крови.
Чтобы снять болезненные ощущения у пациента, ему назначают анальгезирующие препараты (Морфин, Трамадол, Промедол). Когда заболевание протекает остро, необходимо вводить препараты внутривенно. После снятия обострения их применяют перорально.
Вывести лишнее железо из организма можно с помощью использования некоторых лекарственных препаратов, например, с помощью Дефероксамина.
При гемолитическом кризе пациенту показана кислородотерапия, адекватное восполнение запасов жидкости, анальгетиков, препаратов для купирования судорог и пр.
При проникновении в организм инфекции, больному назначают антибиотики, которые позволяют предупредить сепсис. Это могут быть такие препараты, как Цефуроксим, Амоксициллин, Эритромицин.
Обязательно все пациенты с серповидноклеточной анемией должны придерживаться следующих врачебных рекомендаций:
Вести здоровый образ жизни и полностью отказаться от вредных привычек.
Исключить подъемы на высоту.
Исключить чрезмерные физические нагрузки.
Пить достаточное количество воды.
Не допускать перегрева и переохлаждения.
Питаться здоровыми продуктами.
Профилактика и прогноз

Полностью вылечить серповидноклеточную анемию невозможно. Однако если пациент придерживается всех врачебных рекомендаций, то он может дожить до 50 лет и более.
К осложнениям анемии, которые могут спровоцировать гибель больного, относят:
Бактериальные инфекции, которые могут протекать очень тяжело.
Сепсис.
Инсульт.
Мозговое кровоизлияние.
Нарушения в функционировании мочевыделительной, сердечно-сосудистой и гепатобилиарной системы.
Что касается профилактических мероприятий, то они отсутствуют. Это заболевание развивается вследствие генетических мутаций, предупреждать которые наука пока не в состоянии. Если у конкретного человека в семье имелись случаи серповидноклеточной анемии, то прежде чем приступать к планированию беременности, следует получить консультацию генетика. Врач обследует мужчину и женщину и определит вероятность появления у них ребенка с серповидноклеточной анемией.

Автор статьи: Шутов Максим Евгеньевич | Гематолог
Образование:
В 2013 году закончен Курский государственный медицинский университет и получен диплом «Лечебное дело». Спустя 2 года окончена ординатура по специальности «Онкология». В 2016 году пройдена аспирантура в Национальном медико-хирургическом центре имени Н. И. Пирогова.
Наши авторы
Серповидноклеточная анемия: причины, диагностика, лечениеЭтиология и встречаемость серповидноклеточной анемии. Серповидноклеточная анемия (MIM № 603903) — аутосомно-рецессивное заболевание гемоглобина, вызванное миссенс-мутацией гена бета-субъединицы, заменяющей валин на глутаминовую кислоту в 6 положении. Болезнь чаще вызвана гомозиготностью по мутации серповидноклеточности, хотя серповидноклеточную анемию также может вызывать компаундная (составная) гетерозиготность по аллелю серповидноклеточности и аллелям HbC или бета-талассемии. Распространение серповидноклеточной анемии широко изменяется среди популяций в соответствии с прошлым и настоящим распространением малярии. Мутация серповидноклеточности, как оказалось, несколько повышает сопротивляемость малярии, таким образом, давая преимущество выживания гетерозиготным носителям мутации. Патогенез серповидноклеточной анемииГемоглобин формируется из четырех субъединиц: двух а-субъединиц, кодируемых геном ЯВА в хромосоме 16, и двух бета-субъединиц, кодируемых геном ЯВВ в хромосоме 11. Мутация Glu6Val в бета-субъединице уменьшает растворимость ненасыщенного кислородом гемоглобина и вызывает формирование сети жестких волокнистых полимеров, искажающих строение эритроцита, придавая ему форму серпа. Серповидные эритроциты закупоривают капилляры и вызывают инфаркты. Первоначально обогащение кислородом заставляет полимер гемоглобина растворяться, и эритроциты восстанавливают нормальную форму; тем не менее, регулярное нарушение формы приводит к необратимому переходу клеток в серповидную форму, впоследствии такие эритроциты удаляются из кровотока в селезенке. Скорость удаления эритроцитов из кровотока превышает возможность их синтеза в костном мозге, что приводит к гемолитической анемии. Аллельная гетерогенность часто встречается при большинстве менделирующих заболеваний, особенно когда мутантные аллели вызывают снижение функции. Серповидноклеточная анемия — важное исключение из этого правила, поскольку в данном случае единственная специфическая мутация ответственна за уникальные новые свойства HbS. HbC тоже менее растворим, чем HbA, и тоже стремится кристаллизоваться в эритроцитах, уменьшая их деформируемость в капиллярах и вызывая легкий гемолиз, но HbC не формирует полимерные волокна, как HbS. Неудивительно, что другие мутации с новыми функциями, например, мутации в гене FGFR3, вызывающие ахондроплазию, часто имеют аналогичное снижение аллельной гетерогенности, когда фенотип зависит от специфического, уникального изменения функции белка.
Фенотип и развитие серповидноклеточной анемииКлиническая картина у больных серповидноклеточной анемией обычно проявляется в течение первых двух лет жизни анемией, задержкой развития, спленомегалией, регулярными инфекциями и дактилитами (болезненными припухлостями кистей или стоп, вызванными закупоркой капилляров в небольших костях, обнаруженных у приведенной в примере пациентки). Инфаркты вследствие закупорки сосудов происходят во многих тканях, вызывая инсульты мозга, острый кардиальный синдром, почечный папиллярный некроз, инфаркты селезенки, язвы ног, приапизм, асептический некроз костей и снижение зрения. Окклюзия сосудов костей вызывает приступы болей, при отсутствии лечения эти болезненные эпизоды могут продолжаться в течение нескольких дней и даже недель. Функциональная аспления вследствие инфарктов и других недостаточно ясных факторов, предрасполагает к бактериальным инфекциям, например, пневомококковому или сальмонеллезному сепсису и остеомиелиту. Инфекция — основная причина смерти во всех возрастных группах, хотя прогрессирующая почечная и дыхательная недостаточность также нередкие причины смерти на четвертом и пятом десятилетиях жизни. Пациенты также имеют высокий риск развития угрожающей жизни апластической анемии после парвовирусной инфекции, поскольку парвовирусы вызывают временное прекращение образования эритроцитов. Гетерозиготные носители мутации («признака» серповидноклеточности) не имеют анемии и обычно клинически здоровы. Однако в условиях серьезной гипоксии, например, при восхождении в горы, эритроциты пациентов с «признаком» серповидноклеточности могут принимать форму серпа, вызывая симптомы, подобные наблюдаемым при серповидноклеточной анемии. Особенности фенотипических проявлений серповидноклеточной анемии: Лечение серповидноклеточной анемииКонкретному больному серповидноклеточной анемией дать точный прогноз тяжести течения болезни невозможно. Хотя молекулярная основа болезни стала известной раньше других моногенных заболеваний, лечение остается только симптоматическим. Никакой специфический терапии, предохраняющей от процесса образования серповидных эритроцитов, не найдено. Существенно снижает тяжесть болезни персистенция HbE Исследуется несколько фармакологических препаратов, нацеленных на увеличение концентрации HbF, в этих целях одобрено использование гидрокси-мочевины. Хотя генотерапия имеет шанс улучшить или излечить эту болезнь, эффективная пересадка гена b-глобина не достигнута. Пересадка костного мозга остается единственным доступным в настоящее время лечением, способным помочь при серповидноклеточной анемии. Из-за 11% смертности, вызванной сепсисом в первые 6 мес жизни, большинство штатов в США проводит неонатальный скрининг на серповидноклеточную анемию с целью проведения профилактики антибиотиками, продолжающейся до 5-летнего возраста. Риски наследования серповидноклеточной анемииПоскольку серповидноклеточная анемия — аутосомно-рецессивное заболевание, будущие сибсы больного ребенка имеют 25% риск серповидноклеточной анемии и 50% риск носительства серповидноклеточности. Используя ДНК плода, полученную при БВХ или амниоцентезе, можно провести пренатальную диагностику обнаружением мутации. Пример серповидноклеточной анемии. Второй раз за полгода семейная пара карибского происхождения обратилась со своей 24-месячной дочерью в отделение неотложной помощи, поскольку девочка не может стоять. В анамнезе отсутствуют повышение температуры, инфекция или травма, и в остальном медицинская история ничем не примечательна; данные предыдущих осмотров соответствовали норме, за исключением низкого уровня гемоглобина и слегка увеличенной селезенки. При текущем осмотре патологии не найдено, за исключением пальпируемого края селезенки и отека стоп. Стопы болезненны при пальпации, и девочка не хотела вставать на ноги. Оба родителя имели сибсов, умерших в детстве от инфекций, и других сибсов, вероятно, имевших серповидноклеточную анемию. С учетом анамнеза и повторного болезненного увеличения стоп врач проверил ребенка на наличие серповидноклеточной анемии методом электрофореза гемоглобина. Результат этого теста подтвердил наличие HbS. – Также рекомендуем “Болезнь Тея-Сакса: причины, диагностика, лечение” Оглавление темы “Врожденные болезни”:
|