Внутрисосудистый гемолиз при анемии
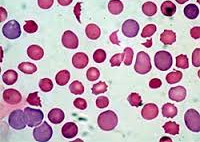
Гемолиз – разрушение клеток естественного гемопоэза вследствие физиологических и патологических причин. Термин происходит от греческих слов haima – кровь и lysis – расщепление. Острый и хронический внутрисосудистый гемолиз сопровождается тяжёлым течением и высоким процентом летальности, поэтому изучение его патогенетических механизмов и клинических особенностей представляет большой интерес для здравоохранения.
О причинах, механизмах развития, симптоматике, принципах диагностики и лечения этого заболевания – в нашем обзоре и видео в этой статье.

Проблема встречается как в норме, так и при патологии
Жизненный цикл клеток крови
Эритроциты – один из ключевых элементов кроветворения. Эти небольшие двояковогнутые клетки содержат вещество гемоглобин, которое способно присоединять молекулы кислорода и переносить их по всему организму. Таким образом, эритроциты участвуют в газообмене и необходимы для нормального функционирования организма.

Главная функция эритроцитов – перенос кислорода в организме
В организме здорового человека постоянно происходит замена отслуживших, «старых» эритроцитов новыми. В норме клетки крови живут в среднем 3,5-4 месяца. Затем эритроциты подвергаются физиологическому гемолизу – разрушению клетки с разрывом ее оболочки и выходом гемоглобина наружу.
Виды патологии
Существует несколько патогенетических механизмов развития гемолиза:
- естественный – происходит в организме непрерывно;
- осмотический – развивается в гипертонической среде;
- температурный – возникает при резком изменении температуры крови (например, замораживании);
- биологический – вызван действием токсинов бактерий и вирусов, насекомых, а также при переливании крови несовместимой группы;
- механический – происходит при сильном прямом повреждающем действии на клетки крови.
В зависимости от того, где произошло разрушение эритроцитов, гемолиз бывает:
- внутриклеточным;
- внутрисосудистым.
Внутриклеточная форма происходит в цитоплазме клеток системы макрофагов, то есть в селезёнке, печени, костном мозге. Относится к физиологическим процессам, однако может встречаться и при некоторых заболеваниях – талассемии, наследственном микросфероцитозе.

Медики часто называют селезенку (на фото – фиолетового цвета) «кладбищем» эритроцитов
Обратите внимание! Одним из главных специфических признаков патологического внутриклеточного гемолиза является увеличение печени и селезенки (гепатоспленомегалия).
Внутрисосудистый вид гемолиза считается патологическим. При нем эритроциты разрушаются непосредственно в кровеносном русле. Он развивается при отравлении некоторыми ядами, гемолитической анемии и др.
Таблица: Внутрисосудистый и внутриклеточный гемолиз: характерные отличия:
| Признаки | Внутриклеточный | Внутрисосудистый |
| Преимущественная локализация | Ретикулоэндотелиальная сеть клеток | Артериальная и капиллярная сеть |
| Патогенетический фактор | Различные аномалии формы клеток | Действие гемолитических веществ, ферментов |
| Увеличение печени и селезенки | Выражено | Незначительное |
| Изменения со стороны красных кровяных телец |
| Анизоцитоз – отклонение размеров эритроцитов от нормальных величин, как в большую, так и в меньшую сторону |
| Преимущественная локализация гемосидероза – чрезмерного отложения пигмента гемосидерина | Костный мозг, печень, селезенка | Почки |
| Данные лабораторного обследования |
|
|
Почему развивается патология
Причины развития гемолиза внутри сосудистого русла разнообразны. Среди них выделяют:
- токсины бактерий (брюшного тифа, стрептококков);
- вирусы;
- некоторые паразитарные частицы (например, малярийного плазмодия);
- токсические вещества (уксусная кислота, свинец, мышьяк, бензин);
- биологические яды (гадюки, тарантула, пчел);
- некоторые лекарственные средства (сульфаниламиды, феницитин);
- реакция организма в ответ на аутоиммунные процессы;
- грубое механическое воздействие на эритроциты у пациентов с искусственным кровообращением или сердечным клапаном;
- гемотрансфузиологическая реакция;
- резус-конфликт между беременной женщиной и плодом;
- гемолитическая желтуха детей первого месяца жизни.
Важно! Любой из указанных выше факторов лежит в основе приобретенных гемолитических анемий.
Гемолиз in vitro
В некоторых случаях гемолиз эритроцитов возможен вне человеческого организма, например, в лаборатории после забора крови у пациента. В результате разрушения красных кровяных телец анализ будет недостоверным, и его придется пересдавать.
Среди основных причин такого феномена в этом случае могут стать:
- неправильный забор крови;
- загрязнение пробирки;
- нарушение хранения биоматериала;
- замораживание образцов крови;
- сильное встряхивание пробирок.

Иногда медики вынуждены признать, что анализ «не получился»
Чтобы минимизировать возможность гемолиза in vitro, медработникам следует соблюдать правила забора, транспортировки и хранения образцов крови. Простая инструкция для медсестер процедурного кабинета поможет обеспечить высокую результативность лабораторных тестов.
Клинико-лабораторные показатели при разрушении эритроцитов
В зависимости от процентного соотношения разрушившихся эритроцитов меняется степень тяжести заболевания.
Симптоматика при гемолизе может быть:
- Лёгкой степени тяжести: слабость, утомляемость, озноб, приступы тошноты по утрам. Возможно окрашивание склер в желтоватый оттенок.
- Тяжёлой степени: нарастающие слабость, сонливость, головные боли. Возможна частая рвота, боли в эпигастральной области, правом подреберье. Иногда первым проявлением болезни становится гемоглобинурия – окрашивание мочи в насыщенный красный цвет. Чуть позже у больного развивается повышение температуры тела до 38-39 °С, развивается увеличение печени и грубые нарушения ее функциональной активности. Спустя несколько дней основным симптомом заболевания становится гемолитическая желтуха – окрашивание кожи и слизистых оболочек в ярко-желтый цвет с лимонным оттенком.

Ребенок с гемолитической желтухой
Обратите внимание! Даже для массивного гемолиза характерен 6-8-часовой латентный период, не имеющий клинической симптоматики.
Принципы лечения
Вне зависимости от причин, вызвавших внутрисосудистое разрушение эритроцитов, принципы лечения патологии схожи.
Врачебная инструкция по ведению пациентов включает:
- Ликвидация фактора, вызывающего гибель красных кровяных телец.
- Дезинтоксикационные мероприятия (форсированный диурез, промывание желудка, очищение кишечника, гемодиализ и др.).
- Коррекция жизненных показателей и терапия острых осложнений.
- При развитии печеночной, почечной недостаточности – их лечение.
- Симптоматическая терапия.

Лечение тяжелых форм патологии проводится в условиях стационара
Наследственные гемолитические анемии плохо поддаются лечению. Пациенты находятся на пожизненном диспансерном учёте, их наблюдает врач гематолог. Основными методами терапии остаются переливание крови, стимуляция эритропоэза и своевременное устранение возникших осложнений.
Острый гемолиз – угрожающее состояние, имеющие крайне негативные последствия для для здоровья и жизни. При его формировании важно обратиться за медицинской помощью как можно раньше, ведь цена промедления может быть слишком высока. Понимание механизмов развития и знание клинических особенностей внутрисосудистого разрушения клеток позволит вовремя распознать патологию и начать интенсивную терапию как можно раньше.
Источник
При наличии гемолиза деструкция происходит преждевременно, что обусловливает снижение периода жизни эритроцитов (<120 дней).
Анемия развивается, когда синтез эритроцитов в костном мозге больше не может обеспечить длительную компенсацию укорочения продолжительности их жизни; это состояние называется гемолитической анемией.
Причины гемолитических анемий
Гемолиз может быть обусловлен как аномалиями эритроцитов, так и внешним воздействием на них.
Внешние причины
Большинство внешних причин гемолиза имеют приобретенный характер; эритроциты пациента имеют нормальное строение, об этом свидетельствует разрушение в кровотоке как аутологичных клеток, так и клеток донора. К внешним причинам относятся ретикулоэндотелиальная гиперактивность (гиперспленизм), иммунологические отклонения, механическое повреждение (травматическая гемолитическая анемия), некоторые инфекции. Инфекционные агенты могут вызывать развитие гемолитической анемии путем прямого токсического воздействия, инвазии и деструкции эритроцитов (плазмодии, бартонеллы).
Внутренние причины
Внутренними причинами гемолиза являются нарушения одного или более компонентов или функций эритроцитов: структуры мембран, клеточного метаболизма, строения гемоглобина. К ним относятся наследственные или приобретенные дефекты клеточных мембран (к примеру, сфероцитоз), нарушения эритроцитарного метаболизма (недостаточность глюкозо-6-фосфатдегидрогена-зы), гемоглобинопатии.
Патофизиология гемолитических анемий
Гемолиз может иметь острый, хронический или эпизодический характер. Хронический гемолиз может осложняться апластическим кризом (временное прекращение эритропоэза), обычно он обусловлен инфекциями, чаще парвовирусными. Гемолиз может быть внесосудистым, внутрисосудистым или комбинированным.
Нормальный процессинг эритроцитов
Стареющие эритроциты утрачивают мембрану и элиминируются из кровотока. Разрушение гемоглобина в этих клетках обусловлено в первую очередь наличием гемоксигеназной активности. Железо сохраняется и реутилизируется, а гем разрушается с образованием билирубина, который в печени конъюгируется с глюкуроновой кислотой и выводится с желчью.
Внесосудистый гемолиз
В большинстве случаев гемолиз является внесосудистым, он наблюдается при повреждении аномальных эритроцитов и удалении их из кровотока при участии клеток селезенки, печени, костного мозга. Сходный процесс также происходит при элиминации старых эритроцитов. Гемолиз, происходящий в селезенке, как правило, обусловлен незначительными аномалиями строения эритроцитов или наличием тепловых антител на поверхности клеток. При увеличении селезенки может наблюдаться разрушение даже нормальных эритроцитов. Эритроциты с выраженными аномалиями строения либо имеющие холодовые антитела и фракции комплемента на своей поверхности разрушаются непосредственно в кровотоке либо в печени, где возможно эффективное удаление поврежденных клеток в связи с хорошим кровоснабжением.
Внутрисосудистый гемолиз
Внутрисосудистый гемолиз является существенной причиной преждевременного разрушения эритроцитов и обычно наблюдается при тяжелых повреждениях клеточных мембран различной этиологии. Данный тип гемолиза может быть обусловлен в т.ч. аутоиммунной реакцией, прямой травмой (маршевая гемоглобинурия), гемодинамическим ударом (при наличии дефектов искусственных клапанов сердца), воздействием токсинов (клостридиальная интоксикация, укус змеи).
Внутрисосудистый гемолиз приводит к развитию гемоглобинемии в тех случаях, когда количество высвобождаемого гемоглобина превышает гемоглобинсвязывающую способность белка гаптоглобина. При наличии гемоглобинемии свободные димеры гемоглобина фильтруются в мочу и реабсорбируются в клетках почечных канальцев; когда способность к реабсорбции превышена, возникает гемоглобинурия. В канальцевых клетках железо включается в синтез гемосидерина; часть железа используется для реутилизации, остальное количество попадает в мочу в связи с перегрузкой канальцевых клеток.
Последствия гемолиза
Когда конверсия гемоглобина в билирубин превышает конъюгационную и экскреторную способность печени, развивается неконъюгированная билирубинемия и желтуха. Вследствие катаболизма билирубина повышается содержание стеркобилина в кале, уробилиногена в моче, иногда возникает холелитиаз.
Костный мозг отвечает на снижение количества эритроцитов усилением их продукции и высвобождения, что приводит к ретикулоцитозу.
Симптомы и признаки гемолитических анемий
Системные проявления аналогичны другим анемиям и включают следующие симптомы: бледность, утомляемость, головокружение, возможна гипотензия. Гемолитический криз (острый, тяжелый гемолиз) встречается редко. При тяжелом гемолизе возникают желтуха и спленомегалия. При гемоглобинурии моча приобретает красную или красновато-коричневую окраску.
Диагностика
- Мазок периферической крови, количество ретикулоцитов, сывороточный билирубин, ЛДГ, АлАТ.
- Иногда проводится измерение содержания гемосидерина в моче, гаптоглобина в сыворотке крови.
- Реже проводится измерение времени жизни эритроцитов с помощью радиоизотопных методов.
Гемолиз необходимо подозревать у пациентов с анемией и ретикулоцитозом. При подозрении на данную патологию выполняется мазок периферической крови, определяется уровень билирубина, ЛДГ и АлАТ в сыворотке крови. Если эти методы не дают результата, необходимо исследование содержания гемосидерина в моче и гаптоглобина в сыворотке крови.
Морфологические аномалии эритроцитов реже являются диагностическими критериями, однако они часто свидетельствуют о причине гемолиза. К данным, позволяющим предполагать гемолитическую анемию, относятся повышение уровня ЛДГ и непрямого билирубина в сыворотке крови при нормальном значении АлАТ, наличие уробилиногена в моче. Наличие внутрисо-судистого гемолиза также можно предполагать по результатам исследования содержания гемосидерина в моче. Гемоглобинурия, так же как гематурия и миоглобинурия, характеризуется положительным бензидиновым тестом (по экспресс-полоске); дифференциальная диагностика гемолиза и гематурии может быть основана на отсутствии эритроцитов при микроскопическом исследовании мочи. Кроме того, свободный гемоглобин придает плазме красновато-коричневый цвет, что часто может быть заметно при центрифугировании крови; миоглобин данным свойством не обладает.
Хотя наличие гемолиза, как правило, может быть установлено по этим простым критериям, окончательный диагноз основан на определении срока жизни эритроцитов путем проведения радиоизотопного исследования (к примеру, с радиоактивным хромом 51Сr). Путем измерения продолжительности жизни меченых эритроцитов можно установить факт гемолиза, а также идентифицировать место их разрушения с помощью расчета площади поверхности тела. Тем не менее данный метод применяется редко.
После подтверждения наличия гемолиза необходимо выявить его специфическую причину. Применяются следующие методы сужения дифференциального диагноза гемолитических анемий: учет факторов риска (географический регион, наследственность, сопутствующие заболевания), выявление спленомегалии, выполнение прямого антиглобулинового теста и мазка периферической крови; в большинстве случаев будут наблюдаться отклонения как минимум одного из данных показателей, что определит тактику дальнейшего исследования (для установления причины гемолиза), которое может включать следующие лабораторные методы:
- количественный электрофорез гемоглобина;
- анализ ферментов эритроцитов;
- флоуцитометрия;
- выявление холодовых агглютининов;
- осмотическая резистентность.
Хотя существуют методы, позволяющие отличить внутрисосудистый гемолиз от внесосудистого, иногда их достаточно тяжело разграничить. При разрушении эритроцитов обычно вовлечены оба механизма, хотя и в различной степени.
Лечение гемолитических анемий
На начальных этапах лечения аутоиммунного гемолиза, обусловленного наличием тепловых антител, эффективны кортикостероиды. Многократные гемотрансфузии могут вызывать избыточную аккумуляцию железа в организме, что требует применения хелатной терапии. 8 некоторых ситуациях необходимо выполнение спленэктомии. По возможности спленэктомия выполняется через 2 недели после иммунизации вакцинами против пневмококка, гемофильной палочки и менингококка. При болезни холодовых антител пациенту рекомендуется находиться в тепле. При длительно существующем гемолизе необходима заместительная терапия фолиевой кислотой.
Источник

Гемолитическая анемия – патология эритроцитов, отличительным признаком которой является ускоренное разрушение красных кровяных телец с высвобождением повышенного количества непрямого билирубина. Для данной группы заболеваний типично сочетание анемического синдрома, желтухи и увеличения размеров селезенки. В процессе диагностики исследуется общий анализ крови, уровень билирубина, анализ кала и мочи, УЗИ органов брюшной полости; проводится биопсия костного мозга, иммунологические исследования. В качестве методов лечения используется медикаментозная, гемотрансфузионная терапия; при гиперспленизме показана спленэктомия.
Общие сведения
Гемолитическая анемия (ГА) – малокровие, обусловленное нарушением жизненного цикла эритроцитов, а именно преобладанием процессов их разрушения (эритроцитолиза) над образованием и созреванием (эритропоэзом). Данная группа анемий очень обширна. Их распространенность неодинакова в различных географических широтах и возрастных когортах; в среднем патология встречается у 1% населения. Среди прочих видов анемий на долю гемолитических приходится 11%. Патология характеризуется укорочением жизненного цикла эритроцитов и их распадом (гемолизом) раньше времени (через 14-21 день вместо 100-120 суток в норме). При этом разрушение эритроцитов может происходить непосредственно в сосудистом русле (внутрисосудистый гемолиз) или в селезенке, печени, костном мозге (внесосудистый гемолиз).

Гемолитическая анемия
Причины
Этиопатогенетическую основу наследственных гемолитических синдромов составляют генетические дефекты мембран эритроцитов, их ферментных систем либо структуры гемоглобина. Данные предпосылки обусловливают морфофункциональную неполноценность эритроцитов и их повышенное разрушение. Гемолиз эритроцитов при приобретенных анемиях наступает под влиянием внутренних факторов или факторов окружающей среды, среди которых:
- Аутоиммунные процессы. Образование антител, агглютинирующих эритроциты, возможно при гемобластозах (остром лейкозе, хроническом лимфолейкозе, лимфогранулематозе), аутоиммунной патологии (СКВ, неспецифическом язвенном колите), инфекционных заболеваниях (инфекционном мононуклеозе, токсоплазмозе, сифилисе, вирусной пневмонии). Развитию иммунных гемолитических анемий могут способствовать посттрансфузионные реакции, профилактическая вакцинация, гемолитическая болезнь плода.
- Токсическое действие на эритроциты. В ряде случаев острому внутрисосудистому гемолизу предшествует отравление мышьяковистыми соединениями, тяжелыми металлами, уксусной кислотой, грибными ядами, алкоголем и др. Вызывать разрушение клеток крови может прием определенных лекарств (противомалярийных препаратов, сульфаниламидов, производных нитрофуранового ряда, анальгетиков).
- Механическое повреждение эритроцитов. Гемолиз эритроцитов может наблюдаться при тяжелых физических нагрузках (длительной ходьбе, беге, лыжном переходе), при ДВС-синдроме, малярии, злокачественной артериальной гипертензии, протезировании клапанов сердца и сосудов, проведении гипербарической оксигенации, сепсисе, обширных ожогах. В этих случаях под действием тех или иных факторов происходит травматизация и разрыв мембран изначально полноценных эритроцитов.

Гемолитическая анемия
Патогенез
Центральным звеном патогенеза ГА является повышенное разрушение эритроцитов в органах ретикулоэндотелиальной системы (селезенке, печени, костном мозге, лимфатических узлах) или непосредственно в сосудистом русле. При аутоиммунном механизме анемии происходит образование антиэритроцитарных АТ (тепловых, холодовых), которые вызывают ферментативный лизис мембраны эритроцитов. Токсические вещества, являясь сильнейшими окислителями, разрушают эритроцит за счет развития метаболических, функциональных и морфологических изменений оболочки и стромы красных кровяных телец. Механические факторы оказывают прямое воздействие на клеточную мембрану. Под влиянием этих механизмов из эритроцитов выходят ионы калия и фосфора, а внутрь поступают ионы натрия. Клетка разбухает, при критическом увеличении ее объема наступает гемолиз. Распад эритроцитов сопровождаются развитием анемического и желтушного синдромов (так называемой «бледной желтухой»). Возможно интенсивное окрашивание кала и мочи, увеличение селезенки и печени.
Классификация
В гематологии гемолитические анемии подразделяются на две большие группы: врожденные (наследственные) и приобретенные. Наследственные ГА включают следующие формы:
- эритроцитарные мембранопатии (микросфероцитоз – болезнь Минковского-Шоффара, овалоцитоз, акантоцитоз) – анемии, обусловлены структурными аномалиями мембран эритроцитов
- ферментопении (энзимопении) – анемии, вызванные дефицитом тех или иных ферментов (глюкозо-6-фосфатдегидрогеназы, пируваткиназы и др.)
- гемоглобинопатии – анемии, связанные с качественными нарушениями структуры гемоглобина или изменением соотношения его нормальных форм (талассемия, серповидно-клеточная анемия).
Приобретенные ГА подразделяются на:
- мембранопатии приобретенные (пароксизмальная ночная гемоглобинурия – б-нь Маркиафавы-Микели, шпороклеточная анемия)
- иммунные (ауто- и изоиммунные) – обусловлены воздействием антител
- токсические – анемии, обусловленные воздействием химических веществ, биологических ядов, бактериальных токсинов
- механические – анемии, вызванные механическим повреждением структуры эритроцитов (тромбоцитопеническая пурпура, маршевая гемоглобинурия)
Симптомы
Наследственные мембранопатии, ферментопении и гемоглобинопатии
Наиболее распространенной формой данной группы анемий является микросфероцитоз, или болезнь Минковского-Шоффара. Наследуется по аутосомно-доминантному типу; обычно прослеживается у нескольких представителей семьи. Дефектность эритроцитов обусловлена дефицитом в мембране актомиозиноподобного белка и липидов, что приводит к изменению формы и диаметра эритроцитов, их массивному и преждевременному гемолизу в селезенке. Манифестация микросфероцитарной ГА возможна в любом возрасте (в младенчестве, юношестве, старости), однако обычно проявления возникают у детей старшего возраста и подростков. Тяжесть заболевания варьирует от субклинического течения до тяжелых форм, характеризующихся часто повторяющимися гемолитическими кризами. В момент криза нарастает температура тела, головокружение, слабость; возникают боли в животе и рвота.
Основным признаком микросфероцитарной гемолитической анемии служит желтуха различной степени интенсивности. Вследствие высокого содержания стеркобилина кал становится интенсивно окрашенным в темно-коричневый цвет. У пациентов с болезнь Минковского-Шоффара наблюдается склонность к образованию камней в желчном пузыре, поэтому часто развиваются признаки обострения калькулезного холецистита, возникают приступы желчной колики, а при закупорке холедоха конкрементом – обтурационная желтуха. При микросфероцитозе во всех случаях увеличена селезенка, а у половины пациентов – еще и печень. Кроме наследственной микросфероцитарной анемии, у детей часто встречаются другие врожденные дисплазии: башенный череп, косоглазие, седловидная деформация носа, аномалии прикуса, готическое нёбо, полидактилия или брадидактилия и пр. Пациенты среднего и пожилого возраста страдают трофическими язвами голени, которые возникают в результате гемолиза эритроцитов в капиллярах конечностей и плохо поддаются лечению.
Энзимопенические анемии связаны с недостатком определенных ферментов эритроцитов (чаще – Г-6-ФД, глутатион-зависимых ферментов, пируваткиназы и др). Гемолитическая анемия может впервые заявлять о себе после перенесенного интеркуррентного заболевания или приема медикаментов (салицилатов, сульфаниламидов, нитрофуранов). Обычно заболевание имеет ровное течение; типична «бледная желтуха», умеренная гепатоспленомегалия, сердечные шумы. В тяжелых случаях развивается ярко выраженная картина гемолитического криза (слабость, рвота, одышка, сердцебиение, коллаптоидное состояние). В связи с внутрисосудистым гемолизом эритроцитов и выделением гемосидерина с мочой последняя приобретает темный (иногда черный) цвет. Особенностям клинического течения гемоглобинопатий – талассемии и серповидно-клеточной анемии посвящены самостоятельные обзоры.
Приобретенные гемолитические анемии
Среди различных приобретенных вариантов чаще других встречаются аутоиммунные анемии. Для них общим пусковым фактором выступает образование антител к антигенам собственных эритроцитов. Гемолиз эритроцитов может носить как внутрисосудистый, так и внутриклеточный характер. Гемолитический криз при аутоиммунной анемии развивается остро и внезапно. Он протекает с лихорадкой, резкой слабостью, головокружением, сердцебиением, одышкой, болями в эпигастрии и пояснице. Иногда острым проявлениям предшествуют предвестники в виде субфебрилитета и артралгий. В период криза стремительно нарастает желтуха, не сопровождающаяся кожным зудом, увеличивается печень и селезенка. При некоторых формах аутоиммунных анемий больные плохо переносят холод; в условиях низких температур у них может развиваться синдром Рейно, крапивница, гемоглобинурия. Вследствие недостаточности кровообращения в мелких сосудах возможны осложнения в виде гангрены пальцев ног и рук.
Токсические анемии протекают с прогрессирующей слабостью, болями в правом подреберье и поясничной области, рвотой, гемоглобинурией, высокой температурой тела. Со 2-3 суток присоединяется желтуха и билирубинемия; на 3-5 сутки возникает печеночная и почечная недостаточность, признаками которых служат гепатомегалия, ферментемия, азотемия, анурия. Отдельные виды приобретенных гемолитических анемий рассмотрены в соответствующих статьях: «Гемоглобинурия» и «Тромбоцитопеническая пурпура», «Гемолитическая болезнь плода».
Осложнения
Каждый вид ГА имеет свои специфические осложнения: например, ЖКБ – при микросфероцитозе, печеночная недостаточность – при токсических формах и т.д. К числу общих осложнений относятся гемолитические кризы, которые могут провоцироваться инфекциями, стрессами, родами у женщин. При остром массивном гемолизе возможно развитие гемолитической комы, характеризующейся коллапсом, спутанным сознанием, олигурией, усилением желтухи. Угрозу жизни больного несут ДВС-синдром, инфаркт селезенки или спонтанный разрыв органа. Неотложной медицинской помощи требуют острая сердечно-сосудистая и почечная недостаточность.
Диагностика
Определение формы ГА на основе анализа причин, симптоматики и объективных данных относится к компетенции гематолога. При первичной беседе выясняется семейный анамнез, частота и тяжесть протекания гемолитических кризов. В процессе осмотра оценивается окраска кожных покровов, склер и видимых слизистых, производится пальпация живота для оценки величины печени и селезенки. Сплено- и гепатомегалия подтверждается при проведении УЗИ печени и селезенки. Лабораторный диагностический комплекс включает:
- Исследование крови. Изменения в гемограмме характеризуются нормо- или гипохромной анемией, лейкопенией, тромбоцитопенией, ретикулоцитозом, ускорением СОЭ. В биохимических пробах крови определяется гипербилирубинемия (увеличение фракции непрямого билирубина), увеличение активности лактатдегидрогеназы. При аутоиммунных анемиях большое диагностическое значение имеет положительная проба Кумбса.
- Анализы мочи и кала. Исследование мочи выявляет протеинурию, уробилинурию, гемосидеринурию, гемоглобинурию. В копрограмме повышено содержание стеркобилина.
- Миелограмму. Для цитологического подтверждения выполняется стернальная пункция. Исследование пунктата костного мозга обнаруживает гиперплазию эритроидного ростка.
В процессе дифференциальной диагностики исключаются гепатиты, цирроз печени, портальная гипертензия, гепатолиенальный синдром, порфирии, гемобластозы. Пациента консультируют гастроэнтеролог, клинический фармаколог, инфекционист и другие специалисты.

Аутоиммунная гемолитическая анемия
Лечение
Различные формы ГА имеют свои особенности и подходы к лечению. При всех вариантах приобретенной гемолитической анемии необходимо позаботиться об устранении влияния гемолизирующих факторов. Во время гемолитических кризов больным необходимы инфузии растворов, плазмы крови; витаминотерапия, по необходимости – гормоно- и антибиотикотерапия. При микросфероцитозе единственно эффективным методом, приводящим к 100 % прекращению гемолиза, является спленэктомия.
При аутоиммунной анемии показана терапия глюкокортикоидными гормонами (преднизолоном), сокращающая или прекращающая гемолиз. В некоторых случаях требуемый эффект достигается назначением иммунодепрессантов (азатиоприна, 6-меркаптопурина, хлорамбуцила), противомалярийных препаратов (хлорохина). При резистентных к медикаментозной терапии формах аутоиммунной анемии выполняется спленэктомия. Лечение гемоглобинурии предполагает переливание отмытых эритроцитов, плазмозаменителей, назначение антикоагулянтов и антиагрегантов. Развитие токсической гемолитической анемии диктует необходимость проведения интенсивной терапии: дезинтоксикации, форсированного диуреза, гемодиализа, по показаниям – введение антидотов.
Прогноз и профилактика
Течение и исход зависят от вида анемии, тяжести протекания кризов, полноты патогенетической терапии. При многих приобретенных вариантах устранение причин и полноценное лечение приводит к полному выздоровлению. Излечения врожденных анемий добиться нельзя, однако возможно достижение длительной ремиссии. При развитии почечной недостаточности и других фатальных осложнений прогноз неблагоприятен. Предупредить развитие ГА позволяет профилактика острых инфекционных заболеваний, интоксикаций, отравлений. Запрещается бесконтрольное самостоятельное использование лекарственных препаратов. Необходимо тщательная подготовка пациентов к гемотрансфузиям, вакцинации с проведением всего комплекса необходимых обследований.
Источник
