Врожденная дизэритропоэтическая анемия это

Врожденные дизэритропоэтические анемии – классификация, диагностика, лечение
Врожденные дисэритропоэтические анемии (ВДА) составляют особую группу наследственных анемий, характеризующихся неэффективностью эритропоэза, специфической морфологией костномозговых эритробластов, вторичным гемохроматозом и устойчивостью к лечению.
По изменениям эритробластов, установленным с помощью оптического микроскопа и условиям, ведущим к расплавлению эритроцитов в пробирке, Heimpel и Wendt выделили следующие три вида хронической дисэритропоэтической анемии: mun I — характеризующийся наличием мегалобластоидных эритробластов с межядерными хроматинными мостиками; тип II — характеризующийся наличием многоядерных эритробластов и положительной реакцией расплавления с подкисленной сывороткой (Ham); III тип — характеризующийся наличием многоядерных эритробластов.
В 1969 г. Crookston предложил следующее название для II типа врожденной дизэритропоэтической анемии: “hereditary erythroblastic multinuclearity with a positive acidified serum test (HEMPAS)”. Недавно была описана разновидность ВДА типа II, при которой реакция Ham дала отрицательный результат (Weatherall D.J. и сотр., Hurby М.А. и сотр., McBride J.A. и сотр.), равно как и вариант специфического серологического поведения но без характерных морфологических аномалий (Van Dorpe A.).
Тип I врожденной дизэритропоэтической анемии встречается исключительно редко. До настоящего времени имеются лишь 23 сообщения о выявленных в 20 семьях случаях заболевания (Verwilghen и сотр.). Болезнь передается аутосомально, рецессивно. Анемия умеренная. На мазке крови выявляется выраженный анизоцитоз эритроцитов и макроцитоз. Исследование костного мозга выявляет крупные морфологические аномалии проэритробластов и базофильных эритробластов, имеющих «мегалобластоидный» аспект. В клетках ядерный хроматин организован в виде толстых полос, распределен нерегулярно и перемежается с неравномерными просвечивающими участками.
У отдельных эритробластов хроматинная структура стертая, со слабо окрашенными однородными поверхностями а ядро не отграничено четко от окружающей его цитоплазмы. К другим характерным морфологическим изменениям относятся: сегментирование ядра с неполным делением; двухядрышковые клетки с ядрами разных величины, строения и окрашиваемости; пары эритробластов, связанные между собой мостиками хроматина разной длины. В макрофагах костного мозга показатель гемосидерина завышен. Число сидеробластов умеренно большое. Под электронным микроскопом выявляются расширение пор клеточной оболочки, уплотнение, вакуолизация и распад ядерного хроматина.
В отдельных случаях при врожденной дисэритропоэтической анемии типа I испытание на расплавление с применением сыворотки анти-i дает положительный результат.
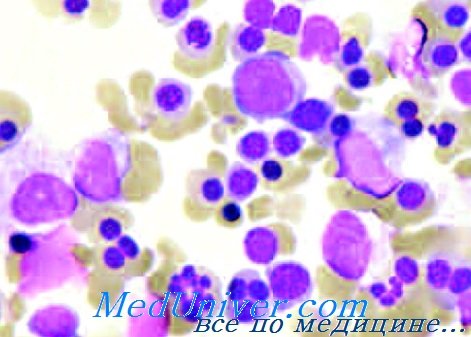
Мазок крови при врожденной дизэритропоэтической анемии
Тип II врожденной дизэритропоэтической анемии наиболее частый. Имеются сообщения о 84 случаях в 55 семьях (Verwilghen и сотр.). Способ передачи болезни аутосомальнорецессивный. К основным клиническим признакам относятся: проявления анемии, желтуха, гепатоспленомегалия, страдания желчного пузыря. Анемия умеренная. Эритроциты характеризуются умеренными анизоцитозом и пойкилоцитозом. Иногда на мазке крови выявляются редкие двухядерные эритробласты. Число ретикулоцитов в норме или меньше. В костном мозге наблюдается выраженная гиперплазия эритроидного ряда.
10—35% полихроматофильных и оксифильных эритробластов — двух- или многоядрышковые, притом отмечается наличие значительного числа кариорексисов. У некоторых больных обнаруживаются макрофаги, пожирающие эритробластов и клетки „Gaucher-like” или гистиоцитов с синей зернистостью. В макрофагах костного мозга показатель гемосидерина завышен, в то время как в увеличенном проценте сидеробластов обнаруживаются крупные многочисленные зерна железа. Двух- или многоядерные эритробласты дают шикотрицательную реакцию. Под электронным микроскопом у 90% эритробластов наблюдаются оболочковые структуры (цистерны), расположенные параллельно клеточной оболочке. Подобное строение отмечается также у малого процента (1%) эритроцитов крови.
Ауторентгенографическое исследование костномозговых клеток с помощью тимидина Н3 выявляет тот факт, что двух- и многоядрышковые клетки остаются немаркированными. При врожденной дисэритропоэтической анемии типа II эритроциты напоминают о таковых при ночной пароксизмальной гемоглобинурии, поскольку они расплавляются под влиянием некоторых нормально подкисленных сывороток. Однако кислое расплавление крови не выявляется в сыворотке больного. Под воздействием сывороток анти-i и анти-I эритроциты врожденной дисэритропоэтической анемии типа II подвергаются процессам агглютинации и расплавления. Испытание с водой и сахаром дает отрицательный результат.
Серологическая аномалия связана с пороком оболочки эритроцита. Объяснение положительного результата реакции Ham следует искать в наличии специфического антигена HEMPAS реагирующего с естественным ИгМ, который находится в 30% нормальных сывороток. В эритроцитах наблюдается высокая концентрация антигена I и сохранение антигена i плодного типа. Антигены, неправильно расположенные на поверхности эритроцитов при врожденной дисэритропоэтической анемии типа II — результат сокращения покровной неураминовой кислоты и недостатков в сокращающихся элементах оболочки (Lewis S.M., Verwilghen R.L.).
У страдающих врожденной дисэритропоэтической анемией типа II наблюдается выраженное повышение активности отдельных эритроцитных ферментов (глюкозо-фосфатизомераза, триозо-фосфатизомераза, глиоксалаз I, фосфорил-фосфорибозилтрансфераза). Ацетилхолинэстераза эритроцитов несколько занижена. У 2 больных, страдающих ВДА типа II, определенных в Бухарестской клинике гематологии показатель щелочной фосфатазы лейкоцитов (ЩФЛ) равнялся нулю. Это подсказывает мысль о том, что основное нарушение не ограничивается эритроидным рядом а видимо распространяется и на остальные костномозговые клеточные ряды (дефект полипотентной клетки-штамм?) (Колицэ и сотр.).
Тип III врожденной дизэритропоэтической анемии — это первая описаная разновидность. Сделано сообщение о 22 больных, принадлежащих 4 семьям. Передача болезни аутосомально доминантная. Анемия макроцитная. Исследование мазка выявляет выраженный анизоцитоз эритроцитов. В костном мозге отмечается наличие примерно 30% предшественников многоядерных эритроцитов (с > 12 ядрами). Эти крупные эритробласты (диаметром более 50—60u) получили название «гигантобластов». Цитохимические исследования показывают большое колебание количества ДРНК на каждое ядро эритробласта (Goudsmit и сотр.). В свою очередь серологические исследования обнаруживают агглютинацию эритроцитов сывороткой анти-i и расплавление сывороткой анти-i и анти-I.
Диагностика врожденной дизэритропоэтической анемии. Виды врожденной дисэритропоэтической анемии нетрудно распознать по характерным аномалиям эритробластов костного мозга и отличительному серологическому поведению. Так, например, это заболевание типа II отличается от ночной пароксизмальной гемоглобинуриитем,что испытание на расплавление с помощью подкисленной сыворотки дает положительный результат лишь при использовании определенных сывороток, в то время как результаты испытаний с применением сукроза и подслащенной сахаром воды — отрицательны.
При ночной пароксизмальной гемоглобинурии костный мозг нормобластический, при этом показатели наличия в нем гемосидерина и сидеробластов занижены, в то время как ретикулоцитов — резко завышен. Значительное число двух- или многоядерных эритробластов отмечено при эритролейкемии. У страдающих врожденной дисэритроэпоэтической анемией эритробласты шикотрицательные, в отличие от эритролейкемии, при которой эта реакция дает шикположительный результат.
Терапия врожденной дизэритропоэтической анемии. Назначение железа протршопоказано. Переливание способствует усугублению гемохроматоза. В целях сокращения запасов железа были испробованы лечение препаратом десфериоксамин и вскрытием вены. В отдельных случаях спленэктомия способствовала росту показателя гемоглобина.
– Читать далее “Гипохромные анемии – причины, классификация”
Оглавление темы “Анемии”:
- Диагностика мегалобластической анемии – анализы
- Лечение мегалобластической анемии – препараты
- Врожденные дизэритропоэтические анемии – классификация, диагностика, лечение
- Гипохромные анемии – причины, классификация
- Железодефицитная анемия – история изучения, эпидемиология
- Причины дефицита железа в организме? Этиология железодефицитной анемии
- Клиника железодефицитной анемии – признаки
- Лабораторная диагностика железодефицитной анемии – анализы
- Лечение железодефицитной анемии. Сколько принимать препараты железа?
- Профилактика дефицита железа – железодефицитной анемии

Первичные и вторичные дизэритропоэтические анемии

Схема кроветворения в костном мозге
Дизэритропоэтическая анемия — общее название патологий, при которых угнетаются функции костного мозга в области образования эритроцитов. Недостаточная выработка вызвана повреждением клеток, из которых продуцируются эритроциты. Повреждение может происходить на этапе зарождения либо на последующих стадиях развития эритроцита. В результате эритроциты, не успев обрести зрелую форму, погибают в костном мозге.
Первичная. Включает анемии либо заболевания, провоцирующие их образование, передающиеся по наследству. Определяется патология чаще всего на первом году жизни ребёнка. Характерные симптомы — бледность кожных покровов с желтоватым оттенком, белки глаз пожелтевшие, печень и селезёнка увеличены. Дети проявляют беспокойство, отказываются от еды, частым спутником заболевания становятся инфекции различной природы. Анемии протекают преимущественно в хронической форме.
Вторичная. Анемии приобретённого характера образуются вследствие нехватки микроэлементов либо витаминов, особой чувствительности к компонентам лекарственных средств, радиоактивного облучения, взаимодействия с опасными для здоровья химическими соединениями. Некоторые виды анемий возникают по неустановленной причине. Первыми признаками являются слабость, бледность, головокружения.
Этиология, патогенез

Наличие дефектных генов — причина первичных анемий
Этиология анемий носит различный характер. Первичная форма вызывается дефектными генами, передающимися от обоих родителей ребёнку. Существует ряд заболеваний, относящихся к наследственному виду дизэритропоэтических анемий. Их разделяют на 6 типов, каждый из которых имеет свои отличительные особенности при диагностике.
Патогенез врождённых форм обусловлен наличием повышенной ломкости хромосом. Причина заключается в мутации генов, связанных с рибосомальными белками. Факторы, влияющие на мутацию не установлены.
Анемии, вызванные недостатком элементов для эритропоэза, по своей природе делятся на 2 категории: заболевания при нехватке веществ (белка, железа, меди, витаминов группы В) и на патологии, связанные с некорректной усвояемостью данных веществ. Причины заключаются в дефиците поступающих в организм элементов (диеты, несбалансированное питание); повышенном расходе организмом (заболевания, кровотечения); наличии факторов, влияющих на переработку необходимых микроэлементов (курение, алкоголизм, стрессы, приём медицинских препаратов).
Патогенез сопровождается нарушением развития эритроцита. Например, при отсутствии меди эритроциты замирают на стадии ретикулоцитов и не переходят в зрелую форму.
Этиология анемий, спровоцированных угнетением костного мозга излучением, химическими соединениями и токсическими веществами — радиоактивная терапия, приём лекарств (антибиотики, антидепрессанты, противоопухолевые), взаимодействие с нефтепродуктами, ртутью.
Патогенез. Происходит повреждение стволовых клеток либо нарушение их микроокружения; угнетается процесс синтеза нуклеиновых кислот.
Симптомы

Бледность кожных покровов как один из признаков анемии
Недостаток эритроцитов провоцирует кислородное голодание тканей всех органов. В начальной стадии организм, испытывая дефицит кислорода, начинает качать кровь в ускоренном темпе. Пациент может ощущать учащённое сердцебиение, нехватку воздуха, одышку. Постепенно развиваются и другие симптомы болезни:
- быстрая утомляемость;
- головные и суставные боли;
- бледность или желтизна кожи;
- рассеянность внимания;
- тахикардия;
- ломкость волос и ногтей, возможна деформация ногтевой пластины;
- головокружения, обмороки;
- частые вирусные заболевания, грибковые и бактериальные заражения;
- трещины в уголках рта, кровоточивость дёсен;
- повышение температуры на 1 — 1,5 градуса;
- шум в ушах, появление тёмных точек перед глазами.
Диагностика и терапевтический прогноз

Комплексное обследование пациента — путь к верному диагнозу
Все виды анемий имеют свои отличия в показателях анализов. Для верификации диагноза проводятся дополнительные исследования. Наиболее распространённые показатели при дизэритропоэтической анемии:
- При физикальном обследовании:
- селезёнка увеличена в размерах;
- печень увеличена;
- кожные покровы отличаются бледностью с желтоватым оттенком.
- При исследовании крови:
- увеличение объёма эритроцита;
- патологические включения в эритроцитах;
- формы и структуры ядер изменены;
- повышенный уровень билирубина в сыворотке;
- избыточное отложение железа в митохондриях и лизосомах;
- нарушение структуры оболочки незрелого эритроцита.
- При морфологическом исследовании костного мозга:
- мегалобласты, эритробласты связаны хроматиновыми ядерными мостиками;
- клетки многоядерные (могут содержать до 12 ядер).
Прогноз благоприятен для нетяжёлых форм дизэритропоэтической анемии. При своевременном обнаружении и лечении заболеваний функция костного мозга восстанавливается. Очень тяжёлые формы патологии провоцируют критическое снижение иммунитета, кислородное голодание, риск летальности составляет 80%.
Лечение

Первое и главное в лечении — устранить причину
- Выявление причины и её устранение. При тяжёлых формах пациента помещают в отдельный бокс во избежание инфицирования.
- При анемиях, вызванных нехваткой веществ, назначается курс витаминов и микроэлементов.
- Переливание эритроцитной массы — временная мера для восстановления циркуляции эритроцитов в крови. Не влияет на продуктивность костного мозга.
- Приём стимуляторов эритропоэза, в частности эритропоэтина.
- Пересадка костного мозга. Процедура позволяет полностью возродить работу костного мозга, эффект достигается даже при тяжёлых формах заболевания. Трансплантация — единственный способ оптимизации кроветворения в большинстве случаев врождённых патологий.
Данный раздел заболеваний посвящен анемиям, не связанным с гемолитическими и апластическими анемиями. Как правило, эти заболевания встречаются реже и не так распространены, как железодефицитная или другие анемии, связанные с питанием. Эти виды анемий часто передаются по наследству, реже являются приобретенными.
- Врожденная дизэритропоэтическая анемия
- Дисгемопоэтическая анемия
- Лейкоэритробластная анемия
- Псевдолейкоз
Врожденная дизэритропоэтическая анемия
Врожденная дизэритропоэтическая анемия (CDA) является наследственным заболеванием крови, влияющим на нормальное развитие эритроцитов. Это расстройство является одним из многих видов заболеваний, для которых характерна нехватка красных кровяных клеток. Кровь не может адекватно снабжать кислородом органы и ткани, в результате возникает слабость, усталость, сонливость и другие состояния.
Существует три типа дизэритропоэтической анемии: обозначаются они как тип I, тип II и тип III. Они имеют различные генетические причины и различные, но порой перекликающиеся симптомы и модель проявления.
CDA типа I характеризуется анемией от умеренной до тяжелой степени. Обычно она диагностируется в детском или подростковом возрасте, хотя в некоторых случаях может быть обнаружена еще до рождения.
Больные проявляют характерные симптомы: пожелтение кожи и белков глаз (желтуха) и увеличение печени и селезенки (гепатоспленомегалия). Эти состояния заставляют организм поглощать слишком много железа, которое накапливается и может повредить ткани и органы. В частности, перегрузка железом может привести к аномальному сердечному ритму (аритмии), застойной сердечной недостаточности, диабету и хроническим заболеваниям печени (циррозу). Иногда люди с 1 типом CDA рождаются со скелетными аномалиями, например, сросшимися пальцами рук или ног.
Дизэритропоэтическая анемия II типа протекает с большим количеством симптомов, чем предыдущий тип. Кроме гепатоспленомегалии и желтухи у больных отмечается образование твердых отложений в желчном пузыре. Эта форма заболевания диагностируется в подростковом возрасте или в начале взрослой жизни. Аномальное накопление железа происходит после 20 лет, что приводит к циррозу печени, диабету, болезням сердца.
Анемия III типа обычно протекает в более мягкой форме, чем две предыдущих. Большинство пациентов с дизэритропоэтической анемией 3 типа не имеют желтухи и гепатоспленомегалии, а избыток железа в органах и тканях не накапливается. В зрелом возрасте может наблюдаться аномалия сетчатки, из-за чего ухудшается зрение. Некоторые больные с CDA III страдают от заболевания крови, известного как моноклональная гаммапатия. Оно приводит к множественной миеломе, если не лечить.
Методы лечения: переливания крови, спленэктомия, препарат дефероксамин, флеботомия.
Дисгемопоэтическая анемия
Этот вид анемии связан с аномальной функцией красного костного мозга. Появление такого вида анемии связано с воздействием тяжелых токсинов, облучения, использования цитостатиков (применяются для угнетения роста опухолей). В медицинской терминологии анемии этого вида известны под названием «апластические». Еще одна популярная причина их возникновения — конфликт резусов крови эмбриона и матери. В этом случае повреждаются не только эритроциты, но и лейкоциты.
Обычно стволовая клетка, развиваясь, дает жизнь всем видам клеток крови, дефекты в развитии стволовых клеток приводят, соответственно, к появлению дефектных клеток крови всех типов. Еще один пример дисгемопоэтической анемии — это дефицит витамина В12 и анемия, связанная с ним. Если организму не хватает В12, прекращается производство нуклеотида тимина. Из-за этого красные кровяные клетки не могут делиться в соответствии с необходимой для организма нормой. Эритроциты тем временем продолжают насыщаться гемоглобином, поскольку процесс синтеза РНК продолжается. Вследствие этого образуются мегалобласты и мегалоциты, они похожи на нормальные клетки, но длительность их жизненного цикла намного короче.
Лечение: контроль рациона, переливания крови. Данный вид анемии является врожденным и связан с тем, что костный мозг аномально выполняет свои функции. В случае появления этого заболевания лечение должен назначать врач.
Лейкоэритробластная анемия
Лейкоэритробластная анемия — это вид анемии, возникающий вследствие обширного поражения костного мозга. При данном виде заболевания циркулирующая в организме кровь содержит незрелые эритроциты (гранулоцитарные и ядросодержащие). Это заболевание может быть ответом костного мозга на любой раздражитель, в том числе на инфильтраты. Инфильтративные расстройства, которые могут привести к лейкоэритробластной анемии это:
- миеломы;
- миелофиброз,
- болезнь Гоше.
Также этот вид анемии может возникать в ответ на затяжную и опасную болезнь: сепсис, массивный гемолиз, тяжелая степень мегалобластной анемии, травмы с обширными кровотечениями. Лейкоэритробластная анемия подразумевает наличие в крови ядерных эритроцитов (мегалобластов) и абортивных лейкоцитов.
Особенности лейкоэритробластной анемии:
- нормоцитарная нормохромная анемия с многочисленными пойкилоцитами (эритроцитами измененной формы);
- наличие нормобластов;
- субфебрильный ретикулоцитоз;
- циркулирующие незрелые белые кровяные клетки;
- тромбоцитопения;
- тромбоцитемия.
Псевдолейкоз
Псевдолейкоз также называют перераспределительным лейкозом. Эта форма заболевания характеризуется изменением соотношения пристеночного и циркулирующего объема лейкоцитов в пользу циркулирующего. Абсолютное количество лейкоцитов не повышается. Лейкоциты начинают активнее перемещаться, из-за этого в единице крови их объем возрастает. Основные причины такого состояния:
- активные тренировки, физнагрузка;
- повреждение внутренних органов или обширные внешние повреждения;
- хемотаксис (сигнал лейкоцитам о перемещении к месту повреждения). В результате лейкоциты начинают перемещаться от стенок к месту очага и заполняют собой общий кровоток. Это состояние часто наблюдается у спортсменов, которые тяжело тренируются, а также при анафилактическом шоке.
Этот вид лейкоза временный и не опасен для человека. Часто лейкоциты, которые перемещаются в кровотоке при таком состоянии, называют относительными/ложными. У детей ложный лейкоз может вызываться хронической вирусной инфекцией, ослаблением иммунитета, а также быть следствием затяжной болезни.
Лечение: обычно не требуется специального лечения. Необходимо лишь устранить источник инфекции или очаг повреждения, и со временем количество лейкоцитов нормализуется. Для профилактики ложного лейкоза у детей рекомендуется укреплять иммунитет, закаливать ребенка, следить за уровнем гемоглобина и общим состоянием здоровья.
Источники статьи:
https://www.bloodjournal.org/
https://www.orpha.net/
https://www.ncbi.nlm.nih.gov/
https://ghr.nlm.nih.gov/
https://en.wikipedia.org/
По материалам:
© 2015 by American Society of Hematology
Dr Mayka SANCHEZ FERNANDEZ
National Center for Biotechnology Information,
U.S. National Library of Medicine
Lister Hill National Center for Biomedical Communications
Смотрите также:
У нас также читают:
