Злокачественная анемия это дефицит

Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 21 января 2019;
проверки требуют 6 правок.
Перницио́зная анеми́я (от лат. perniciosus — гибельный, опасный) или B12-дефицитная анемия или мегалобластная анемия или болезнь Аддисона — Бирмера или (устаревшее название) злока́чественное малокро́вие — заболевание, обусловленное нарушением кроветворения из-за недостатка в организме витамина B12. Особенно чувствительны к дефициту этого витамина костный мозг и ткани нервной системы.
Основные сведения[править | править код]
Это синдром, связанный с недостатком B12 и фолиевой кислоты в организме. Характеризуется наличием в костном мозге большого количества крупных незрелых предшественников эритроцитов (мегалобластов).
Витамин B12всасывается в основном в нижней части подвздошной кишки. Анемия может быть вызвана недостаточным потреблением витамина B12 в пищу, недостаточной выработкой внутреннего фактора Касла в париетальных клетках желудка, патологическими процессами в подвздошной кишке с нарушением всасывания или конкуренцией за витамин B12 со стороны ленточных червей или бактерий.
При дефиците витамина B12 на фоне анемической клинической картины (или без неё) могут возникнуть и неврологические расстройства из-за связанного с дефицитом витамина B12 нарушения синтеза жирных кислот. Может наблюдаться демиелинизация и необратимая гибель нервных клеток. Симптомами такой патологии являются онемение или покалывание конечностей и атаксия.
Проявления[править | править код]
- Ярко-красный, а затем «лакированный» язык.
- Желудочная ахилия.
- Малокровие с наличием патологических эритроцитов.
- Поражение нервной системы.
- Желтоватый цвет кожи.
- Образование в костном мозге аномальных крупных клеток вместо эритроцитов (переход на мегалобластический тип кроветворения).
Причины[править | править код]
- Недостаток витамина B12 в питании или нарушение его всасывания
- Расстройство кишечника
- Долгое использование медицинских препаратов, приводящих к уменьшению кислотности в желудке
- Гастрэктомия
- Аутоиммунное поражение внутреннего фактора Касла или париетальных клеток.
- Заражение ленточными червями (лентец широкий)
- Токсическое воздействие на стенку желудка
- Рак желудка
- Наследственный дефект, передается аутосомно-рецессивно
Осложнения[править | править код]
В отсутствие лечения развиваются анемия и дегенерация нервов, так как костный мозг и ткани нервной системы особенно чувствительны к дефициту витамина B12.
Историческая справка[править | править код]
В 1855 году английский врач Томас Аддисон, а затем в 1872 году более подробно немецкий врач Антон Бирмер описали болезнь, которую назвали злокачественной (пернициозной) анемией. Вскоре французский врач Арман Труссо предложил называть эти болезни аддисоновой анемией и болезнью Аддисона.
В 1926 году Дж. Уипл, Дж. Майнот и У. Мерфи сообщили, что пернициозная анемия лечится введением в рацион питания сырой печени и что в основе заболевания лежит врожденная неспособность желудка секретировать вещество, необходимое для всасывания витамина B12 в кишечнике. За это открытие они в 1934 году получили Нобелевскую премию.
См. также[править | править код]
- Внутренний фактор
- https://en.wikipedia.org/wiki/Vitamin_B12_deficiency
Примечания[править | править код]
- ↑ Monarch Disease Ontology release 2018-06-29sonu — 2018-06-29 — 2018.
Ссылки[править | править код]
- Анемия
- Наше здоровье
- [da-med.ru/diseases/cat-60/d-125/ Da-med.ru ::: B12-дефицитная анемия (Пернициозная анемия)]
Некоторые внешние ссылки в этой статье ведут на сайты, занесённые в спам-лист. Эти сайты могут нарушать авторские права, быть признаны неавторитетными источниками или по другим причинам быть запрещены в Википедии. Редакторам следует заменить такие ссылки ссылками на соответствующие правилам сайты или библиографическими ссылками на печатные источники либо удалить их (возможно, вместе с подтверждаемым ими содержимым). Список проблемных доменов |
Источник

Анемия представляет собой патологическое состояние, для которого характерно снижение эритроцитов и/или концентрации гемоглобина в единице объема крови. Анемия не является самостоятельным заболеванием, это симптом, который характерен для самых разнообразных заболеваний, в том числе и для злокачественных опухолей.
Согласно статистике, данное состояние выявляется у каждого третьего онкологического пациента, а при прохождении химиотерапии — более чем в 90% случаев. Опасность анемии в онкологии заключается в том, что вместе с уменьшением уровня гемоглобина и эритроцитов, уменьшается и кислородная емкость крови. Этот фактор неблагоприятно сказывается на течении ракового процесса, снижает эффективность лечения и ухудшает дальнейший прогноз.
Основные причины развития анемии у онкологических пациентов
Снижение уровня эритроцитов и гемоглобина может развиваться вследствие снижения их образования, ускоренного разрушения или в результате потери. Каждой из этих причин способствуют собственные факторы, которые рассмотрим подробнее:
- Недостаточная выработка форменных элементов крови и гемоглобина может развиваться при поражении костного мозга, недостатке железа в организме или некоторых витаминов (фолиевая кислота, витамин В12). Данные состояния могут быть напрямую связаны с напрямую с онкологическим заболеванием. Например, потеря железа может развиваться в результате постоянной рвоты, отсутствия аппетита и нарушения его всасывания в кишечнике, который поражен опухолевым процессом. Некоторые виды препаратов, которые назначают при злокачественных опухолях, подавляют рост не только раковых клеток, но и клеток крови, которые активно делятся. Также анемия может развиваться при непосредственном поражении костного мозга опухолевым процессом.
- Ускоренное разрушение эритроцитов отмечается при воздействии различных лекарственных препаратов и при аномальной активности иммунной системы. Разрушение эритроцитов непосредственно в сосудах называется внутрисосудистым гемолизом. Этот процесс протекает в норме после завершения жизненного цикла эритроцитов, который составляет 120 дней. Однако при воздействии различных факторов (прием антибиотиков, цитостатиков, присоединение вторичной инфекции и др.), этот срок значительно уменьшается, что и приводит к развитию анемии.
- Кровопотеря у онкологических пациентов может быть как острой, так и хронической. Первый вариант встречается при проведении хирургического лечения рака, а также при развитии внутренних кровотечений, которые являются частым осложнением основного заболевания. Развитие анемии при хронической кровопотере отмечается в тех случаях, когда имеется скрытый источник незначительного кровотечения. Например, при колоректальном раке кровь может выделяться с калом незаметно для пациента.
Установление точной причины анемии играет решающее значение при выборе метода лечения. Кроме того, врач учитывает степень тяжести, тип анемии, общее состояние пациента и другие параметры. Получить эту информацию можно на диагностическом этапе.
Как выявить анемию
Обследование традиционно начинается с опроса пациента и сбора анамнеза. Врач должен помнить, что не всегда анемия развивается вследствие основного заболевания. Возможны наследственные или любые другие причины, которые не связаны с опухолевым процессом. Также необходимо установить вид предшествующего противоопухолевого лечения, продолжительность и количество курсов, наименование препаратов, которые применялись. На следующем этапе врач проводит общий осмотр. Анемия может проявляться бледностью кожных покровов, слабостью, потерей аппетита, головокружением и другими симптомами. Очень часто эти проявления отмечаются при различных видах рака, который протекает без анемии, поэтому поставить диагноз исходя только из жалоб пациента невозможно.
Объективную информацию можно получить только при помощи лабораторных исследований. Анемия диагностируется по следующим анализам:
- Количество ретикулоцитов.
- Уровень железа сыворотки крови.
- Уровень белка трансферрина и ферритина.
- Уровень витамина В12 и фолиевой кислоты.
Отдельное внимание уделяется общему анализу крови. В нем определяется уровень гемоглобина, количество эритроцитов и гематокрит (отношение форменных элементов к жидкой составляющей крови). Также определяют средний объем эритроцита, среднее содержание гемоглобина в эритроците и среднее содержание гемоглобина во всей эритроцитарной массе.
При необходимости в программу комплексного обследования при анемии могут включаться и другие лабораторные анализы или специальные методы.
Как классифицируется анемия
В зависимости от значения цветового показателя, степени тяжести и механизма развития, анемия разделяется на несколько категорий. Цветовой показатель крови отражает степень насыщения эритроцитов гемоглобином. Его значение в норме колеблется от 0,85 до 1,05 единиц. Снижение показателя отмечается при гипохромной анемии, а повышение — при гиперхромной. Если цветовой показатель в норме, но уровень гемоглобина все равно низкий, то говорят о нормохромной анемии.
По степени тяжести, анемия разделяется на три группы, в зависимости от концентрации гемоглобина:
- При легкой степени анемии уровень гемоглобина не опускается ниже отметки в 90 г/л.
- При средней степени анемии показатель колеблется в пределах 90-70 г/л.
- Тяжелая анемия характеризуется падением гемоглобина ниже 70 г/л.
Классификация анемии по механизму развития наиболее обширна. Среди распространенных форм отмечаются:
- Железодефицитная анемия. Развивается в результате нарушения всасывания, усиленной потери или недостаточного поступления железа в организм.
- Гемолитическая анемия. Характеризуется разрушением эритроцитов в сосудистом русле или за его пределами. Наиболее частые причины — недостаточность специфических ферментов, аутоиммунные заболевания, воздействие лекарственных препаратов.
- Постгеморрагическая анемия. Данное состояние характерно для острой или хронической кровопотери
- Апластическая анемия. Характеризуется снижением уровня клеток-предшественников эритроцитов в костном мозге. Обычно отмечается снижение и других форменных элементов — тромбоцитов и лейкоцитов.
- В12-дефицитная анемия. При недостатке витамина В12 нарушается процесс образования эритроцитов, снижается их продолжительность жизни. Дефицит витамина может быть связан как с нарушением его всасывания в кишечнике, так и с недостаточным поступлением в организм.
В большинстве случаев определить точный вид анемии можно после нескольких лабораторных тестов, но иногда приходится применять более сложные методы диагностики, например, генетическое исследование. Понимание механизма развития анемии и получение максимально полной информации об изменениях в показателях крови являются важным компонентом эффективной терапии данного симптома.
Методы лечения анемии
Устранить анемию у онкологических пациентов можно тремя способами: переливание эритроцитарной массы, введение эритропоэтина, назначение препаратов, содержащих железо. В отдельных случаях может применяться комбинация этих методов.
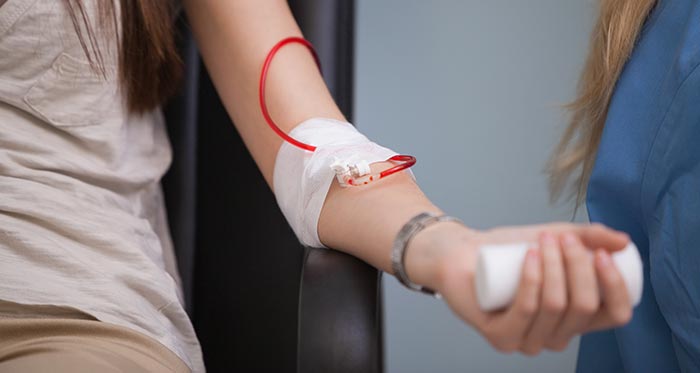
Переливание эритроцитарной массы при анемии
Переливание эритроцитарной массы является самым действенным методом, при помощи которого можно быстро восполнить дефицит эритроцитов, восстановить уровень гемоглобина и гематокрита. Однако без устранения причины анемии, этот способ даст лишь временный эффект. Поэтому переливание эритроцитарной массы не является альтернативой другим методикам и применяется только при наличии показаний. Одним из них является снижение уровня гемоглобина ниже 90 г/л. Переливание проводят при развитии у пациента характерных признаков анемии, среди которых отмечаются:
- Головокружение.
- Потеря сознания.
- Тахикардия.
- Быстрая утомляемость.
- Боль в груди.
- Одышка.
Данный метод лечения анемии также может применяться у пациентов, которые прошли курс химиотерапии или лучевой терапии и у которых отмечается быстрое снижение уровня гемоглобина или эритроцитов.
Применение стимуляторов эритропоэза
Стимуляторы эритропоэза при анемии увеличивают концентрацию гемоглобина и эритроцитов за счет усиления их образования в костном мозге. При сочетании с гемотрансфузиями, данный метод показывает очень хорошие результаты, но при этом имеет и ряд недостатков, которые касаются осложнений. В частности, применение стимуляторов эритропоэза для лечения анемии повышает риск развития тромботических осложнений, который и так является высоким у онкологических пациентов. По данным, полученным в ходе нескольких научных исследований, этот риск увеличивается в 1.4-1.7 раз.
В последнее время обсуждается вопрос о влиянии стимуляторов эритропоэза на выживаемость онкологических пациентов. В частности, специалисты установили, что применение препаратов данной группы при лечении анемии у пациентов с распространенным опухолевым процессом головы и шеи, шейки матки, молочной железы и других диагнозах снижает продолжительность жизни на 10-17%. В связи с этим специалисты предлагают придерживаться следующих правил:
- Если уровень гемоглобина составляет менее 100 г/л и пациент при этом проходит лечение химиопрепаратами, то стимуляторы эритропоэза могут назначаться с целью коррекции анемии и профилактики дальнейшего снижения показателей.
- Если уровень гемоглобина падает до 100 г/л и ниже, но химиотерапия при этом не проводится, то применять стимуляторы эритропоэза не рекомендуется ввиду повышенного риска развития осложнений и снижения продолжительности жизни.
- Во всех остальных случаях применять стимуляторы эритропоэза для лечения анемии у онкологических пациентов следует с осторожностью.
Также на протяжении всего времени лечения важно контролировать динамику лабораторных показателей и при увеличении уровня гемоглобина постепенно снижать дозировку стимуляторов эритропоэза.
Препараты железа при лечении анемии
Препараты железа применяются с целью лечения железодефицитных анемий, которые выявляются у 30-60% онкологический больных. При этом снижение уровня железа может быть связано как с самим опухолевым процессом или проводимым лечением, так и с другими факторами. Например, при назначении стимуляторов эритропоэза, существующего запаса железа в организме становится недостаточно для того, чтобы покрыть потребность, которая возникает в результате активного синтеза гемоглобина в костном мозге.

Для лечения анемии могут применяться как внутривенные, так и пероральные препараты. Второй вариант более удобен для пациента, так как таблетки проще принимать, но при этом данная форма действует медленнее и чаще приводит к осложнениям со стороны ЖКТ. Внутривенное введение позволяет добиться быстрого эффекта, что актуально при проведении химиотерапии.
Таким образом, для лечения анемии современная онкология может предложить различные методы, которые воздействуют на механизмы развития данного симптома. Точный план терапии подбирается индивидуально для каждого пациента, с учетом лабораторных показателей крови, особенностей лечения основного заболевания и других параметров.
Лечение анемии народными способами
Некоторые пациенты по разным причинам отказываются от приема описанных выше препаратов и обращаются к народной медицине. Безусловно, некоторые растения или продукты могут оказывать стимулирующее действие на систему кроветворения. Однако, учитывая основной диагноз и тяжесть анемии, этого действия крайне недостаточно для восстановления уровня гемоглобина и кислородной функции крови. В результате снижается эффективность противоопухолевого лечения, ухудшается прогноз и существенно повышается риск неблагоприятного исхода. Устранить выраженную анемию в домашних условиях при помощи народных методов невозможно. Этим должны заниматься врачи соответствующего профиля, в распоряжении которых имеются современные лекарственные препараты.
Источник
Злокачественная анемия (синоним: пернициозная анемия, болезнь Аддисона — Бирмера) — это эндогенный В12-авитаминоз, вызванный атрофией желез фундального отдела желудка, вырабатывающих гастромукопротеин. Это ведет к нарушению всасывания витамина В12, необходимого для нормального кроветворения, и развитию патологического мегалобластического кроветворения, результатом чего является анемия «пернициозного» типа. Заболевают люди в возрасте после 50 лет.
Характерны нарушения сердечно-сосудистой, нервной, пищеварительной и кроветворной систем. Жалобы больных разнообразны: общая слабость, одышка, сердцебиение, боли в области сердца, отеки ног, ощущение ползанья мурашек в кистях и стопах, расстройство походки, жгучие боли в языке, периодические поносы. Внешний вид больного характеризуется бледностью кожи с лимонно-желтым оттенком. Склеры субиктеричны. Больные не истощены. При исследовании сердечно-сосудистой системы типичны анемические шумы, связанные с понижением вязкости крови и ускорением кровотока. Со стороны органов пищеварения обнаруживаются так называемый гунтеровскпй глоссит (язык ярко-красного цвета, сосочки сглажены), гистаминоустойчивая ахилия (отсутствие свободной соляной кислоты и пепсина в желудочном содержимом). Печень и селезенка увеличены. При значительном снижении числа эритроцитов (ниже 2 млн.) наблюдается лихорадка неправильного типа. Изменения нервной системы связаны с дегенерацией и склерозом задних и боковых столбов спинного мозга (фуникулярный миелоз).
Картина крови: анемия гиперхромного типа, макроциты, мегалоциты, эритроциты с тельцами Жолли, кольцами Кебота, лейкопения, тромбоцитопения (в период обострения).
Лечение проводится витамином В12—100—200 мкг внутримышечно ежедневно или через день до наступления ремиссии. При возникновении анемической комы — срочная госпитализация, переливание крови, лучше эритроцитной массы (150—200 мл). Для предупреждения рецидивов необходима поддерживающая терапия витамином В12. Показано систематическое наблюдение за составом крови у людей со стойкой ахилией, а также перенесших резекцию желудка. Больные, страдающие пернициозной анемией, должны находиться под диспансерным наблюдением (возможно возникновение рака желудка).
1. Злокачественное малокровие (синоним: пернициозная анемия, болезнь Аддисона—Бирмера). Этиология и патогенез. В настоящее время пернициозно-анемический синдром рассматривают как проявление В12-авитаминоза, а болезнь Аддисона— Бирмера — как эндогенный В12-авитаминоз вследствие атрофии фундальных желез, вырабатывающих гастромукопротеин, в результате чего нарушается усвоение витамина В1а, необходимого для нормального, нормобластического, кроветворения, и развивается патологическое, мегалобластическое, кроветворение, приводящее к малокровию «пернициозного» типа.
Клиническая картина (симптомы и признаки). Заболевают лица в возрасте старше 40— 45 лет. Характерны нарушения со стороны сердечно-сосудистой, нервной, пищеварительной и кроветворной систем. Жалобы больных разнообразны: общая слабость, одышка, сердцебиение, боли в области сердца, отеки ног, головокружения, ощущение ползания мурашек в кистях и стопах, расстройство походки, жгучие боли в языке и пищеводе, периодические поносы. Внешний вид больного характеризуется бледностью кожи с лимонно-желтым оттенком. Склеры субиктеричны. Больные не истощены. Лицо одутловато, отечность в области лодыжек и стоп. Отек может достигать больших степеней и сопровождаться асцитом, гидротораксом. Со стороны сердечно-сосудистой системы — появление систолического шума на всех отверстиях сердца и шума «волчка» на луковице яремной вены, что связано с понижением вязкости крови и ускорением кровотока; возможна стенокардия аноксемического характера. При длительной анемии развивается жировое перерождение органов, в том числе сердца («тигровое сердце»), в результате стойкой аноксемии. Со стороны органов пищеварения — так называемый хантеровский (гунтеровский) глоссит, язык чистый, ярко-красного цвета, лишен сосочков. Анализ желудочного сока, как правило, обнаруживает гистаминоустойчивую ахилию. Периодические поносы являются следствием энтерита. Печень увеличена, мягкая; в некоторых случаях — незначительное увеличение селезенки. При значительном падении числа эритроцитов (ниже 2 000 000) наблюдается лихорадка неправильного типа. Изменения со стороны нервной системы связаны с дегенерацией и склерозом задних и боковых столбов спинного мозга (фуникулярный миелоз). Клиническая картина нервного синдрома складывается из сочетаний спастического спинального паралича и табических симптомов (так называемый псевдотабес): спастический парапарез с повышенными и патологическими рефлексами, клонусами, чувство ползания мурашек, онемение конечностей, опоясывающие боли, нарушение вибрационной и глубокой чувствительности, сенсорная атаксия и расстройство функции тазовых органов; реже—бульбарные явления.
Картина крови. Наиболее характерным признаком является анемия гиперхромного типа. Морфологический субстрат гиперхромии — большие, богатые гемоглобином эритроциты — макроциты и мегалоциты (последние достигают 12—14 мк и более). При обострении болезни резко уменьшается количество ретикулоцитов в крови. Появление большого количества ретикулоцитов предвещает близкую ремиссию.
Для обострения болезни характерно появление дегенеративных форм эритроцитов [пойкилоциты, шизоциты, базофильно-пунктированные эритроциты, эритроциты с тельцами Жолли и кольцами Кебота (цветн. таблица, рис. 3)], отдельных мегалобластов (цветн. таблица, рис. 5). Изменения белой крови характеризуются лейкопенией вследствие снижения числа клеток костномозгового происхождения — гранулоцитов. Среди клеток нейтрофильного ряда обнаруживаются гигантские, полисегментоядерные нейтрофилы. Наряду со сдвигом нейтрофилов вправо наблюдается сдвиг влево с появлением юных форм и даже миелоцитов. Количество тромбоцитов в период обострения значительно уменьшено (до 30 000 и менее), однако тромбоцитопения, как правило, не сопровождается геморрагическими явлениями.
Костномозговое кроветворение в период обострения пернициозной анемии совершается по мегалобластическому типу. Мегалобласты являются морфологическим выражением своеобразной «дистрофии» костномозговых клеток в условиях недостаточного подвоза специфического фактора — витамина В12. Под влиянием специфической терапии восстанавливается нормобластическое кроветворение (цветн. таблица, рис. 6).
Симптомы болезни развиваются постепенно. За много лет до заболевания обнаруживается желудочная ахилия. В начале болезни отмечается общая слабость; больные жалуются на головокружение, сердцебиение при малейших физических напряжениях. Затем присоединяются диспептические явления, парестезии; больные обращаются к врачу, будучи уже в состоянии значительной анемизации. Течение болезни характеризуется цикличностью — сменой периодов улучшения и ухудшения. При отсутствии надлежащего лечения рецидивы становятся все более длительными и тяжелыми. До введения в практику печеночной терапии болезнь полностью оправдывала свое название «гибельной» (пернициозной). В период тяжелого рецидива — резчайшей анемизации и бурного прогрессирования всех симптомов болезни — может развиться опасная для жизни кома (coma perniciosum).
Патологическая анатомия. При вскрытии умершего от пернициозной анемии обнаруживается резкое малокровие всех органов, за исключением красного костного мозга; последний, находясь в состоянии гиперплазии, заполняет диафизы костей (цветн. таблица, рис. 7). Отмечается жировая инфильтрация миокарда («тигровое сердце»), почек, печени; в печени, селезенке, костном мозге, лимфатических узлах — гемосидероз (цветн. таблица, рис. 8). Характерны изменения со стороны органов пищеварения: сосочки языка атрофичны, атрофия слизистой оболочки желудка и ее желез — анадения. В задних и боковых столбах спинного мозга отмечаются весьма характерные дегенеративные изменения, обозначаемые как комбинированный склероз, или фуникулярный миелоз.

Рис. 3. Кровь при анемиях: 1 — 4 — эритроциты последнего этапа нормального кроветворения (превращение эритробласта в эритроцит); 5 —9 — распад ядра с образованием телец Жолли в базофильно пунктированных (5, 6) и полихроматофильных (7 — 9) эритроцитах; 10 и 11— тельца Жолли в ортохромных эритроцитах; 12 — хроматиновые пылинки в эритроцитах; 13 — 16 — кольца Кебота в базофильно пунктированных (13, 14) и ортохромных (15, 16) эритроцитах (пернициозная анемия); 17 — 23 — базофильно пунктированные эритроциты при свинцовой анемии; 24 и 25 — полихроматофильные эритроциты (микроцит и макроцит); мегалоцит (26) и пойкилоцит (27) при пернициозной анемии; 28 — нормоцит; 29 — микроциты.

Рис. 5. Кровь при пернициозной анемии (тяжелый рецидив): мегалоциты ортохромные (1) и полихроматофильные (2), эритроциты с кольцами Кебота (3), тельцами Жолли (4) с базофильной пунктацией (5), мегалобласты (6), полисегментоядерный нейтрофил (7), анизоцитоз и пойкилоцитоз (8).

Рис. 6. Костный мозг при пернициозной анемии (начальная ремиссия через 24 часа после введения 30мкг витамина В12): 1 — нормобласты; 2 — метамиелоциты; 3 — палочкоядерный нейтрофил; 4 — эритроцит.

Рис. 7. Миелоидная гиперплазия костного мозга при злокачественной малокровии.
Рис. 8. Гемосидериновая пигментация периферии печеночных долек при пернициозной анемии (реакция на берлинскую лазурь).
Лечение. С 20-х годов для лечения злокачественного малокровия с большим успехом применяется сырая печень, особенно нежирная телячья, пропущенная через мясорубку (200 г в день). Большим достижением в терапии пернициозной анемии явилось изготовление печеночных экстрактов, особенно для парэнтерального введения (камполон, антианемин).Специфичность действия печеночных препаратов при пернициозной анемии обусловлена содержанием в них витамина В12, стимулирующего нормальное созревание эритробластов в костном мозге.
Наибольший эффект достигается при парэнтеральном применении витамина В12. Дневная доза витамина В2—50—100 мкг. Препарат вводится внутримышечно в зависимости от состояния больного — ежедневно или через 1—2 дня. Пероральное применение витамина В12 эффективно только в сочетании с одновременным приемом внутреннего антианемического фактора (гастромукопротеина). В настоящее время получены благоприятные результаты от лечения больных пернициозной анемией путем внутреннего применения препарата муковита (выпускается в виде драже), содержащего витамин В12 (по 200—500 мкг) в сочетании с гастромукопротеином (0,2). Муковит назначается по 3—6 драже в день ежедневно до наступления ретикулоцитарного криза и в дальнейшем 1—2 раза в день до наступления гематологической ремиссии.
Непосредственный эффект антианемической терапии в смысле пополнения крови вновь образованными эритроцитами начинает сказываться с 5—6-го дня лечения подъемом ретикулоцитов до 20—30% и выше («ретикулоцитарный криз»). Вслед за ретикулоцитарным кризом начинает нарастать количество гемоглобина и эритроцитов, которое через 3—4 недели достигает нормального уровня.
Фолиевая кислота, назначаемая внутрь или парэнтерально в дозе 30—60 мг и более (до 120—150 мг) в сутки, вызывает быстрое наступление ремиссии, ноне предотвращает развития фуникулярного миелоза. При фуникулярном миелозе витамин В12 применяется внутримышечно в больших дозах 200—400 мкг, в тяжелых случаях—500— 000 (!) мкг в день] до достижения полной клинической ремиссии. Общая доза витамина В12 в течение 3—4-недельного курса лечения анемии составляет 500—1000 мкг, при фуникулярном миелозе — до 5000— 10 000 мкг и выше.
Эффективность терапии витамином В12 имеет известный предел, по достижении которого рост количественных показателей крови прекращается и анемия приобретает гипохромный характер; в этот период болезни целесообразно применять лечение препаратами железа (по 2—3 г в день, запивать разведенной соляной кислотой).
Вопрос о применении гемотрансфузий при пернициозной анемии в каждом случае решается по показаниям. Безусловным показанием является пернициозная кома, представляющая угрозу жизни вследствие нарастающей гипоксемии. Повторные переливания крови или (лучше) эритроцитной массы (по 250—300 мл) нередко спасают жизнь больных до того момента, когда проявится лечебное действие витамина В12.
Профилактика. Минимальная суточная потребность человека в витамине В12 составляет 3—5 мкг, поэтому с целью профилактики рецидива пернициозной анемии можно рекомендовать вводить в инъекциях 100—200 мкг витамина В12 2 раза в месяц, а весной и осенью (когда чаще бывают рецидивы) — раз в неделю или 10 дней. Следует систематически следить за составом крови у лиц, перенесших обширную резекцию желудка, а также имеющих стойкую ахилию желудка, обеспечивать им полноценную диету, а в случае необходимости применять раннее антианемическое лечение. Следует помнить о том, что пернициозная анемия может быть ранним симптомом рака желудка. Вообще, известно, что больные ахилией желудка и особенно пернициозной анемии чаще других заболевают раком желудка. Поэтому все больные пернициозной анемией должны находиться под диспансерным наблюдением и ежегодно подвергаться контрольному рентгенологическому исследованию желудка.
Источник
