2 3 бфг гемоглобин
Кооперативное взаимодействие
Взаимовлияние протомеров олигомерного белка друг на друга называется кооперативное взаимодействие.
В легких такое взаимодействие субъединиц гемоглобина повышает его сродство к кислороду и ускоряет присоединение кислорода в 300 раз. В тканях идет обратный процесс, сродство снижается и ускорение отдачи кислорода также 300-кратное.
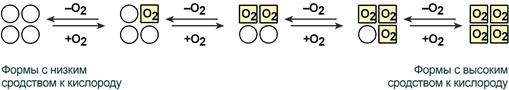
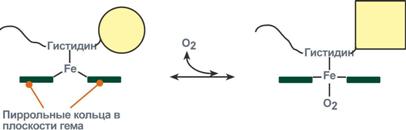
Схема кооперативного взаимодействия субъединиц гемоглобина
Объясняется такой феномен тем, что в легких при присоединении первой молекулы кислорода к железу (за счет 6-й координационной связи) атом железа втягивается в плоскость гема, кислород остается вне плоскости. Это вызывает перемещение участка белковой цепи и изменение конформации первого протомера. Такой измененный протомер влияет на другие субъединицы и облегчает связывание кислорода со второй субъединицей. Это меняет конформацию второй субъединицы, облегчая присоединение последующих молекул кислорода и изменение других протомеров.

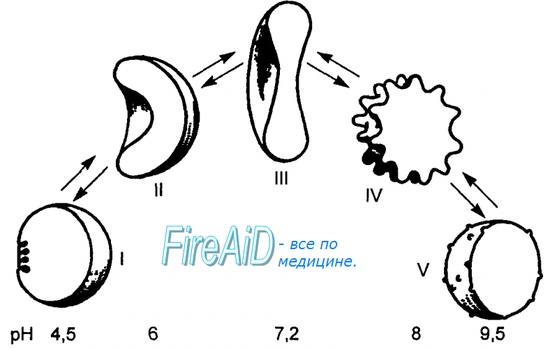
Изменение формы субъединиц гемоглобина
при присоединении и отщеплении кислорода
Дезоксиформа гемоглобина обозначается как Т-форма, напряженная (англ. tense), она обладает существенно более низким сродством к кислороду. Оксигенированная форма, или R-форма (англ. relaxed), обладает высоким сродством к кислороду.
Изменение рН среды
Влияние рН на сродство гемоглобина к кислороду носит название эффекта Бора. При закислении среды сродство снижается, при защелачивании – повышается.
При повышении концентрации протонов (закисление среды) в тканях возрастает освобождение кислорода из оксигемоглобина. В легких после удаления угольной кислоты (в виде СО2) из крови и одновременном увеличении концентрации кислорода высвобождаются ионы Н+ из гемоглобина.
Реакция взаимодействия кислорода с гемоглобином упрощенно имеет вид:

Изменение сродства гемоглобина к кислороду в тканях и в легких при изменении концентрации ионов H+ и О2 обусловлено конформационными перестройками глобиновой части молекулы. В тканях молекула О2 отрывается от железа и ионы водорода присоединяются к остаткам гистидина (глобиновой части), образуя восстановленный гемоглобин (H-Hb) с низким сродством к кислороду. В легких поступающий в больших количествах кислород “вытесняет” ион водорода из связи с остатком гистидина гемоглобиновой молекулы.
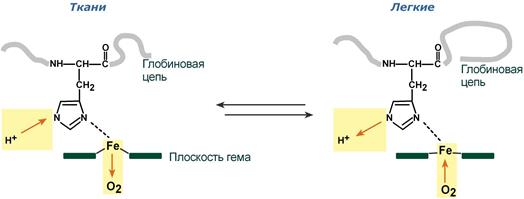
Механизм эффекта Бора
Роль 2,3-дифосфоглицерата
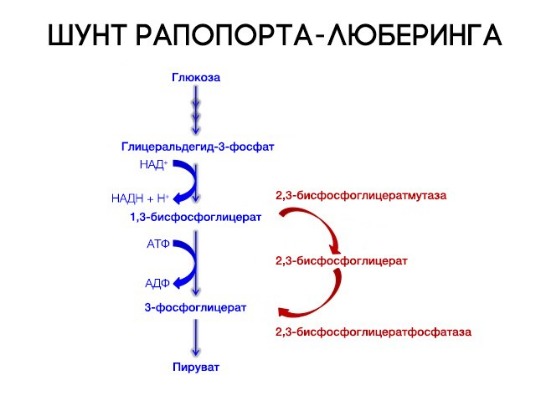
2,3-Дифосфоглицерат образуется в эритроцитах из 1,3-дифосфоглицерата, промежуточного метаболита гликолиза, в реакциях, получивших название шунт Раппопорта.
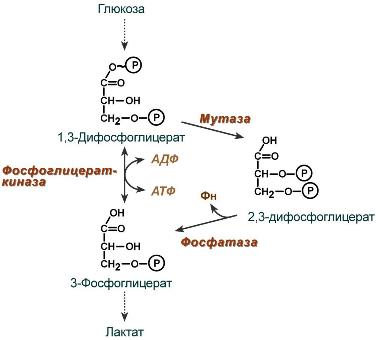
Реакции шунта Раппопорта
2,3-Дифосфоглицерат располагается в центральной полости тетрамера дезоксигемоглобина и связывается с β-цепями, образуя поперечный солевой мостик между атомами кислорода 2,3-дифосфоглицерата и аминогруппами концевого валина обеих β-цепей, также аминогруппами радикалов лизина и гистидина.
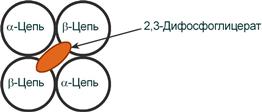
Расположение 2,3-дифосфоглицерата в гемоглобине
Функция 2,3-дифосфоглицерата заключается в снижении сродства гемоглобина к кислороду, что имеет особенное значение при подъеме на высоту и при нехватке кислорода во вдыхаемом воздухе. В этих условиях связывание кислорода с гемоглобином в легких не нарушается, так как концентрация его относительно высока. Однако в тканях за счет 2,3-дифосфоглицерата отдача кислорода возрастает в 2 раза.
Оглавление темы “Вентиляция легких. Перфузия легких кровью.”: Сродство гемоглобина к кислороду. Изменение сродства гемоглобина к кислороду. Эффект Бора.Молекула гемоглобина может находиться в двух формах — напряженной и расслабленной. Расслабленная форма гемоглобина имеет свойство насыщаться кислородом в 70 раз быстрее, чем напряженная. Изменение фракций напряженной и расслабленной формы в общем количестве гемоглобина в крови обусловливает S-образный вид кривой диссоциации оксигемоглобина, а следовательно, так называемое сродство гемоглобина к кислороду. Если вероятность перехода от напряженной формы гемоглобина к расслабленной больше, то возрастает сродство гемоглобина к кислороду, и наоборот. Вероятность образования указанных фракций гемоглобина изменяется в большую или меньшую сторону под влиянием нескольких факторов. Основной фактор — это связывание кислорода с геминовой фуппой молекулы гемоглобина. При этом чем больше геминовых фупп гемоглобина связывают кислород в эритроцитах, тем более легким становится переход молекулы гемоглобина к расслабленной форме и тем выше их сродство к кислороду. Поэтому при низком Р02, что имеет место в метаболически активных тканях, сродство гемоглобина к кислороду ниже, а при высоком Р02 — выше. Как только гемоглобин захватывает кислород, повышается его сродство к кислороду и молекула гемоглобина становится насыщенной при связывании с четырьмя молекулами кислорода.
Когда эритроциты, содержащие гемоглобин, достигают тканей, то кислород из эритроцитов диффундирует в клетки. В мышцах он поступает в своеобразного депо кислорода — в молекулы миоглобина, из которого кислород используется в биологическом окислении мышц. Диффузия кислорода из гемоглобина эритроцитов в ткани обусловлена низким Р02 в тканях — 35 мм рт. ст. Внутри клеток тканей напряжение кислорода, необходимое для поддержания нормального метаболизма, составляет еще меньшую величину — не более 1 кПа. Поэтому кислород путем диффузии из капилляров достигает метаболически активных клеток. Некоторые ткани приспособлены к низкому содержанию Р02 в капиллярах крови, что компенсируется высокой плотностью капилляров на единицу объема тканей. Например, в скелетной и сердечной мышцах Р02 в капиллярах может снизиться чрезвычайно быстро во время сокращения. В мышечных клетках содержится белок миоглобин, который имеет более высокое сродство к кислороду, чем гемоглобин. Миоглобин интенсивно насыщается кислородом и способствует его диффузии из крови в скелетную и сердечную мышцы, где он обусловливает процессы биологического окисления. Эти ткани способны экстрагировать до 70 % кислорода из крови, проходящей через них, что обусловлено снижением сродства гемоглобина к кислороду под влиянием температуры тканей и рН. Эффект рН и температуры на сродство гемоглобина к кислороду. Молекулы гемоглобина способны реагировать с ионами водорода, в результате этой реакции происходит снижение сродства гемоглобина к кислороду. При насыщении гемоглобина менее 100 % низкое рН понижает связывание кислорода с гемоглобином — кривая диссоциации оксигемоглобина смещается вправо по оси х. Это изменение свойства гемоглобина под влиянием ионов водорода называется эффектом Бора. Метаболически активные ткани продуцируют кислоты, такую как молочная, и С02. Если рН плазмы крови снижается от 7,4 в норме до 7,2, что имеет место при сокращении мыщц, то концентрация кислорода в ней будет возрастать вследствие эффекта Бора. Например, при постоянном рН 7,4 кровь отдавала бы порядка 45 % кислорода, т. е. насыщение гемоглобина кислородом снижалось до 55 %. Однако когда рН снижается до 7,2, кривая диссоциации смещается по оси х вправо. В результате насыщение гемоглобина кислородом падает до 40 %, т. е. кровь может отдавать в тканях до 60 % кислорода, что на 1/з больше, чем при постоянном рН.
Метаболически активные ткани повышают продукцию тепла. Повышение температуры тканей при физической работе изменяет соотношение фракций гемоглобина в эритроцитах и вызывает смещение кривой диссоциации оксигемоглобина вправо вдоль оси х. В результате большее количество кислорода будет освобождаться из гемоглобина эритроцитов и поступать в ткани. Эффект 2,3-дифосфоглицерата (2,3-ДФГ) на сродство гемоглобина к кислороду. При некоторых физиологических состояниях, например при понижении Р02 в крови ниже нормы (гипоксия) в результате пребывания человека на большой высоте над уровнем моря, снабжение тканей кислородом становится недостаточным. При гипоксии может понижаться сродство гемоглобина к кислороду вследствие увеличения содержания в эритроцитах 2,3-ДФГ. В отличие от эффекта Бора, уменьшение сродства гемоглобина к кислороду под влиянием 2,3-ДФГ не является обратимым в капиллярах легких. Однако при движении крови через капилляры легких эффект 2,3-ДФГ на снижение образования оксигемоглобина в эритроцитах (плоская часть кривой диссоциации оксигемоглобина) выражен в меньшей степени, чем отдача кислорода под влиянием 2,3-ДФГ в тканях (наклонная часть кривой), что обусловливает нормальное кислородное снабжение тканей. – Также рекомендуем “Углекислый газ. Транспорт углекислого газа.” |
Фетальный гемоглобин
С фетальным гемоглобином (НbF) или гемоглобином плода 2,3-БФГ связывается менее прочно, чем с гемоглобином взрослого человека (НbА). это объясняется тем, что в аллостерическом центре γ-цепей (β-подобный) для связывания 2,3-БФГ находится не Гис 143, а Сер, который не участвует в образовании ионных связей, поэтому HbF стабилизируется бифосфоглицератом в меньшей степени и обладает большим сродством к О2, чем НbА. Такое свойство НbF объяснимо с физиологической точки зрения, т. к. оно обеспечивает направленный транспорт О2 из крови матери в кровь плода.
Блок обучающих заданий.
Тема заданий: Сложные белки. Гемопротеины.
Задание Заполните таблицу: «Классификация сложных белков »
| Классы | Небелковый компонент | |
| Ионы металлов | ||
| Н3РО4 | ||
| ФАД, ФМН | ||
| Нуклеопротеины | ||
| Гемопротеины | ||
| Липопротеины | ||
| Моносахариды,олигосахариды |
Задание. Подберите к белкам (1-8) соответствующий класс (А,Б,В)
1.Рецепторы мембран
2.Иммуноглобулины А. Нуклеопротеины
3.РНК-протеин
4. Каталаза Б. Гемопротеины
5. Миоглобин
6. Гемоглобин В. Гликопротеины
7. Цитохромы
8. Хлорофилл
Задание. Знайте сравнительную характеристику структуры и свойств гемоглобина и миоглобина. Для этого обратите внимание на следующее:
а) оба белка являются гемопротеинами и способны обратимо связывать кислород. Гемоглобин присоединяет кислород из альвеолярного воздуха и с кровотоком доставляет его в ткани, миоглобин акцептирует кислород, доставленный гемоглобином, запасает кислород в тканях и транспортирует внутри клетки в митохондрии.
б) гемоглобин в отличие от миоглобина является олигомерным белком, его молекула содержит 4 субъединицы (a2b2), т.е. Нb обладает более высоким конформационным уровнем.
в) функционирование гемоглобина, в отличие от миоглобина, регулируется компонентами внутренней среды (Н+, СО2, 2,3-БФГ)
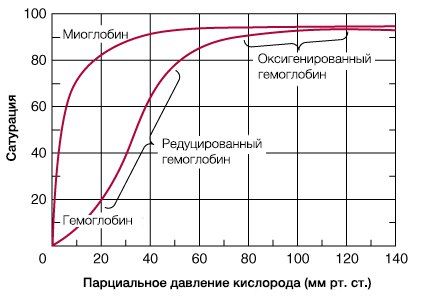
Задание. Рассмотрите кривые насыщения кислородом для миоглобина и гемоглобина. На оси абсцисс отмечены значения рО2, характерные для работающей мышцы и для альвеол легких.
а) обратите внимание на 2 отличия: во-первых при любом значении рО2 насыщение миоглобина кислородом выше (А), чем НЬ (Б), во-вторых кривая диссоциации кислорода миоглобином имеет форму гиперболы, а кривая диссоциации НЬ – S – образную, которая отражает кооперативные изменения в молекуле НЬ при взаимодействии с кислородом.
Кривые насыщения (диссоциации) кислорода для миоглобина и гемоглобина.
При возрастании давления кислорода крутизна кривой увеличивается, отражая увеличение сродства к кислороду частично оксигенированного гемоглобина.
б) при каком парциальном давлении кислорода Мb и Нb имеют 50% насыщения
( Р50 ) ?
в) по графику определите степень насышения Нb и Мb в условиях А, Б и В
| Условия | Гемоглобин (НЬ) | Миоглобин ( МЬ) |
| А. Артериальная кровь, рО2 ~ 100 | ||
| Б. Капилляры мышечной ткани в покое, рО2 ~ 40 | ||
| В. Капилляры активно работающей мышцы, рО2 ~ 10 |
Сделайте заключение о том, какой из акцепторов кислорода обладает большим сродством к кислороду?
Ответ . . . . . .
Ответьте на вопрос: Какой из акцепторов кислорода очень эффективно отдает кислород в тканях.?
Ответ . . . . .
Задание. Сравните две формы Нb (дезоксигемоглобин и оксигемоглобин), правильно расположив в таблице следующие их характеристики: жесткая структура, напряженная структура, расслабленная структура, мягкая структура, Т-форма, R-форма, высокое сродство к О2 , низкое сродство к О2
| Дезоксигемоглобин | Оксигемоглобин | |
| Структура | ||
| Обозначение | ||
| Положение атома железа относительно плоскости гема | ||
| Сродство к О2 |
Задание 8. Рассмотрите схему, иллюстрирующую эффект Бора
а) закончите фразу : « Эффект Бора – это влияние . . . . .
на связывание . . . гемоглобином.
б) укажите на схеме 1) – локализацию процессов А и Б —-
2) – формы НЬ ( С — . . . и Д — . . . )
3) – фермент Е
А С Б
НЬ 4О2
О2 4О2
2НСО3 + 2Н+ 2Н++ 2НСО3-
Ї Ї
2Н2СО3 2Н2СО3
Ї Е – ? Ї Е – ?
2CО2+2Н2О 2С2CО2 + 2Н2О
СО2
НЬ• 2Н+
СО2
? Д катаболизм
Решите задачу: Представление об аллостерическом взаимодействии 2,3-бифосфоглицерата (2,3-БФГ) с гемоглобином.
Рассмотрите рисунок: Связь 2,3-БФГ с дезоксигемоглобином.
О——————–Е ГИС (2) В аллостерическом центре
│
О = С О———-Е ЛИЗ (82) b-цепей НЬ три Е заряжен-
│ │
С – О – Р = О ные группы
│ │
Н С Н О
│
О
│
Р
║
-О О О- ————–Е ГИС (143)
Получите представление о физиологической роль 2,3-БФГ.
а) рассмотрите рисунок и обратите внимание на то что 2,3БФГ снижает сродство Нb к кислороду в 26 раз : Р50 для Нb без БФГ – 1 мм рт ст
Р50 для Нb с БФГ – 26 мм рт ст
Из этого следует, что 2,3БФГ играет очень важную роль в физиологии дыхания. В отсутствии 2,3БФГ гемоглобин проходя через капилляры тканей (рСО2 ~ 26 мм рт ст) высвобождал бы очень мало кислорода.
Некоторых адаптивные механизмы, включающиеся при нарушении снабжения тканей кислородом.
1. Больные, у которых затруднено поступление воздуха в альвеолы. В результате этого рО2 в артериальной крови составляет 50 мм рт ст, т.е. вдвое ниже нормы. Однако, при этом происходит компенсаторный сдвиг в насыщении кислородом, обусловленный изменением концентрации БФГ в периферических тканях в сторону . . При новом содержании БФГ, Р50 НЬ составляет уже не 26, а 31 мм рт ст и сродство НЬ к кислороду при этом . . . , а доставка кислорода в ткани . . . . .
2. Адаптация к высоте. Когда человек поднимается на высоту 5000 м, насыщение артериальной крови кислородом уменьшается, Р50 снижается. Но постепенно (через 2-3 дня ) концентрация БФГ возрастает с 4,5 до 7,0 ммоль и сродство НЬ к кислороду соответственно . . .В результате этого в капиллярной сети периферических тканей кислорода высвобождается . . . . . . При спуске с гор парциальное давление кислорода в атмосферном воздухе повышается и концентрация БФГ возврашается к исходным величинам.
3. Гемоглобин плода НbF, характеризуется более высоким сродством к кислороду, по сравнению с НbА (взрослого человека). Это отличие создает оптимальные условия для транспорта кислорода из крови матери в кровь плода. НbF оксигенируется за счет НbА, находящегося по другую сторону трансплацентарного барьера в кровеносной системе плаценты.
Дополните фразу : НbF связывает 2,3БФГ (слабее,
сильнее) чем НbА и, следовательно, обладает более высоким
сродством к О2.
Рассмотрите график и укажите, какому типу гемоглобина (А или
F) соответствует каждая кривая.
Задача. Впервые поднявшись высоко в горы, пациент испытал приступ болей в конечностях, схожий с кризами, периодически испытываемыми его братом, больным серповидно-клеточной анемией. Ранее подобных проявлений у пациента не отмечалось. Объясните возможные биохимические механизмы, лежащие в основе данного состояния.
Ответ: У гетерозиготных носителей серповидно-клеточности чаще всего патология не проявляется. Однако в случае резкой гипоксии и дегидратации, дезоксигенированная форма HbS полимеризуется, формируя серповидно-клеточные эритроциты.
Одним из самых сложных процессов, что происходят в организме человека, несомненно, является дыхание. И сложность эта не только в танце легких, благодаря которому человек получает кислород, но и в процессах, с помощью которых этот кислород проникает дальше, в ткани, где превращается в углекислый газ, что отправляется в обратное путешествие. О данных процессах и пойдет речь далее.
Итак, приступим. Человек делает вдох, иии… Далеко не весь кислород поступает в легкие, а затем и в кровь. Часть вдыхаемого воздуха остается в так называемом мертвом пространстве. Мертвое пространство, в свою очередь, делится на анатомическое (дыхательные пути), в котором остается около 30 % вдыхаемого воздуха, и функциональное (вентилируемые, но по каким-то причинам не перфузируемые альвеолы).
Ухудшение альвеолярного газообмена может происходить при неглубоком и частом дыхании (причиной может стать перелом ребер, паралич дыхательной мускулатуры различного генеза и др.), а также при увеличении мертвого пространства, вызванном разнообразными причинами (нарушение перфузии альвеол в результате воспалительных заболеваний легких, удаление доли или целого легкого и др.), при снижении скорости кровотока по альвеолярным капиллярам (ТЭЛА, инфаркт легкого), при наличии диффузионного барьера (отек легких) и в результате ослабления альвеолярной вентиляции при обтурации просвета бронха. Газообмен между легкими и кровью происходит путем диффузии в соответствии с законом Фика. В легочных капиллярах она происходит за счет разности парциальных давлений в альвеолах и эритроцитах.
В альвеолах парциальное давление кислорода значительно превышает таковое для углекислого газа и составляет примерно 13,3 кПа (100 мм рт. ст.) и 5,3 кПа (40 мм рт. ст.) соответственно. Альвеолы омываются приносимой легочными артериями венозной кровью, в которой соотношение парциальных давлений этих двух газов обратно пропорционально и составляет приблизительно 5,3 кПа (40 мм рт. ст.) для кислорода и 6,1 кПа (46 мм рт. ст.) для углекислого газа. В среднем разница парциальных давлений составляет около 8 кПа (60 мм рт. ст.) для кислорода и около 0,8 кПа для углекислого газа.
Как уже было сказано выше, кислород путем диффузии проникает в кровь легочных капилляров. Диффузионное расстояние для кислорода при этом составляет 1–2 мкм, то есть именно на такое расстояние он проникает внутрь капилляра. Обмен крови в легочном капилляре происходит примерно за 0,75 секунды, но этого времени хватает на то, чтобы парциальные давления в альвеолах и в крови пришли в равновесие.
Кровь, в которой показатели парциального давления для кислорода и углекислого газа примерно равны таковым в альвеолах, называется артериализированной. Однако за счет наличия в легких артериовенозных шунтов и притока венозной крови из бронхиальных вен такой она остается недолго. В результате парциальное давление кислорода в аорте составляет примерно 12,0 кПа (как уже было сказано выше, парциальное давление в артериализированной крови равно таковому в альвеолах и составляет 13,3 кПа), а давление углекислого газа меняется незначительно и не приводит к затруднению его диффузии из крови в альвеолы.
Но кислород непосредственно в ткани попадает лишь в крайне незначительных количествах: для свободного перемещения по организму ему необходим транспортер. Эту функцию выполняет содержащийся в эритроцитах белок — гемоглобин. Гемоглобин существует в оксигенированной и неоксигенированной формах. В дезокси-гемоглобине железо находится на уровне порфиринового кольца и стабилизируется электростатическими силами, что обеспечивает поддержание всей структуры. Появившись, кислород начинает «тянуть» за железо, которое переносится на проксимальный гистидин на другом конце полипептидной цепи и меняет структуру всего протеина.
В результате гемоглобин переходит в оксигенированную форму, альфа- и бета-цепи при этом поворачиваются относительно друг друга на 15 градусов, облегчая присоединение остальных молекул кислорода. В итоге каждый из четырех содержащихся в нем атомов двухвалентного железа обратимо связывается с молекулой кислорода, что превращает молекулу гемоглобина в оксигемоглобин. По сравнению с миоглобином гемоглобин имеет низкое сродство к кислороду, однако оно не статично. Так, миоглобин может связывать кислород только одним участком, поэтому кривая его связывания — гипербола. Кривая связывания гемоглобина с кислородом имеет S-образную форму, демонстрируя, что при его связывании с первой молекулой кислорода гемоглобин имеет очень низкое сродство к кислороду, но при связывании последующих молекул кислорода сродство остальных его субъединиц к нему значительно увеличивается и в конечном счете повышается примерно в 500 раз.
При этом альфа-цепи связывают кислород легче, чем бета-цепи. Этот процесс назван кооперативным взаимодействием. По мере снижения парциального давления кислорода в крови происходит его высвобождение из гемоглобина и поступление в ткани. Например, парциальное давление кислорода в работающих мышцах составляет всего 26 мм рт. ст, и при прохождении эритроцитов через капилляры, кровоснабжающие мышцы, происходит высвобождение и поступление в мышечные клетки примерно ⅓ всего переносимого гемоглобином кислорода. При повышении температуры тела также возрастает потребность в кислороде, что, в свою очередь, стимулирует высвобождение и поступление его в ткани. При снижении температуры, напротив, развивается гипоксия тканей, способствующая компенсаторному увеличению сродства гемоглобина к кислороду.
Гемоглобин также осуществляет перенос от тканей к легким продуктов тканевого дыхания — углекислого газа и ионов водорода. В ходе окислительных процессов в клетке выделяется углекислый газ, в результате гидратации которого образуются ионы водорода, что, в свою очередь, приводит к снижению рН. Давно известно, что снижение рН и повышение концентрации углекислого газа в крови оказывает сильное влияние на способность гемоглобина связывать кислород.
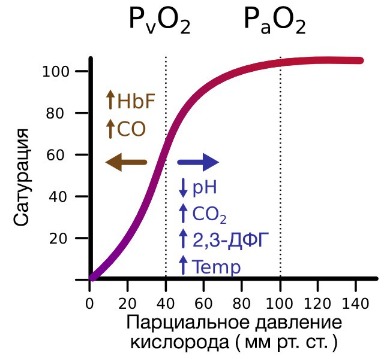
В периферических сосудах показатели рН низкие, и по мере связывания гемоглобина с ионами водорода и углекислым газом происходит снижение его сродства к кислороду. Это влияние величины рН и концентрации углекислого газа на способность гемоглобина связывать кислород называют эффектом Бора.
Обратная ситуация имеет место в альвеолярных капиллярах, где присоединение кислорода к гемоглобину превращает тот в более сильную кислоту.
При этом сродство гемоглобина к углекислому газу снижается, а повышение кислотности гемоглобина приводит к высвобождению излишка ионов водорода и образованию в крови из бикарбоната угольной кислоты, которая затем распадается на воду и углекислый газ. В обоих случаях углекислый газ из крови поступает в альвеолы, а затем в атмосферу. Данный процесс назван эффектом Холдейна. Стоит отметить, что важную роль в образовании углекислого газа в эритроцитах играет ион хлора, поступающий в плазму крови в обмен на бикарбонат при участии белка-переносчика АЕ1. Данный процесс в англоязычной литературе получил название «Chloride shift» или «перенос Хамбургера».
На сродство гемоглобина к кислороду оказывает влияние и присутствующее в эритроцитах вещество, получившее название 2,3-бисфосфоглицерат (БФГ). Его образование — своего рода побочная реакция анаэробного гликолиза, происходящего в эритроцитах в ходе ферментативного превращения глюкозы в пируват под действием фермента бифосфоглицератмутазы. БФГ способен самостоятельно связываться с неоксигенированной формой гемоглобина, образуя солевой мостик между двумя его бета-субъединицами и снижая сродство к кислороду.
При этом гемоглобин способен связать только одну молекулу БФГ, а при присоединении кислорода БФГ вытесняется из полости. В обычных условиях в эритроцитах крови содержится достаточно большое количество БФГ, которое может увеличиваться в условиях гипоксии (например, у дайверов при погружении на глубину), а также при восхождении на большую высоту. В первые часы подъема концентрация БФГ в эритроцитах будет возрастать, а сродство кислороду снижаться. Но на большой высоте парциальное давление будет значительно ниже такового на уровне моря, а значит, оно снизится и в тканях. При этом БФГ будет облегчать передачу кислорода от гемоглобина к тканям.
Некоторые вещества способны прочно связываться с гемоглобином или же вовсе менять его структуру. Одним из них является угарный газ, чье сродство к гемоглобину в 200 раз превышает таковое для кислорода. Отравления угарным газом часто происходят в помещениях с печным отоплением, при пожарах и авариях на производстве. Со временем кислород вытесняет угарный газ из гемоглобина, и в легких случаях пациенты помещаются под наблюдение и получают ингаляции с увлажненным кислородом. Необходимой мерой при тяжелых отравлениях угарным газом является переливание эритроцитарной массы.
К веществам, способным изменять структуру гемоглобина, относятся метгемоглобинобразователи — соединения, способные окислять двухвалентное железо в геме до трехвалентного. К ним относятся нитриты, нитраты, некоторые местные анестетики, аминофенолы, хлораты, примахин и некоторые сульфаниламиды. Состояние, характеризующееся появлением в крови окисленного гемоглобина, называют метгемоглобинемией. При высокой метгемоглобинемии капля крови, помещенная на фильтровальную бумагу, имеет характерный коричневый цвет, а при пропускании кислорода через пробирку с такой кровью ее цвет не меняется. Метгемоглобинемия выше 70 % от общего содержания гемоглобина часто приводит к гибели пациента еще до момента постановки диагноза.
Источники:
- Harrison’s hematology and oncology Longo, Dan L (Dan Louis), Third edition. New York : McGraw-Hill Education Medical, 2017.
- Наглядная физиология, С. Зильбернагль, А. Деспопулос, 2013.
- Ленинджер А. Основы биохимии: В 3-х т. Т. 1. /Д. Нельсон, М. Кокс ; Пер. с англ.-М.: БИНОМ: Лаборатория знаний, 2011.- 694 с.
Нашли опечатку? Выделите фрагмент и нажмите Ctrl+Enter.