Анемии вследствие нарушения эритропоэза
Анемии вследствие нарушения кровообразования представлены так называемыми дефицитными анемиями, возникающими при недостатке железа, витамина В12, фолиевой кислоты, гипо- и апластическими анемиями.
Анемии вследствие недостатка железа или железодефицитные анемии. Они могут развиваться прежде всего при недостаточном поступлении железа с пищей (алиментарная железодефицитная анемия детского возраста). Они возникают также при экзогенной недостаточности железа в связи с повышенными запросами организма у беременных и кормящих женщин, при некоторых инфекционных заболеваниях, у девушек при «бледной немочи» (ювенильный хлороз). В основе железодефицитной анемии может лежать и резорбционная недостаточность железа, встречающаяся при заболеваниях желудочно-кишечного тракта, а также после резекции желудка (агастрическая анемия) или кишечника (анэнтеральная анемия). Анемии вследствие недостатка железа – гипохромные.
В последнее время выделяют анемии, связанные с нарушением синтеза или утилизации порфиринов. Среди них различают наследственные (Х-сцепленные) и приобретенные (свинцовая интоксикация).
Анемия вследствие недостатка витамина B 12 и/или фолиевой кислоты. Их характеризует извращение эритропоэза. Это мегалобластические гиперхромные анемии. Витамин B 12 и фолиевая кислота являются необходимыми факторами гемопоэза.
Витамин B12 поступает в организм через желудочно-кишечный тракт (внешний фактор). Всасывание витамина B 12 в желудке возможно только в присутствии внутреннего фактора Касла, или гастромукопротеина, который вырабатывается добавочными клетками фундальных желез желудка. Соединение витамина Bi2 с гастромукопротеином ведет к образованию белково-витаминного комплекса, который всасывается слизистой оболочкой желудка и тонкой кишки, откладывается в печени и активирует фолиевую кислоту. Поступление витамина Bi2 и активированной фолиевой кислоты в костный мозг определяет нормальный гормональный эритропоэз, стимулирует созревание клеток красной крови.
Эндогенная недостаточность витамина B 12 и/или фолиевой кислоты вследствие выпадения секреции гастромукопротеина и нарушенной ассимиляции пищевого витамина B 12 ведет к развитию пернициозной и пернициозоподобных анемий.
Пернициозная анемия впервые описана в 1855 г. Аддисоном, в 1868 г. ее описал Бирмер (анемия Аддисона – Бирмера). Заболевание развивается обычно в зрелом возрасте (после 40 лет). Долгое время, до установления роли витамина В 12, фолиевой кислоты и гастромукопротеина в патогенезе пернициозной анемии, она протекала злокачественно (злокачественная анемия) и, как правило, заканчивалась смертью больных.
Этиология и патогенез. Развитие болезни обусловлено выпадением секреции гастромукопротеина в связи с наследственной неполноценностью фундальных желез желудка, завершающейся их преждевременной инволюцией (описаны случаи семейной пернициозной анемии). Большое значение имеют аутоиммунные процессы – появление трех типов аутоантител: первые блокируют соединение витамина В 12 с гастромукопротеином, вторые – гастромукопротеин или комплекс гастромукопротеин – витамин B 12, третьи – париетальные клетки. Эти антитела встречаются у 50-90% больных пернициозной анемией. В результате блокады гастромукопротеина и витамина Bi2 наступает извращение кроветворения, эритропоэз совершается по мегалобластическому типу, причем процессы кроворазрушения преобладают над процессами кроветворения. Распад мегалобластов и мегалоцитов происходит прежде всего в костном мозге и очагах внекостномозгового кроветворения еще до выхода клеток в периферическую кровь. Поэтому эритрофагоцитоз при анемии Аддисона – Бирмера особенно хорошо выражен в костном мозге, значительная часть гемоглобиногенных пигментов (порфирин, гематин) не используется, а только циркулирует в крови и выводится из организма.
С разрушением элементов красной крови связан общий гемосидероз, а с нарастающей гипоксией – жировая дистрофия паренхиматозных органов и нередко общее ожирение. Недостаток витамина B 12 ведет к изменениям образования миелина в спинном мозге.
Патологическая анатомия. При наружном осмотре трупа определяются бледность кожных покровов (кожа с лимонно-желтым оттенком), желтушность склер. Подкожный жировой слой развит обычно хорошо. Трупные гипостазы не выражены. Количество крови в сердце и крупных сосудах уменьшено, кровь водянистая. В коже, слизистых и серозных оболочках видны точечные кровоизлияния. Внутренние органы, особенно селезенка, печень, почки, на разрезе ржавого вида (гемосидероз). Наиболее ярко изменения выражены в желудочно-кишечном тракте, костном и спинном мозге.
В желудочно-кишечном тракте имеются атрофические изменения. Язык гладкий, блестящий, как бы полированный, покрыт красными пятнами. При микроскопическом исследовании находят резкую атрофию эпителия и лимфоидных фолликулов, диффузную инфильтрацию подэпителиальнои ткани лимфоидными и плазматическими клетками. Эти изменения обозначают как гунтеровский глоссит (по имени впервые описавшего эти изменения Гунтера). Слизистая оболочка желудка, особенно фундальной части, истонченная, гладкая, лишена складок. Железы уменьшены и расположены на значительном расстоянии друг от друга; эпителий их атрофичен, сохранны лишь главные клетки. Лимфоидные фолликулы также атрофичны. Эти изменения слизистой оболочки желудка завершаются склерозом. В слизистой оболочке кишечника развиваются такие же атрофические изменения.
Печень увеличена, плотная, на разрезе имеет буроржавый оттенок (гемосидероз) . Отложения железа обнаруживают не только в звездчатых ретикулоэндотелиоцитах, но и в гепатоцитах. Поджелудочная железа плотная, склерозирована.
Костный мозг плоских костей малиново-красный, сочный; в трубчатых костях он имеет вид малинового желе. В гигтерплазированном костном мозге преобладают незрелые формы эритропоэза – эритробласты, нормобласты и особенно мегалобласты, которые находятся и в периферической крови. Эти элементы крови подвергаются фагоцитозу макрофагами (эритрофагия) не только костного мозга, но и селезенки, печени, лимфатических узлов, что обусловливает развитие общего гемосидероза.
Селезенка увеличена, но незначительно, дряблая, капсула морщинистая, ткань розово-красная, с ржавым оттенком. При гистологическом исследовании обнаруживают атрофичные фолликулы со слабовыраженными зародышевыми центрами, а в красной пульпе – очаги экстрамедуллярного кроветворения и большое число сидерофагов.
Лимфатические узлы не увеличены, мягкие, с очагами экстрамедуллярного кроветворения, иногда на значительном протяжении вытесняющими лимфоидную ткань.
В спинном мозге, особенно в задних и боковых столбах, выражен распад миелина и осевых цилиндров.
Этот процесс называют фуникулярным миелозом. Иногда в спинном мозге появляются очаги ишемии и размягчения. Такие же изменения редко наблюдаются в коре головного мозга.
Течение анемии Аддисона – Бирмера обычно прогрессирующее, но периоды обострения болезни чередуются с ремиссиями. За последние годы как клиническая, так и морфологическая картина пернициозной анемии благодаря лечению препаратами витамина B 12 и фолиевой кислоты резко изменилась. Летальные случаи наблюдаются редко.
С дефицитом гастромукопротеина связано развитие пернициозоподобных В 12-дефицитных анемий при раке, лимфогранулематозе, сифилисе, полипозе, коррозивном гастрите и других патологических процессах в желудке. При этих патологических процессах в желудке вторично возникают воспалительные, дистрофические и атрофические изменения в железах дна с нарушением секреции гастромукопротеина и эндогенной недостаточностью витамина B 12. Такой же генез имеет пернициозоподобная анемия, возникающая спустя несколько лет после удаления желудка (агастрическая В-дефицитная анемия).
Нарушение всасывания витамина B 12 и/или фолиевой кислоты в кишечнике лежит в основе ряда В 12-(фолиево)дефицитных анемий. Это глистная – дифиллоботриозная – анемия при инвазии широким лентецом, анемия при спру – спру-анемия, а также анемия после резекции тонкой кишки – анэнтеральная В 12-(фолиево)дефицитная анемия.
Причиной развития В12-(фолиево)дефицитных анемий может быть также экзогенная недостаточность витамина В12 и/или фолиевой кислоты алиментарной природы, например у детей при вскармливании козьим молоком (алиментарная анемия) или при лечении некоторыми лекарственными препаратами (медикаментозная анемия).
Гипо- и апластические анемии. Эти анемии являются следствием глубокого угнетения кроветворения, особенно молодых элементов гемопоэза.
Причиной развития таких анемий могут быть как эндогенные, так и экзогенные факторы. Среди эндогенных факторов большое место занимают наследственные, с которыми связано развитие семейной апластической анемии (Фанкони) и гипопластической анемии (Эрлиха).
Семейная апластическая анемия (Фанкони) встречается очень редко, обычно у детей, чаще у нескольких членов семьи. Тяжелая хроническая гиперхромная анемия характеризуется мегалоцитозом, ретикулоцитозом и микроцитозом, лейко- и тромбопениеи, геморрагиями, аплазией костного мозга. Она нередко сочетается с пороками развития.
Гипопластическая анемия (Эрлиха) имеет острое и подострое течение, характеризуется прогрессирующей гибелью активного костного мозга, сопровождается кровоточивостью, иногда присоединением сепсиса. В крови наблюдается уменьшение числа всех форменных элементов крови без признаков регенерации.
Для эндогенных гипо- и апластических анемий наиболее характерно поражение эритробластического ростка крови (эритрона) с потерей способности костного мозга к регенерации. Происходит гибель активного костного мозга плоских и трубчатых костей, он замещается желтым, жировым. Среди массы жира в костном мозге встречаются единичные кроветворные клетки. В случаях полного опустошения костного мозга и замещения его жиром говорят о «чахотке» костного мозга – панмиелофтизе.
В качестве экзогенных факторов, ведущих к развитию гипопластиче-ских и апластических анемий, могут выступать лучевая энергия (радиационная анемия), токсические вещества (токсическая, например, бензольная анемия), такие лекарственные препараты, как цитостатические, амидопирин, атофан, барбитураты и др. (медикаментозная анемия).
Нарушения системы эритроцитов. Анемии.
Механизмы развития
Ключевые понятия
Эритроцитозы (греч. erythros – красный + kytos – клетка + osis) – патологическая реакция, характеризующаяся повышением в крови содержания гемоглобина и количества эритроцитов.
Анемия (anaemia; греч. an – частица отрицания, haima – кровь; син. малокровие) – типовой патологический процесс, существенным проявлением которого является уменьшение количества гемоглобина, эритроцитов и изменение их функции и структуры.
Физиологические регенеративные изменения эритроцитов – качественные изменения эритроцитарной системы, характеризующиеся появлением в крови эритробластов, нормобластов (нормоцитов), ретикулоцитов (полихроматофилов) в результате стимуляции нормобластического эритропоэза в костном мозге.
Патологические регенеративные изменения эритроцитов – качественные изменения эритроцитарной системы, характеризующиеся появлением в крови и костном мозге эмбриональных эритроцитов (мегалобластов, мегалоцитов, ядерных включений – телец Жолли и колец Кэбота).
Дегенеративные изменения эритроцитов – качественные изменения эритроцитарной системы, характеризующиеся появлением в крови эритроцитов разных размеров (анизоцитоз) и формы (пойкилоцитоз), эритроцитов с признаками гипо- и анизохромии, с базофильной зернистостью.
Гемоглобинопатии (haemoglobinopathia) – наследственные гемолитические анемии, происхождение которых связано с нарушением скорости синтеза или структуры полипептидных цепей гемоглобина А (a 2ß 2).
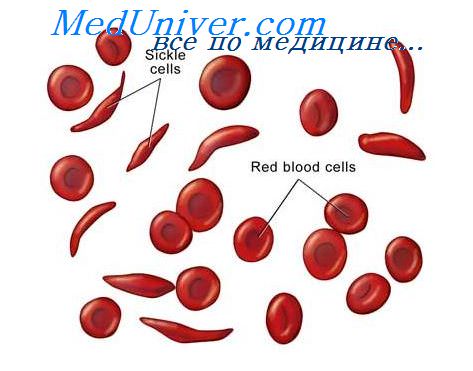
Анемия серповидно-клеточная (anaemia meniscocytica; син. S-гемоглобинопатия, серповидно-клеточная болезнь) – это наследственная гемолитическая анемия, при которой в ß -полипептидной цепи гемоглобина (ß -4) глутамат заменяется валином.
Анемия энзимопеническая (anaemia enzymopenica; греч. en – внутри; zyme – закваска; penia – бедность, недостаток; син.: энзимопатии) – групповое название гемолитических анемий, возникающих в результате наследственной недостаточности определенных ферментов эритроцитов, например, Г-6-ФДГ.
Эритроцитопатии (эритроциты + греч. pathos – страдание, болезнь; син.: мембранопатия эритроцитов) – группа наследственных гемолитических анемий, связанная с аномалиями белковых или липидных компонентов оболочки эритроцитов, что является причиной изменения их формы и преждевременного их разрушения.
Эритроцитопения (erythrocytopenia; эритроцит + греч. penia – бедность, недостаток) – патологическая реакция, сопровождающаяся абсолютным или относительным уменьшением содержания эритроцитов в периферической крови.
Учебные элементы
I. Oбщая характеристика нарушений системы эритроцитов
– эритроцитозы: определение понятия
– анемии: определение понятия
– эритропении: определение понятия
II. Анемии как типовой патологический процесс
принципы классификации анемий
причины развития анемий
характеристика гемограммы при анемиях
патофизиологические проявления анемий
III. Принципы классификации анемий
– классификация анемий по патогенезу
– анемии вследствие кровопотери
острые постгеморрагические анемии
хронические постгеморрагические анемии
– анемии вследствие угнетения эритрона
анемии вследствие нарушения нейрогормональной регуляции
дизэритропоэтические анемии
– анемии вследствие повышенного разрушения эритроцитов (гемолитические анемии)
приобретённые гемолитические анемии
наследственные гемолитические анемии
IV. Анемии вследствие кровопотери
острая постгеморрагическая анемия
снижение кислородной ёмкости крови – гемическая гипоксия
физиологические регенеративные изменения эритроцитов
нормоциты (нормобласты), ретикулоцитоз
хроническая постгеморрагическая анемия
дегенеративные изменения эритроцитов в периферической крови (анизоцитоз, пойкилоцитоз, гипохромия), нерезко выраженные регенеративные изменения (нормоциты – нормобласты, ретикулоциты)
V. Aнемии вследствие угнетения эритрона
– нарушение нейрогормональной регуляции эритропоэза
– дизэритропоэтические анемии
B12-фолиеводефицитные анемии
железодефицитные анемии
анемии при нарушении синтеза гема
сидеробластные анемии
гипо- и апластические анемии
VI. Анемии при недостаточности витамина В12 и фолиевой кислоты (мегалобластическая анемия)
мегалобластический (эмбриональный) тип эритропоэза
регенеративные изменения эритроцитов патологического типа (мегалобласты, мегалоциты, ядерные включения: тельца Жолли, кольца Кэбота), дегенеративные изменения эритроцитов (макроцитоз, пойкилоцитоз, гиперхромия)
недостаток эритропоэтина
анемии недоношенных
VII. Железодефицитные анемии
неусвоение (ахрезия) железа
нарушение образования гема: изменения эритроцитов – микроцитоз, пойкилоцитоз, гипохромия, нормоциты (нормобласты)
гипо- и апластические анемии
гипоплазия (аплазия) костного мозга
VIII. Анемии при нарушении синтеза гема
блокада свинцом сульфгидрильных групп гем-синтетазы
снижение активности пиридоксальфосфата (витамина B6)
нарушение связи железа с протопорфирином
нарушение синтеза гема
– характеристика гемограммы
регенеративные изменения эритроцитов физиологического типа (ретикулоцитоз)
увеличение в костном мозге образования сидеробластов
дегенеративные изменения эритроцитов (гипохромия, базофильная зернистость в эритроцитах)
IX. Анемии вследствие повышенного разрушения эритроцитов (гемолитические анемии)
приобретённые гемолитические анемии
токсикогемолитические
патоиммунные механизмы
гемолитическая болезнь новорожденных
регенеративные (нормобласты, ретикулоциты) и дегенеративные (микросфероцитоз, нормо-, гиперхромия, базофильная зернистость) изменения эритроцитов
наследственные гемолитические анемии
гемоглобинопатии (серповидно-клеточная, мишеневидная анемии)
талассемии
эритроцитопатии (микросфероцитарная, овалоцитарная анемии)
эритроэнзимопатии (дефицит Г-6-ФДГ в эритроцитах)
X. Патофизиологические проявления анемий
гемическая гипоксия
бледность кожных покровов и слизистых оболочек полости рта
кровоточивость
гемолитическая желтуха
XI. Компенсаторно-приспособительные процессы при анемиях
Классификация анемий. Виды анемий.Нормохромная: при острых кровотечениях, при некоторых гемолитических формах, при инфекционно-токсических формах. Гиперхромная: при некоторых гемолитических формах, при отсутствии антианемического фактора (витамина В12), при некоторых токсических формах (например, при уремии). Важные указания дает также величина эритроцитов. Величину эритроцитов определяют или морфологически в мазке крови, или с помощью кривых Прайс—Джонса, или, всего вернее, путем расчета среднего объема отдельного эритроцита. Анемии Макроцитарная: при токсических формах (уремия, цирроз печени), при некоторых приобретенных гемолитических анемиях. Микроцитарная: при дефиците железа, при конституциональной гемолитической желтухе (шаровидно-клеточной анемии) и при некоторых других гемолитических формах. Подразделение анемий по содержанию красящего вещества и величине эритроцитов по своему значению, естественно, уступает патогенетической классификации анемий. Старое деление анемий на первичные и вторичные более неприемлемо.
А. Анемии после кровотечения (постгеморрагические анемии) наружного или внутреннего. б) приобретенные формы (пароксизмальная ночная ге-моглобинурия: анемия Маркиафава (Marchiafava). Гемолиз, вызванный экзогенными причинами:а) генолиз, вызванный гемолизинами и агглютининами (гемолитические анемии, вызванные аутоиммунными и изоиммуиными телами); Анемии вследствие нарушения процессов эритропоэза.1. При дефиците веществ, необходимых для созревания эритроцитов (антианемический фактор — витамин В12),— мегалобластичские анемии. Анемии на почве нарушения построения гемоглобина.1. Железодефицитные анемии. – Также рекомендуем “Постгеморрагическии анемии. Гемолитические анемии.” Оглавление темы “Дифференциальная диагностика. Анемия у больного.”: |
