Анемия аддисона бирмера патологическая анатомия
Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 21 января 2019; проверки требуют 6 правок.
Перницио́зная анеми́я (от лат. perniciosus — гибельный, опасный) или B12-дефицитная анемия или мегалобластная анемия или болезнь Аддисона — Бирмера или (устаревшее название) злока́чественное малокро́вие — заболевание, обусловленное нарушением кроветворения из-за недостатка в организме витамина B12. Особенно чувствительны к дефициту этого витамина костный мозг и ткани нервной системы.
Основные сведения[править | править код]
Это синдром, связанный с недостатком B12 и фолиевой кислоты в организме. Характеризуется наличием в костном мозге большого количества крупных незрелых предшественников эритроцитов (мегалобластов).
Витамин B12всасывается в основном в нижней части подвздошной кишки. Анемия может быть вызвана недостаточным потреблением витамина B12 в пищу, недостаточной выработкой внутреннего фактора Касла в париетальных клетках желудка, патологическими процессами в подвздошной кишке с нарушением всасывания или конкуренцией за витамин B12 со стороны ленточных червей или бактерий.
При дефиците витамина B12 на фоне анемической клинической картины (или без неё) могут возникнуть и неврологические расстройства из-за связанного с дефицитом витамина B12 нарушения синтеза жирных кислот. Может наблюдаться демиелинизация и необратимая гибель нервных клеток. Симптомами такой патологии являются онемение или покалывание конечностей и атаксия.
Проявления[править | править код]
- Ярко-красный, а затем «лакированный» язык.
- Желудочная ахилия.
- Малокровие с наличием патологических эритроцитов.
- Поражение нервной системы.
- Желтоватый цвет кожи.
- Образование в костном мозге аномальных крупных клеток вместо эритроцитов (переход на мегалобластический тип кроветворения).
Причины[править | править код]
- Недостаток витамина B12 в питании или нарушение его всасывания
- Расстройство кишечника
- Долгое использование медицинских препаратов, приводящих к уменьшению кислотности в желудке
- Гастрэктомия
- Аутоиммунное поражение внутреннего фактора Касла или париетальных клеток.
- Заражение ленточными червями (лентец широкий)
- Токсическое воздействие на стенку желудка
- Рак желудка
- Наследственный дефект, передается аутосомно-рецессивно
Осложнения[править | править код]
В отсутствие лечения развиваются анемия и дегенерация нервов, так как костный мозг и ткани нервной системы особенно чувствительны к дефициту витамина B12.
Историческая справка[править | править код]
В 1855 году английский врач Томас Аддисон, а затем в 1872 году более подробно немецкий врач Антон Бирмер описали болезнь, которую назвали злокачественной (пернициозной) анемией. Вскоре французский врач Арман Труссо предложил называть эти болезни аддисоновой анемией и болезнью Аддисона.
В 1926 году Дж. Уипл, Дж. Майнот и У. Мерфи сообщили, что пернициозная анемия лечится введением в рацион питания сырой печени и что в основе заболевания лежит врожденная неспособность желудка секретировать вещество, необходимое для всасывания витамина B12 в кишечнике. За это открытие они в 1934 году получили Нобелевскую премию.
См. также[править | править код]
- Внутренний фактор
- https://en.wikipedia.org/wiki/Vitamin_B12_deficiency
Примечания[править | править код]
- ↑ Monarch Disease Ontology release 2018-06-29sonu — 2018-06-29 — 2018.
Ссылки[править | править код]
- Анемия
- Наше здоровье
- [da-med.ru/diseases/cat-60/d-125/ Da-med.ru ::: B12-дефицитная анемия (Пернициозная анемия)]
Некоторые внешние ссылки в этой статье ведут на сайты, занесённые в спам-лист. Эти сайты могут нарушать авторские права, быть признаны неавторитетными источниками или по другим причинам быть запрещены в Википедии. Редакторам следует заменить такие ссылки ссылками на соответствующие правилам сайты или библиографическими ссылками на печатные источники либо удалить их (возможно, вместе с подтверждаемым ими содержимым). Список проблемных доменов |
Анемия Бирмера (анемия Аддисона-Бирмера, бирмеровская анемия) – хроническое заболевание аутоимунной природы, являющееся наследственной формой мегалобластных анемий. Протекает циклически – рецидив сменяется ремиссией.
Раньше это заболевание называли прогрессивным злокачественным малокровием, поскольку оно всегда приводило к летальному исходу, но теперь благодаря лечению этого не случается, поэтому анемию называют по имени ее исследователей. А после того, как доказали роль витамина В12 в ее возникновении, бирмеровскую анемию называют одной из форм (пернициозной) В12-дефицитной анемии, при которой поражаются кроветворная функция, пищеварительная и нервная системы. Обычно болеют женщины в возрасте 50-60 лет.
Признаки
Анемия начинается постепенно и очень незаметно. Появляются жалобы на быструю утомляемость, слабость, головные боли, головокружение, сердцебиение и одышку при движениях. Иногда основными признаками являются диспептические явления (понос, отрыжка, тошнота, жжение в кончике языка). Иногда появляются такие нарушения нервной системы, как парестезии (спонтанно возникающие неприятные ощущения «мурашек», онемения, покалывания), похолодание конечностей, шаткость походки.
Цвет кожи – бледный с лимонным оттенком, склеры немного желтушны, лицо одутловато, иногда отечны голени и стопы. Грудина болезненна при поколачивании. Температура субфебрильная (чуть выше 37), но в период рецидива повышается до 38—39°.
При изменениях в пищеварительном тракте появляется глоссит Гентера (появление на языке красноватых неправильно очерченных, зудящих пятен). Язык иногда болит и жжется, постепенно становится гладким (полированным). У половины больных увеличивается печень и у пятой части – селезенка.
При поражении сердечно-сосудистой системы появляются тахикардия (учащенный пульс), гипотония (пониженное давление), увеличение размеров сердца, глухость тонов и т.д.
Со стороны нервной системы и психики — адинамия (резкий упадок сил).
Описание
Доказано, что природа болезни Аддисона-Бирмера – аутоиммунная. Она бывает у больных такими аутоиммунными заболеваниями, как диффузный токсический зоб, первичная надпочечниковая недостаточность, хронический лимфоцитарный тиреоидит (эутиреоидный или гипотиреоидный), витилиго и гипопаратиреоз.
Важную роль играет также наследственность – родственники людей с бирмеровской анемией чаще страдают этим заболеванием
Бирмеровская анемия может быть связана с атрофией слизистой оболочки желудка. Причина этой анемии – нарушение выработки желудком особого белка – гастромукопротеина (внутренний фактор Касла), который обеспечивает всасывание в кишечнике витамина B12. Такие дефицитные анемии возникают при сифилисе, полипозе, раке, лимфогранулематозе и других патологических процессах в желудке, а также при его удалении. Они возможны при глистных заражениях широким лентецом, спру, после удаления тонкой кишки, при лечении некоторыми лекарственными препаратами, а также при беременности.
Прием глюкокортикоидов вызывает ремиссию – временное ослабление или исчезновение признаков заболевания.
Диагностика
Диагностировать заболевание можно по клиническим признакам дефицита витамина В12. Кроме того, проводятся морфологические исследования крови, костного мозга и определяется кислотность желудочного сока.
Лечение
Лечение наследственных форм мегалобластных анемий проводится после установления диагноза и специального обследования больного в специализированных гематологических клиниках. Наиболее эффективным средством лечения является витамин В12. Его правильное применение полностью и навсегда устраняет нарушения, вызванные дефицитом витамина В12, если до лечения не возникли необратимые изменения в нервной ткани. Но больные остаются уязвимыми к появлению аденоматозных полипов желудка и раза в два чаще болеют раком желудка. Им показано наблюдение, включающее регулярное проведение специальной пробы, а также, если нужно, дополнительных исследований.
В случаях пернициозно-анемической комы немедленно переливается кровь (не более 150—200 мл) или (что лучше) эритроцитарная масса (иногда повторная) вместе с ударными дозами витамина B12.
Если причиной бирмеровской анемии является широкий лентец, то вылечивают ее дегельментизацией.
Если причиной стал сифилис, назначается специфическое лечение.
Больные анемией Бирмера в период ремиссии находятся на диспансерном учете. Им систематически проводятся ежемесячный анализ периферической крови и периодические исследования нервной системы, а также рентгеноскопия желудка для исключения рака, который возможен при бирмеровской анемии.
Профилактика
Анемия Аддисона-Бирмера занимает 2-е место по важности и частоте в группе дефицитных анемий. Для ее профилактики необходимо вовремя:
- лечить гастриты (с повышенной и пониженной кислотностью);
- лечить паразитарные заболевания (глистные и т.д.);
- применять витамин В12 после резекций желудка, при хронических поносах, воспалительных заболеваниях или пороках развития тонкого кишечника;
- лечить алкоголизм;
- контролировать функцию печени;
- при имеющейся наследственности или аутоиммунных заболеваниях принимать препараты или поливитамины, содержащие витамин В12.
- не использовать длительное время препараты, уменьшающие кислотность желудка.
С целью профилактики рецидивов больным систематически вводят витамин B12 (1-2 раза в месяц) или камполон (2 раза в месяц). В весенне-осенние месяцы, когда рецидивы учащаются, инъекции делают 1 раз в неделю. Больные анемией должны понимать, что ремиссия – это не выздоровление, и поэтому все рекомендации врача нужно строго выполнять.
© Доктор Питер
Анемия Аддисона также известна под такими названиями, как анемия Аддисона-Бирмера, первичная анемия, пернициозная анемия и пагубная анемия. Это – серьезное заболевание, которое относится к редким расстройствам нормальной функции крови и заключается в неспособности организма правильно использовать витамин В12, необходимый для развития красных кровяных клеток.
- Механизм развития и причины анемии Аддисона
- Факторы риска развития анемии Аддисона
- Диагностика анемии Аддисона
- Симптомы анемии Аддисона-Бирмера
- Лечение анемии Аддисона, профилактика
Открыто это заболевание было в 1855 году англичанином Т. Аддисоном, а спустя почти 20 лет немец А. Бирмер детально описал этот вид анемии. Таким образом, этому состоянию было решено присвоить название аддисоновой анемии.
Спустя почти 70 лет после открытия (в 1926 г.), врачи Мёрфи, Майнот и Уипл установили, что пернициозная анемия подлежит лечению сырой говяжьей печенью, и что основная причина заболевания – это невозможность желудочной поверхности вырабатывать специальное вещество для всасывания В12. В 1934 г. этим врачам была вручена Нобелевская премия за произведенное открытие.
Механизм развития и причины анемии Аддисона
Нервные клетки и клетки крови нуждаются в витамине В12, чтобы нормально функционировать. Этот витамин человек получает из таких пищевых продуктов, как мясо, птица, моллюски, яйца и молочные продукты.
Специальный белок, называемый внутренним фактором, помогает кишечнику усваивать витамин В12. Этот белок выделяется клетками в желудке. Когда желудок не вырабатывает достаточное количество внутреннего фактора, кишечник не может правильно усваивать витамин В12.
В большинстве случаев анемия Аддисона развивается в результате отсутствия желудочного белка. Также известны такие описания этого заболевания:
- врожденная злокачественная анемия из-за дефицита внутреннего фактора;
- взрослая пагубная анемия;
- ювенальная кишечная мальабсорбция витамина В12.
Устаревшая форма этого состояния – злокачественное малокровие.
Существует и редкая врожденная форма анемии Аддисона. В таком случае дети сразу рождаются с неспособностью производить полноценный внутренний фактор. Отдельная форма заболевания описана и у несовершеннолетних, причем, развитие заболевания обычно протекает медленно и может тянуться десятилетиями. Если его вовремя не диагностировать, это может привести к неврологическим осложнениям.
Общие причины анемии Аддисона:
- атрофический гастрит (ослабление функции внутренней поверхности желудка);
- аутоиммунное заболевание, при котором иммунная система организма атакует белок внутреннего фактора или клетки поверхности желудка, вырабатывающие его;
- в самых редких случаях анемия Аддисона-Бирмера передается по наследству. Тогда она называется врожденной злокачественной (пагубной) анемией.
У взрослых заболевание обычно проявляется после 60 лет.
Факторы риска развития анемии Аддисона
Вероятность получить данное заболевание выше у жителей Скандинавии или Северной Европы, а также у тех, в чьих семьях уже встречались подобные заболевания, и даже не в одном поколении. Дополнительные факторы, повышающие риск заболевания:
- хронический тиреоидит;
- болезнь Грейвса (токсический зоб, болезнь Перри);
- гипопаратиреоз (дефицит специфического паратгормона, отвечающего за обмен фосфора и калия в организме);
- гипопитуитаризм (практически полный отказ гипофиза от выработки гормонов);
- миастения (нервно-мышечная дисфункция, слабость мышц, человек с таким заболеванием не может поднимать тяжести);
- вторичная аменорея (из-за недостатка витаминов у женщин детородного возраста прекращается менструация);
- сахарный диабет 1 типа (инсулинозависимость);
- дисфункция яичек (следовательно, бесплодие);
- витилиго (заболевание кожи с нарушением пигментации, на поверхности тела появляются более светлые пятна, отличающиеся по цвету от основного тона).
Диагностика анемии Аддисона
Для окончательного диагноза необходимо провести полный спектр исследований, в частности:
- полный анализ крови;
- уровень витамина В12;
- уровень метилмалоновой кислоты;
- показатель уровня ретикулоцитов;
- тест Шиллинга (проба Шиллинга, при помощи которой можно узнать, как желудок усваивает В12);
- показатели билирубина;
- уровень холестерина;
- показатель щелочной фосфатазы лейкоцитов;
- мазок периферической крови;
- способность TIBC (железосвязывающая способность организма. Если она ниже 43 мкмоль /л, есть причины для беспокойства).
Симптомы анемии Аддисона-Бирмера
Основные симптомы такого вида анемии:
- повышенное чувство усталости;
- утомляемость;
- слабость, отсутствие концентрации;
- постоянная сонливость;
- периодическое расстройство желудка;
- тахикардия;
- болезненные ощущения в грудной клетке;
- аномальный желтый оттенок кожи.
Некоторые пациенты не испытывают никаких симптомов заболевания длительное время. Однако понять, что что-то не в порядке, можно, отметив наличие некоторых состояний. Например:
- желание съесть лёд или другие, не используемые в каждодневном рационе продукты и материалы (например, мел);
- диарея, сменяющаяся запором;
- бледность кожи;
- отекший, опухший язык и кровоточащие десны;
- одышка при любой физической активности.
Возможное повреждение нервной системы из-за недостатка В12 может выражаться в депрессивном состоянии, потере равновесия, онемении рук и ног и покалывании конечностей, спутанности сознания и проблемах с запоминанием.
Лечение анемии Аддисона, профилактика
Лечение зависит от причин появления этого вида анемии. Если они наследственные, необходим постоянный контроль рациона и периодические обследования в стационаре, а также поддержание нервной функции при помощи правильно подобранных препаратов.
Большинство пациентов устраняет проблему при помощи дополнительных курсов препаратов с В12, однако более эффективным методом избавления от анемии Аддисона является предотвращение (или профилактика) такого состояния.
Веганы могут использовать альтернативные источники белка – орехи, семена, авокадо, брокколи, а люди, находящиеся на обычном рационе, должны включать в рацион яйца, мясо птицы, морскую рыбу, молочные продукты (молоко, творог, натуральные йогурты без сахара).
Любое повреждение нервной системы, точнее, её нормальной функции, может быть необратимым для организма. При ощущении слабости, расстройствах стула, проблемах с кожей и сердечной деятельностью, можно принимать комплексы, содержащие В12 или употреблять этот витамин внутрь (ампулы, капсулы, таблетки).
У людей, занимающихся физическим трудом повышенной сложности, расход всех витаминов и ресурсов организма в целом намного выше, чем у людей с сидячей работой или тех, кто занят трудом интеллектуальным. Поэтому на фоне интенсивных тренировок у спортсменов-женщин часто возникает аменорея (прекращение менструаций), а у мужчин нарушается репродуктивная функция.
По материалам:
American Autoimmune Related Diseases Association, Inc.
NIH/National Heart, Lung and Blood Institute
Genetic and Rare Diseases (GARD) Information Center
Autoimmune Information Network, Inc.
European Society for Immunodeficiencies
Смотрите также:
У нас также читают:
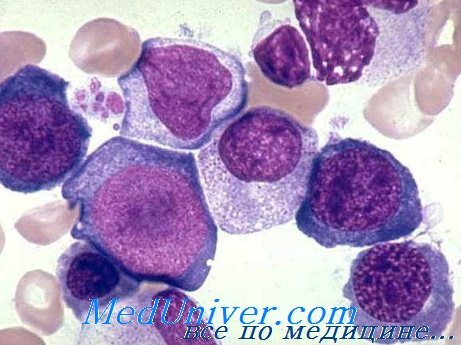
Болезнь Бирмера (Аддисона-Бирмера, злокачественная анемия) – история изучения, причиныБолезнь Бирмера (Аддиссона-Бирмера) или «злокачественная анемия» наиболее частая и лучше изученная форма дефицита витамина В12. Бирмеру мы обязаны анатомоклиническим описанием «злокачественной анемии» (1868—1872), хотя большинство рассмотренных им случаев видимо в действительности, составляли виды анемии за счет недостатка фолиевой кислоты (Castle, 1970). Описание мегалобласта Эрлихом в 1908 г. заложило основу морфологического диагноза, увенчавшегося в дальнейшем практикой костномозговых пункций. На основе современных знаний болезнь Бирмера можно определить как болезненное состояние, характеризующееся изменениями мегалобластического вида клеток периферической крови и костного мозга и дегенеративными поражениями слизистых оболочек пищеварительного тракта и нервной системы в связи с недостаточным поглощением витамина В12 по причине отсутствия внутреннего фактора, что, видимо создается каким-то аутоиммунным механизмом на наследственном фоне. Частота заболевания значительно колеблется в зависимости от географической области при этом болезнь чаще в странах, населенных «северными расами» (Голландия, Скандинавский полуостров, Англия, США, Канада), чем на востоке и юге Европы и совсем редко встречается на Дальнем Востоке и среди негроз (Gummert). Более высокий показатель частоты у женского пола (5:2) не подтвержден всеми авторами. По возрастным группам наиболее высокий показатель приходится на группу 45—55 лет, однако процент заболевших растет неуклонно в последующих группах. Экономические и трудовые (профессиональные) условия не оказывают существенного влияния на показатель частоты этого заболевания «эндогенного детерминизма» (в отличие от мегалобластической анемии за счет недостатка фолиевой кислоты).
В болезни Бирмера роль строения и наследственности была выявлена при описании первых случаев (Аддисон). В дальнейшем высказывалось предположение о взаимосвязи с определенными соматическими, нервными или эндокринными строениями, была отмечена частота отдельных соматических черт (широкое лицо, отдаленные глаза, белесный цвет волос, раннее появление седины и пр.), которые, в, настоящее время, не считаются показательными. По материалам Вернера (цит. Бегеманном), проводившего исследования в ряде семей страдающих, у 9% обследованных были отмечены иные явные случаи заболевания, а в 15% — частичные проявления [скрытые или исходные признаки болезни]. Среди близких родственников больного наиболее часто наблюдались заниженность или отсутствие кислотности (19%), желудочно-кишечные расстройства (33%), холе-цистопатия (15%) (реже — 8%—изменения языка), парестезия (25%) (в некоторых семьях наблюдалось развитие заболевания в сопровождении невропатии); из числа гематологических сдвигов отмечены мокроцитоз, овалицотоз, гиперсегментирование (примерно в 23% случаев). Болезнь Бирмера описана и у одножелточных близнецов (Arbo и Mohr). По одному из предложенных генетических объяснений болезнь передается посредством гена, вовлеченного в процесс образования внутреннего фактора, при этом дефицит передается доминантным способом, но с небольшой проницаемостью; гомозитотное состояние видимо обусловливает ювенильную форму заболевания (при врожденном отсутствии внутреннего фактора), в то время как для проявления болезни в гетерозиготных условиях (обычной у взрослых) предполагается необходимым образование, во времени, атрофических поражений слизистой оболочки желудка (под воздействием каких-то эпигенетических факторов). Вероятность наличия полигенетического механизма подсказывается относительно большой частотой случаев «конституционной гипохромной анемии» (с заниженным выделением желудочного сока, воспалением слизистой оболочки языка и пр.) среди родственников больного. Второй основной вопрос патогенеза болезни Бирмера связан с нали чием аутоиммунных антител у большинства больных. В сыворотке примерно 40% страдающих имеются антитела против ВФ, в то время как у примерно 90% — антитела против пристеночных клеток. Последние (примерно в размере 30% случаев) выявляются и при других заболеваниях аутоиммунного патогенеза, таких как тиреоз Хашимото, тиреотоксикоз, генуинная недостаточность надпочечной железы (Ирвине и сотр.). С другой стороны у 40—50% страдающих отмечается наличие противощитовидных антител. Однако антитела против пристеночных клеток встречаются и при простом атрофическом гастрите (60%) или даже у лиц, страдающих невыявимыми заболеваниями (5—8%), особенно у женщин старше 60 лет (Ирвине и сотр.). Поставлен вопрос о том, не составляет ли развитие этих аутоантител вторичное явление изменению антител клеточных структур. Антитела против внутреннего фактора находятся в разной пропорции в слюне и желудочном соке страдающих бирмеровской болезнью; их роль в сокращении поглощения витамина В1а доказана. Что касается роли антител против пристеночных клеток в патогенезе поражения слизистой оболочки желудка вопрос остается еще невыясненным (участвуют иммунологические механизмы гуморального и клеточного видов в обстановке разных эндо- и экзогенных факторов). С диагностической точки зрения в случае мегалобластической анемии присутствие антител против пристеночных клеток указывает, с большой вероятностью, на наличие болезни Бирмера, в то время как выявление антител против внутреннего фактора свидетельствует о развитии этого заболевания почти с достоверностью (Williams). Другим аргументом в пользу аутоиммунного патогенеза болезни Бирмера служит способность глюкокортикостероидов обусловливать (временно) регрессию поражений слизистой желудка и понижение коэффициента антител против внутреннего фактора (Robro и сотр.). На сонове этих аргументов, выступающих, с одной стороны, за наследственный характер болезни, а с другой, за аутоиммунный фактор патогенеза в настоящее время многие авторы склонны рассматривать болезнь Бирмера как результат генетического недостатка, вызывающего иммунологическое нарушение, которое заключается в низкой иммуной переносимости в отношении клеток желудочного эпителия (и других клеток одинакового эмбриологического происхождения), в связи с чем проявляются аутоантитела (под воздействием добавочных факторов). – Также рекомендуем “Клиника болезни Аддисона-Бирмера (злокачественной анемии) – признаки” Оглавление темы “Анемии”:
|
