Анемия г 6 фд
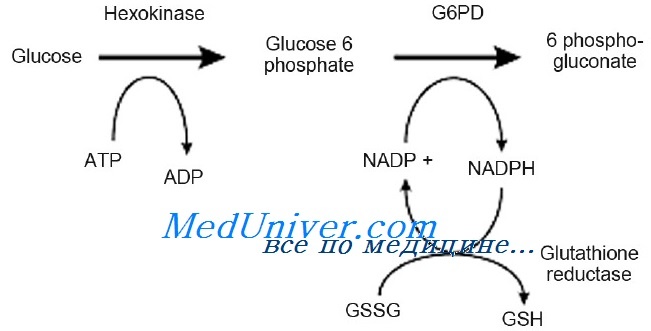
Недостаточность глюкозо-6-фосфат дегидрогеназы (Г6ФД): причины, диагностика, лечениеЭтиология и встречаемость недостаточности глюкозо-6-фосфат дегидрогеназы (Г6ФД). Недостаточность глюкозо-6-фосфат дегидрогеназы (Г6ФД) (MIM №305900), наследственная склонность к гемолизу, — Х-сцепленное заболевание антиоксидантного гомеостаза, вызванное мутациями в гене G6PD. В областях, эндемичных по малярии, недостаточность глюкозо-6-фосфат дегидрогеназы (Г6ФД) имеет распространенность от 5-25%; в неэндемичных областях распространенность менее 0,5%. Подобно серповидноклеточной анемии, недостаточность глюкозо-6-фосфат дегидрогеназы (Г6ФД) имеет высокую частоту на некоторых территориях, поскольку вызывает у гетерозиготных носителей повышенную сопротивляемость к малярии, и таким образом дает им селективное преимущество. Патогенез недостаточности глюкозо-6-фосфат дегидрогеназы (Г6ФД)Глюкозо-6-фосфат дегидрогеназы (Г6ФД) — первый фермент в гексозомонофосфатном шунте, метаболическом пути, критически важном для синтеза НАДФ. НАДФ необходим для восстановления окисленного глутатиона. В эритроцитах восстановленный глутатион используется для детоксикации оксидантов, образующихся при взаимодействии гемоглобина и кислорода с внешними факторами, такими как лекарства, инфекции или метаболический ацидоз. Чаще всего недостаточность глюкозо-6-фосфат дегидрогеназы (Г6ФД) возникает вследствие мутаций в Х-сцепленном гене G6PD, снижающих либо каталитическую активность, либо устойчивость фермента, либо и то и другое. Когда активность глюкозо-6-фосфат дегидрогеназы (Г6ФД) достаточно низкая, дефицит НАДФ приводит к недостаточному восстановлению окисленного глутатиона во времени окислительного стресса. Это вызывает окисление и накопление внутриклеточных белков (телец Хайнца) и образование ригидных эритроцитов, легко подвергающихся гемолизу. Наиболее частые аллели G6PD, приводящие к неустойчивости белка, вызывают преждевременное старение эритроцитов. Поскольку эритроциты не имеют ядра, новая мРНК глюкозо-6-фосфат дегидрогеназа (Г6ФД) не синтезируется; поэтому эритроциты не в состоянии заменять глюкозо-6-фосфат дегидрогеназу (Г6ФД) по мере его деградации. Следовательно, при действии окислительных агентов гемолиз начинается с более старых эритроцитов и постепенно захватывает все более молодые эритроциты, в зависимости от степени окислительного стресса.
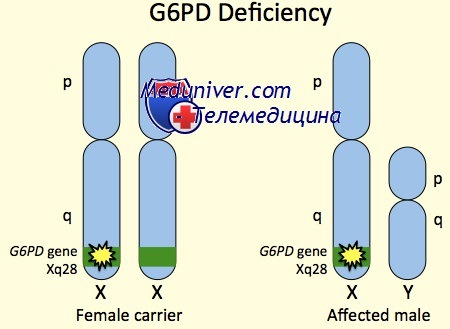
Фенотип и развитие недостаточности глюкозо-6-фосфат дегидрогеназы (Г6ФД)Так как заболевание Х-сцепленное, недостаточность глюкозо-6-фосфат дегидрогеназы (Г6ФД) преимущественно и наиболее сильно поражает мужчин. Редкие женщины с клинической симптоматикой имеют смещение инактивации Х-хромосомы, у которых в предшественниках эритроцитов активна Х-хромосома, несущая аллель болезни недостаточности глюкозо-6-фосфат дегидрогеназы (Г6ФД). Кроме пола, тяжесть недостаточности глюкозо-6-фосфат дегидрогеназы (Г6ФД) зависит от конкретной мутации гена G6PD. В общих чертах мутации, часто встречающиеся в Средиземноморском бассейне (Г6ФД В или средиземноморские), приводят к более тяжелым формам, чем африканские (Г6ФД А- варианты). В эритроцитах пациентов со средиземноморскими вариантами активность глюкозо-6-фосфат дегидрогеназы (Г6ФД) падает до недостаточного уровня за 5-10 дней после их появления в кровотоке, тогда как в эритроцитах пациентов с глюкозо-6-фосфат дегидрогеназы (Г6ФД) А- вариантами активность ГбФд снижается до недостаточного уровня только через 50-60 дней. Следовательно, у пациентов с тяжелыми формами недостаточности глюкозо-6-фосфат дегидрогеназы (Г6ФД) средиземноморского типа гемолизу подвержены большинство эритроцитов, а у пациентов с вариантами глюкозо-6-фосфат дегидрогеназы (Г6ФД) А- – только 20-30%. Чаще всего недостаточность глюкозо-6-фосфат дегидрогеназы (Г6ФД) обнаруживается или как неонатальная желтуха, или как острая гемолитическая анемия. Максимальная встречаемость неонаталь-ной желтухи происходит в течение 2-3-го дня жизни. Тяжесть желтухи колеблется от преклинической до ядерной желтухи; связанная анемия редко бывает тяжелой. Эпизоды острой гемолитической анемии обычно начинаются во время окислительного стресса и заканчиваются после гемолиза эритроцитов с недостаточностью глюкозо-6-фосфат дегидрогеназы (Г6ФД); следовательно, тяжесть анемии, связанной с острыми гемолитическими кризами, прямо пропорциональна степени недостаточности глюкозо-6-фосфат дегидрогеназы (Г6ФД) и выраженности окислительного стресса. Наиболее частые пусковые механизмы — вирусные и бактериальные инфекции, но также к гемолизу могут приводить множество лекарственных средств и токсинов. Название заболевания — «фавизм» происходит от гемолиза, вызванного употреблением конских бобов Vicia fava пациентами с тяжелыми формами недостаточности глюкозо-6-фосфат дегидрогеназы (Г6ФД), например, средиземноморскими; бобы содержат b-гликозиды, оксиданты естественного происхождения. Помимо неонатальной желтухи и острой гемолитической анемии, недостаточность глюкозо-6-фосфат дегидрогеназы (Г6ФД) иногда вызывает врожденную или хроническую несфероцитарную гемолитическую анемию. Пациенты с хронической не-сфероцитарной гемолитической анемией обычно имеют выраженную недостаточность глюкозо-6-фосфат дегидрогеназы (Г6ФД), вызывающую хроническую анемию и повышенную предрасположенность к инфекциям. Предрасположенность к инфекциям возникает в связи с тем, что поступления НАДФ в гранулоциты недостаточно, чтобы поддерживать окислительную реакцию, необходимую для разрушения фагоцитированных бактерий. Особенности фенотипических проявлений недостаточности глюкозо-6-фосфат дегидрогеназы (Г6ФД):
Лечение недостаточности глюкозо-6-фосфат дегидрогеназы (Г6ФД)Недостаточность глюкозо-6-фосфат дегидрогеназы (Г6ФД) следует заподозрить у пациентов африканского, средиземноморского или азиатского происхождения, имеющих острый гемолитический эпизод или неонатальную желтуху. Недостаточность глюкозо-6-фосфат дегидрогеназы (Г6ФД) диагностируют измерением активности глюкозо-6-фосфат дегидрогеназы (Г6ФД) в эритроцитах; эта активность должна быть измерена только в том случае, если пациент не имел переливаний крови или острого гемолиза (поскольку недостаточность глюкозо-6-фосфат дегидрогеназы (Г6ФД) первоначально развивается в более старых эритроцитах, измерение активности глюкозо-6-фосфат дегидрогеназы (Г6ФД) преимущественно в молодых эритроцитах во время или немедленно после гемолитического эпизода, часто дает ложноотрицательный результат). Ключ к оказанию помощи при недостаточности глюкозо-6-фосфат дегидрогеназы (Г6ФД) — предотвращение гемолиза быстрым лечением инфекций и исключением лекарств с оксидантным эффектом (например, сульфаниламидов, сульфонов, нитрофуранов) и токсинов (например, нафталина). Хотя большинство пациентов во время гемолитического эпизода не нуждаются в медицинском вмешательстве, в случае выраженной анемии и гемолиза может потребоваться переливание эритроцитарной массы и интенсивное наблюдение. Пациенты с неонатальной желтухой хорошо отвечают на такую же терапию, как и при неонатальной желтухе другого генеза (регидратацию, светотерапию и обменные переливания крови). Риски наследования недостаточности глюкозо-6-фосфат дегидрогеназы (Г6ФД)Все мальчики у матери, несущей мутацию в гене G6PD, имеют 50% шансы быть больными, а все дочери — 50% шансов оказаться носительницами. Все дочери больного отца будут носительницами, но сыновья будут здоровы, поскольку больной отец не передает X хромосому сыновьям. Риск того, что девочки-носительницы будут иметь клинически значимые симптомы, низкий, так как достаточное смещение инактивации Х-хромосомы встречается сравнительно редко. Пример недостаточности глюкозо-6-фосфат дегидрогеназы (Г6ФД). Л.М., ранее здоровый 5-летний мальчик, поступил в неотложное отделение с лихорадкой, бледностью, тахикардией, одышкой, заторможенностью; в остальном результаты его клинического осмотра оказались без особенностей. Утром перед поступлением он был здоров, но в течение дня появились боли в животе, головная боль, поднялась температура тела; вечером начались одышка и заторможенность. Он не принимал никаких лекAPCтвенных средств или известных токсинов, результаты токсикологического анализа мочи оказались отрицательными. Результаты других лабораторных тестов показали огромный внутрисосудистый гемолиз и гемоглобинурию. После реанимации ребенок переведен в отделение; гемолиз разрешился без дальнейшего вмешательства. Пациент по этнической принадлежности — грек; его родители были не осведомлены о случаях гемолиза в семье, хотя мать имела несколько дальних родственников в Европе с «проблемами крови». Дальнейший опрос выяснил, что утром перед заболеванием ребенок поел конские бобы в саду, пока мать работала во дворе. Врач объяснил родителям, что ребенок, вероятно, имеет недостаточность глюкозо-6-фосфат дегидрогеназы (Г6ФД), из-за чего и заболел после употребления конских бобов. Последующее измерение активности глюкозо-6-фосфат дегидрогеназы (Г6ФД) в эритроцитах подтвердило недостаточность фермента. Родителям даны рекомендации относительно риска острого гемолиза у ребенка после применения определенных лекарств и токсинов, дан список веществ, которых необходимо избегать. – Также рекомендуем “Наследственный гемохроматоз: причины, диагностика, лечение” Оглавление темы “Генетические болезни”:
|
- Недостаточность глюкозо-6-фосфатдегидрогеназы. Фавизм Г-6-ФД-дефицитная анемия
- Нарушения глутатионового обмена
- Недостаточности ферментов (за исключением Г-6-ФД), связанных с гексозомонофосфатным шунтом метаболического пути
- Гемолитическая несфероцитарная анемия (наследственная) типа 1
Недостаточность глюкозо-6-фосфатдегидрогеназы. Фавизм Г-6-ФД-дефицитная анемия
Дефицит глюкозо-6-фосфатдегидрогеназы (далее Г-6-ФД или G6PD) является генетическим заболеванием, которое чаще встречается у мужчин. Это заболевание в основном поражает эритроциты, которые переносят кислород из легких в ткани во всем организме. У таких больных этот фактор вызывает преждевременный распад красных кровяных клеток. Это разрушение эритроцитов называется гемолиз.
Наиболее распространенной медицинской проблемой, связанной с дефицитом глюкозо-6-фосфатдегидрогеназы является гемолитическая анемия, которая возникает, когда красные кровяные клетки разрушаются быстрее, чем организм успевает их заменять.
Симптомы Г-6-ФД-дефицитной анемии
Этот тип анемии приводит к бледности, пожелтению кожи и белков глаз (желтуха). Появляется темная моча. Больной чувствует усталость, наблюдается одышка и учащенное сердцебиение. У людей с таким типом ферментного расстройства гемолитическая анемия чаще всего вызвана бактериальной или вирусной инфекцией или употреблением некоторых видов лекарств. Например, антибиотиков и некоторых лекарственных препаратов, используемых для лечения малярии.
Гемолитическая анемия может возникать после употребления в пищу бобов или вдыхания пыльцы растений (эта реакция называется примахиновой анемией).
Анемия Г-6-ФД также является важной причиной легкой и тяжелой степени желтухи у новорожденных. Многие люди живут с этим расстройством, однако никогда не испытывают каких-либо его признаков или симптомов. В то время как у других на фоне подобного состояния появляется хроническая анемия. При необходимых мерах предосторожности ребенок, рожденный с дефицитом G6PD, может вести здоровый и активный образ жизни.
Больше об анемии Г-6-ФД
Г6ФД является одним из многих ферментов, которые помогают углеводам, поступающим в организм, превращаться в энергию. Фермент также защищает красные кровяные клетки от потенциально вредных побочных продуктов, которые могут накапливаться, когда человек принимает определенные лекарства или когда организм борется с инфекцией.
Гемолитическая анемия в данном случае возникает, когда костный мозг (мягкая, губчатая часть кости, которая производит новые клетки крови) не может компенсировать разрушение эритроцитов за счет увеличения их производства.
Заболевание передается генами одного или обоих родителей ребенка. Ген, ответственный за этот недостаток, располагается на Х-хромосоме.
Наиболее распространена такая анемия у афроамериканских мужчин. Многие афроамериканские женщины являются носителями данного дефекта, а значит, могут передать ген дефицита своим детям. Сами носители симптомов не имеют, и лишь немногие из них каким-либо образом испытывают последствия этого фактора.
Средиземноморское население, в том числе итальянцы, греки, арабы и евреи-сефарды тоже склонны к дефициту Г6ФД.
Причины такой географической склонности
Известно, что Африка и Средиземноморский бассейн находятся в области высокого риска инфекционного заболевания — малярии. Исследователи обнаружили доказательства того, что паразит, который вызывает эту болезнь, не выживает в Г6ФД-дефицитных клетках. Таким образом, они полагают, что такой дефицит является генетической защитой от малярии.
Нарушения глутатионового обмена
Дефицит глутатиона синтетазы — это расстройство, которое препятствует производству важной молекулы под названием глутатион.
Глутатион помогает предотвратить повреждение клеток путем нейтрализации вредных молекул, образующихся при производстве энергии. Глутатион также играет важную роль в обработке лекарственных препаратов и канцерогенных соединений (канцерогенов), в создании ДНК, белков и других важных клеточных компонентов.
Типы нарушений глутатионового обмена
Недостаточность глутатион синтетазы может быть классифицирована на три типа: мягкий (слабый), умеренный и тяжелый. Мягкая недостаточность приводит к разрушению красных кровяных клеток (гемолитическая анемия). Кроме того, пострадавшие пациенты могут отличаться большим количеством соединения под названием 5-оксопролин в моче. Такое состояние называется 5-оксопролинурия. Это соединение накапливается, когда глутатион неправильно обрабатывается клетками.
Пациенты с умеренным дефицитом глутатиона синтетазы могут испытывать симптомы этого состояния вскоре после рождения. Обычно оно проявляется в виде гемолитической анемии, 5-оксипролонурии и повышенной кислотности крови и тканей (метаболический ацидоз).
В дополнение к симптомам, присутствующим при умеренном дефиците глутатиона синтетазы, люди, страдающие его тяжелой формой, могут испытывать еще и симптомы со стороны ЦНС. К ним относятся следующие состояния: судороги, замедление физических реакций, движений, речи и психомоторного развития.
Кроме того, наблюдается интеллектуальная недееспособность, потеря координации (атаксия). Некоторые пациенты с тяжелой недостаточностью глутатиона синтетазы подвергаются интенсивному развитию рецидивирующих бактериальных инфекций.
Причины дефицита глутатиона синтетазы
Генная мутация GSS является причиной такого дефицита. Глутатион синтетаза участвует в процессе, называемом циклом гамма-глутамила, который происходит в большинстве клеток организма. Этот цикл необходим для получения молекулы глутатиона, которая защищает клетки от повреждений, вызванных нестабильными кислородсодержащими молекулами. Эти молекулы являются побочными продуктами производства энергии. Глутатион считается антиоксидантом из-за его роли в защите клеток от разрушающего воздействия этих нестабильных молекул. Мутации в гене GSS не позволяют клеткам принять адекватное количество глутатиона, что приводит к появлению симптомов дефицита глутатиона синтетазы.
Данное заболевание наследуется по аутосомно-рецессивному признаку. Это означает, что родители ребенка несут одну копию мутантного гена, но не проявляют признаков болезни.
Симптомы недостаточности глутатиона синтетазы
Фенотипические проявления дефицита:
- гемолитическая анемия;
- нервные нарушения;
- бессонница;
- замедленная реакция на раздражители;
- снижение интеллектуальных способностей.
Тяжелым фенотипическим проявлением данного расстройства является 5-оксопролонурия. В моче больного при таком состоянии может содержаться большое количестве органических кислот. Происходит метаболический ацидоз, повреждения ЦНС.
Недостаточности ферментов (за исключением Г-6-ФД), связанных с гексозомонофосфатным шунтом метаболического пути
Распределение углеводов (глюкозы) происходит в организме путем гликолиза с последующим циклом трикарбоновых кислот (цикл Кребса), в результате чего происходит выход энергии в клетки в виде АТФ.
Глюкоза может пройти альтернативный путь для производства других продуктов, необходимых клеткам. Одним из этих альтернативных путей является пентозофосфатный путь или так называемый гексозомонофосфатный шунт метаболического пути. При таком процессе происходит окисление глюкозо-6-фосфата с целью получения пентозы.
Такой процесс проходит в два этапа: окисление и неокисление.
У млекопитающих этот процесс происходит исключительно в цитоплазме, и установлено, что наиболее активно в организме человека он происходит в печени, молочной железе и коре надпочечников.
Пентоза может при необходимости трансформироваться к гексозу. Нарушение этого сложного цикла является прямым путем к окислительному стрессу в клетках.
Не углубляясь в медицинскую терминологию, можно сказать, что при отсутствии таких важных процессов или неправильном их протекании человеческий организм, а точнее все его клетки, теряют способность противостоять вредным веществам, атакующим клетки каждую минуту.
Гемолитическая несфероцитарная анемия (наследственная) типа 1
Гемолитическая несфероцитарная (или мегалоцитарная) анемия – это генетическое (передающееся по наследству) заболевание крови, которое характеризуется нормальным количеством гемоглобина в пределах аномально больших красных кровяных клеток. Количество эритроцитов при таком состоянии является предельно низким.
Симптомы несфероцитарной наследственной анемии
Для несфероцитарной наследственной анемии характерны такие симптомы:
- уменьшение количества полноценных эритроцитов;
- потеря аппетита, бледность кожи губ и век;
- хрупкость ногтей;
- боль при жевании, усталость, слабость;
- головокружение, головная боль.
На ранних стадиях заболевания наблюдаются проблемы со сном, затрудненное глотание, бледность, одышка, тахикардия.
На поздних стадиях наблюдается нарушение когнитивных способностей, двигательные нарушения, холодная кожа.
Источники статьи:
https://emedicine.medscape.com
https://kidshealth.org
https://en.wikipedia.org
https://ghr.nlm.nih.gov
https://ghr.nlm.nih.gov
https://emedicine.medscape.com
https://jn.nutrition.org
https://en.wikipedia.org
https://pharmaxchange.info
https://www.rightdiagnosis.com
По материалам:
1.2015 PharmaXChange.info
2.Wikimedia Foundation, Inc.,
3.Guoyao Wu,Yun-Zhong Fang, Sheng Yang, Joanne R. Lupton, and Nancy D. Turner
4.1994-2015 by WebMD LLC
5.Lister Hill National Center for Biomedical Communications
6.U.S. National Library of Medicine, National Institutes of Health
7.Department of Health & Human Services, USA.gov
8.1995-2015 The Nemours Foundation.
Смотрите также:
У нас также читают: