Анемия гипопластическая и апластическая
Гипопластическая и апластическая анемия – Anaemia hipoplastica et aplastica –называются остро протекающие заболевания системы крови, развивающееся в результате недостаточности (истощения) костномозгового кроветворения и проявляющиеся нормоцитарной, иногда макроцитарной, нормохромной анемией с сопутствующей тромбо- и гранулоцитопенией (панцитопенией).
Этиология. Причины дефицитных анемий – алиментарные факторы: недостаток в рационе кормления животных протеина, отдельных аминокислот, микроэлементов (железа, меди, кобальта), витаминов (В12, А, Д, С и других). Гипопластические анемии могут служить симптомами хронических гастро-энтероколитов, гепатитов, дистрофий печени, обусловленных пониженной усвояемостью питательных веществ (даже при полноценном кормление животных). Миелотоксические анемии у животных возникают в результате инфекций, инвазий и интоксикаций, чаще при хроническом течении (туберкулез, паратуберкулез, лептоспироз, листериоз, диктиокаулез, аскаридоз, мониезиоз, микозы, кетозы, эндометриты и др.). Анапластические анемии являются следствием воздействия на организм животного в больших дозах ионизирующей радиации (лучевая болезнь), отравления бензолом, соединениями свинца, ртути и других тяжелых интоксикациях.
Патогенез изучен слабо. Под влиянием вышеуказанных этиологических факторов у больного животного вначале развивается гипоплазия, а затем наступает аплазия костного мозга, если доза того или иного фактора достаточно долговременная. Причинные факторы, подавляющие костно — мозговое кроветворение, не вызывают разрушения эритроцитов, анемия развивается в основном за счет уменьшения их регенерации, да и не только их, а и всех клеточных элементов костного мозга. Поэтому наряду с развитием анемии отмечается лейкопения и тромбопения. Происходит одновременно повышение ломкости и порозности кровеносных сосудов, в результате у больного животного появляются кровоизлияния. В последующем пониженная фагоцитарная активность элементов соединительной ткани на фоне лейкопении и резко сниженной способности выработки антител ведет к развитию у животного бактериемии и сепсису.
Патологоанатомические изменения. Слизистые и серозные оболочки у павших животных бледные, часто с точечными и полосчатыми кровоизлияниями. В селезенке кровоизлияния. В легких, иногда в печени, почках и желудочно – кишечном тракте застойная гиперемия. В паренхиматозных органах и коже нередко устанавливаем некрозы. Костный мозг, особенно в трубчатых костях — бледный, местами желтый – жировой. В миокарде, печени и почках выраженная дистрофия.
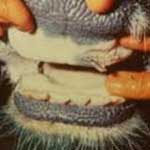
Клинические признаки. На фоне основного заболевания (инфекция, инвазия, отравление) при гипопластической анемии у больного животного прогрессирует общая слабость, быстрая утомляемость, угнетение, отмечаем снижение продуктивности и работоспособности, появляются симптомы расстройства желудочно- кишечного тракта, сухость и взъерошенность кожного покрова, понижается эластичность кожи. При клиническом исследование больного животного устанавливаем характерный признак болезни — бледность видимых слизистых оболочек, склеры и кожи. При апластической анемии в сильной степени выражены общая слабость (иногда больные животные не в состоянии стоять на ногах), животные апатичные, при клиническом осмотре отмечаем бледность видимых слизистых оболочек и кровоизлияния на слизистых оболочках и коже.
Наряду с развитием у больного животного анемии отмечаем быстрое снижение количества лейкоцитов в крови и клеточных элементов в костном мозге. Количество гранулоцитов крови, молодых эритробластических форм и гранулофилоцитов в костном мозге снижается до минимума.
В лейкоцитарной формуле происходит нарастание процента нейтрофилов, а в миелограмме – миелобластических форм. При стахиоботриотоксикозе, чуме количество лейкоцитов крови снижается до 500-100 в 1мм³, резко выражен относительный лимфоцитоз, нейтропения, эозинофилы и моноциты исчезают, нарастает тромбопения. СОЭ ускорена. В костном мозге миелоидные элементы подвергаются дегенеративным изменениям. При тяжелом течении апластической анемии костный мозг становится опустошенным – отмечается бледность клеточными элементами костного мозга (панмиелофтиз). При исследовании обнаруживают в основном только гистиоцитарные и плазматические клетки, и единичные эритробластические формы.
В результате уменьшения массы кроветворной ткани эритропоэз становится явно недостаточным для поддержания состава крови на необходимом уровне; анемия прогрессирует, ее характер может отклонится в сторону гиперхромии. Гемоглобинизация эритроблостав совершается по типу эмбрионального эритропоэза; исчезновение ядра из клетки замедленно и совершается только путем кариорексиса.
Течение чаще острое и отличается своей злокачественностью. На фоне аплазии кроветворной ткани в организме развиваются вторичные инфекции, очаги некрозов, кровотечения и сепсис. Но бывают случаи медленного течения, причем патологические симптомы анемии постепенно усиливаются.
Диагноз на апластическую анемию ставится с учетом анамнеза (интоксикация, инфекция, инвазия), клинических симптомов (анемия, слабость) и анализа крови. Гематологически при гипо- и апластических анемиях устанавливают понижение уровня гемоглобина, лейкопению с преобладанием зрелых форм нейтрофилов, повешенную СОЭ. Характерной особенностью этих групп анемий в отличие от постгеморрагических и гемолитических является пониженное содержание в каждом эритроците гемоглобина при незначительном уменьшении в крови количества эритроцитов, что обуславливает низкий цветовой показатель (обычно хромных) эритроцитов, измененных патологических форм и размеров: пойкилоцитоз, анизоцитоз, большое количество микроцитов (малых размеров по сравнению с нормой), встречаются анулоциты (в виде колец), шизоцыты (в виде обрывков) и др. При исследовании пунктата костного мозга обнаруживают бледность клеточными элементами всех ростков, кровоизлияния.
Дифференциальный диагноз. Заболевание необходимо дифференцировать от гипопластических анемий, анемий при лейкозах у животных, лучевой болезни, ИНАН лошадей, чумы свиней.
Прогноз неблагоприятный.
Лечение. Прежде чем приступить к лечению, необходимо устранить этиологические факторы вызвавшие заболевание и угнетающие кроветворение. При наличии у больного животного тех или иных инвазионных, инфекционных заболеваний и отравлений необходимо проводить соответствующее лечение при данных заболеваниях. Больных животных обеспечивают полноценным рационом кормления с достаточным количеством содержания протеина, полным набором аминокислот, витаминов, макро- и микроэлементов. Для стимулирования костно- мозгового кроветворения необходимо применять препараты железа, кобальта, меди, мышьяка, кампонол, витамины К, В12, фолиевую кислоту и другие. Хорошее лечебное действие оказывает переливание гомогенной стабилизированной крови, внутримышечные или подкожные введения гомогенной или гетерогенной крови, гамма — и полиглобулинов согласно инструкциям и в дозах исходя из наставления по их применению.
При нарастающих симптомах интоксикации при комплексном лечении применяют сердечные средства, 20-40% раствор глюкозы с аскорбиновой кислотой.
При септических осложнениях применяют антибиотики, в том числе современные цефалоспоринового ряда. При полном истощении костного мозга лечить больное животное не целесообразно.
Сущность гипопластической (и апластической) анемии состоит в резком угнетении костномозгового кроветворения, что сопровождается снижением количества эритроцитов, лейкоцитов и тромбоцитов. Известна также парциальная форма гипопластической анемии с угнетением образования только эритроцитов.
Апластическая анемия (АА) является относительно редким заболеванием. Она встречается с частотой примерно 0,5 на 100 000 населения. По мере увеличения возраста от 1 года до 20 лет число случаев болезни увеличивается; различий в частоте заболевания в период от 20 до 60 лет не выявлено, однако после 60 лет число больных возрастает. В некоторых семьях существует генетическая предрасположенность к болезни.
Этиология.К резкому угнетению костномозгового кроветворения приводят различные причины:
• внешние факторы, оказывающие миелотоксическое действие (иони
зирующая радиация, цитостатические препараты, различные хими
ческие вещества, лекарственные средства);
• внутренние причины (эндогенные): влияние токсичных веществ
при уремии, гипотиреозе и др.;
• идиопатические формы, когда не удается выявить никаких причин
развития анемии (у 50 % больных).
Патогенез.Механизм развития гипоплазии (аплазии) костного мозга окончательно не выяснен. Предполагают несколько механизмов развития АА: 1) поражение полипотентной стволовой клетки костного мозга; 2) подавление кроветворения, связанное с воздействием иммунных механизмов (клеточных, гуморальных); 3) нарушения в функционировании элементов «микроокружения»; 4) дефицит факторов, стимулирующих кроветворение.
Содержание веществ, непосредственно участвующих в процессе кроветворения (железо, витамин Bi2, протопорфирин), не снижено, но они не могут быть использованы кроветворной тканью.
Клиническая картинаболезни чрезвычайно разнообразна и связана в основном с цитопенией и зависит от степени ее выраженности. Соответственно этому проявления болезни чрезвычайно разнообразны: существуют переходные формы от частичного угнетения кроветворения до выраженной аплазии костного мозга.
Можно выделить три основных синдрома: цитопенический, септико-некротический и геморрагический. Их различная выраженность обусловливает пестроту данных, получаемых на различных этапах диагностического поиска.
На I этапе диагностического поиска выявляют такие неспецифические признаки, как повышенная утомляемость, слабость. Часто больные адаптируются к анемии и обращаются к врачу лишь при развернутой картине болезни. Геморрагический синдром проявляется различными кровотечениями (носовыми, маточными), развитием кровоподтеков.
На II этапе в начальных стадиях болезни, а также при хроническом течении выявляется лишь умеренная бледность кожных покровов и видимых слизистых оболочек, иногда кровоподтеки. При остром течении, кроме выраженной бледности, отмечаются значительный геморрагический синдром, некрозы слизистых оболочек, высокая лихорадка. Различные воспалительные заболевания (пневмония) проявляются характерными симптомами. Печень и селезенка обычно не увеличены, но при обнаружении антител к эритроцитам (аутоиммунная форма болезни) могут определяться умеренная спленомегалия, а также легкая желтушность кожи и склер вследствие наличия гемолитического компонента.
Основным в выявлении заболевания является III э т а п. В периферической крови определяется выраженная анемия, обычно нормохромная. Содержание гемоглобина снижается до 20 — 30 г/л. Содержание ретику-лоцитов снижено, что свидетельствует о гипорегенераторном состоянии костного мозга. Характерны выраженные лейкопения, гранулоцитопения. Содержание лимфоцитов не изменено. Число тромбоцитов снижается иногда до нуля. В большинстве случаев значительно увеличивается СОЭ (до 30-50 мм/ч).
В костном мозге уменьшено содержание миелокариоцитов, увеличено число лимфоцитов, тучных и плазматических клеток. Мегакариоциты могут полностью отсутствовать. При гистологическом исследовании костного мозга обращает внимание почти полное исчезновение костномозговых элементов и замещение их жировой тканью.
Содержание железа сыворотки у большинства больных увеличено, насыщение трансферрина железом практически 100 %.
Диагностика.Распознавание болезни основывается на данных цитологического исследования периферической крови и цитоморфологическо-го исследования костного мозга. При подозрении на АА обязательно выполнение трепанобиопсии. Необходимо провести дифференциальную диагностику с рядом заболеваний, протекающих с цитопенией: дебютом острого лейкоза, метастазами рака в костный мозг, костномозговой формой хронического лимфолейкоза. Панцитопения у пожилых людей может быть также проявлением В^-дефицитной анемии (однако при этом в костном мозге обнаруживаются мегалобласты, при патоморфологическом изу-
чении трепаната выявляется гиперплазия костного мозга в противоположность аплазии при АА). Следует подчеркнуть, что диагноз АА является «диагнозом исключения» и устанавливается лишь в случае, если перечисленные причины развития аплазии полностью исключены.
Течение.Согласно международным критериям, принято выделять две основные формы АА. Критериями тяжелой формы являются: содержание нейтрофилов в периферической крови менее 0,5109/л, тромбоцитов — менее 20109/л, ретикулоцитов — менее 10 %о; при исследовании костного мозга отмечается выраженное снижение клеточности или умеренная гипоплазия с количеством гемопоэтических клеток менее 30 %. Если показатели периферической крови соответствуют хотя бы двум критериям, а результаты исследования костного мозга — одному, то можно поставить диагноз тяжелой формы АА. При нетяжелой форме болезни прогноз намного лучше (все перечисленные показатели изменены существенно меньше).
Формулировка развернутого клинического диагнозаапластической (гипопластической) анемии учитывает следующие компоненты: 1) анемии (в данном случае апластической); 2) характер течения (острый, под-острый, хронический); 3) наиболее выраженные синдромы (геморрагический, септико-некротический) и 4) осложнения.
ЛечениеАА — непростая задача, она должна включать:
• ликвидацию (или хотя бы ограничение) контакта больного с лица
ми, страдающими инфекционными заболеваниями (в том числе и
неспецифическими );
• устранение воздействия этиологического фактора (например, ле
карственных или химических средств, если доказана связь между
их приемом и развитием болезни);
• трансфузионную терапию;
• спленэктомию;
• введение антилимфоцитарного глобулина;
• трансплантацию костного мозга.
Объем перечисленных мероприятий несколько различен при разном течении болезни, однако проведение части из них обязательно для всех больных.
Больного АА, особенно при содержании гранулоцитов менее 0,5-109/л, изолируют в специально выделенную палату с боксом (где медицинский персонал меняет обувь и одежду); кожа больного обрабатывается антисептическим мылом, обязательна санация ротовой полости. Для ликвидации кишечной флоры назначают неадсорбируемые антибиотики. Для уменьшения менструальных кровопотерь на длительный срок рекомендуются препараты, уменьшающие кровопотерю или полностью прекращающие менструации (гормональные комбинированные средства).
При глубокой анемии переливают эритроцитную массу или отмытые эритроциты. При количестве тромбоцитов 20-109/л или при наличии геморрагического синдрома осуществляют трансфузии тромбоцитной массы.
При нетяжелой форме эффективна спленэктомия (селезенка является органом, в котором образуются антитела, участвующие в цитотоксических реакциях). Эффект спленэктомии проявляется не сразу.
При тяжелой форме АА эффективен антилимфоцитарный (антимоно-цитарный) глобулин; препарат вводят внутривенно в течение 5 — 8 дней.
Пятилетняя выживаемость после лечения глобулином составляет 50 — 70 %. Антилимфоцитарный глобулин сочетают с циклоспорином А (сан-диммуном), представляющим собой препарат, воздействующий на функцию лимфоцитов путем подавления образования и секреции лимфокинов (возможно, иммуносупрессорный эффект циклоспорина А обусловливает подавление продукции антител против клеток костного мозга и периферической крови). Циклоспорин А назначают внутривенно, а затем внутрь.
При тяжелой форме АА показана трансплантация костного мозга от HLA-совместимого донора; показания к трансплантации ограничиваются возрастом (не старше 40 лет).
Прогноз.При нетяжелой форме А А прогноз более благоприятен. Применение спленэктомии и антилимфоцитарного глобулина обусловливают 5-летнюю выживаемость около 80 % больных. При тяжелой форме болезни прогноз значительно хуже — в течение 6 мес умирают 50 % больных; год прожить могут лишь 20 %.
Профилактика.Исключают контакт с различными внешними факторами (ионизирующая радиация, бензол, цитостатические средства). Меры первичной профилактики идиопатической формы аплазии костного мозга неизвестны.
Сущность гипопластической (апластической)
анемии состоит в резком угнетении
костномозгового кроветворения, что
сопровождается снижением количества
эритроцитов, лейкоцитов и тромбоцитов.
Известна также парциальная форма
гипопластической анемии с угнетением
образования только эритроцитов.
Апластическая анемия (АА) – относительно
редкое заболевание. Его регистрируют
с частотой около 0,5 случая на 100 тыс.
населения. По мере увеличения возраста
пациентов от одного года до 20 лет число
случаев болезни увеличивается. Различий
в частоте заболевания среди лиц в
возрасте от 20 до 60 лет не обнаружено, но
после достижения возраста 60 лет число
больных увеличивается. В некоторых
семьях существует генетическая
предрасположенность к болезни.
Этиология
К резкому угнетению костномозгового
кроветворения приводят различные
причины:
• внешние факторы, оказывающие
миелотоксическое действие (инфекционные
заболевания, ионизирующая радиация,
цитостатические препараты и другие
лекарственные средства, различные
химические вещества);
• внутренние (эндогенные) причины
(влияние токсических веществ при уремии,
гипотиреозе и др.);
• аутоагрессия и образование антител
к кроветворным клеткам;
• идиопатические формы, когда не
удается обнаружить никаких причин
развития анемии (у 50% больных).
Патогенез
Механизм развития гипоплазии (аплазии)
костного мозга окончательно не выяснен.
Предполагают несколько механизмов
развития АА:
• поражение полипотентной стволовой
клетки костного мозга;
• подавление кроветворения, связанное
с воздействием иммунных механизмов
(клеточных, гуморальных);
• нарушения функционирования
элементов микроокружения;
• дефицит факторов, стимулирующих
кроветворение.
Содержание веществ,
непосредственно участвующих в процессе
кроветворения (железо, витамин B12,
протопорфирин), не снижено, но они не
могут быть использованы кроветворной
тканью.
Клиническая картина
Клиническая картина болезни чрезвычайно
разнообразна, в основном связана с
цитопенией и зависит от степени ее
выраженности. Существуют переходные
формы заболевания – от частичного
угнетения кроветворения до выраженной
аплазии костного мозга.
Клиническая картина представлена тремя
основными синдромами: цитопеническим,
септико-некротическим и геморрагическим.
Их различная выраженность обусловливает
разнообразие данных, получаемых на
различных этапах диагностического
поиска.
На первом
этапе диагностического поиска обнаруживают
такие неспецифические признаки, как
повышенная утомляемость и слабость.
Часто больные адаптируются к анемии и
обращаются к врачу лишь при развернутой
картине болезни. Геморрагический синдром
манифестирует различными кровотечениями
(носовыми, маточными) и образованием
кровоподтеков.
На втором
этапе в
начальных стадиях болезни, а также при
хроническом течении обнаруживают лишь
умеренную бледность кожного покрова и
видимых слизистых оболочек, иногда –
кровоподтеки. При остром течении кроме
выраженной бледности отмечают значительный
геморрагический синдром, некроз слизистых
оболочек и высокую лихорадку. Различные
воспалительные заболевания (пневмония)
сопровождаются характерными симптомами.
Печень и селезенка обычно не увеличены,
но при обнаружении антител к эритроцитам
(аутоиммунная форма болезни) возможны
умеренная спленомегалия, а также легкая
желтушность кожи и склер, что связано
с существованием гемолитического
компонента.
Основным считают третий
этап диагностики. В
периферической крови определяют
выраженную анемию (обычно – нормохромную).
Содержание гемоглобина снижается до
20-30 г/л. Количество ретикулоцитов
уменьшается, что свидетельствует о
гипорегенераторном состоянии костного
мозга. Характерны выраженная лейкопения
и гранулоцитопения. Число лимфоцитов
не изменено. Количество тромбоцитов
иногда снижается до нуля. В большинстве
случаев значительно увеличивается СОЭ
(до 30-50 мм/ч).
В костном мозге уменьшено содержание
миелокариоцитов (клеток красного
костного мозга, содержащих ядро),
увеличено число лимфоцитов, тучных и
плазматических клеток. Мегакариоциты
могут полностью отсутствовать. При
гистологическом исследовании костного
мозга обращает на себя внимание почти
полное исчезновение костномозговых
элементов и их замещение жировой тканью.
Содержание железа в крови у большинства
больных увеличено, а насыщение трансферрина
железом достигает практически 100%.
Диагностика
Диагностика заболевания
основана на данных цитологического
анализа периферической крови и
цитоморфологического исследования
костного мозга. При подозрении на АА
обязательно выполнение трепанобиопсии.
Необходимо провести дифференциальную
диагностику с рядом заболеваний,
сопровождающихся цитопенией: дебютом
ОЛ, метастазами рака в костный мозг и
костномозговой формой ХЛЛ. Панцитопения
у пожилых людей также может быть признаком
В12ДА,
но при этом в костном мозге обнаруживают
мегалобласты. При патоморфологическом
изучении трепаната отмечают гиперплазию
костного мозга в противоположность
аплазии при АА. Следует подчеркнуть,
что диагноз АА – диагноз исключения,
устанавливаемый лишь в том случае, если
перечисленные причины развития аплазии
полностью исключены.
Течение
Согласно международным
критериям, принято выделять две основные
формы АА. Критерии тяжелой формы:
количество нейтрофилов в периферической
крови менее 0,5х109/л,
тромбоцитов – менее 20х109/л,
ретикулоцитов – менее 10%. При исследовании
костного мозга отмечают выраженное
снижение клеточности или умеренную
гипоплазию с количеством гемопоэтических
клеток менее 30%. Если показатели
периферической крови соответствуют
хотя бы двум критериям, а результаты
исследования костного мозга – одному,
то можно диагностировать тяжелую форму
АА. При нетяжелой форме заболевания
прогноз намного лучше (все перечисленные
показатели изменены существенно меньше).
Формулировка развернутого клинического
диагноза АА (гипопластической анемии)
должна включать следующие компоненты:
• название анемии (в данном случае
АА);
• характер течения (острый, подострый,
хронический);
• наиболее выраженные синдромы
(геморрагический, септико-некротический);
• осложнения.
Лечение
Лечение АА – непростая задача, включающая:
• ликвидацию (ограничение) контакта
больного с лицами, страдающими
инфекционными заболеваниями (в том
числе и неспецифическими);
• устранение воздействия этиологического
фактора (например, лекарственных или
химических средств, если доказана связь
между их приемом и развитием болезни);
• трансфузионную терапию;
• спленэктомию;
• введение иммуноглобулина
антитимоцитарного;
• применение глюкокортикоидов и
циклоспорина;
• трансплантацию костного мозга.
Объем перечисленных мероприятий при
разном течении болезни неодинаков, но
проведение части из них обязательно
для всех больных.
Больного АА, особенно при
содержании гранулоцитов менее 0,5х109/л,
изолируют в специально выделенную
палату с боксом, где медицинский персонал
меняет обувь и одежду. Кожу пациента
обрабатывают антисептическим мылом;
обязательна санация ротовой полости.
Для ликвидации кишечной микрофлоры
назначают неадсорбируемые антибактериальные
препараты. Для уменьшения менструальных
кровопотерь рекомендовано длительное
применение средств, уменьшающих
кровопотерю или полностью прекращающих
менструации (гормональные комбинированные
препараты).
При глубокой анемии переливают
эритроцитарную массу или отмытые
эритроциты. При количестве тромбоцитов
20х109/л
или геморрагическом синдроме проводят
трансфузии тромбоцитарной массы.
При нетяжелой форме эффективна
спленэктомия, так как селезенка – орган,
в котором образуются антитела, участвующие
в цитотоксических реакциях. Эффект
спленэктомии возникает не сразу.
При тяжелой форме АА эффективен
иммуноглобулин антитимоцитарный.
Препарат вводят внутривенно в течение
5-8 дней. Пятилетняя выживаемость после
лечения им составляет 50-70%. Применение
иммуноглобулина антитимоцитарного
сочетают с назначением циклоспорина –
препарата, влияющего на функцию лимфоцитов
посредством подавления образования и
секреции лимфокинов. Возможно,
иммуносупрессивный эффект циклоспорина
обусловливает подавление продукции
антител против клеток костного мозга
и периферической крови. Сначала назначают
внутривенное введение препарата, а
затем – прием внутрь.
При тяжелой форме АА рекомендована
трансплантация костного мозга от
HLA-совместимого донора. Показания к ней
ограничены возрастом (не старше 40 лет).
Прогноз
При нетяжелой форме АА прогноз более
благоприятный. Выполнение спленэктомии
и применение иммуноглобулина
антитимоцитарного обусловливает
пятилетнюю выживаемость около 80% больных.
При тяжелой форме заболевания прогноз
значительно хуже: в течение 6 мес умирают
50% больных; в течение года живут лишь
20% пациентов.
Профилактика
Исключают контакт с различными внешними
факторами (ионизирующая радиация,
бензол, цитостатические средства). Меры
первичной профилактики идиопатической
формы аплазии костного мозга неизвестны.
Соседние файлы в предмете [НЕСОРТИРОВАННОЕ]
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
