Апластическая анемия у животных

 Гипопластическая и апластическая анемия – Anaemia hipoplastica et aplastica –называются остро протекающие заболевания системы крови, развивающееся в результате недостаточности (истощения) костномозгового кроветворения и проявляющиеся нормоцитарной, иногда макроцитарной, нормохромной анемией с сопутствующей тромбо- и гранулоцитопенией (панцитопенией).
Гипопластическая и апластическая анемия – Anaemia hipoplastica et aplastica –называются остро протекающие заболевания системы крови, развивающееся в результате недостаточности (истощения) костномозгового кроветворения и проявляющиеся нормоцитарной, иногда макроцитарной, нормохромной анемией с сопутствующей тромбо- и гранулоцитопенией (панцитопенией).
Этиология. Причины дефицитных анемий – алиментарные факторы: недостаток в рационе кормления животных протеина, отдельных аминокислот, микроэлементов (железа, меди, кобальта), витаминов (В12, А, Д, С и других). Гипопластические анемии могут служить симптомами хронических гастро-энтероколитов, гепатитов, дистрофий печени, обусловленных пониженной усвояемостью питательных веществ (даже при полноценном кормление животных). Миелотоксические анемии у животных возникают в результате инфекций, инвазий и интоксикаций, чаще при хроническом течении (туберкулез, паратуберкулез, лептоспироз, листериоз, диктиокаулез, аскаридоз, мониезиоз, микозы, кетозы, эндометриты и др.). Анапластические анемии являются следствием воздействия на организм животного в больших дозах ионизирующей радиации (лучевая болезнь), отравления бензолом, соединениями свинца, ртути и других тяжелых интоксикациях.
Патогенез изучен слабо. Под влиянием вышеуказанных этиологических факторов у больного животного вначале развивается гипоплазия, а затем наступает аплазия костного мозга, если доза того или иного фактора достаточно долговременная. Причинные факторы, подавляющие костно — мозговое кроветворение, не вызывают разрушения эритроцитов, анемия развивается в основном за счет уменьшения их регенерации, да и не только их, а и всех клеточных элементов костного мозга. Поэтому наряду с развитием анемии отмечается лейкопения и тромбопения. Происходит одновременно повышение ломкости и порозности кровеносных сосудов, в результате у больного животного появляются кровоизлияния. В последующем пониженная фагоцитарная активность элементов соединительной ткани на фоне лейкопении и резко сниженной способности выработки антител ведет к развитию у животного бактериемии и сепсису.
Патологоанатомические изменения. Слизистые и серозные оболочки у павших животных бледные, часто с точечными и полосчатыми кровоизлияниями. В селезенке кровоизлияния. В легких, иногда в печени, почках и желудочно – кишечном тракте застойная гиперемия. В паренхиматозных органах и коже нередко устанавливаем некрозы. Костный мозг, особенно в трубчатых костях — бледный, местами желтый – жировой. В миокарде, печени и почках выраженная дистрофия.
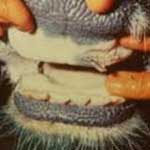
Клинические признаки. На фоне основного заболевания (инфекция, инвазия, отравление) при гипопластической анемии у больного животного прогрессирует общая слабость, быстрая утомляемость, угнетение, отмечаем снижение продуктивности и работоспособности, появляются симптомы расстройства желудочно- кишечного тракта, сухость и взъерошенность кожного покрова, понижается эластичность кожи. При клиническом исследование больного животного устанавливаем характерный признак болезни — бледность видимых слизистых оболочек, склеры и кожи. При апластической анемии в сильной степени выражены общая слабость (иногда больные животные не в состоянии стоять на ногах), животные апатичные, при клиническом осмотре отмечаем бледность видимых слизистых оболочек и кровоизлияния на слизистых оболочках и коже.
Наряду с развитием у больного животного анемии отмечаем быстрое снижение количества лейкоцитов в крови и клеточных элементов в костном мозге. Количество гранулоцитов крови, молодых эритробластических форм и гранулофилоцитов в костном мозге снижается до минимума.
В лейкоцитарной формуле происходит нарастание процента нейтрофилов, а в миелограмме – миелобластических форм. При стахиоботриотоксикозе, чуме количество лейкоцитов крови снижается до 500-100 в 1мм³, резко выражен относительный лимфоцитоз, нейтропения, эозинофилы и моноциты исчезают, нарастает тромбопения. СОЭ ускорена. В костном мозге миелоидные элементы подвергаются дегенеративным изменениям. При тяжелом течении апластической анемии костный мозг становится опустошенным – отмечается бледность клеточными элементами костного мозга (панмиелофтиз). При исследовании обнаруживают в основном только гистиоцитарные и плазматические клетки, и единичные эритробластические формы.
В результате уменьшения массы кроветворной ткани эритропоэз становится явно недостаточным для поддержания состава крови на необходимом уровне; анемия прогрессирует, ее характер может отклонится в сторону гиперхромии. Гемоглобинизация эритроблостав совершается по типу эмбрионального эритропоэза; исчезновение ядра из клетки замедленно и совершается только путем кариорексиса.
Течение чаще острое и отличается своей злокачественностью. На фоне аплазии кроветворной ткани в организме развиваются вторичные инфекции, очаги некрозов, кровотечения и сепсис. Но бывают случаи медленного течения, причем патологические симптомы анемии постепенно усиливаются.
Диагноз на апластическую анемию ставится с учетом анамнеза (интоксикация, инфекция, инвазия), клинических симптомов (анемия, слабость) и анализа крови. Гематологически при гипо- и апластических анемиях устанавливают понижение уровня гемоглобина, лейкопению с преобладанием зрелых форм нейтрофилов, повешенную СОЭ. Характерной особенностью этих групп анемий в отличие от постгеморрагических и гемолитических является пониженное содержание в каждом эритроците гемоглобина при незначительном уменьшении в крови количества эритроцитов, что обуславливает низкий цветовой показатель (обычно хромных) эритроцитов, измененных патологических форм и размеров: пойкилоцитоз, анизоцитоз, большое количество микроцитов (малых размеров по сравнению с нормой), встречаются анулоциты (в виде колец), шизоцыты (в виде обрывков) и др. При исследовании пунктата костного мозга обнаруживают бледность клеточными элементами всех ростков, кровоизлияния.
Дифференциальный диагноз. Заболевание необходимо дифференцировать от гипопластических анемий, анемий при лейкозах у животных, лучевой болезни, ИНАН лошадей, чумы свиней.
Прогноз неблагоприятный.
Лечение. Прежде чем приступить к лечению, необходимо устранить этиологические факторы вызвавшие заболевание и угнетающие кроветворение. При наличии у больного животного тех или иных инвазионных, инфекционных заболеваний и отравлений необходимо проводить соответствующее лечение при данных заболеваниях. Больных животных обеспечивают полноценным рационом кормления с достаточным количеством содержания протеина, полным набором аминокислот, витаминов, макро- и микроэлементов. Для стимулирования костно- мозгового кроветворения необходимо применять препараты железа, кобальта, меди, мышьяка, кампонол, витамины К, В12, фолиевую кислоту и другие. Хорошее лечебное действие оказывает переливание гомогенной стабилизированной крови, внутримышечные или подкожные введения гомогенной или гетерогенной крови, гамма — и полиглобулинов согласно инструкциям и в дозах исходя из наставления по их применению.
При нарастающих симптомах интоксикации при комплексном лечении применяют сердечные средства, 20-40% раствор глюкозы с аскорбиновой кислотой.
При септических осложнениях применяют антибиотики, в том числе современные цефалоспоринового ряда. При полном истощении костного мозга лечить больное животное не целесообразно.
Анемия – патологическое состояние, характеризующееся уменьшением содержания гемоглобина, снижением гематокрита и числа эритроцитов в единице обьёма крови.
Анемия апластическая – заболевание, обусловленное угнетением кроветворной функции костного мозга.
Механизм развития апластической анемии связан, вероятно, с иммунными процессами. Заболевание может быть вызвано или обострено гормональным дисбалансом, повреждением костного мозга или генетической предрасположенностью.
Характерны сонливость, бледность, петехиальные кровоизлияния или кровоточивость слизистых оболочек, гематурия, кровохаркание, мелена вследствие тромбоцитопении, периодическое повышения температуры тела, частые или длительные воспалительные процессы лейкопении.
Диагностика
Апластическую анемию дифференцируют с инфекцией и интоксикациями, а также пролиферативным и инфильтративным процессами в костном мозге.
Используюются пробы на панцитопению (эрлихиоз, вирус лейкоза кошек), на антитела к эритроцитам (проба Кумбса), лейкоцитам и тромбоцитам, на другие аутоиммунные болезни (антинуклеарные антитела к системной красной волчанке). Аспирационная биопсия костного мозга может выявить недостаточное число гемопоэтических элементов и значительное количество жира.
Лечение
Проводят антибиотикотерапию, переливание крови или тромбоцитарной массы, назначают глюкокортикоиды и другие иммуносупресанты, анаболические стероиды и колонниестимулирующие факторы поотдельности или в комбинации.
При появлении сонливости, лихорадки и кровоизлияний, возникающих при рецидиве анемии, лейкопении и тромбоцитопении следует немедленно обратиться к врачу. Необходимо ежедневно пальпировать лимфатические узлы, измерять температуру тела. Выздоровление может наступить через 1 или несколько месяцев в зависимости от результатов клинического анализа крови (степень уменьшения числа кровяных клеток и тромбоцитов), возраста и общего состояние животного, а также причины болезни.
Анемия аутоиммунная гемолитическая
Анемия, обусловленная разрушением эритроцитов аутоантителами с последующим их захватом макрофагами и депонированием в селезёнке.
Специфические аутоантитела вырабатываются против антигенов мембраны неизменных (первичная аутоиммунная гемолитическая анемия) или повреждённых (вторичная аутоиммунная гемолитическая анемия) эритроцитов.
При аутоиммунной гемолитической анемии поражаются кроветворная, лимфатическая и иммунная системы. Если печень и желчевыводящие пути не могут справиться с билирубиновой нагрузкой, развиваются гипербилирубинемия и желтуха.
Гипоксия может привести к центрилобулярному некрозу печени. Также гипоксия вызывает тахикардию, а снижение вязкости и турбулентности тока крови – приглушенность сердечных тонов. При хронической анемии развивается сердечная недостаточность на фоне высокого сердечного выброса. Со стороны дыхательной системы наблюдается тахипноэ, со стороны почек и почечных путей – некроз почечных канальцев.
В анамнезе отмечают эпизоды потери сознания, вялость, сонливость, потерю аппетита, одышку, учащённое дыхание, рвоту, понос, иногда полиурию и полидипсию.
При обследовании обращают на себя внимание бледность слизистых, тахикардия, тахипноэ, желтуха, тёмная моча окрашенная гемоглобином или билирубином), лихорадка, увеличение селезёнки, печени и лимфатических узлов, систолический шум, ритм галопа. При сопутствующей тромбоцитопении при синдроме диссеминированного сосудистого свёртывания крови могут наблюдать петехии, экхимозы или мелена.
Диагностика
При общем клиническом анализе крови выявляются: анемия, увеличенный средний объём эритроцитов (через 3-5 дней после гемолитического криза), сдвиг лейкоцитарной формулы влево. В моче – гемоглобин.
В пунктате костного мозга обычно определяются гиперплазия эритроидного отростка, при арегенераторной анемии прекращается созревание и наблюдается цитопения юных клеток, а при хронической форме – миелофиброз.
При физикальном обследовании определяются гепатоспленомегалия, реактивное увеличение лимфатических узлов, признаки застойной сердечной недостаточности (отёк лёгких, кардиомегалия, мускатная печень), тромбоэмболия лёгочной артерии, синдром диссеминированного внутрисосудистого свёртывания.
Лечение
 При остром гемолитическом кризе лечение проводят в стационаре, до стабилизации гематокрита, прекращения гемолиза и устранения анемии. При развитии осложнений (синдром дессиминированнного внутрисосудистого свёртывания, , тромбоэмболия лёгочной артерии, тромбоцитопения, желудочно-кишечные кровотечения, сердечная недостаточность), при необходимости в повторных гемотрансфузиях показана госпитализация. Хронический внесосудистый гемолиз лёгкой степени госпитализации не требует, если анемия клинически не проявляется.
При остром гемолитическом кризе лечение проводят в стационаре, до стабилизации гематокрита, прекращения гемолиза и устранения анемии. При развитии осложнений (синдром дессиминированнного внутрисосудистого свёртывания, , тромбоэмболия лёгочной артерии, тромбоцитопения, желудочно-кишечные кровотечения, сердечная недостаточность), при необходимости в повторных гемотрансфузиях показана госпитализация. Хронический внесосудистый гемолиз лёгкой степени госпитализации не требует, если анемия клинически не проявляется.
Следует понимать, что аутоиммунная гемолитическая анемия и её осложнения, представляют опасность для жизни, и может потребоваться пожизненная терапия, в ряде случаев сопровождающаяся тяжёлыми побочными реакциями, и что болезнь может рецидивировать.
При выборе медикаментозной и инфузионной терапии, вызвавшую заболевание (инфекция, лекарственные препараты при вторичной аутоиммунной гемолитической анемией). Назначают преднизолон, при отсутствие эффекта назначают иммунодепрессанты.
В острую фазу аутоиммунной гемолитической анемии необходимо ежедневно определять гематокрит, чтобы оценить эффективность терапии и потребность в переливании крови. В стационаре несколько раз в сутки сосчитывают частоту дыхания и сердечных сокращений, проводят общий и биохимический анализы крови. При подозрении на тромбоэмболию лёгочной артерии часто проводят рентгенографию грудной клетки и исследование газов артериальной крови.
В течение первого месяца амбулаторного лечения до стабилизации состояния раз в неделю исследуют гематокрит, затем – каждые 2 недели в течение 2 месяцев
Анемия гемолитическая Хайнца (Эрлиха)
Анемия, обусловленная проникновением в организм оксидантов и разрушением гемоглобина.
Фрагменты последнего, обнаруживаемые в эритроцитах, названные тельцами Хайнца (Эрлиха), или включениями.
Дефектные эритроциты депонируются или подвергаются лизису в селезёнке. В ряде случаев болезнь сопровождается метгемоглобинемией.
Чаще наблюдается у кошек, гемоглобин которых более чувствителен к действию оксидантов. Окислительными свойствами обладают лук, вещества содержащие цинк, D, I, L-метионин (у кошек); а также лекарственные средства – ацетаминофен (у кошек) и фенацетин (у собак)
Диагностика
При тяжёлой анемии в крови и моче определяется свободный гемоглобин. Гематокрит и число ретикулоцитов указывают на тяжесть регенеративной анемии.
Лечение
Бывает достаточно исключить травмирующий фактор – оксиданты, , и проводить симптоматическую терапию (переливание крови, кислородотерапия, ограничение активности).
Необходимо периодически исследовать гематокрит, число ретикулоцитов и процент эритроцитов, содержащих тельца Хайнца, документируя процесс исчезновения последних и восстановления числа нормальных эритроцитов. Если удалось преодолеть гемолиз эритроцитов, прогноз благоприятный.
Анемия железодефицитная
патологическое состояние, обусловленное дефицитом железа в организме.
При недостаточности поступление этого элемента нарушается эритропоэтическая функция костного мозга. Самая распространённая причина железодефицитной анемии – кровопотеря, источником которой чаще всего является ЖКТ, реже мочевыводящие пути. Причиной анемии могут быть новообразования, сильное поражение блохами, а также нематодная инвазия.
Железодефицитная анемия чаще встречается у собак, реже – у взрослых кошек. У 50% 5-10- недельных котят развивается так называемая преходящая железодефицитная анемия новорождённых.
Диагностика
В крови обнаруживают микроцитоз, гипохромия – характерный признак. Низкое содержание железа в плазме крови подтверждают диагноз.
Лечение
Восполнение запаса железа – для парентерального введения используют феррум-лек. Каждые 1-4 недели необходим контроль гемограммы. У некоторых животных восстановление нормальной восстановление нормальной формулы эритроцитов может происходить в течение нескольких месяцев.
Анемия гипопластическая макроцитарная
Наследственное заболевание, характеризующиеся остановкой развития ядра в клетке предшественнице эритроцита вследствие нарушения синтеза ДНК при нормальном развитии цитоплазмы.
Выявлено несколько факторов, предрасполагающих к макроцитарной анемии или провоцирующих её:
-Инфекция (вирус лейкоза кошек)
-Несбалансированное кормление (нехватка фолиевой кислоты, дефицит витамина В12)
-Токсины (интоксикация дилантином, отравление метотрексатом или другими токсическими веществами)
-Наследственные (той пудель)
Макроцитарная анемия обычно протекает в лёгкой форме
Диагностика
Классическая макроцитарная анемия (большой средний обьем эритроцитов) и сопутствующая нормохромия (средняя концентрация гемоглобина.
Из специфических исследований важны тесты для определения вируса лейкоза и иммунодефицита кошек: ретровирусная инфекция является наиболее частой причиной мегалобластной анемии у кошек. Заключительный диагноз ставят на основании исследования костного мозга, часто во всех клеточных линиях.
Лечение
Направлено на устранение причины болезни. Эффективность лечения определяют по результатам общего анализа крови (еженедельно) и костного мозга (индивидуально).
У кошек с положительной реакцией на вирус лейкоза прогноз осторожный. У животных с лекарственно-обусловленной анемией прогноз благоприятен при условии своевременной отмены препарата.
Анемия при хронических заболеваниях почек (прогрессирующей почечной недостаточностью)
характеризуется низким гематокритом, уменьшением количества эритроцитов и содержания в них гемоглобина, гипоплазией эритроидных элементов костного мозга.
Причиной анемии могут быть врождённые и приобретённые формы почечной недостаточности ( пиелонефрит, гломерулонефрит, амилоидоз )
Диагностика
При клиническом и биохимическом анализах крови и мочи выделяются нормоцитарная нормохромная арегенераторная анемия, высокий уровень азота мочевины крови, креатенина, фосфора, кальция, низкий гидрокарбоната и калия. Отмечаются нарушения мочеотделения, умеренная протеинурия, наличие активного осадка. На рентгенограммах видны небольшие неправильной формы почки с нарушенной структурой.
Лечение
Если появляются симптомы анемии, необходимо увеличить количество эритроцитов. Для коррекции анемии при хронической почечной недостаточности используют эритропоэтин. Для лечения язв и кровотечений ЖКТ – ранитидин, сукралфат. Следуют лечить также системную гипертензию.
Определение гематокрита осуществляют в первые 3 месяца еженедельно, затем 1 раз в 1-2 месяца, артериальное давление измеряют 1-2 раза в месяц.
Апластическая анемия – состояние, характеризующееся снижением гематопоэтической активности (депрессией) костного мозга с развитием наряду с анемией также лейко- и тромбоцитопении.
Этиологии и патогенез.
Апластическая анемия может развиться при воздействии ряда миелотоксических факторов:
ионизирувщего излучения,
химических веществ – бензола, солей золота, мышьяка;
лекарственных средств – хлорамфеникола (левомицетина), фенилбутазона (бутадион), хлорпромазина (аминозин), мепробамата, дилантина, антиметаболитов (б-меркаптопурина, метотрексата), алкилирующих (циклофосфана, хлорбутина)
и некоторых других средств.
Миелотоксический эффект от воздействия одних факторов (ионизирующее излучение, антиметаболиты) возникает всегда при достаточно большой дозе, других – проявляется индивидуально.
Причина индивидуальной чувствительности, в частности к некоторым лекарственным средствам не всегда ясна, но может быть связана с генетическими дефектами кронетнорных клеток.
Это относится, например, к хлорамфениколу и фенилбутазону, которые вызывают супрессию (в зависимости от дозы) эритропоэза с частотой соответственно 1:24000 и 1:40000 лиц, их принимающих.
Наследственный характер индивидуальной чувствительности эритропоэтических клеток к данным лекарственным веществам подтверждается развитием аплазии костного мозга у разных членов одной семьи и у однояйцевых близнецов.
В других случаях вероятна связь индуцированного лекарственными веществами угнетения кроветворения с иммунными меха низмами появлением антител к эритроцитарным предшественникам.
Описаны случаи возникновения апластической анемии после острого вирусного гепатита (возможно, вследствие способности вируса гепатита изменять кариотип клеток, что было прослежено на культуре лейкоцитов), перенесенной инфекции вирусом Эпстайна – Барра, парвовирусом.
Существует и наследственная форма апластической анемии – анемия Фанкони.
Более чем у половины больных не удается выявить какие-либо причинные факторы – это так называемая идгопатическая апластическая анемия.
Механизмы, лежащие в основе идиопатической формы анемии, неясны.
Возможен аутоиммунный механизм, связанный с воздействием на клетки костного мозга аутоантител при участии иммунных лимфоцитон.
Показано, что лимфоциты (Т-супрессоры) больных тормозят образование эритроцитных колоний костного мозга донора и могут нарушать дифференциацию и пролиферацию гематопоэтических предшественников.
Предполагают также, что основой апластической анемии может быть поражение (внутренний дефект) стволовой клетки, о чем свидетельствует восстановление кроветворения у больных после трансплантации им аллогенного костного мозга, содержащего нормальные стволовые клетки.
Существуют экспериментальные данные, свидетельствующие о значении для развития апласткческого процесса и нарушений микроокружения – первичного дефекта стромальных клеток костного мозга.
Однако суть этих клеточных дефектов остается неясной, так же как и их первичность.
Возможно, что при разных формах апластической анемии патогенетические механизмы неодинаковы.
Клиническая картина.
Идиопатическая апластическая анемия может начинатьсл остро и иметь быстро прогрессирующее течение, но чаще болезнь развивается постепенно.
Клинические проявления зависят от выраженности цитопении.
При физическом исследовании отмечаются бледность кожных покровов, одышка, тахикардия, выслушивается систолический шум в области сердца.
Геморрагический синдром соответствует степени тромбоцитопении, наблюдаются петехиальные высыпания на коже и слизистых оболочках, кровоточивость десен, носовые и маточные кровотечения.
Следствием нейтропении являются инфекционные осложнения – ангины, пневмонии, инфекция мочевых путей, сепсис.
Селезенка обычно не увеличена.
Лабораторные данные.
Гематологическими признаками аплазии костного мозга являются выраженная анемия (концентрация гемоглобина может падать до 20 – 30 г/л), лейкопения (нейтропения с относительным лимфоцитозом) и тромбоцитопения, иногда до полного исчезновения тромбоцитов из крови.
Анемия чаще нормохромная и макроцитарная (СЭО) 94 мкм’ отмечается примерно у 60 – 65 % больных), число ретикулоцитов снижено.
Содержание железа в сыворотке крови нормальное или повышенное, насыщение трансферрина близко к 100 %.
В ряде случаев отмечается повышение уровня фетального гемоглсбина (НЬР составляет до 15% от общего гемоглобина) и эритропоэтина (поскольку продукция эритроцитов резко снижена, то либо существует ингибитор эритропоэтина, либо костный мозг к нему нечувствителен).
СОЭ обычно увеличена до 40 – 60 мм/ч.
При пункционной биопсии костного мозга получают малое количество ядросодержащих клеток (миелокариоцитов) или они совсем отсутствуют, при гистологическом исследоваиии отмечают замещение гемопоэтической ткани жировой тканью.
Однако даже если биопсию производят в разных местах, то она не отражает состояние всего костного мозга:
на аутопсии часто обнаруживают островки кроветворения (регенерации), содержащие двуядерные и многоядерные эритроидные клетки, среди значительно опустошенного костного мозга.
При быстром прогрессировании болезни смерть может наступить через несколько месяцев, при хроническом течении происходит смена обострения и ремиссий.
Иногда наблюдается полное выздоровление.
Апластическая анемия Фанкони – наследственная, часто семейная аномалия, передающаяся по аутосомнорецессивному типу;
выявляется у молодых, характеризуется, помимо аплазии костного мозга и панцитопении, также рядом соматических и метаболических нарушений:
задержкой роста, дефектами формирования скелета, микроцефалией, гипогонадизмом, гипоплазией почек, аминоацидурией, глюкозурией, гиперпигментацией кожи.
Изменения показателей крови часто менее выражены, чем при идиопатической форме апластической анемии.
Наблюдается склонность к развитию острого лейкоза.
Диагноз и дифференциальный диагноз.
Апластическую анемию предполагают при снижении в крови количества эритроцитов, лейкоцитов и тромбоцитов (панцитопения).
Диффереициальную диагностику следует проводить с острым лейкозом и В12-дефицитной анемией.
Важное значение имеет стернальная пункция:
при обнаружении гиперплазии эритроцитарного ростка апластическая анемия исключается.
Если увеличенные в количестве эритроидные элементы имеют морфологические черты мегалобластов, то вероятно наличие у больного В12-дефицитной анемии, но при этом необходимо иметь в виду и возможность эритромиелоза.
Присутствие в костномозговом пунктате большого количества бластных клеток свидетельствует об остром лейкозе.
Получение при пункции скудного материала еще не может быть расценено как указание на аплазию костного мозга, так как такая картина бывает и при остром алейкемическом лейкозе.
Для уточнения диагноза производят трепанобиопсию кости; уменьшение активного кроветворного костиого мозга и увеличение жировой ткани подтверждает диагноз апластической анемии.
Апластическую анемию необходимо дифференцировать и с иммунной периферической цитопенией.
Для диагностики иммунной цитопении имеют значение обнаружение увеличенной селезенки, положительные проба Кумбса или агрегатгемагглютационная проба, нормальное количество мегакариоцитов в костном мозге.
Отграничение апластической анемии от пароксизмальной ночной гемоглобинурии и гемолизиновых форм аутоиммунной гемолитической анемии основывается на отсутствии при апластической анемии признаков внутрисосудистого гемолиза, ретикулоцитоза, увеличения селезенки.
Лечение и прогноз.
Лечение направлено на коррекцию цитопенического синдрома и костномозговой недостаточности и борьбу с осложнениями.
Вначале отменяют все лекарственные средства, к которым у собаки имеется индивидуальная повышенная чувствительность и которые могут быть причастны к развитию анемии.
При тяжелой анемии проводят заместительные трансфузии отмытых эритроцитов, при выраженной тромбоцитопении и геморрагиях – переливания тромбоцитарной массы (от одного донора).
При инфекционных осложнениях применяют антибиотики широкого спектра действия.
Наиболее перспективным методом лечения апластической анемии является трансплантация аллогенного совместимого по НЕА-антигенам костного мозга.
Трансплантация костного мозга показана животным молодого возраста, особенно с тяжелыми, прогностически неблагоприятными формами болезни
(уровень тромбоцитов ниже 20 ° 10’/л, нейтрофилов менее 0,5 ° 10′!л, количества ретикулоцитов после коррекции менее чем 1 % и числа клеток костного мозга менее 25 % от общего объема).
Трансплантация при наличии подходящего донора должна быть ранней, когда аллоиммунизация вследствие заместительной терапии еще невелика.
В случаях невозможности трансплантации предпринимают попытку лечения преднизолоном в высоких дозах (60 – 80 мг/сут),
при отсутствии эффекта – в небольших дозах, в основном с гемостатической целыо.
У ряда животных (по некоторым данным, более чем у половины) оказывается успешной спленэктомия (в связи с удалением органа, вырабатывающего антитела).
Спленэктомия показана при менее тяжелых формах болезни – отсутствии большой кровоточивости и признаков сепсиса.
Эффект наступает через 2 – 5 мес после операции, но кровоточивость обычно уменьшается сразу.
После спленэктомии проводят лечение анаболическими гормонами (неробол по 20 мг/сут, анаполон по 200 мг/сут в течение полугода).
Для лечения апластической анемии применяют также антилимфоцитарный глобулин, по данным зарубежных авторов, использование коммерческого антилимфоцитарного глобулина эффективно у 40 – 50% пациентов, что позволяет рекомендовать его на ранних этапах лечения.
По опыту отечественных гематологов антилимфоцитарный глобулин целесообразно назначать после спленэктомии (при ее неэффективности или как подкрепляющую терапию), кроличий и козий антилимфоцитарный глобулин отечественного производства вводят внутривенно по 120 – 160 мг 10 – 15 раз.
 Супертёплый дом-термос для Вашей собаки!
Супертёплый дом-термос для Вашей собаки!
