Что такое окисленный гемоглобин
Молекула гемоглобина: 4 субъединицы окрашены в разные цвета
Структура гемоглобина человека. Железосодержащие гем-группы показаны зелёным. Красным и синим показаны альфа- и бета- субъединицы.
Гемоглоби́н (от др.-греч. αἷμα «кровь» + лат. globus «шар») (Hb или Hgb) — сложный железосодержащий белок животных, обладающих кровообращением, способный обратимо связываться с кислородом, обеспечивая его перенос в ткани. У позвоночных животных содержится в эритроцитах, у большинства беспозвоночных растворён в плазме крови (эритрокруорин) и может присутствовать в других тканях[1]. Молекулярная масса гемоглобина человека — около 66,8 кДа. Молекула гемоглобина может нести до четырёх молекул кислорода. Один грамм гемоглобина может переносить до 1.34 мл. O2
Гемоглобин появился более чем 400 миллионов лет назад у последнего общего предка человека и акул в результате 2 мутаций, приведших к формированию четырёхкомпонентного комплекса гемоглобина, сродство которого к кислороду достаточно для связывания кислорода в насыщенной им среде, но недостаточно, чтобы удерживать его в других тканях организма.[2][3]
Большой вклад в исследование структуры и функционирования гемоглобина внёс Макс Фердинанд Перуц, получивший за это в 1962 году Нобелевскую премию[4].
Нормальным содержанием гемоглобина в крови человека считается: у мужчин — 130—160 г/л (нижний предел — 120, верхний предел — 180 г/л), у женщин — 120—160 г/л; у детей нормальный уровень гемоглобина зависит от возраста и подвержен значительным колебаниям. Так, у детей через 1—3 дня после рождения нормальный уровень гемоглобина максимален и составляет 145—225 г/л, а к 3—6 месяцам снижается до минимального уровня — 95—135 г/л, затем с 1 года до 18 лет отмечается постепенное увеличение нормального уровня гемоглобина в крови[5].
Во время беременности в организме женщины происходит задержка и накопление жидкости, что является причиной гемодилюции — физиологического разведения крови. В результате наблюдается относительное снижение концентрации гемоглобина (при беременности уровень гемоглобина в норме составляет 110—155 г/л). Кроме этого, в связи с внутриутробным ростом ребёнка происходит быстрое расходование запасов железа и фолиевой кислоты. Если до беременности у женщины был дефицит этих веществ, проблемы, связанные со снижением гемоглобина, могут возникнуть уже на ранних сроках беременности[6].
Главные функции гемоглобина: перенос кислорода и буферная функция. У человека в капиллярах лёгких в условиях избытка кислорода последний соединяется с гемоглобином. Потоком крови эритроциты, содержащие молекулы гемоглобина со связанным кислородом, доставляются к органам и тканям, где кислорода мало; здесь необходимый для протекания окислительных процессов кислород освобождается от связи с гемоглобином. Кроме того, гемоглобин способен связывать в тканях небольшое количество диоксида углерода (CO2) и освобождать его в лёгких.
Монооксид углерода (CO) связывается с гемоглобином крови намного сильнее (в 250 раз[7]), чем кислород, образуя карбоксигемоглобин (HbCO). Впрочем, монооксид углерода может быть частично вытеснен из гема при повышении парциального давления кислорода в лёгких. Некоторые процессы приводят к окислению иона железа в гемоглобине до степени окисления +3. В результате образуется форма гемоглобина, известная как метгемоглобин (HbOH) (metHb, от «мета-» и «гемоглобин», иначе гемиглобин или ферригемоглобин, см. Метгемоглобинемия). В обоих случаях блокируются процессы транспортировки кислорода.
Строение[править | править код]
Гемоглобин является сложным белком класса гемопротеинов, то есть в качестве простетической группы здесь выступает гем — порфириновое ядро, содержащее железо. Гемоглобин человека является тетрамером, то есть состоит из 4 протомеров. У взрослого человека они представлены полипептидными цепями α1, α2, β1 и β2. Субъединицы соединены друг с другом по принципу изологического тетраэдра. Основной вклад во взаимодействие субъединиц вносят гидрофобные взаимодействия. И α-, и β-цепи относятся к α-спиральному структурному классу, так как содержат исключительно α-спирали. Каждая цепь содержит восемь спиральных участков, обозначаемых буквами от A до H (от N-конца к C-концу).
Гем представляет собой комплекс протопорфирина IX, относящегося к классу порфириновых соединений, с атомом железа(II). Этот кофактор нековалентно связан с гидрофобной впадиной молекул гемоглобина и миоглобина.
Железо(II) характеризуется октаэдрической координацией, то есть связывается с шестью лигандами. Четыре из них представлены атомами азота порфиринового кольца, лежащими в одной плоскости. Две другие координационные позиции лежат на оси, перпендикулярной плоскости порфирина. Одна из них занята азотом остатка гистидина в 93-м положении полипептидной цепи (участок F). Связываемая гемоглобином молекула кислорода координируется к железу с обратной стороны и оказывается заключённой между атомом железа и азотом ещё одного остатка гистидина, располагающегося в 64-м положении цепи (участок E).
Всего в гемоглобине человека четыре участка связывания кислорода (по одному гему на каждую субъединицу), то есть одновременно может связываться четыре молекулы. Гемоглобин в лёгких при высоком парциальном давлении кислорода соединяется с ним, образуя оксигемоглобин. При этом кислород соединяется с гемом, присоединяясь к железу гема на 6-ю координационную связь. На эту же связь присоединяется и монооксид углерода, вступая с кислородом в «конкурентную борьбу» за связь с гемоглобином, образуя карбоксигемоглобин.
Связь гемоглобина с монооксидом углерода более прочная, чем с кислородом. Поэтому часть гемоглобина, образующая комплекс с монооксидом углерода, не участвует в транспорте кислорода. В норме у человека образуется 1,2 % карбоксигемоглобина. Повышение его уровня характерно для гемолитических процессов, в связи с этим уровень карбоксигемоглобина является показателем гемолиза.
Физиология[править | править код]
Изменение состояний окси- и дезоксигемоглобина
В отличие от миоглобина гемоглобин имеет четвертичную структуру, которая придаёт ему способность регулировать присоединение и отщепление кислорода и характерную кооперативность: после присоединения первой молекулы кислорода связывание последующих облегчается. Структура может находиться в двух устойчивых состояниях (конформациях): оксигемоглобин (содержит 4 молекулы кислорода; напряжённая конформация) и дезоксигемоглобин (кислорода не содержит; расслабленная конформация).
Устойчивое состояние структуры дезоксигемоглобина усложняет присоединение к нему кислорода. Поэтому для начала реакции необходимо достаточное парциальное давление кислорода, что возможно в альвеолах лёгких. Изменения в одной из 4-х субъединиц влияет на оставшиеся, и после присоединения первой молекулы кислорода связывание последующих облегчается.
Отдав кислород тканям, гемоглобин присоединяет к себе ионы водорода и углекислый газ, перенося их в лёгкие[8].
Гемоглобин является одним из основных белков, которыми питаются малярийные плазмодии — возбудители малярии, и в эндемичных по малярии районах земного шара весьма распространены наследственные аномалии строения гемоглобина, затрудняющие малярийным плазмодиям питание этим белком и проникновение в эритроцит. В частности, к таким имеющим эволюционно-приспособительное значение мутациям относится аномалия гемоглобина, приводящая к серповидноклеточной анемии. Однако, к несчастью, эти аномалии (как и аномалии строения гемоглобина, не имеющие явно приспособительного значения) сопровождаются нарушением кислород-транспортирующей функции гемоглобина, снижением устойчивости эритроцитов к разрушению, анемией и другими негативными последствиями. Аномалии строения гемоглобина называются гемоглобинопатиями.
Гемоглобин высокотоксичен при попадании значительного его количества из эритроцитов в плазму крови (что происходит при массивном внутрисосудистом гемолизе, геморрагическом шоке, гемолитических анемиях, переливании несовместимой крови и других патологических состояниях). Токсичность гемоглобина, находящегося вне эритроцитов, в свободном состоянии в плазме крови, проявляется тканевой гипоксией — ухудшением кислородного снабжения тканей, перегрузкой организма продуктами разрушения гемоглобина — железом, билирубином, порфиринами с развитием желтухи или острой порфирии, закупоркой почечных канальцев крупными молекулами гемоглобина с развитием некроза почечных канальцев и острой почечной недостаточности.
Ввиду высокой токсичности свободного гемоглобина в организме существуют специальные системы для его связывания и обезвреживания. В частности, одним из компонентов системы обезвреживания гемоглобина является особый плазменный белок гаптоглобин, специфически связывающий свободный глобин и глобин в составе гемоглобина. Комплекс гаптоглобина и глобина (или гемоглобина) затем захватывается селезёнкой и макрофагами тканевой ретикуло-эндотелиальной системы и обезвреживается.
Другой частью гемоглобинообезвреживающей системы является белок гемопексин[en], специфически связывающий свободный гем и гем в составе гемоглобина. Комплекс гема (или гемоглобина) и гемопексина затем захватывается печенью, гем отщепляется и используется для синтеза билирубина и других жёлчных пигментов, или выпускается в рециркуляцию в комплексе с трансферринами для повторного использования костным мозгом в процессе эритропоэза.
Экспрессия генов гемоглобина до и после рождения.
Также указаны типы клеток и органы, в которых происходит экспрессия гена (данные по Wood W. G., (1976). Br. Med. Bull. 32, 282.).[9]
Гемоглобин при заболеваниях крови[править | править код]
Дефицит гемоглобина может быть вызван, во-первых, уменьшением количества молекул самого гемоглобина (см. анемия), во-вторых, из-за уменьшенной способности каждой молекулы связать кислород при том же самом парциальном давлении кислорода.
Гипоксемия — это уменьшение парциального давления кислорода в крови, её следует отличать от дефицита гемоглобина. Хотя и гипоксемия, и дефицит гемоглобина являются причинами гипоксии.
Если дефицит кислорода в организме в общем называют гипоксией, то местные нарушения кислородоснабжения называют ишемией.
Прочие причины низкого гемоглобина разнообразны: кровопотеря, пищевой дефицит, болезни костного мозга, химиотерапия, отказ почек, атипичный гемоглобин.
Повышенное содержание гемоглобина в крови связано с увеличением количества или размеров эритроцитов, что наблюдается также при истинной полицитемии. Это повышение может быть вызвано: врождённой болезнью сердца, лёгочным фиброзом, слишком большим количеством эритропоэтина.
См. также[править | править код]
- Гемоглобин А
- Гемоглобин С (мутантная форма)
- Эмбриональный Гемоглобин (эмбриональный)
- Гемоглобин S (мутантная форма)
- Гемоглобин F (фетальный)
- Кобоглобин
- Нейроглобин
- Анемия
- Порфирия
- Талассемия
- Эффект Вериго — Бора
Примечания[править | править код]
- ↑ Haemoglobins of invertebrate tissues. Nerve haemoglobins of Aphrodite, Aplysia and Halosydna
- ↑ Ученые выяснили происхождение гемоглобина. РИА Новостей, 20.05.2020, 18:59
- ↑ Michael Berenbrink. Evolution of a molecular machine/Nature, NEWS AND VIEWS, 20 MAY 2020
- ↑ Лауреаты нобелевской премии. Макс Перуц.
- ↑ Назаренко Г. И., Кишкун А. А. Клиническая оценка результатов лабораторных исследований. — 2005.
- ↑ Общий анализ крови и беременность Архивная копия от 10 марта 2014 на Wayback Machine
- ↑ Hall, John E. Guyton and Hall textbook of medical physiology (англ.). — 12th ed.. — Philadelphia, Pa.: Saunders/Elsevier, 2010. — P. 1120. — ISBN 978-1416045748.
- ↑ Степанов В. М. Структура и функции белков : Учебник. — М. : Высшая школа, 1996. — С. 167—175. — 335 с. — 5000 экз. — ISBN 5-06-002573-X.
- ↑ Айала Ф., . Современная генетика: В 3-х т = Modern Genetics / Пер. А. Г. Имашевой, А. Л. Остермана, . Под ред. Е. В. Ананьева. — М.: Мир, 1987. — Т. 2. — 368 с. — 15 000 экз. — ISBN 5-03-000495-5.
Литература[править | править код]
- Mathews, CK; KE van Holde & KG Ahern (2000), Biochemistry (3rd ed.), Addison Wesley Longman, ISBN 0-8053-3066-6
- Levitt, M & C Chothia (1976), “Structural patterns in globular proteins”, Nature
Ссылки[править | править код]
- Eshaghian, S; Horwich, TB; Fonarow, GC (2006). “An unexpected inverse relationship between HbA1c levels and mortality in patients with diabetes and advanced systolic heart failure”. Am Heart J. 151 (1): 91.e1—91.e6. DOI:10.1016/j.ahj.2005.10.008. PMID 16368297.
- Kneipp J, Balakrishnan G, Chen R, Shen TJ, Sahu SC, Ho NT, Giovannelli JL, Simplaceanu V, Ho C, Spiro T (2005). “Dynamics of allostery in hemoglobin: roles of the penultimate tyrosine H bonds”. J Mol Biol. 356 (2): 335—53. DOI:10.1016/j.jmb.2005.11.006. PMID 16368110.
- Hardison, Ross C. (2012). “Evolution of Hemoglobin and Its Genes”. Cold Spring Harbor Perspectives in Medicine. 2 (12): a011627. DOI:10.1101/cshperspect.a011627. ISSN 2157-1422. PMC 3543078. PMID 23209182.
Аномальная форма гемоглобина, при которой атомы двухвалентного железа окисляются до трёхвалентного под воздействием токсичных веществ, кислородсодержащих лекарственных препаратов либо по причине наследственных нарушений молекул гемоглобина называется метгемоглобином.
Перевоплощение природного гемоглобина в метагемоглобин происходит путем его окисления, в результате чего формула железа Fe2+ переходит в трехвалентное состояние – Fe3+.
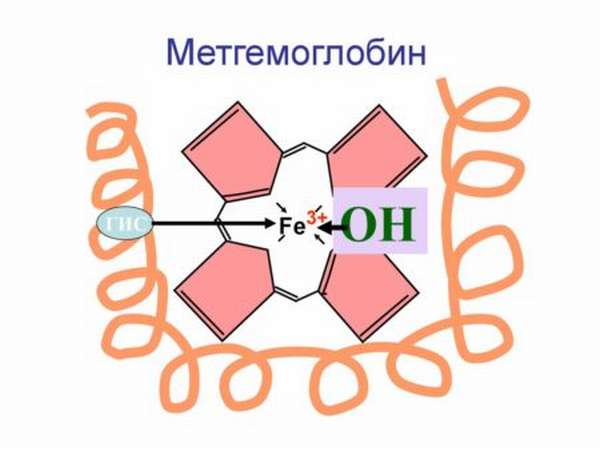
Особенности
Главная отличительная особенность метгемоглобина в том, что он не способен соединяться с молекулами кислорода и переносить его к человеческим органам и тканям, вследствие чего наступает кислородное голодание организма.
В крови здорового человека метгемоглобин присутствует в незначительных количествах. Норма метгемоглобина в крови составляет примерно 1% (с погрешностью до 3%). Если его присутствие превышает указанную норму, наступает заболевание – метгемоглобинемия.
Метгемоглобин: норма в крови, понятие и разновидности
Метгемоглобинемией называют заболевание, при котором в эритроцитах значительная часть гемоглобина содержит окисленное трехвалентное железо. Гемоглобин, как важнейший элемент, отвечает за транспортировку кислорода по организму. Окисляясь до метгемоглобина, он теряет это свойства, что приводит к гипоксии органов и тканей.
Различают три формы метгемоглобинемии:
- Врождённая. Крайне редкая форма заболевания. Не влияет на продолжительность и качество жизни.
- Генетическая. При этой форме заболевания причиной увеличения доли метгемоглобина становится генетическая предрасположенность. В этом случае происходит врождённая метаболическая ошибка, которая приводит организм в состояние метгемоглобинемии. Последствиями этой формы болезни очень серьезные: умственная отсталость, микроцефалия. Продолжительность жизни короткая, как правило, люди умирают в молодом возрасте.
- Приобретенная. Данная форма более распространена. Возникает по причине воздействия на организм веществ, вызывающих метгемоглобинемию. Происходит в результате приема ряда лекарств или под воздействием токсичных веществ.
Диагностика и лечение метгемоглобинемии у взрослых и детей
Симптоматические признаки и последствия метгемоглобинемии зависят от формы и уровня метгемоглобина:
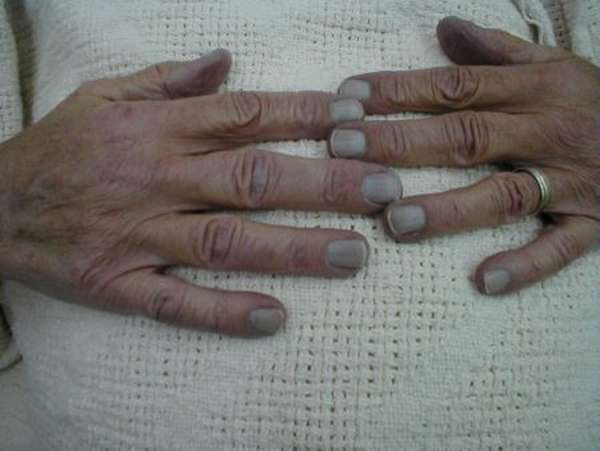
- Уровень 3-15% – появляется характерный бледный, серый либо синюшный оттенок кожи, утолщение ногтевых пластин.
- Уровень 15-20 % – появляется цианоз.
- Уровень 25-50% – отмечаются физиологические последствия: мигрень, общая слабость, одышка, боль в груди, спутанность сознания.
- Уровень 50-70% – обмороки, психические расстройства, судороги, коматозное состояние.
- Уровень более 70% – летальный исход.
Заболеванию метгемоглобинемии подвержены и взрослые, и дети, в том числе новорожденные.

Характерный признак для всех форм метгемоглобинемии – шоколадно-коричневый оттенок крови, при заборе анализов она не меняет свой цвет.
Для диагностики заболевания у взрослого пациента врач оценивает симптомы, назначает лабораторные исследования. При постановке диагноза очень важно выявить причину гипоксии. Если это состояние вызвано отравлением, необходимо исключить возможность попадания в кровь угарного газа. При попадании этого вещества в кровь образуется прочное соединение – карбоксигемоглобин. Как и метгемоглобин, он не способен транспортировать кислород к клеткам и тканям. Отличительным признаком отравления карбоксигемоглобином становится ярко-красный цвет крови.
Чрезмерное количество метгемоглобина в крови может наблюдаться и у женщин, и у мужчин. Однако мужчины подвержены этому заболеванию на 66.59% меньше, чем женщина. Случаи летального исхода при заболевании мужчин метгемоглобинемией не зафиксированы.
Для диагностирования метгемоглобинемии у новорожденных детей врачом проводятся специальные анализы и исследования, позволяющие измерить уровень содержания метгемоглобина в крови.
В частности, к таким исследованиям относится:
- Цвет крови. При заболевания она приобретает насыщенный коричневый цвет.
- Биохимия крови. Повышенный билирубин при биохимическом анализе может свидетельствовать о метгемоглобинемии.
- Анализ на концентрацию метгемоглобина в крови ребенка.
- Общий анализ крови. Если ребенок болен, уровень СОЭ понижается, а гемоглобин и эритроциты повышаются.
У детей с наследственным заболеванием нередко наблюдаются следующие внешние признаки болезни:
- Ярко выраженный цианоз на коже и слизистых оболочках.
- Деформация формы черепа.
- Отставание в психомоторном развитии.
Метгемоглобинемии подвержены дети и мужского, и женского пола. Однако новорожденные девочки рискуют приобрести заболевание наследственным или врождённым путем гораздо чаще, чем мальчики.
Токсические вещества, синтезирующие метгемоглобин
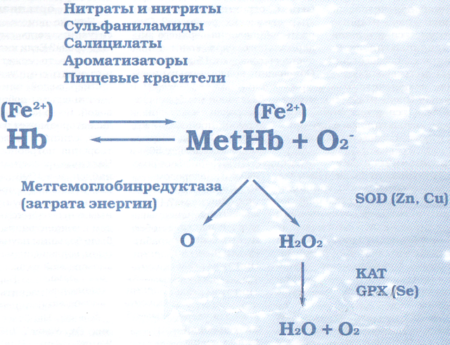
Главная причина концентрации в крови метгемоглобина – попадание в организм патогенных химических веществ в результате передозировки лекарственных препаратов на основе анилина и его производных. Вещество, которое способно преобразовать гемоглобин в метгемоглобин, называется метгемоглобинообразователем.
Основные метгемоглобинообразователи:
- местные анестетики,
- нитраты и нитриты,
- оксид азота,
- примахин,
- нафталин,
- производные гидразина,
- сульфаниламиды.
Стоит с особой осторожностью относиться к лекарственным препаратам, произведенным на основе метгемоглобинообразователей. Перед употреблением лекарственного препарата необходимо ознакомиться с инструкцией применения и дозировкой.

Способы предотвращения окисления железа гемоглобина
Для поддержания здоровья стоит знать, как предотвратить образование излишнего метгемоглобина в крови. Для этой цели есть два способа.
- Предотвратить патогенное воздействие, проникших в эритроциты крови окислителей железа до того, как они повредят молекулы гемоглобина. Для этого в кровь вводится энзим глутатионпероксидаза. При этом восстановленный глутатион воздействует на патогенные окислители в крови, обезвреживает их и предотвращает синтез метгемоглобина. Данный способ поможет предотвратить дальнейшее развитие метгемоглобинемии, однако может привести к образованию в крови веществ, полученных в результате денатурации гемоглобина – телец Гейнтца.
- Восстановить повреждённые окисленным железом молекулы гемоглобина. Данный способ применяется при помощи двух ферментативных систем: НАНД-зависимой и НАНДФ-зависимой метгемоглобинредуктазы. В первой системе восстанавливающими повреждённый гемоглобин веществами выступают продукты анаэробного этапа переработки глюкозы (НАНД), во второй – гексозомонофосфатного преобразования (НАНДФ). В результате гексозомонофосфатного превращения при воздействии гексозо-6-фосфатдегидрогеназы (Г-6ф-ДГ) синтезируется восстанавливающий агент – никатинамид – адениндинуклеотд фосфат (НАНДФН). Он принимает участие в трансформации метгемоглобина в гемоглобин в присутствии НАДФН-метгемоглобинредуктазы, а также в результате восстановления окисленного трехвалентного железа при участии НАНДФ-зависимой глутатионредуктазы.
Метгемоглобин – опасное для здоровья вещество. Синтезирование гемоглобина в метгемоглобин приводит к серьезным нарушениям состава и качества крови. Во избежание концентрации его в организме необходимо систематически проводить профилактические процедуры и следить за дозировкой применяемых лекарств.
О влиянии нитратов на организм человека рассказывается в представленном видеосюжете:
Загрузка…
