Фуникулярный миелоз фолиеводефицитная анемия
Фуникулярный миелоз — поражение спинного мозга, развивающееся вследствие недостаточности витамина В12. Как правило, сочетается с пернициозной анемией. Проявляется расстройством глубокой чувствительности, двигательными нарушениями в виде вялых нижних параличей с пирамидными знаками, отклонениями в психической сфере. Диагностируется фуникулярный миелоз путем определения уровня В12 в крови, проведения неврологического, гематологического и гастроэнтерологического обследований. Лечение состоит в восполнении дефицита витамина В12, соблюдении богатой витамином В12 диеты, введении других витаминов группы В. Прогноз благоприятный.
Общие сведения
Фуникулярный миелоз развивается вследствие дегенеративных процессов, происходящих в задних и боковых спинномозговых канатиках на фоне авитаминоза В12 (недостаточности цианокобаламина). Поскольку дефицит В12 также приводит к возникновению злокачественной пернициозной анемии, то она практически всегда сопровождает фуникулярный миелоз. Первое описание этой сочетанной патологии дал Лихтгейм в 1887 г.
Фуникулярный миелоз может развиться в любом возрасте, однако чаще (около 90% случаев) встречается после 40-летнего возраста. Причиной болезни может выступать как экзогенный авитаминоз В12, т. е. недостаточное поступление цианокобаламина с пищей, так и эндогенный авитаминоз В12, обусловленный нарушениями всасывания при различной патологии ЖКТ. Кроме того, более чем в 50% случаев фуникулярный миелоз сопровождается образованием антител к внутреннему фактору Касла и формированием атрофического гастрита, что свидетельствует об имеющихся иммунных нарушениях. В связи с выше сказанным, фуникулярный миелоз находится в кругу интересов нескольких клинических дисциплин: неврологии, гастроэнтерологии, иммунологии.

Фуникулярный миелоз
Причины фуникулярного миелоза
Экзогенный авитаминоз В12 возникает при анорексии, полном исключении из рациона богатых цианокобаламином мясных, рыбных и молочных продуктов, длительном голодании или неполноценном питании, приводящем к алиментарной дистрофии. Эндогенный авитаминоз В12 связан с нарушением всасывания цианокобаламина. Для успешного всасывания необходима трансформация витамина В12 в его усвояемую форму, которая осуществляется благодаря синтезируемому желудком гастромукопротеиду — внутреннему фактору Касла. Синтез последнего существенно уменьшается при ахилии, опухолях желудка, резекции желудка или гастрэктомии, что приводит к нарушению всасывания цианокобаламина. Это наиболее частая причина, вызывающая фуникулярный миелоз.
Различные заболевания кишечника, сопровождающиеся синдромом мальабсорбции, также могут быть причиной недостаточного всасывания В12. К ним относятся: болезнь Крона, туберкулезный энтерит, спру, целиакия, болезнь Уиппла, пеллагра, пострезекционный синдром короткой кишки и др. Уменьшенное поступление цианокобаламина в организм бывает обусловлено его чрезмерным поглощением кишечной флорой, избыток которой наблюдается при образовании застойной «слепой» петли кишечника после формирования энтероанастомоза, при дивертикулезе кишечника и дифиллоботриозе.
Патогенез детерминирующих фуникулярный миелоз патологических изменений в спинном мозге до конца не установлен. Основным считают дисфункцию метионинсинтазы и метилмалонил-КоА-мутазы — ферментов, участвующих в процессах образования миелина и формирования миелиновой оболочки нервных волокон. Морфологически фуникулярный миелоз сопровождается демиелинизацией волокон, проходящих в задних и боковых спинномозговых столбах. Причем процесс демиелинизации наиболее выражен в задних столбах, где проходят пути глубокой чувствительности (пути Голля и Бурдаха). В боковых столбах очаги демиелинизации затрагивают проводящие пути двигательной активности (пирамидный, спиномозжечковый, спиноталамический и др.). В некоторых случаях отмечается демиелинизация волокон зрительного нерва.
Симптомы фуникулярного миелоза
Клиническая картина складывается из сенсорно-двигательных расстройств и психических нарушений. Заболевание дебютирует с появления парестезий и общей слабости Парестезии в виде покалываний, преходящего онемения, ползанья мурашек, жара возникают в пальцах конечностей, потом охватывают плечи, грудь и живот. Поражается мышечно-суставная чувствительность, затем — вибрационная. В результате развивается сенситивная атаксия, сопровождающаяся дискоординацией движений, неустойчивостью, шаткой походкой. Затем возникает слабость в конечностях, преимущественно в ногах (нижний парапарез). Изначально парез носит спастический характер с повышением сухожильных рефлексов, мышечной гипертонией, клонусом стоп. Затем тонус мышц снижается, рефлексы угасают. Парез приобретает черты периферического. Однако сохраняются патологические стопные рефлексы, свидетельствующие о поражении пирамидного пути. С течением времени пациент утрачивает способность ходить. Присоединяются тазовые расстройства (энкопрез, недержание мочи, импотенция).
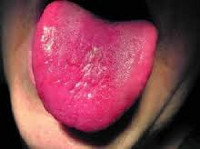
Психические расстройства имеют вариативный характер. Возможна депрессия, апатия, раздражительность, гиперсомния, иногда — острый психоз. В ряде случаев развивается нейропатия зрительного нерва, манифестирующая прогредиентным снижением остроты зрения с выпадением центрального участка зрительного поля (центральная скотома). Наряду с неврологическими и офтальмологическими проявлениями, фуникулярный миелоз сопровождается симптомами пернициозной анемии: бледностью, малиновым цветом языка, глосситом и/или стоматитом, тахикардией, одышкой и пр.
Диагностика фуникулярного миелоза
Сочетание неврологических симптомов с проявлениями анемии сразу вызывает подозрение о существовании недостаточности цианокобаламина. С целью подтверждения этого предположения проводят анализ содержания В12 в крови. Дальнейшая диагностика проводится неврологом совместно с гастроэнтерологом и гематологом. Для подтверждения диагноза и установления причины авитаминоза необходимы: клинический анализ крови, исследование секреторной функции желудка (гастроскопия, желудочное зондирование, анализ желудочного сока), анализ на антитела к внутреннему фактору Касла, обследование кишечника (обзорная рентгенография, рентгенография пассажа бария).
Визуализация спинальных морфологических изменений (очагов демиелинизации) возможна при помощи МРТ позвоночника. Она позволяет также отдифференцировать фуникулярный миелоз от компрессионной миелопатии при опухолях позвоночника, вертеброгенной миелопатии, спинальных опухолей и кист. Люмбальная пункция и исследование цереброспинальной жидкости проводятся для исключения инфекционного миелита и гематомиелии. При необходимости исключения нейросифилиса назначается RPR-тест. С целью диагностики гематологических нарушений производится стернальная пункция с последующим исследованием миелограммы. При зрительных расстройствах показана консультация офтальмолога с проведением визометрии, периметрии и офтальмоскопии.
Лечение фуникулярного миелоза
Терапия заключается в основном в коррекции недостаточности цианокобаламина. В начале лечения препараты цианокобаламина вводят внутримышечно ежедневно. Спустя 5-10 дней препарат вводят раз в неделю, через 4 недели — раз в месяц. При наличии показаний возможно пожизненное назначение ежемесячных инъекций витамина В12. Рекомендуется диета с употреблением нутриентов, богатых витаминами группы В (разные сорта рыб, говядина, творог, сыр, куриные яйца, крабы). Параллельно с лечением витамином В12 проводится курсовое введение других препаратов этой группы: тиамина (В1) и пиридоксина (В6).
Наличие дефицита фолиевой кислоты является показанием для ее назначения. Однако лечение фолиевой кислотой лучше начинать после восполнения дефицита цианокобаламина, поскольку в противном случае она может усугубить тяжесть неврологических симптомов. По показаниям проводится коррекция секреторной функции желудка и нарушений всасывания в кишечнике, профилактика урогенитальной инфекции. Для скорейшего и наиболее полного восстановления сенсомоторных функций проводится массаж, физиотерапия и ЛФК.
Как правило, фуникулярный миелоз имеет подострое или медленное течение. До установления причины его возникновения заболевание в течение 2-х лет приводило к летальному исходу. При своевременной терапии витамином В12 прогноз благоприятный. При начале лечения спустя несколько месяцев от дебюта заболевания можно добиться стабилизации состояния, однако нельзя рассчитывать на полный регресс неврологической симптоматики.
Содержание
- Фолиеводефицитная анемия
- Причины фолиеводефицитной анемии
- Симптомы фолиеводефицитной анемии
- Диагностика фолиеводефицитной анемии
- Лечение и профилактика фолиеводефицитной анемии
Фолиеводефицитная анемия — мегалобластическая анемия, обусловленная нарушением костномозгового кроветворения вследствие дефицита фолиевой кислоты (витамина B9). При фолиеводефицитной анемии развиваются все признаки анемического синдрома (бледность, слабость, тахикардия, снижение АД), незначительная желтуха, увеличение селезенки, анорексия, неустойчивый стул. С целью подтверждения диагноза проводится исследование гемограммы, костного мозга, определение уровня фолиевой кислоты в эритроцитах и сыворотке крови. Лечение B9-дефицитной анемии требует проведения заместительной терапии фолиевой кислотой.
Фолиеводефицитная анемия
Фолиеводефицитная анемия — комплекс клинико-гематологических проявлений, вызванных недостаточностью фолиевой кислоты вследствие ее ограниченного поступления, снижения абсорбции или повышенного расходования. Фолиеводефицитная анемия встречается реже, чем В12-дефицитная, однако часто сочетается с последней, а также нередко сопутствует железодефицитной анемии. Особую опасность фолиеводефицитная анемия представляет для беременных, поскольку может приводить к формированию пороков развития нервной системы плода, повышать риск отслойки плаценты, преждевременных родов и рождения недоношенного ребенка. Это обусловливает актуальность проблемы не только в рамках гематологии, но также педиатрии, акушерства и гинекологии.
Причины фолиеводефицитной анемии
Фолиевая кислота (витамин Вс, В9) поступает в организм в составе соединений — фолатов, присутствующих в овощах (бобовых, брокколи, шпинате, салате, спарже), печени, мясе, шоколаде, дрожжах и др. Запасы фолатов в организме составляют 5-10 мг, а минимальная ежесуточная потребность в них — 50 мкг (в период беременности в 2-3 раза выше). После прекращения поступления фолиевой кислоты извне, истощение ее эндогенных запасов наступает через 3-5 месяцев. Клинические проявления фолиеводефицитной анемии развиваются при снижении уровня витамина В9 в сыворотке крови менее 4 нг/мл.
Этиология фолиеводефицитной анемии может быть связана с недостаточным экзогенным поступлением витамина В9, нарушением его всасывания в кишечнике или повышенным выведением из организма. Чаще всего дефицит фолиевой кислоты носит алиментарный характер; он может быть обусловлен несбалансированным или недостаточным питанием, длительной термической обработкой пищи, вскармливанием детей козьим молоком и т. п.
Повышенную потребность в фолиевой кислоте испытывают беременные и кормящие женщины, недоношенные дети, подростки, онкобольные, пациенты с гемолитической анемией, гемобластозами, эксфолиативным дерматитом, псориазом. Эти категории лиц находятся в группе риска по развитию фолиеводефицитной анемии.
Нарушение абсорбции фолиевой кислоты в ЖКТ наблюдается при хроническом алкоголизме, состоянии после обширной резекции тонкого кишечника, целиакии, лимфоме кишечника, болезни Крона, спру, недостатке витамина В12, приеме антагонистов фолатов (противосудорожных препаратов, барбитуратов, оральных контрацептивов и др.). Чрезмерному выведению фолиевой кислоты из организма могут способствовать цирроз печени, гемодиализ, сердечная недостаточность.
Всасывание фолиевой кислоты происходит в двенадцатиперстной и начальном отделе тощей кишки. После поступления в кровоток она связывается с белками плазмы и транспортируется в печень, где значительная часть фолиевой кислоты откладывается в депо, остальная часть выводится с мочой.
В организме фолиевая кислота присутствует в виде коферментной формы — тетрагидрофолиевой кислоты, активно участвующей в синтезе глутаминовой кислоты, пиримидиновых и пуриновых оснований, а также тимидинмонофосфата – компонента ДНК. При фолиеводефицитной анемии, в первую очередь, нарушается синтез нуклеиновых кислот активно делящихся кроветворных клеток, в результате чего нормобластическое кроветворение сменяется на мегалобластическое. Следствием неэффективного гемопоэза служит развитие анемии, сочетающейся с лейкопенией и тромбоцитопенией.
Симптомы фолиеводефицитной анемии
Фолиеводефицитная анемия чаще развивается у молодых пациентов и беременных женщин. Среди клинических проявлений преобладают признаки анемического синдрома: бледность кожи с оттенком субиктеричности, слабость, тахикардия, артериальная гипотония, головокружения.
В отличие от пернициозной анемии, при дефиците фолиевой кислоты не развиваются неврологические нарушения (фуникулярный миелоз), а расстройства функции желудочно-кишечного тракта выражены незначительно. В числе последних иногда отмечается анорексия, неустойчивость стула, атрофический гастрит, глоссит, незначительная спленомегалия. При углубленном обследовании может выявляться миокардиодистрофия.
У пациентов с эпилепсией, шизофренией, психическими нарушениями фолиеводефицитная анемия усугубляет течение основного заболевания. Дефицит фолиевой кислоты в период беременности является фактором риска формирования дефектов нервной трубки (анэнцефалии, гидроцефалии, менингоцеле), врожденных пороков сердца, расщепления губы и нёба («заячьей губы» и «волчьей пасти»), гипотрофии плода. Кроме этого, у беременной повышается вероятность выкидыша, кровотечения, преждевременного родоразрешения.
После родов женщины с фолиеводефицитной анемией в большей степени подвержены развитию послеродовой депрессии, а дети раннего возраста — задержке психомоторного развития, нарушению работы кишечника, снижению иммунитета.
Диагностика фолиеводефицитной анемии
В общем анализе крови при фолиеводефицитной анемии отмечается гиперхромия, макроцитоз, лейкопения, тромбоцитопения, снижение количества ретикулоцитов. Подтверждению диагноза способствует определение снижения фолиевой кислоты в сыворотке крови (норма 6-20 нг/мл) и эритроцитах (норма – 100-450 нг/л). При исследовании миелограммы выявляется гиперплазия красного ростка, мегалобластный тип кроветворения.
При фолиеводефицитной анемии проба с гистидином, принятым внутрь, оказывается положительной: экскреция формиминглутаминовой кислоты с мочой значительно увеличивается (>18 мг). При миокардиодистрофии, по данным ЭКГ, имеет место нарушение реполяризации миокарда левого желудочка. С помощью УЗИ органов брюшной полости определяется увеличение селезенки. Фолиеводефицитную анемию приходится дифференцировать с В12-дефицитной анемией, острым эритромиелозом, миелодиспластическим синдромом, пароксизмальной ночной гемоглобинурией, гипопластической и аутоиммунной гемолитической анемией.
Лечение и профилактика фолиеводефицитной анемии
Лечение фолиеводефицитной анемии требует нормализации питания, устранения провоцирующих факторов, проведения заместительной терапии. Пациентам назначается прием фолиевой кислоты внутрь в дозе 1-5 мг в сутки в течение 4-6 недель под контролем лабораторных показателей крови. При терапии антагонистами витамина В9 назначается его парентеральное введение. Пациенты с нарушением всасывание фолиевой кислоты, должны находиться под наблюдением гематолога и пожизненно получать заместительную терапию.
В профилактическом приеме фолиевой кислоты нуждаются беременные, больные с талассемией, гемолитической анемией. В целях предупреждения патологии плода и акушерских осложнений прием фолиевой кислоты по 0,4 мг/сутки необходимо начинать еще в рамках прегравидарной подготовки (за несколько месяцев до зачатия) и продолжать на протяжении всей беременности и грудного вскармливания. Известно, что профилактический прием фолиевой кислоты, начатый еще до наступления беременности, позволяет снизить частоту рождения детей с врожденными пороками ЦНС в 3,5 раза.
ФУНИКУЛЯРНЫЙ МИЕЛОЗ (лат. funiculus канатик + греч. myelos костный мозг; син. подострый комбинированный склероз спинного мозга) — заболевание спинного мозга, обычно сочетающееся с пернициозной анемией и проявляющееся парестезиями, сенситивной атаксией и центральным парезом ног.
Впервые Ф. м. описан в 1887 г. Лихтгеймом (L. Lichtheim).
Этиология и патогенез
Причиной развития Ф. м. является дефицит в организме витамина B12 (см. Цианокобаламин), реже дефицит витамина B12 и фолиевой кислоты (см.) или только фолиевой к-ты. Патогенез полностью не выяснен. Ф. м. почти постоянно сочетается с пернициозной анемией (см.), однако роль ее как непосредственной причины поражения нервной системы опровергается наличием типичных случаев Ф. м., не сопровождающихся пернициозной анемией и изменениями красного костного мозга. Отсутствует также корреляция между степенью тяжести анемии и частотой развития Ф. м. Вместе с тем дефицит витамина B12 является решающим звеном как в патогенезе пернициозной анемии, так и в патогенезе Ф. м. Витамин B12 утилизируется организмом с помощью внутреннего фактора (гастромукопротеида), вырабатываемого желудком (см. Касла факторы). Отсутствие внутреннего фактора ведет к нарушению всасывания витамина B12 в кишечнике, в результате чего не происходит превращения фолиевой к-ты в ее активную форму — фолиновую кислоту. При этом изменяется процесс крове творения (см.), нарушается синтез ДНК в эритробластах. Ф. м. развивается в случаях недостатка витамина B12 в пище (напр., у вегетарианцев, исключающих из пищи молочные продукты); при нарушении секреции внутреннего фактора — при ахилии желудка (см.), после гастрэктомии (см.), при синдроме мальабсорбции (см. Мальабсорбции синдром), обусловленном спру (см.), терминальным илеитом (см. Крона болезнь), целиакией (см.), туберкулезным энтеритом (см.), пеллагрой (см.); в случаях так наз. конкурентного расхода витамина B12, когда последний поглощается избыточной кишечной флорой — при дивертикулезе кишечника (см.), синдроме «слепой петли» при энтероэнтероанастомозах (см.) — или гельминтами (см. Дифиллоботриозы). Определенную роль в патогенезе играют иммунные нарушения: более чем у половины больных пернициозной анемией диагностируют аутоиммунный атрофический гастрит, а в плазме крови обнаруживают антитела к внутреннему фактору (см. Аутоантитела).
В экспериментах на обезьянах было показано, что исключение из пищи витамина B12 через 3—4 года вызывает изменения в нервной системе, идентичные Ф. м., хотя анемия при этом не развивается.
Патологическая анатомия
Макроскопические изменения заключаются в умеренной атрофии спинного мозга (см.). Микроскопическое исследование обнаруживает очаги некроза и дегенерации в нежном и клиновидном пучках задних канатиков, в пирамидных и частично спинно-мозжечковых проводниках боковых канатиков. На срезах, окрашенных на миелин, выявляется демиелинизация афферентных и эфферентных проводников, наиболее выраженная в задних и боковых канатиках спинного мозга (заднебоковой склероз). Изменения вначале возникают в нижнешейных и верхнегрудных отделах, затем распространяются по спинному мозгу вверх и вниз (восходящая и нисходящая дегенерация). Наряду с распадом миелина наблюдается гибель осевых цилиндров с образованием пустот (вакуолей), разделенных тонкими глиальными тяжами. Прогрессирующее разрушение белого вещества спинного мозга не возмещается разрастанием глии, т. к. глиальная реакция при Ф. м. незначительна. В поздних стадиях болезни на поперечных срезах спинного мозга видна лишь узкая полоса непораженного белого вещества вокруг неизмененного серого вещества. Сходные морфол. изменения, но значительно менее выраженные, обнаруживают иногда в белом веществе полушарий головного мозга (см.). Поражаются и толстые миелинизированные чувствительные волокна в дистальных отделах периферических нервов. В большинстве случаев выявляются изменения, характерные для пернициозной анемии: глоссит, атрофия слизистой оболочки желудка, гиперплазия красного костного мозга, увеличение селезенкиг включения железа в клетках системы мононуклеарных фагоцитов.
Клиническая картина
Ф. м. встречается одинаково часто у мужчин т женщин. Примерно в 90% наблюдений первые признаки заболевания появляются в возрасте старше 40 лет., однако могут наблюдаться в детском: и старческом возрасте. Появляются парестезии (см.) в виде чувства онемения, жара, покалывания, ползанья мурашек, возникающие обычно в пальцах ног, реже в пальцах, рук, к-рые постепенно распространяются вверх на проксимальные отделы конечностей, а затем на живот и грудь. Иногда отмечаются ломящие боли в ногах. Постепенно присоединяются прогрессирующие нарушения мышечно-суставного чувства (см. Проприоцепторы) и вибрационной чувствительности (см.), также более выраженные в ногах, развивается сенситивная атаксия (см.). Иногда наступает снижение поверхностной чувствительности в конечностях с распространением на туловище, обычно без четкой верхней границы. Нередко отмечается болезненность при сдавлении икроножных мышц. Наряду с нарушениями чувствительности появляются и двигательные расстройства, к-рые проявляются слабостью ног и реже рук. При умеренно выраженном поражении спинного мозга парезы носят спастический характер, при более грубом повреждении задних канатиков возникает мышечная гипотония и парезы становятся вялыми (см. Параличи, парезы). Постепенно нарастающая тяжесть поражения задних и боковых канатиков спинного мозга определяет характер изменения сухожильных рефлексов (см.): в начальных стадиях Ф. м. сухожильные рефлексы бывают повышены, но более чем у половины больных отмечается снижение, а затем и выпадение ахилловых рефлексов; позднее исчезают и коленные рефлексы. В развитой стадии болезни постоянна обнаруживаются стопные патол. рефлексы (см. Рефлексы патологические) — симптом Бабинского (см. Бабинского рефлекс) и др. Сочетание пирамидных симптомов с вялыми парезами является особенностью клин, картины Ф. м. Отмечаются также нарушения функции тазовых органов (импотенция, императивные позывы к мочеиспусканию, задержка или недержание мочи и кала). Типичные формы Ф. м. характеризуются сочетанием сенситивной атаксии и параплегии (см.), выраженной преимущественно в йогах (атактическая параплегия). Однако неврол. нарушения могут быть и диссоциированными: возможны изолированные сенситивная атаксия или спастический пара- или тетра-парез. Нередко Ф. м. сочетается с полнневропатией (см. Невропатия), когда в процесс наряду со спинным мозгом вовлекаются и периферические нервы. Примерно в 5% случаев Ф. м. наблюдается снижение зрения из-за развития атрофии зрительных нервов (см. Зрительный нерв) и появления центральных скотом (см. Скотома), изредка бывает миоз (см.) при сохраненных зрачковых реакциях. В ряде случаев развивается сонливость. апатия, возникают нарушения психики, проявляющиеся депрессией, эмоциональной лабильностью, иногда острыми психотическими реакциями. В цереброспинальной жидкости (см.) иногда отмечается небольшое увеличение содержания белка. На электроэнцефалограмме (см. Электроэнцефалография) может выявляться диффузная медленная активность, исчезающая на фоне приема витамина B12.
Течение Ф. м. различное. Наряду с обычным постепенным развитием заболевания в отдельных случаях отмечается острое развитие неврол. нарушений, при к-ром в течение 2—3 нед. возникает картина поперечного поражения спинного мозга с нижней параплегией, выпадением всех видов чувствительности, тазовыми расстройствами.
В настоящее время Ф. м. характеризуется полиморфной клин, картиной с атипичным течением почти в 50% наблюдений. В связи с применением витамина B12 классические развернутые формы Ф. м. развиваются редко.
Диагноз
Диагноз при типичной клин, картине Ф. м., развившегося на фоне пернициозной анемии, не представляет трудностей. Дифференцировать следует с B12-дефицитной полиневропатией, к-рая отмечается примерно у 40% больных пернициозной анемией и также характеризуется дистальными парестезиями, сенситивной атаксией и арефлексией. Дифференциально-диагностическим признаком, свидетельствующим в пользу Ф. м., является поражение пирамидной системы, и прежде всего наличие патол. рефлекса Бабинского или других стопных патол. рефлексов.
Основные трудности дифференциальной диагностики возникают в тех случаях, когда неврол. симптомы Ф. м. развиваются раньше появления признаков пернициозной анемии. Диагноз Ф. м. подтверждается при обнаружении ахилического гастрита и мега лоб ластов в материале, полученном при стернальной пункции.
Ф. м., протекающий с доминированием клин, симптомов поражения задних канатиков, напоминает спинную сухотку (см.), однако при Ф. м.
отсутствует синдром Аргайлла Робертсона (см. Аргайлла Робертсона синдром) и отрицательны серологические тесты на сифилис (см.) в крови и цереброспинальной жидкости. Клин, форма Ф. м. с преимущественным поражением боковых канатиков может напоминать рассеянный склероз (см.). Для рассеянного склероза в отличие от Ф. м. характерна многоочаговость поражения (включая и симптомы поражения головного мозга), повышение в большинстве случаев ахилловых рефлексов, а также, как правило, ремиттирующее течение. Сочетанное поражение задних и боковых канатиков наблюдается при компрессии спинного мозга опухолью или при вертеброгенной шейной миелопатии (см.). Диагностика компрессии спинного мозга основывается на обнаружении с помощью ликвородинамических проб (см.) блокады подпаутинного пространства и выявлении характерной картины при миелографии, спинальной радиоизотопной сцинтиграфии, компьютерной томографии. Во многих случаях компрессии спинного мозга разного происхождения в отличие от Ф. м. определяется четкая верхняя граница расстройств чувствительности. Предположение о Ф. м. нередко возникает при обследовании больных, страдающих так наз. параплегией среднего или пожилого возраста, при к-рой развивается прогрессирующий на протяжении многих лет спастический пара- или тетрапарез при нормальном составе цереброспинальной жидкости и отрицательных данных миелографического исследования. Диагноз Ф. м. в этих случаях ставят на основании выявления дефицита витамина B12. Важным критерием в диагностике Ф. м. служит симметричность возникающих неврол. дефектов. Выраженная асимметрия парезов или расстройств чувствительности, сколько-нибудь длительно существующая, свидетельствует против Ф. м.
Лечение
Лечение направлено на ликвидацию дефицита в организме витамина B12.
Лечение начинают с внутримышечного введения 500—1000 мкг витамина B12 (цианокобаламина) ежедневно или через 1 — 2 дня. После 5 инъекций препарата в этой дозе витамин B12 вводят по 100 мкг 1 раз в неделю в течение полугода. Поддерживающая терапия в последующие годы заключается в инъекциях 100 мкг витамина B12 1 раз в месяц. В случае возникновения инфекционного заболевания или почечной недостаточности доза витамина B12 должна быть увеличена. При возможности необходимо устранение причин нарушения всасывания витамина B12 в жел.-киш. тракте. Показана диета с большим содержанием витаминов группы В, целесообразно парентеральное введение витаминов B1 и B6, а также фосфадена по 60 мг два раза в день на протяжении 4—8 нед. (повторными циклами). Назначение фолиевой к-ты в дозе 5 —15 мг в сутки допустимо только при редко обнаруживаемой фолиево-дефицитной форме Ф. м. В противном случае возможно обострение неврол. процесса. Назначают массаж, ЛФК. При значительном повышении тонуса мышц в пораженных конечностях показан прием седуксена, баклофена, мидокалма. При параплегии необходимы тщательный уход за кожей для предупреждения развития пролежней и профилактика урогенной инфекции.
Прогноз и Профилактика
Прогноз определяется гл. обр. длительностью существования неврол. симптомов до начала лечения; возраст больных и тяжесть анемии существенной прогностической роли не играют. При начале лечения через несколько недель после появления симптомов спинального поражения можно ожидать выздоровления больных; если к лечению приступили через несколько месяцев — значительного улучшения. В поздних стадиях Ф. м. возможно лишь незначительное улучшение или стабилизация процесса. Основной регресс симптомов отмечают в первые 3—6 мес. лечения, в дальнейшем восстановление нарушенных функций идет более медленно.
Профилактика предполагает своевременное выявление и адекватное лечение пернициозной анемии, а также тщательное наблюдение за неврол. статусом таких больных с целью возможно более раннего обнаружения у них симптомов поражения спинного мозга.
Библиогр.: Алимов И. Ю. и Манд-риченко В. М. Фуникулярный миелоз при Аддисоновой болезни, Здравоохр. Таджикистана, № 1, с. 90, 1983; Давгаденков С. Н. Клинические лекции по нервным болезням, в. 4, с. 172, JI., 1961; Мартынов Ю. С., Малкова Е. В. и Чекнева Н. С. Изменения нервной системы при заболеваниях внутренних органов, М., 1980; Многотомное руководство по неврологии, под ред. С. Н. Давиденкова, т. 3, кн. 2, с. 902, М., 1962, библиогр.; Руководство по гематологии, под ред. А. Воробьева и Ю. И. Лорие, с. 376, М., 1979; Evans D. L., Е del sohn G. А. a. Golden R. N. Organic psychosis without anemia or spinal cord symptoms in patients with vitamin B12 deficiency, Amer. J. Psychiat., v. 140, p. 218, 1983; Folic acid in neurology, psychiatry, and internal medicine, ed. by М. I. Botez a. E. H. Reynolds, p. 427, N. Y., 1979; Reynolds E. H. Pathogenesis of subacute combined degeneration, Lancet, v. 2, p. 1109, 1981; Shorvon S. D. a. o. The neuropsychiatry of megaloblastic anaemia, Brit. med. J., v. 281, p. 1036, 1980.
Д. P. Штульман.
