Гемоглобин поступает в плазму

Одним из самых сложных процессов, что происходят в организме человека, несомненно, является дыхание. И сложность эта не только в танце легких, благодаря которому человек получает кислород, но и в процессах, с помощью которых этот кислород проникает дальше, в ткани, где превращается в углекислый газ, что отправляется в обратное путешествие. О данных процессах и пойдет речь далее.
Итак, приступим. Человек делает вдох, иии… Далеко не весь кислород поступает в легкие, а затем и в кровь. Часть вдыхаемого воздуха остается в так называемом мертвом пространстве. Мертвое пространство, в свою очередь, делится на анатомическое (дыхательные пути), в котором остается около 30 % вдыхаемого воздуха, и функциональное (вентилируемые, но по каким-то причинам не перфузируемые альвеолы).
Ухудшение альвеолярного газообмена может происходить при неглубоком и частом дыхании (причиной может стать перелом ребер, паралич дыхательной мускулатуры различного генеза и др.), а также при увеличении мертвого пространства, вызванном разнообразными причинами (нарушение перфузии альвеол в результате воспалительных заболеваний легких, удаление доли или целого легкого и др.), при снижении скорости кровотока по альвеолярным капиллярам (ТЭЛА, инфаркт легкого), при наличии диффузионного барьера (отек легких) и в результате ослабления альвеолярной вентиляции при обтурации просвета бронха. Газообмен между легкими и кровью происходит путем диффузии в соответствии с законом Фика. В легочных капиллярах она происходит за счет разности парциальных давлений в альвеолах и эритроцитах.
В альвеолах парциальное давление кислорода значительно превышает таковое для углекислого газа и составляет примерно 13,3 кПа (100 мм рт. ст.) и 5,3 кПа (40 мм рт. ст.) соответственно. Альвеолы омываются приносимой легочными артериями венозной кровью, в которой соотношение парциальных давлений этих двух газов обратно пропорционально и составляет приблизительно 5,3 кПа (40 мм рт. ст.) для кислорода и 6,1 кПа (46 мм рт. ст.) для углекислого газа. В среднем разница парциальных давлений составляет около 8 кПа (60 мм рт. ст.) для кислорода и около 0,8 кПа для углекислого газа.
Как уже было сказано выше, кислород путем диффузии проникает в кровь легочных капилляров. Диффузионное расстояние для кислорода при этом составляет 1–2 мкм, то есть именно на такое расстояние он проникает внутрь капилляра. Обмен крови в легочном капилляре происходит примерно за 0,75 секунды, но этого времени хватает на то, чтобы парциальные давления в альвеолах и в крови пришли в равновесие.
Кровь, в которой показатели парциального давления для кислорода и углекислого газа примерно равны таковым в альвеолах, называется артериализированной. Однако за счет наличия в легких артериовенозных шунтов и притока венозной крови из бронхиальных вен такой она остается недолго. В результате парциальное давление кислорода в аорте составляет примерно 12,0 кПа (как уже было сказано выше, парциальное давление в артериализированной крови равно таковому в альвеолах и составляет 13,3 кПа), а давление углекислого газа меняется незначительно и не приводит к затруднению его диффузии из крови в альвеолы.
Но кислород непосредственно в ткани попадает лишь в крайне незначительных количествах: для свободного перемещения по организму ему необходим транспортер. Эту функцию выполняет содержащийся в эритроцитах белок — гемоглобин. Гемоглобин существует в оксигенированной и неоксигенированной формах. В дезокси-гемоглобине железо находится на уровне порфиринового кольца и стабилизируется электростатическими силами, что обеспечивает поддержание всей структуры. Появившись, кислород начинает «тянуть» за железо, которое переносится на проксимальный гистидин на другом конце полипептидной цепи и меняет структуру всего протеина.
В результате гемоглобин переходит в оксигенированную форму, альфа- и бета-цепи при этом поворачиваются относительно друг друга на 15 градусов, облегчая присоединение остальных молекул кислорода. В итоге каждый из четырех содержащихся в нем атомов двухвалентного железа обратимо связывается с молекулой кислорода, что превращает молекулу гемоглобина в оксигемоглобин. По сравнению с миоглобином гемоглобин имеет низкое сродство к кислороду, однако оно не статично. Так, миоглобин может связывать кислород только одним участком, поэтому кривая его связывания — гипербола. Кривая связывания гемоглобина с кислородом имеет S-образную форму, демонстрируя, что при его связывании с первой молекулой кислорода гемоглобин имеет очень низкое сродство к кислороду, но при связывании последующих молекул кислорода сродство остальных его субъединиц к нему значительно увеличивается и в конечном счете повышается примерно в 500 раз.
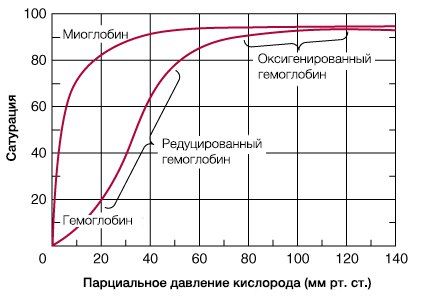
При этом альфа-цепи связывают кислород легче, чем бета-цепи. Этот процесс назван кооперативным взаимодействием. По мере снижения парциального давления кислорода в крови происходит его высвобождение из гемоглобина и поступление в ткани. Например, парциальное давление кислорода в работающих мышцах составляет всего 26 мм рт. ст, и при прохождении эритроцитов через капилляры, кровоснабжающие мышцы, происходит высвобождение и поступление в мышечные клетки примерно ⅓ всего переносимого гемоглобином кислорода. При повышении температуры тела также возрастает потребность в кислороде, что, в свою очередь, стимулирует высвобождение и поступление его в ткани. При снижении температуры, напротив, развивается гипоксия тканей, способствующая компенсаторному увеличению сродства гемоглобина к кислороду.
Гемоглобин также осуществляет перенос от тканей к легким продуктов тканевого дыхания — углекислого газа и ионов водорода. В ходе окислительных процессов в клетке выделяется углекислый газ, в результате гидратации которого образуются ионы водорода, что, в свою очередь, приводит к снижению рН. Давно известно, что снижение рН и повышение концентрации углекислого газа в крови оказывает сильное влияние на способность гемоглобина связывать кислород.
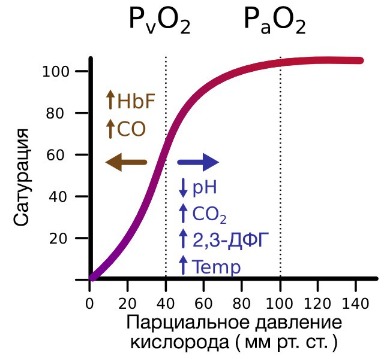
В периферических сосудах показатели рН низкие, и по мере связывания гемоглобина с ионами водорода и углекислым газом происходит снижение его сродства к кислороду. Это влияние величины рН и концентрации углекислого газа на способность гемоглобина связывать кислород называют эффектом Бора.
Обратная ситуация имеет место в альвеолярных капиллярах, где присоединение кислорода к гемоглобину превращает тот в более сильную кислоту.
При этом сродство гемоглобина к углекислому газу снижается, а повышение кислотности гемоглобина приводит к высвобождению излишка ионов водорода и образованию в крови из бикарбоната угольной кислоты, которая затем распадается на воду и углекислый газ. В обоих случаях углекислый газ из крови поступает в альвеолы, а затем в атмосферу. Данный процесс назван эффектом Холдейна. Стоит отметить, что важную роль в образовании углекислого газа в эритроцитах играет ион хлора, поступающий в плазму крови в обмен на бикарбонат при участии белка-переносчика АЕ1. Данный процесс в англоязычной литературе получил название «Chloride shift» или «перенос Хамбургера».
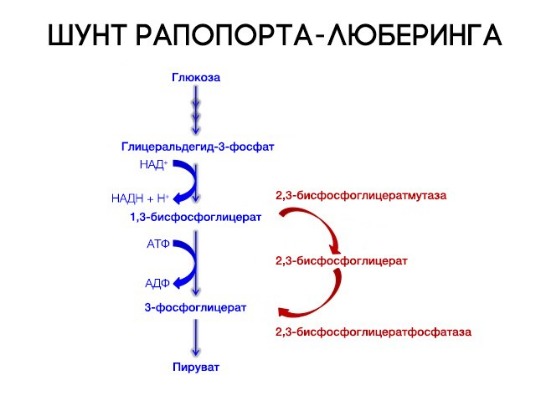
На сродство гемоглобина к кислороду оказывает влияние и присутствующее в эритроцитах вещество, получившее название 2,3-бисфосфоглицерат (БФГ). Его образование — своего рода побочная реакция анаэробного гликолиза, происходящего в эритроцитах в ходе ферментативного превращения глюкозы в пируват под действием фермента бифосфоглицератмутазы. БФГ способен самостоятельно связываться с неоксигенированной формой гемоглобина, образуя солевой мостик между двумя его бета-субъединицами и снижая сродство к кислороду.
При этом гемоглобин способен связать только одну молекулу БФГ, а при присоединении кислорода БФГ вытесняется из полости. В обычных условиях в эритроцитах крови содержится достаточно большое количество БФГ, которое может увеличиваться в условиях гипоксии (например, у дайверов при погружении на глубину), а также при восхождении на большую высоту. В первые часы подъема концентрация БФГ в эритроцитах будет возрастать, а сродство кислороду снижаться. Но на большой высоте парциальное давление будет значительно ниже такового на уровне моря, а значит, оно снизится и в тканях. При этом БФГ будет облегчать передачу кислорода от гемоглобина к тканям.
Некоторые вещества способны прочно связываться с гемоглобином или же вовсе менять его структуру. Одним из них является угарный газ, чье сродство к гемоглобину в 200 раз превышает таковое для кислорода. Отравления угарным газом часто происходят в помещениях с печным отоплением, при пожарах и авариях на производстве. Со временем кислород вытесняет угарный газ из гемоглобина, и в легких случаях пациенты помещаются под наблюдение и получают ингаляции с увлажненным кислородом. Необходимой мерой при тяжелых отравлениях угарным газом является переливание эритроцитарной массы.
К веществам, способным изменять структуру гемоглобина, относятся метгемоглобинобразователи — соединения, способные окислять двухвалентное железо в геме до трехвалентного. К ним относятся нитриты, нитраты, некоторые местные анестетики, аминофенолы, хлораты, примахин и некоторые сульфаниламиды. Состояние, характеризующееся появлением в крови окисленного гемоглобина, называют метгемоглобинемией. При высокой метгемоглобинемии капля крови, помещенная на фильтровальную бумагу, имеет характерный коричневый цвет, а при пропускании кислорода через пробирку с такой кровью ее цвет не меняется. Метгемоглобинемия выше 70 % от общего содержания гемоглобина часто приводит к гибели пациента еще до момента постановки диагноза.
Источники:
- Harrison’s hematology and oncology Longo, Dan L (Dan Louis), Third edition. New York : McGraw-Hill Education Medical, 2017.
- Наглядная физиология, С. Зильбернагль, А. Деспопулос, 2013.
- Ленинджер А. Основы биохимии: В 3-х т. Т. 1. /Д. Нельсон, М. Кокс ; Пер. с англ.-М.: БИНОМ: Лаборатория знаний, 2011.- 694 с.
Нашли опечатку? Выделите фрагмент и нажмите Ctrl+Enter.
Гемоглобин – сложный железосодержащий белок; основной дыхательный пигмент и главный компонент эритроцита. Молекула гемоглобина состоит из гема, содержащего атом двухвалентного железа и белка глобина. Основная функция гемоглобина – это перенос кислорода из легких в ткани и углекислого газа из тканей в легкие.
Но, при попадании гемоглобина в плазму крови нарушается его способность присоединять кислород, то есть образовывать оксигемоглобин, вследствие чего прекращается снабжение тканей кислородом, следовательно, возникает состояние кислородного голодания всего организма в целом. Происходит понижение кислородной емкости крови вследствие инактивации гемоглобина при гемической гипоксии. Наиболее чувствительными к кислородному голоданию являются ЦНС, сердечная мышца, ткани почек и печени. Попадание гемоглобина в плазму крови могло бы вызвать:
1) Повышение пульса до 5600 ударов в минуту
Растворенный в плазме крови гемоглобин не способен в полной мере взаимодействовать с кислородом, следовательно, ухудшается снабжение кислородом тканей (возникает тканевая гипоксия). Итак, для нормального функционирования всего организма следует доставлять кислород к тканям в необходимом для жизни объеме, что и достигается увеличением пульса. Но такое резкое повышение пульса почти в 80 раз (с 60-80 ударов до 5600), естественно, сказывается на работе сердца не в лучшую сторону и приводит к износу сердечной мышцы.
2) Увеличение объема перекачиваемой крови (до 365л)
Увеличение объема крови в организме стабилизировало бы поступление достаточного количества кислорода в ткани и органы, но привело бы к большой нагрузке на сердце и износу сердечной мышцы, так как увеличился объем перекачиваемой жидкости. Все это стало бы причиной рабочей или компенсаторной гипертрофии сердца (большая нагрузка привела к увеличению размеров сердца).
3) Повышение осмотического давления
Растворение гемоглобина в плазме крови создавало бы повышение осмотического давления (более 100мм рт. ст.), что исключало бы возможность фильтрации крови в почках. Это привело бы к попаданию вредных (токсичных) веществ в кровь, следовательно, привело бы к отравлению всего организма, в том числе и сердца. Гемоглобин представляет собой соединение железа с протопорфирином, который способен образовывать комплексы с различными металлами, такими как Cu, Zn, Mg. К тому же, в водных растворах под действием кислорода воздуха и других окислителей гемм окисляется, железо переходит в окисную форму, теряя один электрон. При этом образуется гемин – комплекс окисного железа с протопорфирином. Гемин является катионом, следовательно, может образовывать соединения, взаимодействуя с анионами. Например, хлоргемин, йодгемин, бромгемин и т.д. В щелочной среде гемин может присоединять ион гидроксила (OH). При этом получается гематин. Кроме образования оксигемоглобина и карбгемоглобина возможно образование других его производных, таких как метгемоглобин, карбоксигемоглобин, сульфгемоглобин, гемохром и метгемальбумин.
Увеличение концентрации солей и белков способствует изменению онкотического давления, что приводит к нарушению водного обмена (Это привело бы к тому, что вода начала бы оставаться и накапливаться во внутренней среде организма). Возможно скопление жидкости в полости перикарда (в количестве более 30мл). При этом наблюдается одышка, снижается систолическое давление и появляется застой крови в органах. Гидроперикард при большом количестве жидкости затрудняет работу сердца и приводит к увеличению его размеров.
4) Большое количество белков в плазме крови, вызванное растворением гемоглобина повышает вязкость крови, что вызывает нарушение процессов гемодинамики, следовательно, возникает затруднение циркуляции крови на уровне капилляров, как следствие недостаток кислорода тканям – тканевая гипоксия.
5) При растворении гемоглобина нарушается работа почек, так как нарушается процесс всасывания в капсуле Шумлянского – Боумена, что приводит к нарушению процесса фильтрации крови в почках, а следовательно, происходит забивание (закупорка) почечных канальцев, приводящее к некрозу почечных канальцев и ОПН (острой почечной недостаточности), которые приводят к нарушению сердечно – сосудистой деятельности и развитию анемии. Все это приводит к поражению организма токсичными веществами. В первую очередь страдает ЦНС и сердечная мышца.
6) Отравление организма продуктами распада гемоглобина, такими как билирубин, биливердин, железо, порфирины с развитием острой порфирии и желтухи. При желчнокаменной болезни в составе желчных камней наряду с их основным компонентом – холестерином обнаруживается непрямой билирубин, который вследствие плохой растворимости выпадает в осадок в желчном пузыре в виде билирубината кальция, который и участвует в формировании камней. Итак, токсичные продукты распада гемоглобина поражают ЦНС, а так же сердечную мышцу.
Железо входит в состав гемоглобина (включено в состав молекулы гема), ще выполняет важнейшую функцию связывания и доставки кислорода клеткам организма человека. Поэтому железо необходимо для синтеза и функционирования гемоглобина.
Общее содержание железа в организме «стандартного» человека составляет около 4,2 г. Примерно 75—80% его общего количества входит в состав гемоглобина. 20—25% является резервным, 5-Ю% входят в состав миоглобина, около 1% содержится вдыхательных ферментах, катализирующих процессы дыхания в клетках и тканях. Резервное железо запасается главным обра зом в печени, селезенке и костном мозге, где хранится в белках ферритине и гемосиде- рине Часть ферритина присутствует в плазме, а его концентрация служит надежным индикатором состояния запасов железа в организме. Общее содержание железа в организме человека, входящее в состав гемоглобина, составляет 3000 мг, в составе миоглобина содержится около 125 мг, печень содержит около 700 мг, представленного преимущественно ферритином.
() г 3 до 4 мг (0,1% общего количества железа) циркулирует в плазме крови и связи с транспортным белком трансферрином.
Железо осуществляет свою биологическую функцию главным образом в составе других биологически активных соединений (гемоглобин, миоглобин, железосодержащие ферменты), которые выполняют 4 основные функции:
• транспорт электронов (цитохромы, железосеропротеиды),
• транспорт и депонирование кислорода (гемоглобин, миоглобин);
• участие в формировании активных центров окислительно-восстановительных ферментов (оксидазы, гидроксилазы и др.);
• транспорт и депонирование железа (трансферрин, гемоеидерин, ферритин).
Гомеостаз железа в организме обеспечивается в первую очередь регуляцией его всасывания в желудочно-кишечном тракте в связи с ограниченной способностью организма к выделению этого элемента.
Существует выраженная обратная зависимость между обеспеченностью организма человека железом и его всасыванием в пищеварительном тракте.
Всасызание железа зависит от:
• возраста и обеспеченности организма железом;
• состояния желудочно-кишечного тракта;
• количества и химических форм поступающего железа с пищей;
• количества и форм прочих компонентов пищи.
Для оптимального всасывания железа необходима нормальная секреция желудочного сока. Прием соляной кислоты способствует усвоению железа. Аскорбиновая кислота, восстанавливающая железо и образующая с ним хелатные комплексы, повышает доступность этого элемента, так же как и прочие органические кислоты. Другим компонентом пищи, улучшающим всасывание железа7 является фак- I ор животного белка. Улучшают всасывание железа простые угле- иоды: лактоза, фруктоза, сорбит, а также такие аминокислоты, как гистидин, лизин, цистеин, образующие с железом легко всасываемые хелаты. Всасывание железа снижают такие напитки, как кофе и чай, иолифенольные соединения которых прочно связывают этот элемент. Поэтому чай применяется для профилактики повышенного усвоения железа у больных талассемией. Большое влияние на усвоение железа оказывают различные заболевания. Оно усиливается при недостаточности железа, при анемиях (гемолитической, апластической, мега- лобластной), гиповитаминозе В6 и гемохроматозе, что объясняется усилением эритропоэза, истощением запасов железа и гипоксией.
Современные представления о всасывании железа в кишечнике отводят центральную роль двум видам трансферрина — мукозному и плазменному. Мукозный трансферрин секретируется клетками слизистой оболочки кишечника — энтероцитами в просвет кишечника, где он загружается железом, после чего проникает в энтеро- цит. В этой клетке трансферрин освобождается от железа, после чего вступает в новый цикл. Источником мукозного трансферрина является не сам энтероцит, а печень, из которой этот белок поступает в кишечник с желчью. Из энтеронита мукозный трансферрин отдает железо своему плазменному аналогу. Наиболее интенсивное всасывание железа происходит в проксимальных (начальных) отделах тонкой кишки (в двенадцатиперстной рт тощей) и отсутствует в подвздошной кишке.
Плазменный трансферрин доставляет железо к тканям, имеюшим специфические рецепторы. Колртчество железа, поступающего в клетку, прямо пропорционально числу мембранных рецепторов. Наибольшее количество рецепторов содержат клетки костного мозга, клетки ретикулоэндотелиальной системы печени и селезенки. В клетках этих органов происходит высвобождение железа из трансферрина. Затем плазменный трансферрин возвращается в циркуляцию. Повышение потребности клеток в железе при их быстром росте или синтезе гемоглобина ведет к индукции (усилению) биосинтеза рецепторов трансферрина, и, напротив, при повышении запасов железа в клетке число рецепторов на ее поверхности снижается. У взрослого человека в костном мозге железо трансферрина с помощью специфических рецепторов включается в нормоци- ты и ретикулоциты, исполь^уюшие его для синтеза гемоглобина. В прочие ткани трансферрин доставляет в 4 раза меньшее количество железа, чем в костный мозг.
В организме человека хорошо сохраняется железо. После того, как эритроциты, прожив 120 сут, погибают, железо возвращается в резерв костного мозга для образования новых эритроцитов. За счет распада гемоглобина в сутки высвобождается около 21-24 мг железа, что во много раз превышает поступление железа из пищеварительного тракта (1 — 1,5 мг/сут). Более 95% железа поступает в плазму из клеток ретикулоэндотелиальной системы печени и селезенки, которые поглощают путем фагоцитоза более 1011 старых эритроцитов в сутки. Железо, поступившее в клетки ретикулоэндотелиальной системы, либо быстро возвращается в циркуляцию в виде ферритина, либо откладывается про запас. Гемоглобин, поступающий в плазму крови
при распаде эритроцитов, специфически связывается с гаптоглоби- мом, что предупреждает его фильтрацию через почки.
Железо выделяется из организма в основном путем слушивания слизистой оболочки кишечника и с желчью. Оно теряется также с полосами, ногтями, мочой и потом. Общее количество выделяемого |,|ким образом железа составляет у здорового мужчины 0,6-1 мг, а у женщин репродуктивного возраста — более 1,5 мг в сутки.
Нормальная сбалансированная диета обеспечивает поступление и желудочно-кишечный тракт окото 10-15 мг железа ежедневно. Основными источниками железа служат мясо, рыба, овощи и крупы. Железо из животной пищи усваивается в несколько раз лучше, чем из растительной. В норме из пищи всасывается около 10% содержащегося в ней железа (1-1,5 мг в день), что вполне достаточно для возмещения дневных потерь.
Таким образом, концентрация железа в сыворотке зависит от резорбции в желудочно-кишечном тракте, накопления в кишечнике, селезенке и костном мозге, синтеза и распада гемоглобина и его потери организмом.
Оптимальным для хорошего здоровья пациента является состояние, при котором запасы железа в ор1анизме достаточны, но не избы- тчны.
Еще по теме ОБМЕН ЖЕЛЕЗА:
- ЗЛОКАЧЕСТВЕННЫЕ НОВООБРАЗОВАНИЯ ЩИТОВИДНОЙ ЖЕЛЕЗЫ И ДРУГИХ ЭНДОКРИННЫХ ЖЕЛЕЗ (C73-C75)
- Глава 11. ВОДНО-ЭЛЕКТРОЛИТНЫЙ ОБМЕН
- Водный обмен человека
- РЕФЕРАТ. ОБМЕН ВЕЩЕСТВ2017, 2017
- ВЛИЯНИЕ СЕРОТОНИНА НА ОБМЕН ВЕЩЕСТВ
- Водный обмен человека
- Лекарственные сборы при нарушениях обменных процессов
- Влияние глюкокортикоидов на обменные процессы и его связь с побочными эффектами
- ПРИЛОЖЕНИЕ № 1. ОСНОВНОЙ ОБМЕН У ДЕТЕЙ В ЗАВИСИМОСТИ ОТ ИХ МАССЫ И ПОЛА
- НЕКОТОРЫЕ ФУНКЦИОНАЛЬНЫЕ И ОБМЕННЫЕ ИЗМЕНЕНИЯ КАК ПОКАЗАТЕЛИ ГЛЮКОКОРТИКОИДНОЙ НЕДОСТАТОЧНОСТИ ПРИ АЛЛЕРГИЧЕСКИХ ПРОЦЕССАХ
- “Шея. щитовидная железа и паращитовидные железы”
- ОПУХОЛИ ПОДЖЕЛУДОЧНОЙ ЖЕЛЕЗЫ , ДОБРОКАЧЕСТВЕННЫЕ ОПУХОЛИ ПОДЖЕЛУДОЧНОЙ ЖЕЛЕЗЫ
