Гемоглобин s серповидная анемия

Сиклемия (дрепаноцитоз, серповидноклеточная анемия, серповидная анемия, гемоглобиноз S) – история изучения, причиныСиклемия (синонимы: дрепаноцитоз, серповидноклеточная анемия, серповидная анемия, гемоглобиноз S) представляет собой качественное заболевание гемоглобина, при котором основное нарушение состоит в наличии гемоглобина S в эритроцитах. Болезнь характеризуется хронической гемолитической анемией и явлениями сосудистой закупорки, причину которых следует искать в дрепаноцитном преобразовании эритроцитов. Явление сиклизации впервые описал J.P. Herrick в 1919 г. Он обратил внимание на «причудливую серповидную форму» красных кровяных клеток в крови страдавшего анемией чернокожего пациента. Позже, в 1927 г., Halm и Gillespie отметили развитие сиклизации лишь в условиях понижения давления О2. В 1949 г. Neel и Beet доказали наследственный характер болезни, что тяжелая форма отражает гомозиготное состояние, в то время как легкая — гетерозиготное. В том же году Janet Watson высказал мнение о том, что причину заболевания следует искать в наличии иного вида гемоглобина, чем от нормального взрослого человека. Вскрытие первого аномального гемоглобина сделано Pauling и его сотрудниками, которые, в 1949 г. доказали, что картина электрофоретической миграции гемоглобина страдающих анемией, в крови которых имеются серповидные красные кровяные клетки, иная, чем нормального гемоглобина. Уточнение структурной аномалии гемоглобина S принадлежит Ingram в 1956 г. в связи с внедрением техники „fingerprint”. «Выявление первого аномального гемоглобина — гемоглобина S — составило не только новый этап в развитии знаний о гемоглобинопатиях, но и межевой камень медицинского исследования XX века в связи с обоснованием общей концепции о молекулярных болезнях. Клинический этап понимания болезни, предшествующий 1949 г., дополнился, в дальнейшем, познанием глубокого патофизиогенетического механизма по последним знаниям о структуре и аномалиях гемоглобина. В этой связи было доказано, что сиклемия — комплексное клиническое заболевание — результат молекулярной аномалии лишь одного белка, замены одной аминокислоты в молекуле гемоглобина, другой.
Причины сиклемии – серповидноклеточной анемииСиклемия это молекулярное заболевание, причиной которого является генетическая мутация в контролирующих синтез гемоглобина генах. Эпидемиология сиклемии – серповидноклеточной анемииНаибольшая частота заболевания наблюдается среди народов экваториальной зоны африканского материка, также на аравийском полуострове, на юге Индии, Цейлоне, Мадагаскаре и среди цветного населения южной и северной Америк. Что касается Европы очаги гемоглобина S описаны в Турции, Греции, южной Италии, в то время как у остальных народов Европы диагноз гемоглобина S редкое явление. У нас в стране о первых случаях гемоглобина S было сообщено в 1967 г.; в настоящее время на учете коллектива гематологилческого Центра значатся 11 семей с этой генетической аномалией. Следует отметить, что гемоглобин S создает некоторую устойчивость к вызываемой Plasmodium falciparum малярии. Эта отличительная черта составляет один из факторов, объясняющих высокий показатель частоты сиклемии в данной зоне. Так, у аномальных индивидов (АА) смертность от малярии высокая; у индивидов с сиклемией (SS) показатель смертности нысокий в связи с собственно тяжестью заболевания; гетерозиготные больные (AS) устойчивы к малярии и продолжительность жизни укладываетвя в норму. – Также рекомендуем “Клиника сиклемии – серповидноклеточной анемии” Оглавление темы “Гемоглобинопатии”:
|
Серповидно-клеточная анемия (син.: S-гемоглобинонатия, серповидно-клеточная болезнь, дрепаноцитоз, дрепаноцитарная анемия) — гемоглобинопатия, протекающая с гемолитической анемией, для которой характерно наличие в крови серповидных эритроцитов и периодическая закупорка ими микроциркуляторного русла в различных органах и тканях (особенно с замедленным кровотоком).
Термином «серповидно-клеточная анемия» обозначают гетерогенную группу гемоглобинопатий (см.), к к-рой относят собственно Серповидно-клеточную анемию, или гомозиготную SS-гемоглобинопатию, и сочетанные гетерозиготные формы по гемоглобину S и различным вариантам талассемии (микродрепаноцитоз), по гемоглобину S и гемоглобину F (так наз. гемоглобиноз SF), по гемоглобину S и гемоглобину С и D и другим аномальным по структуре гемоглобинам (см. Гемоглобин). В этой группе несколько особо стоит так наз. серповидно-клеточная аномалия эритроцитов, к-рая является гетерозиготным состоянием по гемоглобину S, характеризующаяся наличием в крови примерно равных пропорций гемоглобина А и S и отсутствием клин, проявлений в обычных условиях. У нек-рых таких гетерозиготных носителей беременность, роды, полет в негерметизированном самолете, являющиеся стрессовыми ситуациями, могут вызвать симптоматику, сходную с Серповидно-клеточной анемией.
Впервые Серповидно-клеточную анемию описал Херрик (J. В. Herrick) в 1910 г. Молекулярные основы патологии были открыты в 1949 г. Л. Полингом, Итано (H. A. Itano) и сотр. В 1956 г. Ингрем (V. Ingram) обнаружил, что аномалия гемоглобина S обусловлена замещением глутаминовой к-ты в бета-полипептидной цепи глобина валином.
Гемоглобин S представляет собой систему с балансированного полиморфизма (см. Популяция), существующего в популяциях так наз. малярийного пояса земного шара и обеспечивающего защиту гетерозиготных носителей гемоглобина S от тропической малярии (см.), вызываемой Plasmodium falciparum. В эндемических очагах малярии (напр., в нек-рых р-нах Центральной Африки) гемоглобин S встречается у 40% представителей в популяции; с меньшей частотой — у негров Западной Африки, а также среди популяций Северной Африки, стран Средиземноморья, Ближнего и Среднего Востока, Индии. В США 8% негров являются гетерозиготными носителями гемоглобина S. В СССР, по данным Р. Ш. Рустамова и сотр. (1981), выявлено носительство гемоглобина S у 3% азербайджанцев.

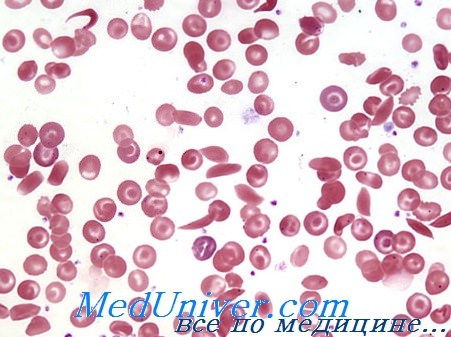
Препарат крови больного серповидно-клеточной анемией: видны эритроциты серповидной формы.
Этиология и патогенез
Причиной Серповидно-клеточной анемии является генная мутация (см.), приводящая в конечном итоге к синтезу аномального гемоглобина S, к-рый в деоксигенированном состоянии обладает свойством полимеризации и в 100 раз менее растворим, чем гемоглобин А. Вследствие этого эритроциты с деоксигемоглобином S приобретают характерную серповидную форму (рис.), в их мембране откладывается кальций. Они становятся ригидными, теряют пластические свойства, закупоривают капилляры и гемолизируются. Скорость и степень образования серповидных эритроцитов зависят от соотношения деокси- и оксигемоглобина S. Этот процесс наиболее интенсивен при гомозиготной форме С. а., при сочетании гетерозиготной С. а. с бета-талассемией (см. Талассемия), а также при гемоглобинозах SC и SD; гемоглобины С и D его усиливают, а другие, напр, гемоглобин F, угнетают. Образование серповидных эритроцитов также усиливается при снижении напряжения кислорода в тканях, повышении осмолярности плазмы, увеличении содержания 2,3-дифосфоглицерата в эритроцитах, снижении pH крови, замедлении кровотока, гипоксии и гипоксемии, при дегидратации организма и повышении температуры тела. Тяжесть гемолиза (см.) коррелирует с числом циркулирующих серповидных эритроцитов.
Длительная закупорка капилляров серповидными эритроцитами вызывает ишемию тканей вплоть до образования множественных инфарктов (см. Инфаркт), к-рые особенно часто локализуются в селезенке, костях, костном мозге, а также в мозговом веществе почек.
Как и большинство гемоглобинопатий С. а. передается по кодоминантному типу наследования.
Патологическая анатомия
При Серповидно-клеточной анемии патологоанатомические изменения такие же, как при других длительно протекающих гемолитических анемиях (см. Гемолитическая анемия). Наряду с признаками гемолиза (желтуха, эритрофагия, гемосидероз печени, селезенки, почек и лимфатических узлов) у больных С. а. отмечают застой или, наоборот, чрезвычайное малокровие внутренних органов вследствие блокады сосудов агглютинированными эритроцитами. Характерны также тромбоз сосудов и инфаркты внутренних органов в результате нарушения микроциркуляции. Вследствие Множественных инфарктов селезенка у детей старше 5—7 лет и взрослых уменьшается в размерах, сморщивается (малая сидерофибротическая селезенка).
Клиническая картина
Клиническая картина зависит от ряда факторов: гетерозиготное или гомозиготное состояние, присоединившаяся инфекция, гипоксия, стресс, беременность, наличие обострений (кризов), осложнений и др.
У взрослых гомозиготная форма при спокойном течении болезни характеризуется умеренной анемией, лишь слегка снижающей трудоспособность больных. Анемия обычно нормохромная, с гематокритным числом ок. 25%; содержание общего гемоглобина составляет 80 r/л, количество ретикулоцитов 10%, необратимо серповидных эритроцитов 12%, средняя продолжительность жизни эритроцитов ок. 17 дней, Усугубление анемии может быть связано с гипопластическим кризом (угнетением эритропоэтической функции костного мозга), гииергемолитическим кризом (повышенный гемолиз под влиянием присоединившейся инфекции, гипоксии, стрессового фактора и др.) и секвестрационным кризом (распад значительной части эритроцитов во внутренних органах, в частности в селезенке). Наиболее специфическими являются болевые кризы, характеризующиеся острой болью в участке эритростаза или инфаркта, лейкоцитозом и лихорадкой. Эти кризы провоцируются инфекциями (у детей), гипоксией, дегидратацией, холодом и др. Иногда их причину установить не удается. В течении болевых кризов различают три фазы: ишемическую (длительностью 2—6 час.), инфарктную (длительностью от 24 до 72 час.), микроэмболическую (длительностью до 1 нед. и более). Ишемическая фаза характеризуется болями в трубчатых костях, позвоночнике и суставах.
Она является обратимой, особенно при энергичном лечении. Инфарктной фазе свойственны боли во многих костях и суставах, лихорадка, потливость, лейкоцитоз и иногда усиление анемии. При микроэмболической фазе наблюдается закупорка сосудов в различных органах и тканях, возникающая в результате микроэмболизации из инфарцированного костного мозга. В зависимости от локализации тромбозов при С. а. можно выделить несколько синдромов — грудной, мышечно-скелетный, абдоминальный (в т. ч. печеночный), мозговой (чаще у детей) и др. Напр., при закупорке легочных капилляров появляются боли в области грудной клетки, плевральный выпот, нарушается дыхание.
Гомозиготная форма в детском возрасте отличается более тяжелым течением, высокой летальностью в результате присоединившейся инфекции.
Осложнениями гомозиготной формы С. а. являются калькулезный холецистит, язвы конечностей (чаще лодыжек), разнообразные поражения костей, напр, переломы, остеомиелит, часто наблюдаются асептические некрозы головок бедренной и плечевой костей, а также ретинопатия (см.), гематурия (почечного происхождения), гиперурикемия (см. Урикемия) и др. У детей могут быть тромбозы сосудов головного мозга (см. Инсульт), а у взрослых — субарахноидальные кровоизлияния (см. Подоболочечные кровоизлияния).
Клин, картина при сочетании гетерозиготной формы С. а. с бета-талассемией имеет следующие особенности: отмечается спленомегалия, появляются мишеневидные эритроциты, повышается содержание гемоглобина F или А2; осложнения в виде тромбозов встречаются сравнительно редко.
Сосудистые новообразования, кровоизлияния в стекловидное тело, ишемия и отслойка сетчатки более характерны для больных с гемоглобинозом SC.
Диагноз
Диагноз основан на анамнезе (с учетом этнической принадлежности больного), данных клин, картины, наличии серповидных эритроцитов в крови, выявляющихся с помощью пробы с метабисульфитом натрия, и характерной медленной полосы гемоглобина S при электрофорезе (см.), а также на результатах семейно-генетического исследования.
Дифференциальную диагностику проводят с болезнью Боткина (см. Гепатит вирусный), желтухами иного происхождения (см. Желтуха), другими формами гемолитических анемий, острым ревматизмом (см.) и ревматоидным артритом (см.), цингой (см.), рахитом (см.), туберкулезом костей у детей и подростков (см. Туберкулез внелегочный, костей и суставов), первичным остеомиелитом (см.), затяжным септическим эндокардитом (см.), врожденными пороками сердца (см. Пороки сердца врожденные), сифилисом (см.), фрамбезией (см.) с нек-рыми инфекционными болезнями, напр. с брюшным тифом (см.); при абдоминальных болевых кризах с острым животом (см.).
Лечение
Лечение симптоматическое. При болевых кризах назначают различные анальгетики, седативные средства, в ряде случаев наркотики, оксигенотерапию (см. Кислородная терапия). В тяжелых случаях, напр, при присоединившейся пневмококковой инфекции (пневмония, острое септическое состояние, менингит), что часто наблюдается у детей с Серповидно-клеточной анемией, применяют антибиотики; в случае оперативного вмешательства больным с С. а. проводят частичные заменные переливания крови (см.) для уменьшения количества серповидных эритроцитов (при этом необходим гематологический и биохим. контроль). В наст. время для предупреждения полимерации гемоглобина S используются препараты тиоловой группы. С целью предотвращения или ослабления агрегации эритроцитов при гемолитическом кризе применяют дезагреганты (небольшие дозы гепарина, ацетилсалициловую к-ту). Профилактические гемотрансфузии производят беременным, страдающим С. а., при усилении тяжести течения или учащении кризов. При этом добиваются уменьшения количества эритроцитов с гемоглобином S (менее 50%). В особо тяжелых случаях в период родов производят частичные заменные гемотрансфузии, при этом по возможности, следует избегать анестезии.
Прогноз
Прогноз собственно Серповидно-клеточной анемии (гомозиготные состояния) неблагоприятный; при гетерозиготных состояниях по гемоглобину SC, SD, SF, 8В+-талассемии — удовлетворительный.
Профилактика
Необходима медико-генетическая консультация (см.) с целью предупреждения браков между гетерозиготными носителями С. а. и рекомендация отказа от потомства.
См. также Талассемия.
Библиография: Алексеев Г. А. и Токарев Ю. Н. Гемоглобинопатии, с. 55, М., 1969;
Кононяченко В. А. и Юшкова Н. М. Серповидноклеточная анемия, М., 1968;
Токарев Ю. Н. и др. Серповидноклеточная болезнь и другие структурные гемоглобинопатии, в кн.: Важнейшие гемоглобинопатии, под ред. О. К. Гаврилова и Ю. Н. Токарева, с. 36, М., 1979; Кark J. a. Lessin L. Sickle cell disease and variants, в кн.: Hematol. a. oncol., ed. by M. A. Lichtman, p. 89, N. Y. a. o., 1980; Lehmann H. a. Huntsman R. G. Man’s haemoglobins, Amsterdam, 1974; Serjeant G. B. The clinical features of sickle cell disease, Amsterdam — N. Y., 1974, bibliogr.; Sickle cell symposium Arch, intern. Med., v. 133, p. 510, 1974
Ю. H. Токарев.
Как и почему возникает клеточная анемия
Это заболевание является своеобразной приспособительной реакцией, возникшей у населения, проживающего в районах с высоким распространением малярии. Возбудитель болезни – плазмодий, передаваемый комарами, живет и размножается в клетках крови. Периодически паразиты выходят в кровоток, вызывая тяжелое состояние, сопровождающееся лихорадкой, сыпью, спутанностью сознания и даже смертельными исходами.
Укус комара
Поэтому местные жители в процессе эволюции приобрели особенность, позволяющую противостоять возбудителям. Часть эритроцитов – красных кровяных клеток изменила свою форму и свойства. Они увеличили плотность и стали не круглыми, а полукруглыми, напоминающими по форме серп. В такой крови плазмодии размножаются гораздо хуже и малярия не развивается.
Однако при такой особенности количество серповидных клеток у каждого больного индивидуально. При небольших концентрациях измененных эритроцитов больные не предъявляют жалоб.
Заболевание является наследственным:
- Дети, один из родителей которых имеет признаки изменения эритроцитов, а у другого нет такой особенности, здоровы.
- Однако если оба родителя имеют в крови серповидные эритроциты, у детей в кровотоке могут полностью отсутствовать нормальные красные кровяные тельца.
Симптомы серповидноклеточной анемии
В начале жизни, пока плодные (фетальные) клетки крови не поменялись на «взрослые», ребенок с такой генетической особенностью чувствует себя нормально. Однако, постепенно его состояние ухудшается – возникает задержка физического и умственного развития, опухают суставы, появляются боль в груди, животе, пожелтение кожи, увеличение селезенки.
Характерно неправильное развитие скелета – череп в виде башни с утолщенными швами, напоминающими гребни, искривление позвоночника.
Признаки серповидной анемии:
- слабость;
- головная боль;
- затрудненное дыхание;
- пациент не может выдержать нагрузку;
- анорексия;
- быстрый сердечный ритм;
- низкое кровяное давление;
- сердечная недостаточность.
Головная боль
Быстрый сердечный ритм
У пациентов периодически наступают гемолитические кризы – состояния, при которых измененные эритроциты разрушаются. Повышается температура, нарушается дыхание, появляются явные признаки желтухи, кровь в моче, кровотечения. Возможны сильные боли в животе, вызванные увеличением селезенки. Без срочного переливания крови больной может очень быстро умереть.
До начала миграции населения проблема серповидноклеточной анемии касалась только стран, где она давно наблюдалась. Однако теперь такие случаи регистрируются в государствах, где малярия никогда не встречалась.
Как диагностируется заболевание?
Подозрения может вызывать история болезни пациента и его семьи. При этом симптомы патологии могут быть специфическими для других состояний, связанных с анемией или гемолизом.
После тщательного физического осмотра пациента, назначаются лабораторные анализы крови, подтверждающие анемию и гемолиз. Точно подтверждает наличие HbS и самого заболевания специальная лабораторная обработка образца крови пациента (электрофорез гемоглобина). Под микроскопом (после надлежащей подготовки) эритроциты приобретают характерную форму серповидных клеток.
Лабораторные нарушения гемолиза с обнаруживаемой анемией включают высокий уровень ЛДГ и высокий уровень билирубина.
Визуальные исследования, в основном, УЗИ брюшной полости, показывают увеличение селезенки или печени.
Лечение серповидноклеточной анемии
До последнего момента, единственным возможным вариантом лечения пациентов с этим видом анемии была трансплантация донорских стволовых клеток. Такая процедура требует соответствующего донора, и сам пациент также должен быть с допустимым состоянием здоровья. Из-за строгих требований лечению подвергался лишь небольшой процент пациентов с гомозиготной серповидно-клеточной анемией.
Для пациентов с симптомами тяжелого кризиса, симптомы облегчаются следующими методами:
- Обезболивание. Во многих случаях требуется сильный анальгетик (морфий).
- Оксигенотерапия.
- Переливание крови. Проводится только по индивидуальным показаниям, в случае угрозы жизни
Переливание крови
Поддержка в течение бессимптомного периода:
- Предотвращение недостатка кислорода.
- Предотвращение обезвоживания.
- Профилактика инфекций везде, где это возможно.
- Антибиотикопрофилактика из-за недостаточной функции селезенки (постоянное применение пенициллина у детей до пяти лет).
- Быстрое и целенаправленное лечение инфекций.
- Вакцинация (против пневмококка, Haemofilus influenzae).
- Прием фолиевой кислоты (спорная рекомендация).
Новые методы лечения серповидной анемии — генная терапия
Раньше больные дети умирали в раннем возрасте, но теперь медицина может продлить им жизнь, а с внедрением новой технологии – избавить от заболевания. Лечение, основанное на реактивации выработки гемоглобина, было представлено на ежегодном собрании Американского общества гематологов в Орландо, штат Флорида.
В процессе лечения у больного изымаются стволовые клетки, которые затем размножаются и вводятся обратно. В большинстве случаев такой метод приводит к излечению. Новую методику уже начали применять в США.
Ученые выяснили, что до рождения и в первые месяцы после появления на свет у ребёнка не вырабатываются серповидные красные кровяные клетки. В его кровотоке циркулирует фетальный (плодный) гемоглобин, имеющий нормальное строение. Поэтому в самом раннем детстве у ребёнка не возникает симптомов заболевания.
Со временем этот тип гемоглобина заменяется взрослым, а эритроциты приобретают серповидную форму. Учёные выяснили, что за этот переход отвечает ген BCL11A и белок с таким же названием. Выключив этот процесс, и оставив гемоглобин в плодном состоянии, можно вылечить больных.
Для этого из организма пациента «вылавливают» стволовые клетки, в которые с помощью специального вируса транспортируют маленькую шпилечную РНК, которая не дает образовываться белку BCL11A. Зачем эритроциты оставляют размножаться в специальных культурах.
Пациенту проводится цитостатическая терапия с помощью препаратов, убивающих костный мозг, как при лечении лейкоза. После этого пациенту вводят выращенные стволовые клетки. Они формируют новый костный мозг, заставляя его вырабатывать фетальный гемоглобин, который находился в кровотоке больного до рождения и в первые месяцы жизни.
Результаты лечения хорошие. Первые трое взрослых пациентов, которым была проведена «подсадка» стволовых клеток через 9,10 и 18 месяцев, чувствуют себя намного лучше. Двое из трех больше не нуждаются в переливания крови. В анализах у них не обнаружено существенных отклонений.
Затем такая процедура была проведена двум подросткам 12 и 16 лет. «Подсадка» была повторена через 5 месяцев. Практически сразу отпала необходимость в переливании крови, и исчезли гемолитические кризы.
Все больные, прошедшие лечение, избавились от риска разрушения сосудов мозга, легочной пневмонии, поражений костей. В дальнейшем планируется продолжить развивать и улучшать такой метод лечения.