Гемолитическая анемия после родов

Гемолитическая анемия
Гемолитические анемии объединяют большую группу заболеваний, при которых основным патологическим процессом является гемолиз.
Патологический гемолиз может быть обусловлен особыми свойствами эритроцитов, нарушением структуры их мембраны, активности ферментов и синтеза глобина. Эта группа гемолитических анемий носит наследственный характер.
Особую группу составляют иммунные, гемолитические анемии, которые характеризуются участием антител в повреждении или преждевременной гибели эритроцитов Гемолиз может происходить как внутриклеточно, подобно обычному физиологическому, так и внутрисосудисто. Он сопровождается уменьшением числа эритроцитов, появлением ретикулоцитоза и увеличением количества эритробластов и нормоцитов в костном мозге. В крови возрастает содержание непрямого билирубина, у больных появляется желтуха. При внутрисосудистом гемолизе возрастают гемоглобинемия и гемоглобинурия (моча имеет бурый или почти черный цвет).
Одной из форм эритроцитопатий является врожденная микросфероцитарная гемолитическая анемия, наиболее часто встречающаяся при беременности. Мы располагаем несколькими наблюдения беременных с указанной патологией. В основе нарушений при микросфероцитозе лежит дефект структуры мембраны эритроцита, что приводит к проникновению в клетку избытка натрия и накоплению воды. Сферическая форма эритроцитов и особенности структуры белка способствуют повышенному разрушению эритроцитов в селезенке.
В клинической картине заболевания центральное место принадлежит гемолитическому синдрому, который проявляется желтухой, спленомегалией, анемией. Важнейшим диагностическим признаком является желтуха, возникающая в детстве, и периодически то усиливающаяся, то ослабевающая. Содержание непрямого билирубина в крови обычно не особенно высоко и равно 102—119 мкмоль/л. Во время гемолитического криза имеется уробилинурия Количество стеркобилина возрастает в 10—25 раз. Желтуха при этом заболевании ахолурическая, так как желчные пигменты и желчные кислоты в моче отсутствуют.
Спленомегалия развивается вторично в связи с повышенным гемолизом эритроцитов в селезенке, который приводит к ее гиперплазии. Если заболевание проявляется в раннем возрасте, размеры селезенки значительно увеличиваются. Нередко больные жалуются на боли в левом подреберье в связи с развивающимся периспленитом. Довольно часто при врожденной гемолитической анемии в желчном пузыре образуются пигментные камни, в связи с чем может наблюдаться печеночная колика. Картина крови характеризуется микросфероцитозом, понижением осмотической резистентности эритроцитов, ретикулоцитозом (иногда до 50% всех эритроцитов)
Заболевание протекает циклически: ремиссии сменяются обострениями. Обострениям заболевания обычно предшествуют инфекции, травмы, а у женщин, что особенно важно, беременность. При обострении заболевания обычно повышается температура тела, так как происходит интенсивный распад крови, усиливается желтуха, увеличивается объем селезенки, появляются боли в области селезенки (периспленит), развивается анемия, которая редко достигает тяжелой степени. В начальной фазе гемолитического криза сфероцитоз резко выражен, ретикулоцитоз снижается; в конечной фазе в результате массового распада эритроцитов наблюдаются исчезновение сфероцитоза и повышение ретикулоцитоза как ответная реакция на повышенный распад крови Во время криза наблюдается умеренный лейкоцитоз (до 10—15·109/л), может быть некоторое снижение содержания тромбоцитов (до 100·109/л).
При лечении заболевания применение железа и печеночных препаратов почти не дает эффекта. Переливание крови показано в случае резкой анемизации. П. А. Герцен указывал, что единственным рациональным способом лечения гемолитической анемии является спленэктомия. Удаление селезенки при врожденной гемолитической анемии быстро приводит к ликвидации явлений повышенного гемолиза. Уровень билирубина и ретикулоцитов снижается, восстанавливается нормальное количество гемоглобина и эритроцитов.
Мы наблюдали беременных с микросфероцитарной анемией до и после операции спленэктомии. В первой группе отмечалось развитие тяжелых гемолитических кризов во второй половине беременности, сопровождавшихся анемизацией (Нb — 62 г/л), желтухой (уровень непрямого билирубина — 126,5 мкмоль/л), усилением болей в левом подреберье, повышением температуры. В связи с ухудшением течения заболевания больным была произведена спленэктомия во время беременности. После операции наступала клиническая и гематологическая ремиссия, беременность закончилась рождением живых детей.
Другую группу составили беременные с врожденной микросфероцитарной анемией, у которых спленэктомия предшествовала беременности. Беременность и роды протекали без осложнений.
Учитывая наследственный характер заболевания — микросфероцитоз наследуется по доминантному типу аутосомно, — необходимо гематологическое обследование новорожденных. В одном из наших наблюдений у ребенка была установлена врожденная гемолитическая микросфероцитарная анемия.
Аутоиммунная гемолитическая анемия возникает в результате образования антител к собственным эритроцитам. Истинно аутоиммунная анемия связана с появлением антител к эритроцитам при нарушении в иммунокомпетентпой системе больного. Все формы аутоиммунной гемолитической анемии подразделяются на симптоматические и идиопатические. Аутоиммунная гемолитическая анемия, вызванная гемобластозом, системной красной волчанкой, неспецифическим язвенным колитом, хроническим гепатитом, относится к симптоматическим. В тех случаях, когда выявить заболевание не удается, говорят об идиопатической форме гемолитической анемии. Эту форму заболевания могут провоцировать острая инфекция, травма, беременность, роды. Заболевание может начинаться остро: появляются резкая слабость, боли в пояснице и в области сердца, одышка, сердцебиения, лихорадка, быстро развивается желтуха В других случаях отмечается постепенное начало болезни, появляются артралгия, боли в животе, субфебрилитет. У большинства больных обнаруживается увеличение селезенки, реже увеличивается печень. При одной из форм аутоиммунной гемолитической анемии наблюдается непереносимость холода У больных мерзнут, белеют и синеют пальцы рук, ног, уши, нос. При острых гемолитических кризах содержание гемоглобина падает до низких цифр. Содержание ретикулоцитов умеренно повышено. У больных с хроническим течением заболевания наблюдается небольшое снижение содержания гемоглобина, анемия нормо- или гиперхромная. Содержание билирубина составляет от 25,6 до 102,6 мкмоль/л за счет непрямого. Достоверным лабораторным тестом является положительная прямая проба Кумбса. Однако и отрицательная проба не исключает заболевания, так как может наблюдаться в период наибольшей остроты болезни.
При всех формах аутоиммунной гемолитической анемии наиболее эффективным является лечение кортикостероидами. Для купирования гемолитического криза назначают большие дозы преднизолона (от 50—60 мг до 80 мг/сут). Начальными признаками эффективности лечения являются снижение температуры, уменьшение общей слабости, прекращение падения уровня гемоглобина. На 3—4-й день после начала лечения начинает повышаться содержание гемоглобина, снижается выраженность желтух. Снижение дозы преднизолона проводится медленно под контролем анализов крови. Даже при отмеченном эффекте лечения проба Кумбса остается положительной Почти у половины больных требуется повторное лечение преднизолоном в связи с рецидивом заболевания. При тяжелых обострениях возникает необходимость в гемотрансфузии Рекомендуется переливание эритромассы, подобранной индивидуально по непрямой пробе Кумбса. Переливание крови без специального подбора опасно для больных. У больных с аутоиммунной гемолитической анемией операция спленэктомии оказывается эффективной в 85% случаев [Идельсон Л. И , 1979]
Сочетание беременности и аутоиммунной гемолитической анемии встречается нечасто. Заболевание протекает с тяжелыми гемолитическими кризами и прогрессирующим падением содержания гемоглобина Нередко наблюдается угроза преждевременного прерывания беременности Прогноз для матери благоприятный, искусственное прерывание беременности не показано. Лечение состоит в назначении преднизолона по 60—80 мг в сутки с постепенным снижением дозы и гемотрансфузии эритромассы после индивидуального подбора до стойкой нормализации гематологических показателей (содержание гемоглобина до 100 г/л, снижение ретикулоцитоза). Рекомендуется поддерживающая доза преднизолона по 10—15 мг в течение всей беременности. Предпочтительна консервативная тактика ведения родов. В родах дозу преднизолона необходимо увеличить Имеются наблюдения повторяющейся аутоиммунной гемолитической анемии при каждой новой беременности. В подобных случаях рекомендуются прерывание беременности и производство стерилизации.
Анемии, связанные с нарушением синтеза глобина, встречаются у беременных значительно реже Эти анемии относятся к числу наследственных заболеваний крови. К ним относятся талассемия и гемоглобинопатия (серповидно-клеточная анемия). Эти заболевания наблюдаются и странах, примыкающих к Средиземному морю, в Юго Восточной Азии, Центральной Африке. В нашей стране они распространены в Азербайджане, Грузии, Средней Азии. Наиболее частой формой гемоглобинопатии является серповидно-клеточная анемия. В мазках крови у больных выявляются серповидные эритроциты, характерна базофильная пунктация эритроцитов Беременность сопровождается высокой материнской и детской заболеваемостью и смертностью. Во время беременности часты тяжелые гемолитические кризы, токсикозы, эмболия легочной артерии, инфекционные осложнения. Перинатальная смертность доходит до 48%. Продолжение беременности сопряжено с большим риском для матери и плода. При более легких формах заболевания вопрос о продолжении беременности решается после медико-генетической консультации в связи с высоким риском рождения больного потомства.
Лейкоз относится к гемобластозам — группе опухолей, возникающих из кроветворных клеток. Различают острый и хронический лейкоз.
Острый лейкоз в настоящее время рассматривают как злокачественную опухоль кроветворной ткани, исходящую из костного мозга, морфологическим субстратом которой являются лейкозные бластные клетки, соответствующие родоначальным элементам одного из ростков кроветворения [Ковалева Л Г, 1978], Классификация острых лейкозов включает лимфобластный, миелобластный, монобластный, промиелоцитарный, эритромиелоз и недифференцируемый лейкоз У взрослых лиц чаще встречается острый миелобластный лейкоз (50—60% больных). В этиологии лейкоза играют роль различные факторы повреждения клетки, ведущие к ее автономному росту. К ним относятся ионизирующая радиация, химические факторы и различные наследственные аномалии.
Клиническая симптоматика острого лейкоза обусловлена процессами гиперплазии опухолевой ткани и подавления нормального кроветворения Ее основой являются четыре основных синдрома:
- гиперпластический—увеличение лимфатических узлов, миндалин, печени и селезенки, появление кожных лейкозных инфильтратов (лейкемиды кожи);
- геморрагический — наблюдается у 50—60% больных, степень клинических проявлений тромбоцитопении различна: от мелкоточечных высыпаний на коже до профузных кровотечений;
- геморрагический синдром является причиной смерти 14 —18% больных острым лейкозом и одной из главных причин летального исхода после родов;
- анемический синдром возникает вследствие угнетения кроветворения и достигает значительной степени, что свидетельствует о быстром прогрессировании процесса;
- интоксикация.
Опыт показывает, что начало лейкоза не имеет клинической симптоматики. Больные чувствуют себя здоровыми до распространения опухолевых клеток по кроветворной системе и развития органных нарушений. К неспецифическим симптомам относятся нарастающая слабость, утомляемость, адинамия, снижение аппетита, сердцебиение и одышка, повышенная кровоточивость, фебрильное повышение температуры
Картина крови и костного мозга при остром лейкозе весьма характерна. Кроме анемии и тромбоцитопении, отмечается изменение числа Лейкоцитов от 0,1·109/л до 100·109/л. Клеточный состав гемограммы и миелограммы представлен в основном властными клетками и единичными зрелыми нейтрофилами. Между властными клетками и зрелыми гранулоцитами почти нет про
межуточных форм (провал в кроветворении — лейкемическое зияние) Особую диагностическую ценность имеет исследование костного мозга. Диагноз устанавливается только морфологически— обнаружение бластных опухолевых клеток в крови или костном мозге. Во всех случаях неясных цитопений необходимо пункционное исследование костного мозга. При остром лейкозе при этом обнаруживаются десятки бластных клеток.
Клиническая картина требует дифференциальной диагностики с апластической анемией, тромбоцитопенией, инфекционным мононуклеозом, острым гемолизом. Дифференциальная диагностика отдельных форм острого лейкоза проводится цитохимически.
Классификация различных форм острого лейкоза основана на цитохимической характеристике клеточного патоморфологического субстрата Наиболее частым является острый миелобластный лейкоз (50—60% больных).
Принципы современной терапии острого лейкоза заключаются в раннем начале лечения, сочетанном применении кортикостероидов и антиметаболитов и непрерывности терапии. Химиотерапия острого лейкоза предусматривает интенсивное комбинированное использование цитостатических средств. Наряду с этим проводятся переливание компонентов крови и лечение инфекционных осложнений антибиотиками.
Сочетание острого лейкоза и беременности до использования химиотерапии было чрезвычайно редким, что было обусловлено быстрым течением заболевания с летальным исходом.
В последние годы в связи с применением цитостатической терапии и увеличением продолжительности жизни больных (в среднем до 12—17 мес) случаи беременности у больных лейкозом участились. В настоящее время описано более 300 наблюдений. Чаще всего имеет место сочетание с беременностью миелобластною и лимфобластного лейкоза.
По мнению большинства авторов [Кассирский И. А, Алексеев Г. А , 1970, Ковалева JI. Г., 1978], беременность ухудшает течение лейкозного процесса, а в ряде случаев выявляет незаметно протекавший лейкоз. Отрицательное влияние оказывает не столько сама беременность, сколько ее завершение, после которого наблюдается значительное ухудшение острого лейкоза и у 25% женщин — наступление смерти в течение первой недели после родов. Некоторые гематологи допускают благоприятное влияние гормональных изменений, присущих беременности, на течение процесса.
Степень усиления клинических симптомов после родов различна: наблюдаются значительная анемизация и интоксикация; нарастание геморрагического синдрома вплоть до профузных кровотечений, приводящих к гибели больных, увеличение числа лейкоцитов и бластных клеток в периферической крови; отмечается выраженная гиперплазия лимфоузлов, печени и селезенки.
Продолжительность жизни при остром лейкозе в сочетании с беременностью существенно сокращается. Устойчивые ремиссии после родов наблюдаются крайне редко. Беременность у больных лейкозом протекает осложненно. Часто наблюдаются самопроизвольное прерывание ее, внутриутробная гибель плода. Течение беременности и ее исход находятся в зависимости от степени тяжести лейкозного процесса.
Большой интерес представляют вопросы влияния лейкоза на развитие плода Возможность трансплацентарной передачи лейкоза плоду большинством исследователей отрицается У больных лейкозом установлена большая частота (32,7%) рождения нежизнеспособных и мертвых детей В этой проблеме важным является и влияние на плод химиопрепаратов, используемых при лечении лейкоза. Установлено, что плацента является проницаемой для цитостатических средств, обладающих тератогенным и эмбриотоксическим действием. Назначаемые высокие дозы кортикостероидов могут вызвать угнетение функции коры надпочечников плода В связи с изложенным противолейкозная терапия не может быть проведена у беременных в полном объеме.
Врачебная тактика при сочетании острого лейкоза и беременности заключается в необходимости прерывания беременности и немедленного интенсивного противолейкозного лечения. При диагностике острого лейкоза в ранние сроки беременности ее прерывание следует считать обязательным Выявление острого лейкоза во II триместре беременности (наиболее часто встречающийся вариант) также требует ее прерывания; в дайной ситуации следует отдать предпочтение консервативному родоразрешению с применением простагландинов и окситоцина. Несмотря на известный риск оперативного родоразрешения, оно оправдано с целью немедленного проведения противолейкозного лечения.
При развитии острого лейкоза в конце беременности и компенсированном состоянии больных допустимы выжидание до срока развития жизнеспособного плода и вызывание родов консервативными методами Как досрочное прерывание беременности, так и родоразрешение требуют специальной подготовки больных: назначения кортикостероидов, гемотрансфузии, больших доз аскорбиновой кислоты, препаратов кальция, рутина. При показаниях применяются антибиотики и кардиотонические препараты.
При решении вопроса о допустимости беременности у молодых женщин с длительными ремиссиями (более 5 лет) следует учитывать возможность рецидива заболевания, хотя в подобной ситуации описаны благоприятные исходы для матери и плода.
Особо необходимо подчеркнуть важность ранней диагностики острого лейкоза, сочетающегося с беременностью, поэтому все случаи неясных анемий, лейкопений и лейкемоидных реакций у беременных требуют тщательного гематологического исследования.
Если вы нашли ошибку, пожалуйста, выделите фрагмент текста и нажмите Ctrl+Enter.
Страницы: 1 2 3 4 5

Гемолитическая анемия – патология эритроцитов, отличительным признаком которой является ускоренное разрушение красных кровяных телец с высвобождением повышенного количества непрямого билирубина. Для данной группы заболеваний типично сочетание анемического синдрома, желтухи и увеличения размеров селезенки. В процессе диагностики исследуется общий анализ крови, уровень билирубина, анализ кала и мочи, УЗИ органов брюшной полости; проводится биопсия костного мозга, иммунологические исследования. В качестве методов лечения используется медикаментозная, гемотрансфузионная терапия; при гиперспленизме показана спленэктомия.
Общие сведения
Гемолитическая анемия (ГА) – малокровие, обусловленное нарушением жизненного цикла эритроцитов, а именно преобладанием процессов их разрушения (эритроцитолиза) над образованием и созреванием (эритропоэзом). Данная группа анемий очень обширна. Их распространенность неодинакова в различных географических широтах и возрастных когортах; в среднем патология встречается у 1% населения. Среди прочих видов анемий на долю гемолитических приходится 11%. Патология характеризуется укорочением жизненного цикла эритроцитов и их распадом (гемолизом) раньше времени (через 14-21 день вместо 100-120 суток в норме). При этом разрушение эритроцитов может происходить непосредственно в сосудистом русле (внутрисосудистый гемолиз) или в селезенке, печени, костном мозге (внесосудистый гемолиз).
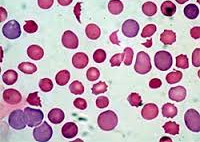
Гемолитическая анемия
Причины
Этиопатогенетическую основу наследственных гемолитических синдромов составляют генетические дефекты мембран эритроцитов, их ферментных систем либо структуры гемоглобина. Данные предпосылки обусловливают морфофункциональную неполноценность эритроцитов и их повышенное разрушение. Гемолиз эритроцитов при приобретенных анемиях наступает под влиянием внутренних факторов или факторов окружающей среды, среди которых:
- Аутоиммунные процессы. Образование антител, агглютинирующих эритроциты, возможно при гемобластозах (остром лейкозе, хроническом лимфолейкозе, лимфогранулематозе), аутоиммунной патологии (СКВ, неспецифическом язвенном колите), инфекционных заболеваниях (инфекционном мононуклеозе, токсоплазмозе, сифилисе, вирусной пневмонии). Развитию иммунных гемолитических анемий могут способствовать посттрансфузионные реакции, профилактическая вакцинация, гемолитическая болезнь плода.
- Токсическое действие на эритроциты. В ряде случаев острому внутрисосудистому гемолизу предшествует отравление мышьяковистыми соединениями, тяжелыми металлами, уксусной кислотой, грибными ядами, алкоголем и др. Вызывать разрушение клеток крови может прием определенных лекарств (противомалярийных препаратов, сульфаниламидов, производных нитрофуранового ряда, анальгетиков).
- Механическое повреждение эритроцитов. Гемолиз эритроцитов может наблюдаться при тяжелых физических нагрузках (длительной ходьбе, беге, лыжном переходе), при ДВС-синдроме, малярии, злокачественной артериальной гипертензии, протезировании клапанов сердца и сосудов, проведении гипербарической оксигенации, сепсисе, обширных ожогах. В этих случаях под действием тех или иных факторов происходит травматизация и разрыв мембран изначально полноценных эритроцитов.

Гемолитическая анемия
Патогенез
Центральным звеном патогенеза ГА является повышенное разрушение эритроцитов в органах ретикулоэндотелиальной системы (селезенке, печени, костном мозге, лимфатических узлах) или непосредственно в сосудистом русле. При аутоиммунном механизме анемии происходит образование антиэритроцитарных АТ (тепловых, холодовых), которые вызывают ферментативный лизис мембраны эритроцитов. Токсические вещества, являясь сильнейшими окислителями, разрушают эритроцит за счет развития метаболических, функциональных и морфологических изменений оболочки и стромы красных кровяных телец. Механические факторы оказывают прямое воздействие на клеточную мембрану. Под влиянием этих механизмов из эритроцитов выходят ионы калия и фосфора, а внутрь поступают ионы натрия. Клетка разбухает, при критическом увеличении ее объема наступает гемолиз. Распад эритроцитов сопровождаются развитием анемического и желтушного синдромов (так называемой «бледной желтухой»). Возможно интенсивное окрашивание кала и мочи, увеличение селезенки и печени.
Классификация
В гематологии гемолитические анемии подразделяются на две большие группы: врожденные (наследственные) и приобретенные. Наследственные ГА включают следующие формы:
- эритроцитарные мембранопатии (микросфероцитоз – болезнь Минковского-Шоффара, овалоцитоз, акантоцитоз) – анемии, обусловлены структурными аномалиями мембран эритроцитов
- ферментопении (энзимопении) – анемии, вызванные дефицитом тех или иных ферментов (глюкозо-6-фосфатдегидрогеназы, пируваткиназы и др.)
- гемоглобинопатии – анемии, связанные с качественными нарушениями структуры гемоглобина или изменением соотношения его нормальных форм (талассемия, серповидно-клеточная анемия).
Приобретенные ГА подразделяются на:
- мембранопатии приобретенные (пароксизмальная ночная гемоглобинурия – б-нь Маркиафавы-Микели, шпороклеточная анемия)
- иммунные (ауто- и изоиммунные) – обусловлены воздействием антител
- токсические – анемии, обусловленные воздействием химических веществ, биологических ядов, бактериальных токсинов
- механические – анемии, вызванные механическим повреждением структуры эритроцитов (тромбоцитопеническая пурпура, маршевая гемоглобинурия)
Симптомы
Наследственные мембранопатии, ферментопении и гемоглобинопатии
Наиболее распространенной формой данной группы анемий является микросфероцитоз, или болезнь Минковского-Шоффара. Наследуется по аутосомно-доминантному типу; обычно прослеживается у нескольких представителей семьи. Дефектность эритроцитов обусловлена дефицитом в мембране актомиозиноподобного белка и липидов, что приводит к изменению формы и диаметра эритроцитов, их массивному и преждевременному гемолизу в селезенке. Манифестация микросфероцитарной ГА возможна в любом возрасте (в младенчестве, юношестве, старости), однако обычно проявления возникают у детей старшего возраста и подростков. Тяжесть заболевания варьирует от субклинического течения до тяжелых форм, характеризующихся часто повторяющимися гемолитическими кризами. В момент криза нарастает температура тела, головокружение, слабость; возникают боли в животе и рвота.
Основным признаком микросфероцитарной гемолитической анемии служит желтуха различной степени интенсивности. Вследствие высокого содержания стеркобилина кал становится интенсивно окрашенным в темно-коричневый цвет. У пациентов с болезнь Минковского-Шоффара наблюдается склонность к образованию камней в желчном пузыре, поэтому часто развиваются признаки обострения калькулезного холецистита, возникают приступы желчной колики, а при закупорке холедоха конкрементом – обтурационная желтуха. При микросфероцитозе во всех случаях увеличена селезенка, а у половины пациентов – еще и печень. Кроме наследственной микросфероцитарной анемии, у детей часто встречаются другие врожденные дисплазии: башенный череп, косоглазие, седловидная деформация носа, аномалии прикуса, готическое нёбо, полидактилия или брадидактилия и пр. Пациенты среднего и пожилого возраста страдают трофическими язвами голени, которые возникают в результате гемолиза эритроцитов в капиллярах конечностей и плохо поддаются лечению.
Энзимопенические анемии связаны с недостатком определенных ферментов эритроцитов (чаще – Г-6-ФД, глутатион-зависимых ферментов, пируваткиназы и др). Гемолитическая анемия может впервые заявлять о себе после перенесенного интеркуррентного заболевания или приема медикаментов (салицилатов, сульфаниламидов, нитрофуранов). Обычно заболевание имеет ровное течение; типична «бледная желтуха», умеренная гепатоспленомегалия, сердечные шумы. В тяжелых случаях развивается ярко выраженная картина гемолитического криза (слабость, рвота, одышка, сердцебиение, коллаптоидное состояние). В связи с внутрисосудистым гемолизом эритроцитов и выделением гемосидерина с мочой последняя приобретает темный (иногда черный) цвет. Особенностям клинического течения гемоглобинопатий – талассемии и серповидно-клеточной анемии посвящены самостоятельные обзоры.
Приобретенные гемолитические анемии
Среди различных приобретенных вариантов чаще других встречаются аутоиммунные анемии. Для них общим пусковым фактором выступает образование антител к антигенам собственных эритроцитов. Гемолиз эритроцитов может носить как внутрисосудистый, так и внутриклеточный характер. Гемолитический криз при аутоиммунной анемии развивается остро и внезапно. Он протекает с лихорадкой, резкой слабостью, головокружением, сердцебиением, одышкой, болями в эпигастрии и пояснице. Иногда острым проявлениям предшествуют предвестники в виде субфебрилитета и артралгий. В период криза стремительно нарастает желтуха, не сопровождающаяся кожным зудом, увеличивается печень и селезенка. При некоторых формах аутоиммунных анемий больные плохо переносят холод; в условиях низких температур у них может развиваться синдром Рейно, крапивница, гемоглобинурия. Вследствие недостаточности кровообращения в мелких сосудах возможны осложнения в виде гангрены пальцев ног и рук.
Токсические анемии протекают с прогрессирующей слабостью, болями в правом подреберье и поясничной области, рвотой, гемоглобинурией, высокой температурой тела. Со 2-3 суток присоединяется желтуха и билирубинемия; на 3-5 сутки возникает печеночная и почечная недостаточность, признаками которых служат гепатомегалия, ферментемия, азотемия, анурия. Отдельные виды приобретенных гемолитических анемий рассмотрены в соответствующих статьях: «Гемоглобинурия» и «Тромбоцитопеническая пурпура», «Гемолитическая болезнь плода».
Осложнения
Каждый вид ГА имеет свои специфические осложнения: например, ЖКБ – при микросфероцитозе, печеночная недостаточность – при токсических формах и т.д. К числу общих осложнений относятся гемолитические кризы, которые могут провоцироваться инфекциями, стрессами, родами у женщин. При остром массивном гемолизе возможно развитие гемолитической комы, характеризующейся коллапсом, спутанным сознанием, олигурией, усилением желтухи. Угрозу жизни больного несут ДВС-синдром, инфаркт селезенки или спонтанный разрыв органа. Неотложной медицинской помощи требуют острая сердечно-сосудистая и почечная недостаточность.
Диагностика
Определение формы ГА на основе анализа причин, симптоматики и объективных данных относится к компетенции гематолога. При первичной беседе выясняется семейный анамнез, частота и тяжесть протекания гемолитических кризов. В процессе осмотра оценивается окраска кожных покровов, склер и видимых слизистых, производится пальпация живота для оценки величины печени и селезенки. Сплено- и гепатомегалия подтверждается при проведении УЗИ печени и селезенки. Лабораторный диагностический комплекс включает:
- Исследование крови. Изменения в гемограмме характеризуются нормо- или гипохромной анемией, лейкопенией, тромбоцитопенией, ретикулоцитозом, ускорением СОЭ. В биохимических пробах крови определяется гипербилирубинемия (увеличение фракции непрямого билирубина), увеличение активности лактатдегидрогеназы. При аутоиммунных анемиях большое диагностическое значение имеет положительная проба Кумбса.
- Анализы мочи и кала. Исследование мочи выявляет протеинурию, уробилинурию, гемосидеринурию, гемоглобинурию. В копрограмме повышено содержание стеркобилина.
- Миелограмму. Для цитологического подтверждения выполняется стернальная пункция. Исследование пунктата костного мозга обнаруживает гиперплазию эритроидного ростка.
В процессе дифференциальной диагностики исключаются гепатиты, цирроз печени, портальная гипертензия, гепатолиенальный синдром, порфирии, гемобластозы. Пациента консультируют гастроэнтеролог, клинический фармаколог, инфекционист и другие специалисты.

Аутоиммунная гемолитическая анемия
Лечение
Различные формы ГА имеют свои особенности и подходы к лечению. При всех вариантах приобретенной гемолитической анемии необходимо позаботиться об устранении влияния гемолизирующих факторов. Во время гемолитических кризов больным необходимы инфузии растворов, плазмы крови; витаминотерапия, по необходимости – гормоно- и антибиотикотерапия. При микросфероцитозе единственно эффективным методом, приводящим к 100 % прекращению гемолиза, является спленэктомия.
При аутоиммунной анемии показана терапия глюкокортикоидными гормонами (преднизолоном), сокращающая или прекращающая гемолиз. В некоторых случаях требуемый эффект достигается назначением иммунодепрессантов (азатиоприна, 6-меркаптопурина, хлорамбуцила), противомалярийных препаратов (хлорохина). При резистентных к медикаментозной терапии формах аутоиммунной анемии выполняется спленэктомия. Лечение гемоглобинурии предполагает переливание отмытых эритроцитов, плазмозаменителей, назначение антикоагулянтов и антиагрегантов. Развитие токсической гемолитической анемии диктует необходимость проведения интенсивной терапии: дезинтоксикации, форсированного диуреза, гемодиализа, по показаниям – введение антидотов.
Прогноз и профилактика
Течение и исход зависят от вида анемии, тяжести протекания кризов, полноты патогенетической терапии. При многих приобретенных вариантах устранение причин и полноценное лечение приводит к полному выздоровлению. Излечения врожденных анемий добиться нельзя, однако возможно достижение длительной ремиссии. При развитии почечной недостаточности и других фатальных осложнений прогноз неблагоприятен. Предупредить развитие ГА позволяет профилактика острых инфекционных заболеваний, интоксикаций, отравлений. Запрещается бесконтрольное самостоятельное использование лекарственных препаратов. Необходимо тщательная подготовка пациентов к гемотрансфузиям, вакцинации с проведением всего комплекса необходимых обследований.
