Гемотрансфузии при железодефицитной анемии

Переливание крови при низком гемоглобине, последствия и особенности процесса каковы? Да, вопрос серьезный.
Мало кто догадывается, что такие названия, как «малокровие», «пониженный гемоглобин» и «анемия» являются названием одного и того же заболевания. Проблема заключается в том, что в крови уменьшается количество эритроцитов. В состав эритроцитов входит сложный железосодержащий белок. Он необходим для снабжения кислородом и своевременной очистки тканей от углекислого газа.
Много людей часто ощущают себя уставшими уже с утра, ночью не могут уснуть, имеют бледный цвет лица в не зависимости от сезона, чувствуют головокружения, но не придают этому особого значения. Это симптомы пониженного гемоглобина.
Норма гемоглобина абсолютно разная для мужчин и женщин, для молодых и пожилых. Указывают такие показатели нормы гемоглобина в крови для взрослого человека: от 120 до 160 г/л.
Понижение гемоглобина в крови в народе называют малокровием. Если заболевание не слишком запущено, то назначают специальную диету и при помощи продуктов стараются нормализовать количество гемоглобина в крови.
Переливание крови при низком гемоглобине делают только в крайнем случае, когда другого пути у человека нет и выбор стоит сложный: между жизнью и смертью. Такую процедуру назначают в случае, если показатели гемоглобина опустились ниже 60г/л. После того, как выполнено переливание крови при низком гемоглобине, наблюдается очень быстрое повышение как самого гемоглобина, так и улучшение самочувствия больного в целом.
Низкий гемоглобин: симптомы и признаки
- Сбой сердечного ритма. Может возникать учащенное сердцебиение или, наоборот, замедленное. У некоторых людей появляется ощущение, что сердце бьется очень быстро, а потом пропускает удары.
- Повышенная сонливость.
- Головокружение. Сначала наблюдаются при резком повороте головы. Со скоростью развития заболевания увеличивается и количество головокружений.
- Периодически возникает потеря сознания.
- Хроническая усталость. Человек с утра просыпается относительно бодрым, а уже к обеду – появляется чувство усталости.
- Головные боли.
- Одышка.
- Частые простудные заболевания.
- Ослабления иммунитета.
Очень редко бывают такие симптомы пониженного гемоглобина, как нарушение кровообращения в конечностях, ощущения холода в руках и ногах, судороги. Наблюдаются изменения в ногтевой пластине. Подросток при этом заболевании медленнее растет. В большом количестве выпадают волосы. К тому же становится очень бледной кожа, в уголках возникают ранки. Изменяется вкусовые качества еды, цвет языка. Легче малокровие переносится женщинами, чем мужчинами. Но радоваться женщинам не стоит, так как это заболевание серьезно поражает весь организм.
Положительная сторона гемотрансфузии
Переливание крови проводится при уровне гемоглобина ниже 60-65 г/л в зависимости от клинической ситуации. Цель этой манипуляции в том, чтобы как можно быстрее стабилизировать состояние пациента. Низкий уровень гемоглобина крайне негативно отражается на состоянии пациента, так как он приводит к следующим изменениям:
- Замедленное заживление тканей.
- Гипоксия органов – в первую очередь, головного мозга и сердца.
- Прогрессирование патологических процессов.
Итак, гемотрансфузия при низком гемоглобине позволяет восстановить нормальное или близкое к нормальному снабжение тканей и клеток кислородом. В итоге это благоприятно сказывается на их функционировании. На этом фоне выздоровление после основного заболевания, которое и привело к тяжелой анемии, протекает намного быстрее и лучше.
Данная манипуляции преследует четкие цели. В большинстве случаев вливание донорского материала обусловлено необходимостью восполнения потерянной крови при обширных кровотечениях. Также гемотрансфузия может быть единственным способом повышения уровня тромбоцитов для улучшения показателей свертываемости. Исходя из этого, показаниями к переливанию плазмы крови являются:
- смертельно опасная кровопотеря;
- шоковое состояние;
- анемия тяжелой степени;
- подготовка к плановому хирургическому вмешательству, предположительно сопровождающемуся внушительными кровопотерями и осуществляемому с использованием приборов для искусственного кровообращения (операции на сердце, сосудах).
Эти показания являются абсолютными. Кроме них, послужить поводом к проведению гемотрансфузии может сепсис, заболевания крови, химическое отравление организма.
Причины, которые приводят к анемии
«Дыма без огня не бывает», гласит народная пословица. У каждого заболевания всегда есть первопричина. А в случае белокровия причин существует великое множество.
Чаще всего к малокровию приводят:
- Хронические инфекционные заболевания.
- Воспалительные процессы в организме.
- Несбалансированное питание.
- Операции, во время которых было утеряно большое количество крови. В том числе и роды.
- Вследствие скрытых кровотечений внутренних органов или хроническом кровоточащем геморрое.
- Ранее перенесенная желтуха.
- Варикозное расширение вен.
- Прием в пищу продуктов, содержащих только углеводы. Для организма и кровообращения необходима белковая пища.
- Переходный возраст.
- Генетическая предрасположенность.
Бывает так, что организм сам показывает наличие заболевания в нем. В таком случае человеку нужно подкрепиться глиной или съесть кусочек мела. Некоторые люди наблюдают за собой и замечают, что им начинает нравиться запах масляной краски и бензина.
Коррекция высоких показателей лейкоцитов при раке
Уровень лейкоцитов при онкологии растет при многих типах лейкозов, во время которых назначается гормональная терапия. Прием кортикостероидов снижает интенсивность симптомов и увеличивает резерв костного мозга.
Гормонотерапия при тяжелой степени лейкоза, способна подавить митотические процессы в очагах поражения, оказывая при этом дополнительное сопротивление опухоли.
Изначально лечение проводится малыми дозами, но если у больного будет отмечаться отрицательная динамика, то вводимые дозы постепенно повышаются. При тяжелых стадиях болезни, а также при ярко протекающем геморрагическом синдроме, лечение проводится максимально допустимыми дозами стероидов.
Как проходит процедура переливания крови?
Для нормализации гемоглобина в крови на запущенной стадии заболевания может помочь только переливание крови. Во время проведения данной процедуры происходит переливание крови от здорового человека больному.
Конечно, такую процедуру не назначают при начальной стадии анемии. Когда показатели гемоглобина в крови не слишком низкие, врач рекомендует «сесть на диету» и снабдить свой рацион такими продуктами питания, как гранат, грецкие орехи и яблоки. Желательно навсегда освободиться от вредных привычек. Например, курения. Рекомендованы вечерние и утренние прогулки по свежему воздуху.
Но что происходит, если процедура переливания крови все же назначена?
- Врач проводит обследование.Необходимо сдать анализ крови, вследствие которого определяется уровень гемоглобина в крови. Если он низкий, то узнают следующие ответы на вопросы. У женщин выясняют наличие детей и симптоматику во время беременности, а также проходила ли раньше процедура переливания крови.
- Определяют группу крови. При этом для точности диагностики резус-фактор определяется не менее двух раз. Если наблюдаются разные показатели, проводят третье исследование и выставляют группу, которая повторилась два раза.
К тому же врач определяет донора по следующим критериям:
- в паспорте обязательно должны быть данные о доноре. Фамилия, имя, отчество. Номер и дата заготовки. Группа крови;
- какой добавлен консервант;
- насколько герметична упаковка;
- учреждения, в котором проходил процесс сбора крови;
- подпись врача;
- срок годности от 3 до 5 недель;
- внешняя характеристика качества крови.
Перепроверяется совпадение группы крови донора и больного.
Проверяют индивидуальную совместимость крови. Для этого на специальное стекло капают капельку крови донора и пациента.
Еще раз перепроверяют совместимость крови по резус-фактору.
Наблюдают индивидуальную реакцию организма. Для этого в организм вводят порционно, с интервалом в 3 минуты, 25 миллиграммов крови. Отслеживают реакцию организма на новую кровь. Замеряют пульс. Наблюдают кожные покровы на лице (нет ли покраснений), а также общее состояние организма.
После проведения всей подготовки наступает время переливания крови. Но при различных заболеваниях переливают не саму кровь, а ее разные ингредиенты. Например, при малокровии вводят эритроцитарную массу.
Кровь вводится потихоньку, медленно, приблизительно со скоростью в среднем 50 капель за минуту. На протяжении всей процедуры присутствует врач, он и следит за успешностью проведения операции. Периодически измеряют пульс, давление, температуру. Наблюдают за цветом кожи и самочувствием. Каждый показатель записывается в медицинскую карточку посетителя.
Небольшое количество крови оставляют на несколько дней в холодильнике.
Это необходимо в случае, если у пациента будут наблюдаться осложнения.
После переливания крови первый день пациент должен провести в состоянии покоя. На второй день необходимо сдать анализы. Если все складывается хорошо, то на третий – пациента выписывают домой.
Каждый, кто проходит эту процедуру, предварительно задается вопросом – опасно ли переливание крови? Для того чтобы чувствовать себя более спокойно, необходимо знать симптомы и последствия неудачной операции.
Негативные последствия переливания крови:
- Боль во всем теле.
- Высыпания на коже.
- Понижение давления.
- Повышение температуры.
- Сильная головная боль.
- Рвота и отечность.
- Сбой сердцебиения.
Показания
Самое распространённое показание к переливанию — это потеря крови. Острой потерей считается потеря пациентом в течение пары часов более 30 % объёма крови. Кроме этого, среди абсолютных показаний к гемотрансфузии — шоковое состояние, непрекращающиеся кровотечения, тяжёлое малокровие, хирургические вмешательства.
Частыми показаниями к переливанию компонентов крови являются анемия, гематологические заболевания, гнойно-септические болезни, тяжёлые токсикозы, острые интоксикации.
Гемотрансфузия была и остаётся крайне рискованной процедурой. Переливание крови может вызвать серьёзные нарушения жизненно важных процессов, поэтому даже при наличии показаний к этой процедуре медики всегда рассматривают наличие или отсутствие противопоказаний, среди которых — сердечная недостаточность при пороках, миокардите, кардиосклерозе, гнойное воспаление внутренней оболочки сердца, гипертония третьей стадии, нарушение кровотока головного мозга, общее нарушение белкового обмена, аллергическое состояние и другие заболевания.
Существует такое понятие как «кровяной допинг», иначе — аутогемотрансфузия. При этой процедуре производится переливание реципиенту его же собственной крови. Это достаточно распространенная методика в спорте, однако официальные структуры приравнивают её к применению допинга. «Кровяной допинг» ускоряет доставку кислорода к мышцам, увеличивая их производительность.
Большую роль играет информация о предыдущих переливаниях, если таковые были. Также в группу риска входят женщины, пережившие тяжёлые роды, выкидыши или рождение детей с желтухой, и пациенты с раковыми опухолями, патологиями крови, продолжительными септическими процессами.
Часто при абсолютных показаниях к переливанию крови процедуру производят несмотря на противопоказания, но при этом организуют профилактические мероприятия, например, для предупреждения аллергической реакции. Иногда при хирургических операциях применяется предварительно заготовленная собственная кровь пациента.
Определение противопоказаний — не менее важный этап в процессе подготовки к процедуре. Согласно правилам переливания плазмы крови, основными препятствиями к данной манипуляции относятся:
- сердечная недостаточность;
- перенесенный в недавнем прошлом инфаркт миокарда;
- ишемическая болезнь сердца;
- врожденные сердечные пороки;
- бактериальный эндокардит;
- гипертонический криз;
- острое нарушение мозгового кровообращения;
- тромбоэмболический синдром;
- отек легких;
- гломерулонефрит на стадии обострения;
- печеночная и почечная недостаточность;
- склонность к аллергии на множество раздражителей;
- бронхиальная астма.
В некоторых случаях, когда трансфузия – единственный способ сохранить больному жизнь, отдельные противопоказания могут игнорироваться. При этом ткани реципиента и донора с целью подтверждения совместимости должны пройти множество проб. Переливанию плазмы также должна предшествовать комплексная диагностика.
Как поднять гемоглобин новорожденным?
В случае если у ребенка определяют пониженный гемоглобин, то есть два варианта решения этой проблемы. Первый – это питание ( рекомендованы яблоки, гранат, печень, мясо крупного рогатого скота). Второй вариант – это медикаментозное лечение. Врачи стараются этот метод восстановления здоровья использовать только в критической ситуации.
Бывают случаи, при которых у беременных женщин наблюдается низкий гемоглобин. Восстанавливают организм в таком случае при помощи лекарств или специальных продуктов. Негативные последствия для организма возникают и тогда, если имеется высокий гемоглобин: кровь становится густой, хуже работают внутренние органы. Возникает предрасположенность к инсультам и инфарктам.
Для того чтобы нормализовать уровень гемоглобина, необходимо пересмотреть свой рацион. Если это не помогает, то следует обратиться к врачу, который припишет медикаментозное лечение.
Причины снижения гемоглобина в крови при онкологии
Уровень гемоглобина во время рака может изменяться по разным причинам
Важно установить причину уменьшения концентрации белка в каждом конкретном случае, чтобы знать, как поднять гемоглобин и предупредить осложнение течения болезни в будущем
Причина может быть связана с внутренним кровотечением. Онкопатология вызывает подобное осложнение часто, особенно при активном прогрессировании злокачественной опухоли или на фоне побочной реакции от назначенной терапии. Отдельно определяются и иные причины, которые могут способствовать снижению уровня сывороточного гемоглобина:
- дисфункция ЖКТ в результате проблем с усвоением железа;
- распространение метастазов в костный мозг;
- потеря возможности полноценного питания (при раке желудка, пищевода или кишечника), в результате возникает дефицит железа в организме;
- применение сильнодействующих лекарственных средств и процедур (химиотерапия или облучение), побочными реакциями которых является снижение способности к кроветворению;
- острая интоксикация организма, по причине постоянного роста и распада злокачественной опухоли на последних стадиях онкологии.
Технология
Перед переливанием крови пациента обязательно проверяют на противопоказания, ещё раз проверяют группу крови и резус-фактор и тестируют кровь донора на индивидуальную совместимость. После этого проводится биологическая проба — пациенту вводят 25–30 мл крови донора и наблюдают за состоянием больного. Если пациент чувствует себя хорошо, то кровь считается совместимой и проводится гемотрансфузия со скоростью 40–60 капель в минуту.
После переливания несовместимой крови могут возникнуть осложнения, сбой дают почти все системы организма. Например, возможно нарушение функций почек и печени, обменных процессов, деятельности желудочно-кишечного тракта, сердечно-сосудистой и центральной нервной систем, дыхания, кроветворения.
 Целью терапии железодефицитной анемии (ЖДА) является устранение дефицита железа и восстановление его запасов в организме. Добиться этого можно только при ликвидации причины, лежащей в основе ЖДА в организме.
Целью терапии железодефицитной анемии (ЖДА) является устранение дефицита железа и восстановление его запасов в организме. Добиться этого можно только при ликвидации причины, лежащей в основе ЖДА в организме.
Основные принципы лечения ЖДА сформулированы Л. И. Идельсоном в 1981 г.:
Возместить дефицит железа без лекарственных железосодержащих препаратов невозможно.
Терапия ЖДА должна проводиться преимущественно препаратами железа для перорального приема.
Терапия ЖДА не должна прекращаться после нормализации уровня гемоглобина.
Гемотрансфузии при ЖДА должны проводиться только строго по жизненным показаниям.
Ранее существовало мнение, что дефицит железа можно устранить назначением диеты, содержащей яблоки, гречневую крупу, гранаты и другие продукты растительного происхождения, содержащие железо. Однако в 60-е гг. ХХ века исследователями было доказано, что железо, содержащееся в продуктах в виде гема (мясо, печень, рыба), лучше усваивается в организме, чем из других соединений. Около 90% железа всасывается в 12-перстной кишке, остальное – в верхнем отделе тощей кишки. При железодефицитных состояниях абсорбционная поверхность тонкого кишечника увеличивается. Железо всасывается в 2-х формах:
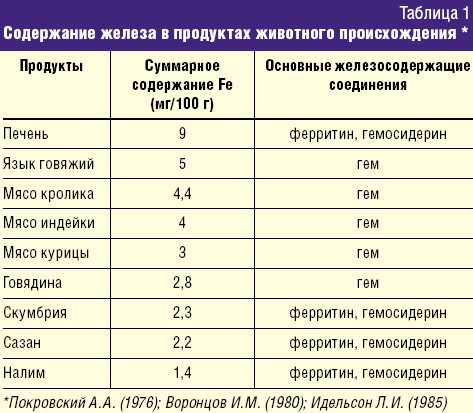
гемовой (10%), источниками которой являются гемоглобин и миоглобин, входящие в состав продуктов животного происхождения (мясо, рыба, птица, печень) (табл. 1);
негемовой (90%), источниками которой являются продукты растительного происхождения (овощи, фрукты, злаки) (табл. 2).

Количество железа, поступающее в течение суток с пищей, содержит около 10–12 мг железа (гемовое + негемовое), но только 1–1,2 мг микроэлемента из этого количества абсорбируется. Установлено, что биодоступность гемового железа в пищевых продуктах более высокая, чем из негемовых соединений, и составляет 25–30%.
Большая часть поступающего с пищей железа представлена негемовой формой. Биодоступность железа из злаковых, бобовых, клубневых, овощей и фруктов значительно ниже, чем из гемовых соединений, и во многом зависит от преобладания в рационе факторов, ингибирующих либо потенцирующих кишечную ферроабсорбцию (табл. 3).

Несмотря на высокое содержание железа в части продуктов растительного происхождения, они не в состоянии обеспечить им организм ребенка. Присутствующие в продуктах питания растительного происхождения вещества (танины, фитины, фосфаты) образуют с Fe (III) нерастворимые соединения и выводятся с калом. Имеются также сведения о неблагоприятном влиянии на абсорбцию железа пищевых волокон, которыми богаты крупы, свежие овощи, фрукты. В кишечнике пищевые волокна практически не перевариваются, железо фиксируется на их поверхности и выводится с калом. Напротив, повышают биодоступность железа аскорбиновая кислота, животный белок (мясо, рыба), которые увеличивают абсорбцию микроэлемента. Необходимо отметить также, что продукты из мяса, печени, рыбы, в свою очередь, увеличивают всасывание железа из овощей и фруктов при одновременном их применении.
Полноценная и сбалансированная по основным ингредиентам диета позволяет лишь «покрыть» физиологическую потребность организма в железе, но не устранить его дефицит.
Естественной профилактикой ЖДА у детей первых месяцев жизни является исключительно грудное вскармливание до 4–6 мес. Известно, что концентрация железа в женском молоке составляет всего 0,2–0,4 мг/л, однако абсорбция железа из него достигает 50%, что обеспечивает потребность ребенка первых 4–6 мес. К моменту удвоения массы тела ребенка (5–6 мес) антенатальные запасы железа в его организме истощаются.
С целью профилактики ЖДА при искусственном вскармливании целесообразно у детей, относящихся к группе риска по развитию ЖДА, использовать смеси, обогащенные железом. Они назначаются доношенным детям, относящимся к группе риска (из двойни, тройни, имеющих большую прибавку в массе), начиная с 3–5 мес жизни, а недоношенным – с 1,5–2 мес. Содержание железа в смесях для искусственного вскармливания детей первого полугодия жизни составляет 3–5–8 мг/л смеси, а для детей второго полугодия – 10–14 мг/л.
Включение в питание детей продуктов прикорма, обогащенных железом (фруктовые соки, фруктовые и овощные пюре, инстантные каши), заметно повышает количество железа, поступающего с пищей в организм ребенка.
Детям в возрасте 4–6 мес, находящимся на грудном вскармливании, и младенцам после 6 мес жизни, не получающим обогащенное железом питание, целесообразно назначать препараты железа в профилактической дозе 1–2 мг/кг/день до 12–18 мес жизни.
ЖДА у детей раннего возраста связывают с ранним использованием в пищу коровьего или козьего молока, содержащего высокий уровень белка. Следует отметить, что развитие ЖДА у этих детей связано не только с низким уровнем железа в коровьем молоке, плохим его усвоением, но и потерей железа за счет микродиапедезных кишечных кровотечений. Многочисленными исследованиями отмечена взаимосвязь между количеством употребляемого неадаптированного продукта (молока, кефира) и степенью выраженности микродиапедезных кишечных кровопотерь у младенцев. Отмечено, что чувствительность к неадаптированным продуктам уменьшается с возрастом и после 2-х лет жизни микродиапедезных кишечных кровотечений на фоне приема коровьего молока не отмечается. Механизм, лежащий в основе повышенной экскреции гемоглобина с калом на фоне приема неадаптированных молочных продуктов, у детей раннего возраста точно не известен. Часть авторов связывают микродиапедезные кишечные кровотечения с непереносимостью белков коровьего молока.
Выбору препарата для коррекции ЖДА придается особое значение, поскольку длительность лечения может составлять от нескольких недель до нескольких месяцев. При этом важны не только эффективность, но и отсутствие побочных эффектов и осложнений, приверженность к проводимой терапии, особенно в педиатрической практике.
В настоящее время все препараты железа разделяют на две группы (табл. 4):
ионные железосодержащие препараты (солевые, полисахаридные соединения железа);
неионные соединения, к которым относятся препараты, представленные гидроксид-полимальтозным комплексом (ГПК) трехвалентного железа.

Терапия железодефицитных состояний должна быть направлена на устранение причины и одновременное восполнение дефицита железа лекарственными Fe-содержащими препаратами.
Терапия железодефицитных состояний должна проводиться преимущественно препаратами железа для приема внутрь.
Пероральный прием препаратов Fe:
повышает уровень гемоглобина только на 2–4 дня позже, чем при парентеральном введении;
в отличие от парентерального крайне редко приводит к серьезным побочным эффектам;
даже при неправильно установленном диагнозе не приводит к развитию гемосидероза.
Парентеральное введение препаратов железа показано лишь по специальным показаниям (синдром нарушенного кишечного всасывания, состояние после обширной резекции тонкого кишечника).
Требования к препаратам железа для приема внутрь, применяемым в детской практике:
хорошая биодоступность;
высокая безопасность;
приятные органолептические свойства;
различные лекарственные формы, удобные для пациентов всех возрастов;
комплаентность.
Детям раннего возраста предпочтительно назначение железосодержащих препаратов, выпускаемых в форме капель, сиропа. Хороши для детей этой возрастной группы Актиферрин (капли, сироп), Мальтофер (капли, сироп), Феррум Лек (сироп), Гемофер (капли) (табл. 5).

Для детей подросткового возраста лучше всего назначать препараты железа типа Феррум Лека (жевательные таблетки) или Тардиферона и Ферроградумента, которые медленно всасываются, обеспечивая пролонгированную и равномерную абсорбцию медикаментозного железа в кишечнике. Как правило, эти препараты хорошо переносятся больными.
После выбора железосодержащего препарата и способа его применения необходимо определить ежедневную суточную дозу лекарственного средства и кратность приема (табл. 6).

Рекомендуемые дозы двухвалентного железа рассчитаны на основе данных, свидетельствующих, что лишь 10–15% поступающего в организм железа всасывается.
Препараты железа (III) – ГПК используются у детей с ЖДА разного возраста в терапевтической дозе 5 мг/кг/сут.
При латентном дефиците железа все препараты железа используются в половинной терапевтической дозе.
Профилактические дозы препаратов железа:
для детей до 3 лет – 1–1,5 мг/кг/сут;
для детей старше 3 лет – 1/2 суточной терапевтической дозы.
Известно, что лечение солевыми препаратами может сопровождаться расстройствами стула, в связи с чем терапию препаратами двухвалентного железа необходимо начинать с дозы, равной 1/4–1/2 от расчетной терапевтической, с последующим постепенным достижением полной дозы в течение 7–14 дней. Темп «постепенного наращивания» дозы до терапевтической зависит как от выраженности дефицита железа, так и от состояния желудочно-кишечного тракта и индивидуальной переносимости препарата. Данная методика позволяет подобрать индивидуальную дозу в зависимости от переносимости и снизить риск побочных эффектов терапии солевыми препаратами железа.
Хорошо известно, что солевые препараты железа в просвете кишечника взаимодействуют с компонентами пищи, лекарствами, затрудняя абсорбцию железа. В связи с этим солевые препараты железа рекомендуют назначать за 1 ч до приема пищи. Назначение препаратов Fe (III) – ГПК не требует применения методики постепенного наращивания дозы. Препараты этой группы назначаются сразу в полной дозе вне зависимости от еды, поскольку пища не влияет на их абсорбцию.
Терапевтический эффект при пероральном приеме железа появляется постепенно. Вначале отмечается клиническое улучшение и лишь спустя некоторое время происходит нормализация гемоглобина. Первым положительным клиническим признаком, появляющимся при лечении препаратами железа, является исчезновение или уменьшение мышечной слабости. Последнее обусловлено тем, что железо входит в состав ферментов, участвующих в сокращении миофибрилл. На 10–12 день от начала лечения повышается содержание ретикулоцитов в периферической крови. Повышение гемоглобина может быть постепенным либо скачкообразным. Чаще всего начало подъема уровня гемоглобина происходит на 3–4 нед от начала терапии. Как показали многочисленные исследования, исчезновение клинических проявлений заболевания отмечается к 1–2 мес терапии, а исчезновение тканевой сидеропении наступает на 3–6 мес лечения. Суточная доза элементарного железа после нормализации уровня гемоглобина должна соответствовать 1/2 терапевтической дозы (табл. 7). Раннее прекращение лечения препаратами железа, как правило, приводит к рецидивам ЖДА. Длительность основного курса лечения препаратами железа составляет 6–10 нед в зависимости от степени тяжести выявленной железодефицитной анемии. Продолжительность профилактического курса препаратами железа с целью создания депо железа в организме составляет:

при анемии легкой степени – 1,5–2 мес;
при анемии средней степени – 2 мес;
при анемии тяжелой степени – 2,5–3 мес.
Критерии эффективности лечения препаратами железа:
появление ретикулоцитарного криза на 7–10 день лечения;
прирост уровня гемоглобина – 10 г/л в неделю;
полная нормализация клинико-лабораторных показателей к концу курса лечения.
Рефрактерность железодефицитной анемии обусловлена неадекватностью назначаемой терапии или анемией, не связанной с дефицитом железа!
Парентеральные препараты при лечении железодефицитной анемии должны использоваться только по строгим показаниям!
Показания к парентеральному введению препаратов железа:
Синдром укороченной тонкой кишки.
Синдром нарушенного всасывания.
Неспецифический язвенный колит.
Хронический энтероколит.
Парентеральные препараты лучше использовать не ежедневно, а с интервалом в 1–2 дня. При этом в первые 1–3 введения можно использовать половинную дозу.
Учитывая длительность проведения ферротерапии, выбор препаратов для коррекции ЖДА у детей раннего возраста требует особого внимания. Как солевые препараты железа, так и препараты Fe(III) — ГПК полимальтозного комплекса являются эффективными при терапии ЖДС. Побочные и нежелательные явления при пероральной ферротерапии ЖДА в основном связаны с превышением рекомендуемых доз и чаще проявляются диспепсией. Побочные реакции и нежелательные эффекты, которые могут развиться при ферротерапии у детей, суммированы в таблице 8.

Парентеральные препараты железа должны применяться только строго по специальным показаниям.
Переливания крови или эритроцитарной массы при ЖДА проводятся крайне редко и строго по жизненным показаниям. Критериями для гемотрансфузии является снижение гемоглобина ниже критического уровня в сочетании с признаками нарушения центральной гемодинамики, геморрагического шока, анемической прекомы, гипоксического синдрома (табл. 9). Гемотрансфузия может проводиться и при значениях гемоглобина и гематокрита выше критических, если имеет место массивная острая кровопотеря.

Эффект от гемотрансфузий при ЖДА кратковременный. Отмечено отрицательное влияние гемотрансфузий на эритропоэз. К тому же сохраняется высокий риск трансфузионного инфицирования реципиента. При наличии витальных показаний для заместительной гемотрансфузии предпочтение отдается эритроцитарной массе или отмытым эритроцитам из расчета 10–15 мл/кг массы. Детям старшего возраста обычно переливают от 150 до 250 мл. Цельную кровь в последние годы в педиатрической практике не используют.
Профилактика ЖДА у детей включает:
1. Антенатальную профилактику:
всем женщинам во второй половине беременности целесообразно профилактическое назначение пероральных ферропрепаратов или поливитаминов, обогащенных железом.
2. Постнатальную профилактику:
естественное вскармливание со своевременным введением прикорма (мясное пюре с 6–7 мес);
детям, находящимся на искусственном вскармливании, с 2–3 мес введение смесей, обогащенных железом (12 мг/л);
недоношенным, детям от многоплодной беременности, родившимся с крупной массой тела, имеющим бурные темпы массо-ростовой прибавки, с 3-го мес до конца первого полугодия рекомендуется профилактический прием препаратов железа в дозе, равной 1/3–1/2 суточной терапевтической дозы элементарного железа (1,0–1,5 мг/кг/сут).
Вакцинация детей с ЖДА проводится после нормализации уровня гемоглобина.
Снятие с диспансерного учета осуществляется через год.
И. Н. Захарова, доктор медицинских наук, профессор
Н. А. Коровина, доктор медицинских наук, профессор
А. Л. Заплатников, доктор медицинских наук, профессор
Н. Е. Малова, кандидат медицинских наук
РМАПО, Москва
