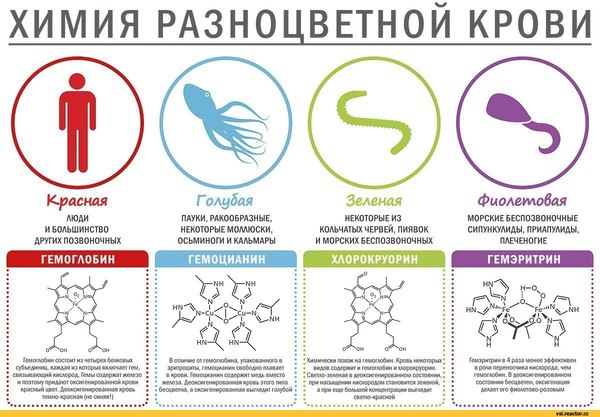
Ионы какого металла входят в состав гемоглобина
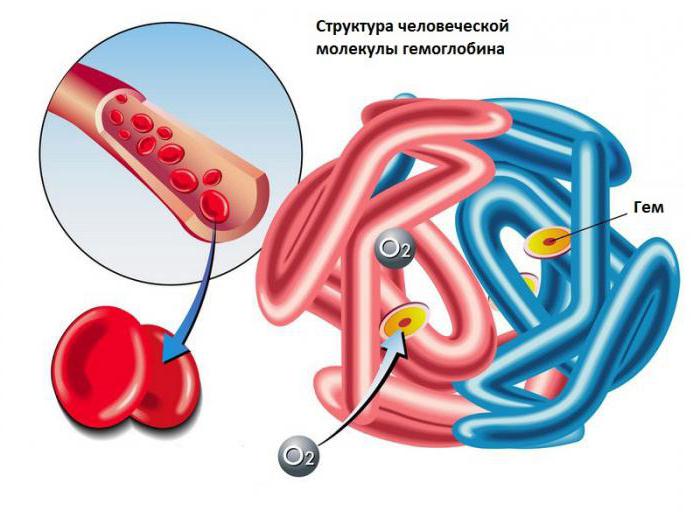
Молекула гемоглобина: 4 субъединицы окрашены в разные цвета
Структура гемоглобина человека. Железосодержащие гем-группы показаны зелёным. Красным и синим показаны альфа- и бета- субъединицы.
Гемоглоби́н (от др.-греч. αἷμα «кровь» + лат. globus «шар») (Hb или Hgb) — сложный железосодержащий белок животных, обладающих кровообращением, способный обратимо связываться с кислородом, обеспечивая его перенос в ткани. У позвоночных животных содержится в эритроцитах, у большинства беспозвоночных растворён в плазме крови (эритрокруорин) и может присутствовать в других тканях[1]. Молекулярная масса гемоглобина человека — около 66,8 кДа. Молекула гемоглобина может нести до четырёх молекул кислорода. Один грамм гемоглобина может переносить до 1.34 мл. O2
Гемоглобин появился более чем 400 миллионов лет назад у последнего общего предка человека и акул в результате 2 мутаций, приведших к формированию четырёхкомпонентного комплекса гемоглобина, сродство которого к кислороду достаточно для связывания кислорода в насыщенной им среде, но недостаточно, чтобы удерживать его в других тканях организма.[2][3]
Большой вклад в исследование структуры и функционирования гемоглобина внёс Макс Фердинанд Перуц, получивший за это в 1962 году Нобелевскую премию[4].
Нормальным содержанием гемоглобина в крови человека считается: у мужчин — 130—160 г/л (нижний предел — 120, верхний предел — 180 г/л), у женщин — 120—160 г/л; у детей нормальный уровень гемоглобина зависит от возраста и подвержен значительным колебаниям. Так, у детей через 1—3 дня после рождения нормальный уровень гемоглобина максимален и составляет 145—225 г/л, а к 3—6 месяцам снижается до минимального уровня — 95—135 г/л, затем с 1 года до 18 лет отмечается постепенное увеличение нормального уровня гемоглобина в крови[5].
Во время беременности в организме женщины происходит задержка и накопление жидкости, что является причиной гемодилюции — физиологического разведения крови. В результате наблюдается относительное снижение концентрации гемоглобина (при беременности уровень гемоглобина в норме составляет 110—155 г/л). Кроме этого, в связи с внутриутробным ростом ребёнка происходит быстрое расходование запасов железа и фолиевой кислоты. Если до беременности у женщины был дефицит этих веществ, проблемы, связанные со снижением гемоглобина, могут возникнуть уже на ранних сроках беременности[6].
Главные функции гемоглобина: перенос кислорода и буферная функция. У человека в капиллярах лёгких в условиях избытка кислорода последний соединяется с гемоглобином. Потоком крови эритроциты, содержащие молекулы гемоглобина со связанным кислородом, доставляются к органам и тканям, где кислорода мало; здесь необходимый для протекания окислительных процессов кислород освобождается от связи с гемоглобином. Кроме того, гемоглобин способен связывать в тканях небольшое количество диоксида углерода (CO2) и освобождать его в лёгких.
Монооксид углерода (CO) связывается с гемоглобином крови намного сильнее (в 250 раз[7]), чем кислород, образуя карбоксигемоглобин (HbCO). Впрочем, монооксид углерода может быть частично вытеснен из гема при повышении парциального давления кислорода в лёгких. Некоторые процессы приводят к окислению иона железа в гемоглобине до степени окисления +3. В результате образуется форма гемоглобина, известная как метгемоглобин (HbOH) (metHb, от «мета-» и «гемоглобин», иначе гемиглобин или ферригемоглобин, см. Метгемоглобинемия). В обоих случаях блокируются процессы транспортировки кислорода.
Строение[править | править код]
Гемоглобин является сложным белком класса гемопротеинов, то есть в качестве простетической группы здесь выступает гем — порфириновое ядро, содержащее железо. Гемоглобин человека является тетрамером, то есть состоит из 4 протомеров. У взрослого человека они представлены полипептидными цепями α1, α2, β1 и β2. Субъединицы соединены друг с другом по принципу изологического тетраэдра. Основной вклад во взаимодействие субъединиц вносят гидрофобные взаимодействия. И α-, и β-цепи относятся к α-спиральному структурному классу, так как содержат исключительно α-спирали. Каждая цепь содержит восемь спиральных участков, обозначаемых буквами от A до H (от N-конца к C-концу).
Гем представляет собой комплекс протопорфирина IX, относящегося к классу порфириновых соединений, с атомом железа(II). Этот кофактор нековалентно связан с гидрофобной впадиной молекул гемоглобина и миоглобина.
Железо(II) характеризуется октаэдрической координацией, то есть связывается с шестью лигандами. Четыре из них представлены атомами азота порфиринового кольца, лежащими в одной плоскости. Две другие координационные позиции лежат на оси, перпендикулярной плоскости порфирина. Одна из них занята азотом остатка гистидина в 93-м положении полипептидной цепи (участок F). Связываемая гемоглобином молекула кислорода координируется к железу с обратной стороны и оказывается заключённой между атомом железа и азотом ещё одного остатка гистидина, располагающегося в 64-м положении цепи (участок E).
Всего в гемоглобине человека четыре участка связывания кислорода (по одному гему на каждую субъединицу), то есть одновременно может связываться четыре молекулы. Гемоглобин в лёгких при высоком парциальном давлении кислорода соединяется с ним, образуя оксигемоглобин. При этом кислород соединяется с гемом, присоединяясь к железу гема на 6-ю координационную связь. На эту же связь присоединяется и монооксид углерода, вступая с кислородом в «конкурентную борьбу» за связь с гемоглобином, образуя карбоксигемоглобин.
Связь гемоглобина с монооксидом углерода более прочная, чем с кислородом. Поэтому часть гемоглобина, образующая комплекс с монооксидом углерода, не участвует в транспорте кислорода. В норме у человека образуется 1,2 % карбоксигемоглобина. Повышение его уровня характерно для гемолитических процессов, в связи с этим уровень карбоксигемоглобина является показателем гемолиза.
Физиология[править | править код]
Изменение состояний окси- и дезоксигемоглобина
В отличие от миоглобина гемоглобин имеет четвертичную структуру, которая придаёт ему способность регулировать присоединение и отщепление кислорода и характерную кооперативность: после присоединения первой молекулы кислорода связывание последующих облегчается. Структура может находиться в двух устойчивых состояниях (конформациях): оксигемоглобин (содержит 4 молекулы кислорода; напряжённая конформация) и дезоксигемоглобин (кислорода не содержит; расслабленная конформация).
Устойчивое состояние структуры дезоксигемоглобина усложняет присоединение к нему кислорода. Поэтому для начала реакции необходимо достаточное парциальное давление кислорода, что возможно в альвеолах лёгких. Изменения в одной из 4-х субъединиц влияет на оставшиеся, и после присоединения первой молекулы кислорода связывание последующих облегчается.
Отдав кислород тканям, гемоглобин присоединяет к себе ионы водорода и углекислый газ, перенося их в лёгкие[8].
Гемоглобин является одним из основных белков, которыми питаются малярийные плазмодии — возбудители малярии, и в эндемичных по малярии районах земного шара весьма распространены наследственные аномалии строения гемоглобина, затрудняющие малярийным плазмодиям питание этим белком и проникновение в эритроцит. В частности, к таким имеющим эволюционно-приспособительное значение мутациям относится аномалия гемоглобина, приводящая к серповидноклеточной анемии. Однако, к несчастью, эти аномалии (как и аномалии строения гемоглобина, не имеющие явно приспособительного значения) сопровождаются нарушением кислород-транспортирующей функции гемоглобина, снижением устойчивости эритроцитов к разрушению, анемией и другими негативными последствиями. Аномалии строения гемоглобина называются гемоглобинопатиями.
Гемоглобин высокотоксичен при попадании значительного его количества из эритроцитов в плазму крови (что происходит при массивном внутрисосудистом гемолизе, геморрагическом шоке, гемолитических анемиях, переливании несовместимой крови и других патологических состояниях). Токсичность гемоглобина, находящегося вне эритроцитов, в свободном состоянии в плазме крови, проявляется тканевой гипоксией — ухудшением кислородного снабжения тканей, перегрузкой организма продуктами разрушения гемоглобина — железом, билирубином, порфиринами с развитием желтухи или острой порфирии, закупоркой почечных канальцев крупными молекулами гемоглобина с развитием некроза почечных канальцев и острой почечной недостаточности.
Ввиду высокой токсичности свободного гемоглобина в организме существуют специальные системы для его связывания и обезвреживания. В частности, одним из компонентов системы обезвреживания гемоглобина является особый плазменный белок гаптоглобин, специфически связывающий свободный глобин и глобин в составе гемоглобина. Комплекс гаптоглобина и глобина (или гемоглобина) затем захватывается селезёнкой и макрофагами тканевой ретикуло-эндотелиальной системы и обезвреживается.
Другой частью гемоглобинообезвреживающей системы является белок гемопексин[en], специфически связывающий свободный гем и гем в составе гемоглобина. Комплекс гема (или гемоглобина) и гемопексина затем захватывается печенью, гем отщепляется и используется для синтеза билирубина и других жёлчных пигментов, или выпускается в рециркуляцию в комплексе с трансферринами для повторного использования костным мозгом в процессе эритропоэза.
Экспрессия генов гемоглобина до и после рождения.
Также указаны типы клеток и органы, в которых происходит экспрессия гена (данные по Wood W. G., (1976). Br. Med. Bull. 32, 282.).[9]
Гемоглобин при заболеваниях крови[править | править код]
Дефицит гемоглобина может быть вызван, во-первых, уменьшением количества молекул самого гемоглобина (см. анемия), во-вторых, из-за уменьшенной способности каждой молекулы связать кислород при том же самом парциальном давлении кислорода.
Гипоксемия — это уменьшение парциального давления кислорода в крови, её следует отличать от дефицита гемоглобина. Хотя и гипоксемия, и дефицит гемоглобина являются причинами гипоксии.
Если дефицит кислорода в организме в общем называют гипоксией, то местные нарушения кислородоснабжения называют ишемией.
Прочие причины низкого гемоглобина разнообразны: кровопотеря, пищевой дефицит, болезни костного мозга, химиотерапия, отказ почек, атипичный гемоглобин.
Повышенное содержание гемоглобина в крови связано с увеличением количества или размеров эритроцитов, что наблюдается также при истинной полицитемии. Это повышение может быть вызвано: врождённой болезнью сердца, лёгочным фиброзом, слишком большим количеством эритропоэтина.
См. также[править | править код]
- Гемоглобин А
- Гемоглобин С (мутантная форма)
- Эмбриональный Гемоглобин (эмбриональный)
- Гемоглобин S (мутантная форма)
- Гемоглобин F (фетальный)
- Кобоглобин
- Нейроглобин
- Анемия
- Порфирия
- Талассемия
- Эффект Вериго — Бора
Примечания[править | править код]
- ↑ Haemoglobins of invertebrate tissues. Nerve haemoglobins of Aphrodite, Aplysia and Halosydna
- ↑ Ученые выяснили происхождение гемоглобина. РИА Новостей, 20.05.2020, 18:59
- ↑ Michael Berenbrink. Evolution of a molecular machine/Nature, NEWS AND VIEWS, 20 MAY 2020
- ↑ Лауреаты нобелевской премии. Макс Перуц.
- ↑ Назаренко Г. И., Кишкун А. А. Клиническая оценка результатов лабораторных исследований. — 2005.
- ↑ Общий анализ крови и беременность Архивная копия от 10 марта 2014 на Wayback Machine
- ↑ Hall, John E. Guyton and Hall textbook of medical physiology (англ.). — 12th ed.. — Philadelphia, Pa.: Saunders/Elsevier, 2010. — P. 1120. — ISBN 978-1416045748.
- ↑ Степанов В. М. Структура и функции белков : Учебник. — М. : Высшая школа, 1996. — С. 167—175. — 335 с. — 5000 экз. — ISBN 5-06-002573-X.
- ↑ Айала Ф., . Современная генетика: В 3-х т = Modern Genetics / Пер. А. Г. Имашевой, А. Л. Остермана, . Под ред. Е. В. Ананьева. — М.: Мир, 1987. — Т. 2. — 368 с. — 15 000 экз. — ISBN 5-03-000495-5.
Литература[править | править код]
- Mathews, CK; KE van Holde & KG Ahern (2000), Biochemistry (3rd ed.), Addison Wesley Longman, ISBN 0-8053-3066-6
- Levitt, M & C Chothia (1976), “Structural patterns in globular proteins”, Nature
Ссылки[править | править код]
- Eshaghian, S; Horwich, TB; Fonarow, GC (2006). “An unexpected inverse relationship between HbA1c levels and mortality in patients with diabetes and advanced systolic heart failure”. Am Heart J. 151 (1): 91.e1—91.e6. DOI:10.1016/j.ahj.2005.10.008. PMID 16368297.
- Kneipp J, Balakrishnan G, Chen R, Shen TJ, Sahu SC, Ho NT, Giovannelli JL, Simplaceanu V, Ho C, Spiro T (2005). “Dynamics of allostery in hemoglobin: roles of the penultimate tyrosine H bonds”. J Mol Biol. 356 (2): 335—53. DOI:10.1016/j.jmb.2005.11.006. PMID 16368110.
- Hardison, Ross C. (2012). “Evolution of Hemoglobin and Its Genes”. Cold Spring Harbor Perspectives in Medicine. 2 (12): a011627. DOI:10.1101/cshperspect.a011627. ISSN 2157-1422. PMC 3543078. PMID 23209182.
Какой микроэлемент входит в состав гемоглобина и эритроцитов? Кровь является самой важной субстанцией организма человека. Она обеспечивает питание, а кроме того, межклеточный обмен.
Гемоглобин представляет собой вещество белковой природы, которое входит в состав кровяных телец, которые отвечают за так называемую транспортировку кислорода между клетками различных органов человека и легкими. В том случае, если гемоглобин в крови человека понижен, то кислород к тканям поступает весьма слабо.
Нарушение столь важного процесса может очень плохо отразиться на общем самочувствии человека. Но также негативно на здоровье сказывается и его повышенный уровень.
Элемент, входящий в состав гемоглобина, интересует многих.
Отклонения содержания гемоглобина в крови
Дефицит данного вещества способен вызывать упадок сил наряду с общей слабостью организма, снижением трудоспособности и нарушением памяти. В качестве сопутствующих симптомов человек может наблюдать у себя частые обморочные состояния либо следующие признаки:
- Высыхание слизистых.
- Высыхание кожных покровов.
- Ослабление ногтей и волос.
Ионы железа
Ионы железа, которые входят в состав гемоглобина, занимаются доставкой кислорода к клеткам всех тканей. Поэтому нехватка данных элементов вызывает так называемую железодефицитную анемию.
Подобные патологические состояния способны вызвать у людей не только снижение уровня железа в гемоглобине. Вероятна обильная потеря этого элемента во время месячных, в процессе родов. Основным источником этого элемента в продуктах выступает животный белок. Собственно, его недостаток и вызывает плохое самочувствие.
Что касается высокого показателя гемоглобина, то это свидетельствует о повышенном уровне сахара, об онкологических процессах либо всевозможных нарушениях работы сердца и так далее. О данном состоянии может свидетельствовать и дефицит фолиевой кислоты, витамина В12. При повышенных показателях гемоглобина кровь обладает высокой вязкостью и густой консистенцией. Такое явление может послужить причиной образования тромбов в сосудах, что гарантированно приводит к инфарктам.

Таким образом, показатель гемоглобина в составе крови обязательно должен находиться в норме. Для того чтобы предупредить столь опасные патологии в организме, как анемия, доктора всегда назначают сдачу крови на гемоглобин.
О чем говорит анализ крови?
Без выполнения общего анализа крови нельзя произвести ни одного диагностирования. Расшифровка составляющих компонентов имеет несколько этапов, позволяющих определить степень опасности заболевания, динамику его развития в рамках проведенного лечения.
Главным в анализе служит значение наличия эритроцитов наряду с лейкоцитами, уровнем гемоглобина, лейкоцитарной формулой, скоростью оседания эритроцитов и гематокритом. Какой микроэлемент входит в состав гемоглобина? Это железо.
Как уже было отмечено, пониженный уровень может послужить причиной возникновения анемии. Показатель эритроцитов сообщает о присутствии красных кровяных телец в клетках, которые в своем составе содержат гемоглобин, играя при этом роль некоего транспорта для кислорода, который нужен тканям. Эритроциты выполняют защитную роль, так как принимают участие в иммунных и аутоиммунных процессах, абсорбируя токсины.
Они, помимо всего прочего, отвечают и за доставку аминокислот от пищеварительных органов к тканям человеческого организма. А вот какие ионы входят в состав гемоглобина?
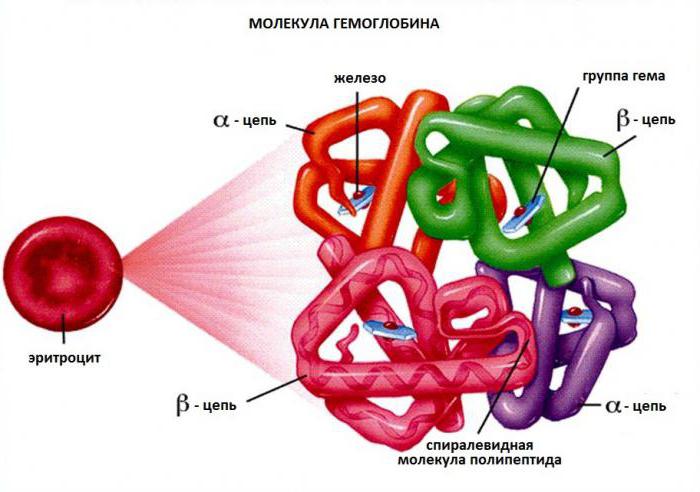
В расшифровке анализа присутствует такой показатель как гематокрит, демонстрирующий соотношение объема эритроцитов к плазме. Собственно, этот показатель и помогает определить, имеются нарушения процесса соединения гемоглобина или нет. Данное значение фиксируют в процентном соотношении. Нормальным показателем у женщин до тридцати лет является 43,5 %, а у мужчин – 49 %. У женщин в возрасте от 50 до 65 лет это значение доходит до 45 %, а у мужчин – до 49 %.
Все приведенные значения при общей совокупности дают возможность доктору своевременно определить начало развития той или иной патологии, осуществить своевременное лечение для пациента.
Что входит в состав гемоглобина?
Итак, гемоглобин служит главным компонентом эритроцитов. В его состав входит «гем», что представляет собой комплексное соединение железа, и «глобин». Непосредственно в крови данный белок присутствует в форме соединения гемоглобина с кислородом.
Также существует форма другого вида гемоглобина, который называется оксигемоглобин. Этот тип остается без кислорода и находится в артериальной крови. Что касается венозной крови, то в ней присутствуют обе представленные формы. Какой микроэлемент входит в состав гемоглобина и эритроцитов?
Гематокрит
Важную роль в рамках диагностирования анемических патологий играет определение значения концентрации гемоглобина, общей величины гематокрита. Напомним, что этот элемент является объемом красных клеток, содержащихся в крови. Таким образом, анемию, как правило, диагностируют при следующих показателях:
Среди мужчин, при факте снижения концентрации гемоглобина менее 140 грамм на литр, а показатель гематокрита ниже 42 %.
Среди женщин, при снижении меньше 120 грамм на литр и 37 % гематокрита.
В том случае, если была диагностирована анемия, концентрация данного вещества, что входит в состав гемоглобина, может колебаться. Это зависит от формы и общей степени ее выраженности.
Анемия, которая вызывается дефицитом железа в крови, сообщает об умеренном снижении гемоглобина, то есть не больше, чем 114 грамм на литр. На фоне сильных кровопотерь данный показатель может приобретать значение, равное 85 граммам на литр. Минимальным показателем этого вещества в крови у живых людей является 10 грамм на литр.
В состав гемоглобина входят молекулы белка.

Заключение
Для того чтобы повысить уровень гемоглобина и предотвратить появление анемии необходимо обратить внимание на питание, которое обязательно должно являться сбалансированным и полноценным. В особенности следует остановиться на продуктах, которые содержат железо.
Самые богатые на это вещество: говядина, куриные яйца, курага и грецкие орехи. В рацион также следует включить и кисломолочные изделия. Так, мы выяснили, что входит в состав гемоглобина.
 æèâûõ îðãàíèçìàõ ìåäü âïåðâûå áûëà îáíàðóæåíà â 1808 ãîäó èçâåñòíûì ôðàíöóçñêèì õèìèêîì Ëóè Âîêëåíîì âûäàþùèìñÿ àíàëèòèêîì ñâîåãî âðåìåíè. Îí ïðîâåë ìíîæåñòâî èññëåäîâàíèé ðàçëè÷íûõ âåùåñòâ è ñ÷èòàåòñÿ îäíèì èç îñíîâîïîëîæíèêîâ õèìè÷åñêîãî àíàëèçà. Ïîçæå, â 1834 ãîäó, áûëî óñòàíîâëåíî ñîäåðæàíèå ìåäè ó ðÿäà áåñïîçâîíî÷íûõ æèâîòíûõ. Òî÷íîå ìåñòîíàõîæäåíèå åå ãåìîëèìôà, êîòîðàÿ èìååò ó íèõ ãîëóáóþ îêðàñêó. Ýòî îòêðûòèå ïðèíàäëåæèò èòàëüÿíñêîìó èññëåäîâàòåëþ Á. Áèçèî. Ãîëóáîé, à èíîãäà äàæå ñèíèé öâåò êðîâè ýòèõ æèâîòíûõ ïðèäàåòñÿ èîíîì ìåäè. Âñïîìíèì: ìíîãèå ñîåäèíåíèÿ ýòîãî ýëåìåíòà èìåþò ãîëóáîé öâåò, íàïðèìåð ìåäíûé êóïîðîñ.
Åùå â 1913 ãîäó ó÷åíèê Â. È. Âåðíàäñêîãî èçâåñòíûé ðóññêèé ãåîëîã è áèîãåîõèìèê ß. Â. Ñàìîéëîâ âûñêàçàë èäåþ îá ýâîëþöèè íå òîëüêî ñêåëåòà îðãàíèçìîâ, íî è êðîâè, ãäå ôóíêöèþ æåëåçà íà ðàçíûõ ñòàäèÿõ ðàçâèòèÿ ìîãëè âûïîëíÿòü òàêèå ìåòàëëû, êàê ìåäü èëè âàíàäèé.  ñàìîì äåëå, íå òîëüêî æåëåçî è ìåäü, íî è âàíàäèé, à òàêæå õðîì, ìàðãàíåö, êîáàëüò, íèêåëü, öèíê ïðèíàäëåæàò ê ýëåìåíòàì ïåðâîé ïåðåõîäíîé ãðóïïû ïåðèîäè÷åñêîé ñèñòåìû. Ýòî ñîñåäè ñî ñõîäíûìè ñâîéñòâàìè. Èìåííî ýòè ñâîéñòâà â òîé èëè èíîé ñòåïåíè è îïðåäåëÿþò ðîëü ïåðå÷èñëåííûõ ìåòàëëîâ â áèîëîãè÷åñêèõ ïðîöåññàõ. Òàê, èîí ìåäè ïî ñðàâíåíèþ ñ èîíàìè äðóãèõ ìåòàëëîâ àêòèâíåå ðåàãèðóåò ñ àìèíîêèñëîòàìè è áåëêàìè, îáðàçóÿ óñòîé÷èâûå êîìïëåêñû, êîòîðûå òðóäíî ðàçðóøèòü. È âîîáùå ìåäü îäèí èç ñàìûõ ðàçíîñòîðîííèõ êàòàëèçàòîðîâ.  ñî÷åòàíèè ñ áåëêàìè åå àêòèâèðóþùåå äåéñòâèå óñèëèâàåòñÿ è ïðèîáðåòàåò ñïåöèôè÷íîñòü, ÷òî òàê âàæíî äëÿ ôåðìåíòîâ. Íàêîíåö, ìåäü ëåãêî ïåðåõîäèò èç îäíîãî âàëåíòíîãî ñîñòîÿíèÿ â äðóãîå. Âñå ýòè ñâîéñòâà ÿâëÿþòñÿ îáùèìè ó ìåäè è ó æåëåçà. Íî åñòü îäíî âàæíîå îáñòîÿòåëüñòâî: ñîåäèíåíèÿ îäíîâàëåíòíîé ìåäè ëåãêî îêèñëÿþòñÿ êèñëîðîäîì âîçäóõà. Ïîýòîìó ìåäüñîäåðæàùèå ôåðìåíòû, êàòàëèçèðóþùèå â îðãàíèçìå ïðîöåññû îêèñëåíèÿ, ñàìè áûñòðî îêèñëÿþòñÿ, â ðåçóëüòàòå ÷åãî èõ ôóíêöèÿ âîññòàíàâëèâàåòñÿ.
Íå âûäåðæàâ ñîñòÿçàíèÿ ñ æåëåçîì â êà÷åñòâå ïåðåíîñ÷èêà êèñëîðîäà â êðîâè âûñøèõ æèâîòíûõ, ìåäü âñå æå îñòàëàñü íåçàìåíèìîé ïðè êðîâåòâîðåíèè. Åñëè ïðîñëåäèòü ïóòü ýòîãî ìåòàëëà â îðãàíèçìå, òî ìû óâèäèì, ÷òî ïðåæäå âñåãî îí ñâÿçûâàåòñÿ ñ áåëêîì ñûâîðîòêè êðîâè àëüáóìèíîì. Çàòåì ìåäü ïåðåõîäèò â ïå÷åíü è îòòóäà ñíîâà âîçâðàùàåòñÿ â ñûâîðîòêó íà ñåé ðàç â ñîñòàâå ãîëóáîãî áåëêà öåðóëîïëàçìèíà, èãðàþùåãî ãëàâíóþ ðîëü â åå õðàíåíèè è, òðàíñïîðòå ó âûñøèõ æèâîòíûõ.
Ñåðîå âåùåñòâî ìîçãà èç ïðàâîãî è ëåâîãî åãî ïîëóøàðèé ñîäåðæèò ðàçíîå êîëè÷åñòâî ìåäè. À âåäü èçâåñòíî, ÷òî ïîëóøàðèÿ ðàçâèòû íåîäèíàêîâî. Ó ÷åëîâåêà ëåâîå ïîëóøàðèå áîëåå àêòèâíî è ñîäåðæèò áîëüøå ðàçëè÷íûõ áèîëîãè÷åñêè àêòèâíûõ ìåòàëëîâ. Áîëüøå âñåãî ìåäè íàõîäèòñÿ â ïîäêîðêîâûõ îáðàçîâàíèÿõ, ñâÿçàííûõ ñ îñóùåñòâëåíèåì äâèãàòåëüíûõ ôóíêöèé. Óñòàíîâëåíî, ÷òî ïðàâîå ïîëóøàðèå ãîëîâíîãî ìîçãà óïðàâëÿåò ëåâîé ïîëîâèíîé íàøåãî òåëà, à ëåâîå ïðàâîé. Èìåííî ïðàâîå ïîëóøàðèå îòâåòñòâåííî çà êîîðäèíàöèþ è ïðîñòðàíñòâåííîå ïåðåìåùåíèå, ëåâîå æå êîíòðîëèðóåò ÿçûê è ðå÷ü. Íî áûâàåò, ÷òî ïðàâîå ïîëóøàðèå ðàçâèâàåòñÿ áûñòðåå ëåâîãî è ñòàíîâèòñÿ áîëåå àêòèâíûì, âûïîëíÿÿ â íåêîòîðîé ñòåïåíè ôóíêöèè è ëåâîãî ïîëóøàðèÿ.  ýòîì ñëó÷àå ÷åëîâåê ñòàíîâèòñÿ ëåâøîé. Ýòî ÿâëåíèå ñâÿçàíî ñ íåêîòîðîé ãîðìîíàëüíîé àíîìàëèåé.
Ñëîâîñî÷åòàíèå «ãîëóáàÿ êðîâü» ïîÿâèëîñü â ëåêñèêîíå íàñåëåíèÿ Åâðîïû îòíîñèòåëüíî íåäàâíî, â XVIII âåêå. Ñ÷èòàåòñÿ, ÷òî ýòî âûðàæåíèå âîçíèêëî â èñïàíñêîé ïðîâèíöèè Êàñòèëèÿ.
Èìåííî òàì óòîí÷åííûå ãðàíäû ãîðäî äåìîíñòðèðîâàëè áëåäíóþ êîæó ñ ïðîñòóïàþùèìè ñèíåâàòûìè ïðîæèëêàìè, ÿâëÿþùóþñÿ äîêàçàòåëüñòâîì òîãî, ÷òî èõ êðîâü íå îñêâåðíåíà ïðèìåñÿìè «ãðÿçíîé» ìàâðèòàíñêîé.
À ñóùåñòâóåò ëè îíà?
Äëÿ îáåñïå÷åíèÿ æèçíåäåÿòåëüíîñòè îðãàíèçì äîëæåí ïîòðåáëÿòü êèñëîðîä è âûäåëÿòü óãëåêèñëûé ãàç. Îäíà èç ãëàâíûõ ôóíêöèé êðîâè – ïåðåíîñ êèñëîðîäà è óãëåêèñëîãî ãàçà. Äëÿ ýòîãî «ïðèñïîñîáëåíû» ñïåöèàëüíûå ýëåìåíòû êðîâè – äûõàòåëüíûå ïèãìåíòû, êîòîðûå ñîäåðæàò èîíû ìåòàëëà, ñïîñîáíûå ñâÿçûâàòü ìîëåêóëû êèñëîðîäà è ïðè íåîáõîäèìîñòè îòäàâàòü èõ. Ó áîëüøèíñòâà æèâîòíûõ äûõàòåëüíûì ïèãìåíòîì êðîâè ÿâëÿåòñÿ ãåìîãëîáèí, â ñîñòàâ êîòîðîãî âõîäÿò èîíû äâóõâàëåíòíîãî æåëåçà. Èìåííî áëàãîäàðÿ ãåìîãëîáèíó íàøà êðîâü êðàñíàÿ.
Ãîëóáóþ êðîâü ó íåêîòîðûõ ïîçâîíî÷íûõ âïåðâûå îïèñàë çíàìåíèòûé ãîëëàíäñêèé íàòóðàëèñò ßí Ñâàììåðäàì åùå â 1669 ãîäó, îäíàêî îáúÿñíèòü ïðèðîäó ýòîãî ÿâëåíèÿ åìó íå óäàëîñü. Òîëüêî ÷åðåç äâà ñòîëåòèÿ, â 1878 ãîäó ôðàíöóçñêèé ó÷åíûé Ë. Ôðåäåðèêî èçó÷èë âåùåñòâî, êîòîðîå ïðèäàâàëî êðîâè ìîëëþñêîâ ãîëóáîé öâåò, è ïî àíàëîãèè ñ ãåìîãëîáèíîì íàçâàë åãî ãåìîöèàíèíîì, îò ñëîâ «òåìà» – «êðîâü» è «öèàíîñ» – «ñèíèé».
Ê ýòîìó âðåìåíè áûëî âûÿñíåíî, ÷òî íîñèòåëÿìè ãîëóáîé êðîâè ÿâëÿþòñÿ ïàóêè, ñêîðïèîíû è íåêîòîðûå ìîëëþñêè. Òàêîé öâåò ïðèäàâàëè íàõîäÿùèåñÿ â íåé èîíû ìåäè. Â ãåìîöèàíèíå îäíà ìîëåêóëà êèñëîðîäà ñâÿçûâàåòñÿ ñ äâóìÿ àòîìàìè ìåäè. Ïðè òàêèõ óñëîâèÿõ è ïðîèñõîäèò ïîñèíåíèå êðîâè.
Ñ òî÷êè çðåíèÿ ñíàáæåíèÿ îðãàíèçìà êèñëîðîäîì ãåìîöèàíèí çíà÷èòåëüíî óñòóïàåò ãåìîãëîáèíó, â êîòîðîì ïåðåíîñ îñóùåñòâëÿåòñÿ æåëåçîì. Ãåìîãëîáèí ñ ýòîé âàæíåéøåé äëÿ æèçíåäåÿòåëüíîñòè îðãàíèçìà çàäà÷åé ñïðàâëÿåòñÿ â ïÿòü ðàç ëó÷øå.
Íî è îò ìåäè, òåì íå ìåíåå, ïðèðîäà íå îòêàçàëàñü ïîëíîñòüþ, à äëÿ íåêîòîðûõ æèâîòíûõ è ðàñòåíèé ñäåëàëà åå ñîâåðøåííî íåçàìåíèìîé. È âîò ÷òî èíòåðåñíî. Îêàçûâàåòñÿ, ðîäñòâåííûå ãðóïïû æèâûõ îðãàíèçìîâ ìîãóò èìåòü ðàçíóþ êðîâü, à ïðîèçîøëè îíè âðîäå áû äðóã îò äðóãà. Íàïðèìåð, ó ìîëëþñêîâ êðîâü áûâàåò êðàñíîé, ãîëóáîé, êîðè÷íåâîé, ñ ðàçíûìè ìåòàëëàìè. Âûõîäèò, ÷òî ñîñòàâ êðîâè íå ñòîëü óæ âàæåí äëÿ æèâûõ îðãàíèçìîâ.
Íåîáû÷íûå ëþäè
 XX âåêå ïðîèñõîæäåíèåì ãîëóáîé êðîâè ñíîâà çàèíòåðåñîâàëèñü ó÷åíûå. Îíè âûäâèíóëè ãèïîòåçó, ÷òî ãîëóáàÿ êðîâü ñóùåñòâóåò, è ëþäè, â êðîâè êîòîðûõ âìåñòî æåëåçà ïðåîáëàäàåò ìåäü -èõ íàçâàëè «êèàíåòèêàìè», – æèëè íà íàøåé ïëàíåòå âñåãäà. Ïðàâäà, íà ñàìîì äåëå êðîâü ñ ïðåîáëàäàíèåì ìåäè öâåò èìååò íå ãîëóáîé, à ëèëîâûé ñ ñèíåâàòûì îòòåíêîì.

Èññëåäîâàòåëè íåïîçíàííîãî ñ÷èòàþò, ÷òî êèàíåòèêè áîëåå æèâó÷è è æèçíåñïîñîáíû ïî ñðàâíåíèþ ñ îáû÷íûìè ëþäüìè. Âî-ïåðâûõ, îíè ìåíåå ïîäâåðæåíû ðàçíîîáðàçíûì çàáîëåâàíèÿì êðîâè. Âî-âòîðûõ, èõ êðîâü îáëàäàåò ëó÷øåé ñâåðòûâàåìîñòüþ, è ëþáûå ðàíû, äàæå î÷åíü òÿæåëûå, íå ñîïðîâîæäàþòñÿ îáèëüíûì êðîâîòå÷åíèåì.
 êà÷åñòâå ïðèìåðà ïðèâîäÿòñÿ îïèñûâàåìûå â èñòîðè÷åñêîé õðîíèêå ñîáûòèÿ, êîãäà èçðàíåííûå ðûöàðè-êèàíåòèêè íå èñòåêàëè êðîâüþ è ïðîäîëæàëè óñïåøíî ñðàæàòüñÿ ñ ìàâðàìè.
Ïî ìíåíèþ íåêîòîðûõ èññëåäîâàòåëåé, êèàíåòèêè ïîÿâèëèñü íà Çåìëå íåñëó÷àéíî. Òàêèì îáðàçîì ïðèðîäà ïîäñòðàõîâûâàëàñü íà ñëó÷àé êàêîé-ëèáî ãëîáàëüíîé êàòàñòðîôû, êîòîðàÿ ìîæåò óíè÷òîæèòü áîëüøóþ ÷àñòü ÷åëîâå÷åñòâà. Îñòàâøèåñÿ â æèâûõ áîëåå æèçíåñòîéêèå ãîëóáîêðîâíûå ñìîãóò äàòü íà÷àëî åùå îäíîé, óæå íîâîé öèâèëèçàöèè.
Íî åñòü è äðóãîå îáúÿñíåíèå ïðîèñõîæäåíèÿ ãîëóáîêðîâíûõ ëþäåé: îíè ïîòîìêè ïðèøåëüöåâ èç äðóãèõ ïëàíåò.
Ïëàíåòà áîãîâ
Âñåëåííàÿ, â êîòîðîé ìû æèâåì, ìíîãîîáðàçíà. Äàæå â ïðåäåëàõ Ñîëíå÷íîé ñèñòåìû ïî ñïåêòðàëüíîìó èçëó÷åíèþ ïëàíåò óñòàíîâëåíî, ÷òî îíè îòëè÷àþòñÿ ïðåîáëàäàþùèìè â èõ ñòðîåíèè ýëåìåíòàìè. Ïîòîìó ìîæíî ïðåäïîëîæèòü, ÷òî ãäå-òî ðàñïðîñòðàíåííîãî íà íàøåé ïëàíåòå æåëåçà, èãðàþùåãî ñòîëü âàæíóþ ðîëü â æèçíåäåÿòåëüíîñòè âíóòðåííèõ îðãàíîâ îðãàíèçìîâ, î÷åíü ìàëî, à ìåäè – íàîáîðîò, î÷åíü ìíîãî. Åñòåñòâåííî, ÷òî òàì ýâîëþöèÿ æèâîòíîãî ìèðà ïîéäåò ïî ïóòè èñïîëüçîâàíèÿ äëÿ òðàíñïîðòà êèñëîðîäà íå æåëåçà, à ìåäè. È ëþäè è æèâîòíûå ýòîé ïëàíåòû áóäóò îáëàäàòü «àðèñòîêðàòè÷åñêîé», ãîëóáîé êðîâüþ.
Âåðñèÿ êðîâè áîãîâ íà îñíîâå ãåìîöèàíèíà (èëè äðóãèõ ñîåäèíåíèé ìåäè) äàåò òàêæå âîçìîæíîñòü ïî èíîìó âçãëÿíóòü íà íåêîòîðûå äàííûå ìèôîëîãèè. Âî-ïåðâûõ, ìåäü îáëàäàåò ñèëüíûìè àíòèáàêòåðèàëüíûìè ñâîéñòâàìè. Ìíîãèå íàðîäû ïðèïèñûâàþò ìåäè öåëåáíûå ñâîéñòâà. Íåïàëüöû, íàïðèìåð, ñ÷èòàþò ìåäü ñâÿùåííûì ìåòàëëîì, êîòîðûé ñïîñîáñòâóåò ñîñðåäîòî÷åíèþ ìûñëåé, óëó÷øàåò ïèùåâàðåíèå è ëå÷èò æåëóäî÷íî-êèøå÷íûå çàáîëåâàíèÿ (áîëüíûì äàþò ïèòü âîäó èç ñòàêàíà, â êîòîðîì ëåæàò íåñêîëüêî ìåäíûõ ìîíåò).  ñòàðèíó ìåäüþ ëå÷èëè ãëèñòíûå çàáîëåâàíèÿ, ýïèëåïñèþ, õîðåþ, ìàëîêðîâèå, ìåíèíãèò. Ìåäü ñïîñîáíà óáèâàòü ìèêðîáîâ; íàïðèìåð, ðàáîòíèêè ìåäíûõ çàâîäîâ íèêîãäà íå áîëåëè õîëåðîé.  òî æå âðåìÿ, íåäàâíî ó÷åíûå óíèâåðñèòåòà Øòàòà Îãàéî âûÿñíèëè, ÷òî ïåðåäîçèðîâêà æåëåçà â ïèùåâîé äèåòå ìîæåò ñïîñîáñòâîâàòü ñêëîííîñòè ê êèøå÷íûì èíôåêöèÿì. Òàêèì îáðàçîì, ïîâûøåííîå ñîäåðæàíèå ìåäè è ïîíèæåííîå ñîäåðæàíèå æåëåçà â ïèùå áîãîâ ïîçâîëÿëî èì óñèëèâàòü àíòèáàêòåðèàëüíûå ñâîéñòâà, êîòîðûìè èòàê îáëàäàëà èõ êðîâü áëàãîäàðÿ ìåäè â ñâîåì ñîñòàâå. Ýòî âïîëíå ìîãëî ïðåäîõðàíÿòü îò çåìíûõ èíôåêöèé è âíîñèòü ñâîþ ëåïòó â «áåññìåðòèå» áîãîâ. Ýôôåêòèâíà ìåäü, êàê îêàçûâàåòñÿ, è äëÿ ëå÷åíèÿ äðóãèõ áîëåçíåé.
Êóçíåöû, îïîÿñàííûå ìåäíîé ïðîâîëîêîé, íèêîãäà íå ñòðàäàëè ðàäèêóëèòàìè. Ïðè ðàäèêóëèòå êðàñíûå ìåäíûå ïÿòàêè óêðåïëÿþò ïëàñòûðåì íà êðåñòöå èëè êëàäóò íà ïîÿñíèöó è íàäåâàþò ïîÿñ èç ñîáà÷åé øåðñòè. Äëÿ ýòèõ æå öåëåé ìîæíî èñïîëüçîâàòü ìåäíûé êàíàòèê èëè àíòåííóþ ïðîâîëîêó, êîòîðóþ îáìàòûâàþò âîêðóã ñåáÿ. Äëÿ ëå÷åíèÿ áîëåé â ñóñòàâàõ, îòëîæåíèÿ ñîëåé èñïîëüçóþò ñòàðèííîå ñðåäñòâî â âèäå ìåäíîãî êîëüöà, êîòîðîå íîñÿò íà ïàëüöå íåñêîëüêî ìåñÿöåâ, áîëè ïðè ýòîì óìåíüøàþòñÿ, à ïîäâèæíîñòü â ñóñòàâàõ óâåëè÷èâàåòñÿ. Îñîáîé ïîïóëÿðíîñòüþ ïîëüçóþòñÿ ìåäíûå áðàñëåòû. Íî îíè ýôôåêòèâíû, åñëè ñîäåðæàíèå ìåäè â íèõ äîñòèãàåò 99%. Áðàñëåò íà ïðàâîé ðóêå ïîìîãàåò èçëå÷èòü èëè óñïîêîèòü ãîëîâíóþ áîëü, áåññîííèöó, ôèçè÷åñêóþ è óìñòâåííóþ óñòàëîñòü, ñàõàðíûé äèàáåò, èìïîòåíöèþ. Íà ëåâîé æå ðóêå íîøåíèå áðàñëåòà ðåêîìåíäóåòñÿ ïðè ïîâûøåííîì êðîâÿíîì äàâëåíèè, ãåìîððîå, ñåðäå÷íîé íåäîñòàòî÷íîñòè, òàõèêàðäèè. Âî âñåì ìèðå îöåíèëè áðàñëåòû èç ÷èñòîé ïåðóàíñêîé ìåäè
Âî-âòîðûõ, ãîëóáîé öâåò êðîâè ïðèäàåò ñîîòâåòñòâóþùèé îòòåíîê è öâåòó êîæè. È êàê òóò íå âñïîìíèòü «ãîëóáîêîæèõ» áîãîâ Èíäèè!..
Â-òðåòüèõ, â ïðèðîäå ìåäíûå ìåñòîðîæäåíèÿ ñîäåðæàò äîâîëüíî ìíîãî ñåðåáðà. Ñåðåáðî áóêâàëüíî ñîïðîâîæäàåò ìåäü ïî÷òè ïîâñþäó. Ýòî íàñòîëüêî ñèëüíî ïðîÿâëÿåòñÿ, ÷òî äàæå âåñîìàÿ ÷àñòü ñîâðåìåííîé äîáû÷è ñåðåáðà îñóùåñòâëÿåòñÿ ïîïóòíî ñ äîáû÷åé ìåäè, ïî÷òè ïÿòàÿ ÷àñòü âñåãî ñåðåáðà íûíå äîáûâàåòñÿ èç ìåäíûõ ìåñòîðîæäåíèé. Ñëåäîâàòåëüíî, íà ïëàíåòå áîãîâ òàêæå äîëæíî áûòü ìíîãî ñåðåáðà (õèìè÷åñêèå è ôèçè÷åñêèå çàêîíû âåäü äåéñòâóþò è òàì). Íî ñåðåáðî, òàêæå êàê è ìåäü, îáëàäàåò ñèëüíûì àíòèáàêòåðèàëüíûì äåéñòâèåì. «Ñåðåáðÿíàÿ âîäà» ýòî âçâåñü ìåëü÷àéøèõ ÷àñòèö ñåðåáðà â âîäå. Îíà îáðàçóåòñÿ ïðè õðàíåíèè âîäû â ñåðåáðÿíûõ ñîñóäàõ èëè ïðè êîíòàêòå âîäû ñ ñåðåáðÿíûìè èçäåëèÿìè. ×àñòèöû ñåðåáðà â òàêîé âîäå óæå ïðè êîíöåíòðàöèè 10-6 ìã/ë îáëàäàþò àíòèñåïòè÷åñêèìè ñâîéñòâàìè, ò. ê. ñåðåáðî ñïîñîáíî áëîêèðîâàòü ôåðìåíòíûå ñèñòåìû ìèêðîáîâ. Àëõèìèêè ñ÷èòàëè, ÷òî ñåðåáðî âõîäèò â ÷èñëî ñåìè ìåòàëëîâ, êîòîðûå îíè íàäåëÿëè öåëèòåëüíîé ñèëîé. Ñåðåáðî èñïîëüçîâàëè äëÿ ëå÷åíèÿ ýïèëåïñèè, íåâðàëãèè, õîëåðû, ãíîéíûõ ðàí.  âîäàõ ñâÿùåííîé èíäèéñêîé ðåêè Ãàíãà ïîâûøåíî ñîäåðæàíèå ñåðåáðà. Âûñîêèå äåçèíôèöèðóþùèå ñâîéñòâà ñåðåáðà ïðåâîñõîäÿò òàêèå æå ñâîéñòâà êàðáîëêè, ñóëåìû è õëîðíîé èçâåñòè. Ñïåöèàëüíî ïðèãîòîâëåííîå ñåðåáðî ïðèìåíÿåòñÿ ïðè ãîëîâíûõ áîëÿõ, ïîòåðå ãîëîñà ó ïåâöîâ, ñòðàõàõ, ãîëîâîêðóæåíèè. Åñëè íîñèòü ñåðåáðî íà ñåáå, òî ýòî óñïîêàèâàåò íåðâíóþ ñèñòåìó. À ýòî îïÿòü ðàáîòàåò íà «áåññìåðòèå» áîãîâ!.. Êðîìå òîãî, èçâåñòíî, ÷òî ïðè äëèòåëüíîì ââåäåíèè ñåðåáðà â îðãàíèçì êîæà ìîæåò ïðèîáðåñòè ãîëóáîé îòòåíîê, ÷òî â ñîâîêóïíîñòè ñ ãîëóáîé êðîâüþ áîãîâ íåèçáåæíî óñèëèâàåò ýôôåêò ãîëóáîé êîæè.
Çà âñå íàäî ïëàòèòü…
Îäíàêî ïðèëåòåâøèå íà Çåìëþ ñ «ìåäíîé» ïëàíåòû áîãè îñòàâèëè çåìëÿíàì íå òîëüêî íà÷àëüíûå íàâûêè â ìåòàëëóðãèè è ñòðåìëåíèå ê âåãåòàðèàíñòâó êàê ïóòü ê íðàâñòâåííîìó ñàìîñîâåðøåíñòâîâàíèþ.
Äëÿ äàëüíèõ ïîòîìêîâ áîãîâ, ó êîòîðûõ â òîé èëè èíîé ñòåïåíè ñîõðàíèëàñü ãîëóáàÿ êðîâü, ïîðîé õàðàêòåðåí èçáûòîê óãëåêèñëîãî ãàçà â êðîâè. Îí íå áûë ïîñòîÿííûì è ïðèâû÷íûì äëÿ èõ îðãàíèçìîâ.
Ýòî ïîäòâåðæäàåòñÿ ïîñòîÿííîé ïîòðåáíîñòüþ òàêèõ ëþäåé â ñïèðòíûõ íàïèòêàõ äëÿ êîìïåíñàöèè âðåäíîãî ãàçà. Ëåãåíäàðíóþ ñîìó, õìåëüíîé êâàñ è ìåä, ïèâî, äåâÿòü ñîðòîâ ñïèðòíûõ íàïèòêîâ, ñäåëàííûõ èç ìàèñà, áîãè äàëè àìåðèêàíñêèì èíäåéöàì è âíåñëè èõ â ñïèñîê æåðòâîïðèíîøåíèé! Áîãè äàæå íå ïðåíåáðåãàëè âèíîãðàäíûì âèíîì, â êîòîðîì ìíîãî æåëåçà. Âèäèìî, òðóäíà áûëà èõ æèçíü íà Çåìëå, ðàç ïîòðåáíîñòü â àëêîãîëå äëÿ êîìïåíñàöèè óãëåêèñëîãî ãàçà áûëà ñòîëü âåëèêà…
Âîîáùå, ñïèðòíûå íàïèòêè îáëàäàþò öåëûì ðÿäîì çàìå÷àòåëüíûõ ñâîéñòâ. Ýòè íàïèòêè ñîäåðæàò áîëüøîå êîëè÷åñòâî îðãàíè÷åñêèõ êèñëîò, áëàãîäàðÿ êîòîðûì îáëàäàþò è áóôåðíûìè ñâîéñòâàìè, íå ïîçâîëÿþùèìè ðÍ ñëèøêîì îïóñêàòüñÿ, è òåì ñàìûì ïðåïÿòñòâóþò óäåðæàíèþ â êðîâè èçëèøêîâ ÑÎ2. Íî îòìåòèì ñðàçó: ýòè ñâîéñòâà ïðèñóùè ïðåæäå âñåãî ñëàáîàëêîãîëüíûì íàïèòêàì! Êðåïêèå ñïèðòíûå íàïèòêè âåäóò ñåáÿ èíà÷å. È ìîæåò áûòü èìåííî ïîýòîìó ñ äðåâíåéøèõ âðåìåí èçâåñòíû ðåöåïòû ëèøü ñëàáîàëêîãîëüíûõ íàïèòêîâ, à êðåïêèå ñïèðòíûå íàïèòêè ïîÿâèëèñü ñðàâíèòåëüíî íåäàâíî (ëèøü â ïîñëåäíåå òûñÿ÷åëåòèå), – áîãàì íå íóæíà áûëà êðåïîñòü…
Îäíàêî âåðíåìñÿ ê äðóãèì ñâîéñòâàì àëêîãîëüíûõ íàïèòêîâ Ïüþùèå âèíî ëþäè ìåíüøå áîëåþò ãðèïïîì, ÷åì íåïüþùèå. Òàêèì îáðàçîì, âèíî îáåñïå÷èâàåò àíòèãðèïïîçíóþ ïðîôèëàêòèêó. Íàáëþäåíèÿ âðà÷åé ñâèäåòåëüñòâóþò, ÷òî ëþäè, ïüþùèå (óìåðåííî) âèíî, ðåæå íå âûõîäÿò íà ðàáîòó èç-çà èíôåêöèîííûõ çàáîëåâàíèé, ÷åì òå, êòî èñïîâåäóåò ïîëíîå àëêîãîëüíîå âîçäåðæàíèå. Ëàáîðàòîðíûå îïûòû ïîêàçàëè, ÷òî êðàñíîå âèíî, äàæå ðàçáàâëåííîå, óíè÷òîæàåò âèðóñ ïîëèîìèåëèòà. Óñòàíîâëåíî, ÷òî ñìåðòíîñòü îò êîðîíàðíîé íåäîñòàòî÷íîñòè îáðàòíî ïðîïîðöèîíàëüíà ïîòðåáëåíèþ àëêîãîëÿ. Íî ñðåäè àëêîãîëüíûõ íàïèòêîâ òîëüêî âèíî îáëàäàåò ÿðêî âûðàæåííûì ïðåâåíòèâíûì ýôôåêòîì â îòíîøåíèå ñåðäå÷íî-ñîñóäèñòûõ çàáîëåâàíèé. Èññëåäîâàíèÿ ïîêàçûâàþò, ÷òî ïðè óìåðåííîì óïîòðåáëåíèè âèíà, îò îäíîé äî ÷åòûðåõ ðþìîê â äåíü (1 ðþìêà âèíà åìêîñòüþ 100ìë è êðåïîñòüþ 12 ãðàäóñîâ ñîäåðæèò 10ã ñïèðòà), ñìåðòíîñòü âñëåäñòâèå êîðîíàðíîé íåäîñòàòî÷íîñòè ñíèæàåòñÿ äî 15-60% ïî ñðàâíåíèþ ñ ðèñêîì ïîäîáíîãî èñõîäà äëÿ ëþäåé, íå ïüþùèõ âèíà. Çàòî íå ïüþùèå âèíà ñîâñåì, ðàâíî êàê è ïüþùèå åãî ÷ðåçìåðíî (îò 60ã àëêîãîëÿ â äåíü è áîëåå), ïîäâåðãàþòñÿ î÷åíü âûñîêîìó ðèñêó ñìåðòåëüíîãî èñõîäà.
«Ñëèøêîì ãóñòàÿ» êðîâü, òî åñòü êðîâü ïîâûøåííîé âÿçêîñòè ñîçäàåò ñåðüåçíûå ïðåäïîñûëêè äëÿ îáðàçîâàíèÿ ñãóñòêîâ, ñïîñîáíûõ çàêóïîðèòü àðòåðèþ, èíà÷å ãîâîðÿ, ïðèâåñòè ê òðîìáîçó. Àëêîãîëü îáëàäàåò ñâîéñòâîì ðàçæèæàòü êðîâü. Ïîèñòèíå, ñîìà (ñïèðòíîé íàïèòîê áîãîâ) äàâàëà ëþäÿì çäîðîâüå, à áîãàì «áåññìåðòèå»!..