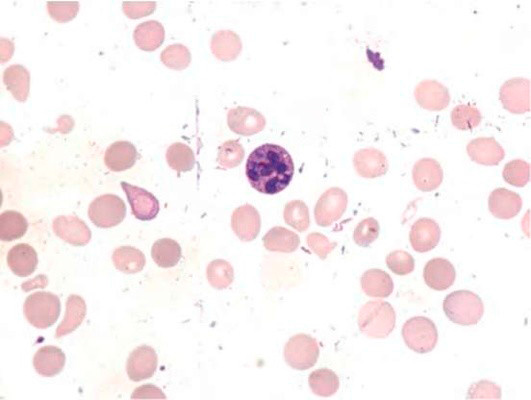
Картина крови при в 12 дефицитной анемии
В12-
и фолиеводефицитная анемия — анемия,
связанная с нарушением синтеза нуклеиновых
кислот и заменой эритробластического
типа кроветворения мегалобластическим
вследствие недостатка в организме
цианокобаламина (витамина В12) и фолиевой
кислоты (мегалобластная анемия).
Этиология. По
этиологии эти анемии могут быть
приобретенными и наследственными.
Причины, общие для В12- и фолиеводефицитной
анемий, следующие:
-недостаток
этих витаминов в пище (вскармливание
грудных детей козьим молоком, сухими
молочными смесями);
-нарушение
всасывания витаминов в тонкой кишке
(при резекции тощей кишки или поражении
ее опухолью, множественными дивертикулами,
при тропическом спру, дифиллоботриозе,
алкоголизме);
-повышенное
расходование витаминов при беременности
нарушение депонирования -витаминов при
диффузном поражении печени (гепатит,
цирроз). Кроме того, дефицит цианокобаламина
возникает в результате нарушения
образования внутреннего фактора Касла
— мукопротеида (транскоррина) — при
наследственном дефекте выработки его
клетками желез желудка, при поражении
слизистой оболочки желудка опухолью,
сифилитической гуммой, большими дозами
алкоголя, при резекции желудка, разрушений
мукопротеида аутоантителами.
Причиной
возникновения пернициозной анемии
(злокачественной, анемии Аддисона —
Бирмера), являющейся разновидностью
В12-дефицитной анемии, могут быть
генетически детерминированный дефицит
транскоррина (наследуется по
аутосомно-рецессивному типу) или же
аутоиммунный процесс, о чем свидетельствует
обнаружение у больных в сыворотке и
желудочном соке антител (IgG, IgA) к антигенам
цитоплазмы париетальных клеток, реже
— к внутреннему фактору.
Патогенез. При
дефиците цианокобаламина (его кофермента
— метилкобаламина) не происходит
превращения фолиевой кислоты в ее
коферментную форму — тетрагидрофолиевую
кислоту, без которой невозможен синтез
тимидинмонофосфата, входящего в состав
ДНК. Нарушается клеточное деление и
прежде всего страдают активно
размножающиеся клетки кроветворной
ткани. В костном мозге задерживается
размножение и созревание эритрокариоцитов.,
эритробластический тип кроветворения
заменяется мегалобластическим, возрастает
неэффективный эритропоэз, укорачивается
продолжительность жизни эритроцитов.
Вследствие нарушения кроветворения и
гемолиза эритроцитов развивается
анемия, при которой клетки патологической
регенерации и эритроциты с признаками
дегенерации появляются не только в
костном мозге, но и в крови. Изменение
лейко- и тромбоцитопоэза проявляется
уменьшением числа лейкоцитов и
тромбоцитов, выраженной атипией клеток.
Возникновение
атипичного митоза и гигантских клеток
эпителия пищевого канала приводит к
развитию воспалительно-атрофических
процессов в слизистой оболочке его
отделов (глоссит, стоматит, эзофагит,
ахилический гастрит, энтерит). Это
усугубляет первичное нарушение секреции
и всасывания внутреннего фактора и,
следовательно, усиливает дефицит
витаминов (порочный круг).
В
результате недостатка цианокобаламина
(его кофермент дезоксиаденозилкобаламин
участвует в образовании янтарной кислоты
из метилмалоновой кислоты) в организме
накапливается метилмалоновая кислота,
токсичная для нервных клеток, а в нервных
волокнах синтезируются жирные кислоты
с измененной структурой, что отражается
на образовании миелина и ведет к
повреждению аксона. Развивается
дегенерация задних и боковых столбов
спинного мозга (фуникулярный миелоз),
поражаются черепные и периферические
нервы с развитием многообразной
неврологической симптоматики.
Картина
крови. В12-
и фолиеводефицитные анемии — это анемии
с мегалобластическим типом кроветворения,
гиперхромные, макроцитарные. Содержание
эритроцитов и гемоглобина в крови при
этих анемиях может резко снижаться,
однако цветовой показатель выше 1
(1,4—1,8) в связи с наличием в крови больших
по объему мегалобластов и мегалоцитов,
насыщенных гемоглобином.
В
мазке крови появляются клетки
патологической регенерации костного
мозга — мегалоциты (интенсивно
окрашенные клетки, не имеющие центрального
просветления, несколько овальной формы)
и единичные мегалобласты (крупные
клетки размером с базофильной,
полихроматофильной или ацидофильной
цитоплазмой и нежносетчатым, обычно
эксцентрично расположенным ядром). В
крови встречается много дегенеративно
измененных эритроцитов: пойкилоцитоз,
анизоцитоз, гиперхромные мегало- и
макроциты, мегалоциты с включениями в
виде телец Жолли, колец Кебота, эритроциты
с базофильной зернистостью. Уменьшается
количество клеток физиологической
регенерации (ретикулоциты, полихроматофилы),
так как в костном мозге наблюдается
раздражение эритроцитарного ростка с
преобладанием мегалобластического
эритропоэза на фоне угнетения
эритробластического кроветворения.
Наблюдается лейко- и тромбоцитопения
с атипическими клетками .
Соседние файлы в предмете Патологическая физиология
- #
- #
- #
- #
- #
- #
- #
26.01.20181.49 Mб63Лечки кратко (Не Кокорева).wiz
- #
- #
- #
- #
Витамин-В12-дефицитная и фолиеводефицитная анемия.
Витамин-В12-дефицитная (пернициозная анемия или болезнь Аддисона-Бирмера)и фолиеводефицитная анемии относятся к мегалобластным анемиям – группе заболеваний, характеризующихся ослаблением синтеза ДНК, в результате чего нарушается деление всех быстропролиферирующих клеток (гемопоэтических клеток, клеток кожи, клеток ЖКТ, слизистых оболочек). Кроветворные клетки относятся к наиболее быстро размножающимся элементам, поэтому анемия, а также нередко нейтропения и тромбоцитопения выходят на первый план в клинике. Основной причиной мегалобластной анемии является дефицит витамина В12 (цианокобаламина) и фолиевой кислоты.
Роль цианкобаламина и фолиевой кислоты в развитии мегалобластной анемии связана с их участием в широком спектре обменных процессов и обменных реакций в организме.
При недостаточности фолатов и (или) цианкобаламина нарушается процесс включения уридина в ДНК развивающихся гемопоэтичеких клеток и образования тимидина, что обуславливает фрагментацию ДНК (блокирование ее синтеза и нарушение клеточного деления). При этом возникает мегалобластоз, происходит накопление больших форм лейкоцитов и тромбоцитов, их раннее внутрикостномозговое разрушение и укорочение жизни циркулирующих клеток крови. В результате гемопоэз оказывается неэффективным, развивается анемия, сочетающаяся с тромбоцитопенией и лейкопенией.
Кроме того, цианкобаламин является коферментом в реакции превращения метилмалонил-КоА в сукцинил-КоА. Эта реакция необходима для метаболизма миелина в нервной системе, в связи с чем при дефиците цианкобаламина наряду с мегалобластной анемией отмечается поражение нервной системы (фуникулярный миелоз), в то время как при недостаточности фолатов наблюдается только развитие мегалобластной анемии.
Цианкобаламин содержится в пищевых продуктах животного происхождения – печени, почках, яйцах, молоке. Для его всасывания необходимо наличие внутреннего фактора (фактора Касла) – секрета, выделяемого париетальными клетками желудка. Внутренний фактор является термолабильным, щелочеустойчивым гликопротеином. В присутствии витамина В12 (внешний фактор) две молекулы внутреннего фактора объединяются и образуют димер, который обеспечивает транспорт витамина В12 через слизистую оболочку кишечника. Запасы витамина В12 настолько велики, что требуется 3-6 лет для развития дефицита витамина при нарушении его всасывания.
 Фолиевая кислота содержится в зеленых листьях растений, фруктах, печени, почках. Запасы фолатов составляют 5-10 мг, минимальная потребность – 50 мкг в день. Мегалобластная анемия может развиться через 4 месяца полного отсутствия поступления фолатов с пищей.
Фолиевая кислота содержится в зеленых листьях растений, фруктах, печени, почках. Запасы фолатов составляют 5-10 мг, минимальная потребность – 50 мкг в день. Мегалобластная анемия может развиться через 4 месяца полного отсутствия поступления фолатов с пищей.
 Провоцирующие факторы развития В12-дефицитной и фолиеводефицитной анемии.
Провоцирующие факторы развития В12-дефицитной и фолиеводефицитной анемии.
Различные этиологические факторы могут вызывать дефицит цианкобаламина или фолиевой кислоты и развитие мегалобластной анемии.
- Дефицит цианкобаламина могут обусловить следующие причины:
- 1) нарушение питания (низкое содержание в рационе; вегетарианство; хронический алкоголизм)
- 2) недостаточное всасывание (дефицит внутреннего фактора; гастрэктомия;
инфильтративные изменения желудка; (лимфома или карцинома); болезнь Крона;
целиакия; резекция подвздошной кишки; повышенная утилизация витамина В12 бактериями при их избыточном росте; состояние после наложения желудочно-кишечного анастомоза; дивертикулы тощей кишки; кишечный стаз или обструкция, обусловленная стриктурами; глистная инвазия (лентец широкий Diphyllobotrium latum); - 3) неадекватная утилизация (врожденное отсутствие транскобаламина 2, заболевание печени, почек, злокачественные опухоли).
- Причинами дефицита фолатов могут быть:
- 1) Недостаточное поступление
– скудный рацион;
– алкоголизм;
– нервно-психическая анорексия;
– парентеральное питание;
– несбалансированное питание у пожилых. - 2) Нарушение всасывания
– мальабсорбция
– изменения слизистой оболочки кишечника
– целиакия и спру
– болезнь Крона
– регионарный илеит
– лимфома кишечника
– уменьшение реабсорбирующей поверхности после резекции тощей кишки
– прием антиконвульсантов - 3)Увеличение потребности
– беременность
– гемолитическая анемия
– эксфолиативный дерматит и псориаз - 4) Нарушение утилизации
– алкоголизм;
– антагонисты фолатов: триметоприм и метотрексат;
– врожденные нарушения метаболизма фолатов.
Клиническая картина
В12-дефицитная анемия развивается относительно медленно и может быть малосимптомной. Клинические признаки анемии неспецифичны: слабость, быстрая утомляемость, одышка, головокружение, сердцебиение. Больные бледны, субиктеричны.
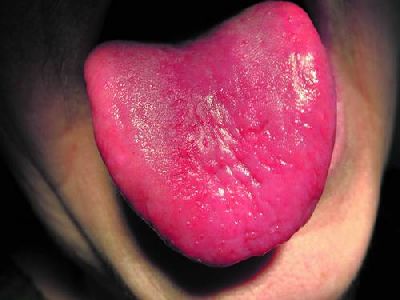
У большей части больных развивается глоссит – сопровождается жжением и болями в языке. Сосочки языка атрофируются, язык становится гладким, блестящим («лакированный язык»). Иногда поражаются слизистые оболочки щек и пищевода. Желудочная секреция резко снижения. При фиброгастроскопии выявляется атрофия слизистой оболочки желудка, которая подтверждается и гистологически. Возможно развитие диареи, вероятно, связанной с ахлоргидрией. Может быть увеличение селезенки и печени.
Наблюдаются и симптомы поражения нервной системы – белого вещества задних и боковых столбов спинного мозга (фуникулярный миелоз), церебральные нарушения и дегенерация периферических нервов. В основе неврологических проявлений лежит демиелинизация нервных волокон. Больные жалуются на покалывание в кончиках пальцев и нарушения чувствительности к холоду. При прогрессировании анемии появляется атаксия, нарушается походка, нарастает общая слабость, развивается гиперрефлексия.
- Таким образом для В12-дефицитной анемии характерна триада:
- – поражение крови;
- – поражение ЖКТ;
- – поражение нервной системы.
- Диагностика В12-дефицитной анемии:
- 1. Клинический анализ крови
– снижение количества эритроцитов
– снижение гемоглобина
– повышение цветного показателя (выше 1.05)
– макроцитоз (относится к группе макроцитарных анемий)
– базофильная зернистость эритроцитов, наличие в них телец Жолли и колец Кебота
– снижение ретикулоцитов
– лейкопения
– тромбоцитопения - 2. В окрашенных мазках – типичная картина: наряду с характерными овальными макроцитами встречаются эритроциты нормального размера, микроциты и шизоциты – пойкило- и анизоцитоз.
- 3. Уровень билирубина повышен за счет непрямой фракции.
- 4. В сыворотке крови уменьшается количество витамина В12 менее 150пг/мл, содержание железа сыворотки обычно нормальное или немного повышено.
- 5. Обязательна пункция костного мозга так как такая картина на периферии может быть при лейкозе, гемолитической анемии, апластических и гипопластических состояниях (однако, необходимо отметить, что гиперхромия характерна именно для В12-дефицитной анемии). Костный мозг клеточный, число ядросодержащих эритроидных элементов увеличено в 2-3 раза против нормы, однако эритропоэз неэффективный, о чем свидетельствует снижение числа ретикулоцитов и эритроцитов на периферии и укорочение их продолжительности жизни (в норме эритроцит живет 120-140 дней). Находят типичные мегалобласты – главный критерий постановки диагноза В12-дефицитная анемия. Это клетки с “ядерно-цитоплазматической диссоциацией” (при зрелой гемоглобинизированной цитоплазме нежное, сетчатого строения ядро с нуклеолами); также обнаруживаются клетки гранулоцитарного ряда большого размера и гигантские мегакариоциты.
Лечение
- Комплекс лечебных мероприятий при В12 – дефицитной анемии следует проводить с учетом этиологии, выраженности анемии и наличия неврологических нарушений. При лечении следует ориентироваться на следующие положения:
- – непременным условием лечения В12 – дефицитной анемии при глистной инвазии является дегельминтизация (для изгнания широкого лентеца назначают фенасал по определенной схеме или экстракт мужского папоротника).
- – при органических заболеваниях кишечника и поносах следует применять ферментные препараты (панзинорм, фестал, панкреатин), а также закрепляющие средства (карбонат кальция в сочетании с дерматолом).
- – нормализация кишечной флоры достигается приемом ферментных препаратов (панзинорм, фестал, панкреатин), а также подбором диеты, способствующей ликвидации синдромов гнилостной или бродильной диспепсии.
- – сбалансированное питание с достаточным содержанием витаминов, белка, безусловным запрещением алкоголя – непременное условие лечения В12 и фолиеводефицитной анемии.
- – патогенетическая терапия осуществляется с помощью парентерального введения витамина В12 (цианкобаламин), а также нормализации измененных показателей центральной гемодинамики и нейтрализации антител к гастромукопротеину (“внутреннему фактору”) или комплексу гастромукопротеин + витамин В12 (кортикостероидная терапия).
Гемотрансфузии проводят лишь при значительном снижении гемоглобина и проявлении симптомов коматозного состояния. Рекомендуется вводить эритроцитарную массу по 250 – 300 мл (5 – 6 трансфузий).
Преднизолон (20 – 30 мг/сут) рекомендуется при аутоиммунной природе заболевания.
- Принципы терапии:
- – насытить организм витамином
- – поддерживающая терапия
- – предупреждение возможного развития анемии
Чаще пользуются цианкобаламином. 1 ампула содержит 500 мкг витамина В12, вводят внутримышечно или подкожно. При тяжелом течении вводят 1000мкг в течение 10 дней, затем 500мкг 1 раз в неделю 4 недели, затем 500мкг 1 раз в месяц 6 месяцев, затем 500мкг 1 раз каждые полгода пожизненно.
При фоливодефицитной анемии назначают фолиевую кислоту по 1 таблетке (1мг) 4 раза в день.
Критерии оценки эффективности терапии:
- – резкий ретикулоцитоз через 5-6 инъекций, если его нет, то имеется ошибка диагностики;
- – полное восстановление показателей крови происходит через 1.5 – 2 месяца, а ликвидация неврологических нарушений в течение полугода.
- Пример общего анализа крови при В12-фолиеводефицитной анемии:
- Эритроциты – 2,1х1012 /л
- Гемоглобин – 90г/л
- Лейкоциты – 3,0 х 109/л (б 1%, э 2%, п/я 1%, с/я 60%, л 30%, м 6%)
- Тромбоциты – 140 х 109 /л
- СОЭ 10 мм/час
- Ретикулоциты – 0,1%.
- MCV 102 фл
- MCH 40 пг.
Медицина / Патология / Патология (статья)
B9- и B12-дефицитные анемии
Статья |
21-10-2018, 18:11
|
 АнемияМегалобластная анемия – одна из форм анемии, представляющая большую группу заболеваний, которые возникают в результате нарушения синтеза ДНК в эритроидных клетках; характеризуется мегалобластным типом кроветворения. Нарушение синтеза ДНК происходит при дефиците витаминов B9 (фолиевая кислота) и B12 (цианокобаламин), некоторых генетических нарушениях (наследственных патологиях, сопровождающихся нарушением активности ферментов, принимающих участи в синтезе коферментов фолиевой кислоты или утилизации оротовой кислоты (оротовая ацидурия)).
АнемияМегалобластная анемия – одна из форм анемии, представляющая большую группу заболеваний, которые возникают в результате нарушения синтеза ДНК в эритроидных клетках; характеризуется мегалобластным типом кроветворения. Нарушение синтеза ДНК происходит при дефиците витаминов B9 (фолиевая кислота) и B12 (цианокобаламин), некоторых генетических нарушениях (наследственных патологиях, сопровождающихся нарушением активности ферментов, принимающих участи в синтезе коферментов фолиевой кислоты или утилизации оротовой кислоты (оротовая ацидурия)).
При мегалобластной анемии в костном мозге определяются клетки с характерными морфологическими признаками: крупные, незрелые по внешнему виду ядра, окруженные относительно более зрелой цитоплазмой. С точки зрения биохимии основной причиной этого состояния является нарушение синтеза ДНК: в S-фазе клеточного цикла клетки прекращают развиваться (при частичной репликации ДНК клетка не может завершить процесс деления). При этом синтез РНК не нарушен. Происходит нарушение дифференцировки ядра. Учитывая, что синтез цитоплазматических компонентов очень интенсивный (особенно гемоглобина), площадь клеток-эритроидных предшественников очень расширена – это способствует образованию макроцитов (гиперхромных эритроцитов крупных размеров) или мегалоцитов. Такие изменения также характерны для гранулоцитарных предшественников и мегакароцитов.
Впервые мегалобласная анемия была описана английским ученым Аддисоном (Addison) в 1849 году. Аддисон обозначил ее как злокачественную (пернициозную). Врач Фенвик (Fenwick) из Лондона в 1870 году при вскрытии больного с пернициозной анемией обнаружил атрофию слизистой оболочки желудка. Немецкий врач Биермер (Biermer, Цюрих) в 1872 году в отношении этой патологии применил термин «прогрессирующая пернициозная анемия». А в 1880 ученый Эрлих (Ehrich) в костном мозге больных пернициозной анемией обнаружил крупные клетки со специфической структурой – мегалобласты. В начале XX века пернициозная анемия была одной из самых распространенных патологий крови и считалась неизлечимой.
Специалистам, которые изучали эту патологию и методы ее лечения, было присвоено пять Нобелевских премий. В 1930 году Касл (Castle) предполагал, что в мясе животных содержится «внешний фактор», который связывается с «внутренним фактором», в результате чего образуется так называемое гемопоэтическое вещество, способное усваиваться и депонироваться в печени. Ученые Минот (Minot), Марфи (Murphy) и Випл (Whipple) получили Нобелевскую премию в области медицины и физиологии за новый метод лечения пернициозной анемии сырой печенью. В 1948 году сразу две группы ученых (в США под руководством Фолкерса (Folkers) и в Великобритании под руководством Лестера-Смита (Lester-Smith)) выделили внешний фактор, витамин B12. Также Нобелевскую премию получила Дороти Кроуфут-Хоткин (Dorothy Crowfoot-Hodgkin) за изучение структуры пенициллина и витамина B12.
Витамин B12 (цианокобаламин) обладает структурой корриноида, в основе которой находится углеродная структура коррина, схожего по строению с порфирином. Цианокобаламин – сложная по структуре молекула с центральным атомом кобальта, который связан с четырьмя пиррольными кольцами и нуклеотидом. Витамин B12 имеет две коферментные формы – аденозилкобаламин и метилкобаламин. В крови человека основная форма витамина B12 – метилкобаламин.
Витамин B12 содержится только в продуктах животного происхождения (печень, почки, мясо, молоке и молочных продуктах). Небольшое количество этого витамина синтезируется в кишечнике человека. Цианокобаламин практически не содержится в продуктах растительного происхождения. У травоядных животных синтез витамина B12 происходит в желудке благодаря микроорганизмам, обитателям бобовых и корнеплодов, затем витамин попадает в паренхиматозные ткани и мышцы этих животных. Максимальная концентрация цианокобаламина в печени и почках животных (примерно 100 мкг/100 г продукта). В мясе содержание цианокобаламина гораздо ниже (примерно 0,5-2,0 мкг/100 г). Содержание витамина B12 в молоке и яйцах еще ниже, кроме этого, из-за прочной связи с протеином кобалафилином, содержащийся в этих продуктах витамин плохо усваивается. Цианокобаламин под действием протеолитических ферментов высвобождается в желудке и при кулинарной обработке продуктов.
Через стенки кишечника цианокобаламин попадает в кровь, где вступает в связь с транскобаламином II (транспортным протеином) и через воротную вену распределяется по кровеносной системе, откуда попадает в ткани-мишени.
Содержание цианокобаламина в организме взрослого человека составляет от 2 до 5 мг. Основной запас витамина B12, которого хватает на несколько лет (3-6), находится в печени. Экскреция (выведение из организма) цианокобаламина осуществляется через кишечник (с калом) и почки (с мочой), и составляет примерно 2-5 мкг в сутки. Суточная потребность организма взрослого человека в витамине B12 составляет 3-7 мкг.
Коферменты витамина B12 принимают участие в процессе синтеза ДНК, а также в регуляции функции системы гемопоэза и нервной системы. В крови содержится в большей степени активная форма витамина – метилкобаламин, который участвует в синтезе тетрагидрофолиевой кислоты, необходимой для образования тимидина.
Дефицит витамина B12 приводит к нарушению метаболизма фолатов и синтеза ДНК, в результате чего пролиферирующие кроветворные клетки не способны полностью созревать и нормально делиться. При этом в костном мозге развивается мегалобластический тип кроветворения, что приводит к появлению гигантских клеток миелопоэза и мегакариоцитопоэза. Из-за дефицита витамина B12 или B9 образуется недостаточное количество тетрагидрофолата, что вызывает развитие мегалобластной анемии по причине снижения синтеза нуклеиновых кислот.
Клиническая картина
Классическая картина B12-дефицитной анемии состоит из трех основных синдромов:
- Анемический синдром (см статью «Анемия. Общие положения. Классификация»)
- Желудочно-кишечный
- Неврологический
B12-дефицитная анемия, как правило, манифестирует в возрасте 50-60 лет (при этом такие пациенты часто выглядят старше своего возраста). Этот вид анемии наиболее широко распространен в Скандинавских странах, что обусловлено предрасположенностью к этой патологии голубоглазых блондинов.
B12-дефицитная анемия имеет три степени тяжести:
I степень: Легкая – концентрация гемоглобина в крови > 90 г/л
II степень: Средняя – концентрация гемоглобина в крови 70-90 г/л
III степень: Тяжелая – концентрация гемоглобина в крови < 70 г/л
Как правило больные обращаются к врачу при средней и тяжелой степени анемии. Часто от появления первых симптомов анемии до постановки диагноза проходит более года.
B12-дефицитная анемия обычно дебютирует анемическим синдромом (больного беспокоит слабость, повышенная утомляемость, тахикардия, одышка при незначительной физической нагрузке). По причине относительно медленного развития патологии выраженность анемии по данным лабораторных анализов часто оказывается большей, чем врачи ожидают при анализе клинических данных. Исключением являются больные, у которых неврологическая симптоматика усиливается быстрее, чем анемический синдром. Бывают случаи, когда характерное при глоссите жжение зыка возникает раньше, чем проявления анемии. У больных могут наблюдаться парестезии. При тяжелых случаях развивается фуникулярный миелоз, характеризующийся нарушениями чувствительности и походки. В случае дальнейшего прогрессирования патологии у больного возникают нарушения зрения, расстройства мочеиспускания. Нарушения функций желудочно-кишечного тракта наблюдаются примерно у 40-50% пациентов, страдающих B12-дефицитной анемией.
Объективное обследование пациента с B12-дефицитной анемией позволяет обнаружить характерную бледность кожи (с лимонно-желтым оттенком), субиктеричность кожи и склер. У ряда больных обнаруживаются объективные признаки глоссита (язык приобретает алый цвет с участками воспаления; сосочки языка сглаженные, иногда атрофированные – «лакированный» язык; отметим, что эти симптомы встречаются очень редко, как и глубокая мегалобластная анемия). Незначительное увеличение печени и селезенки при B12-дефицитной анемии наблюдается у 10-20% пациентов. Но у большинства пациентов патология сопровождается только анемическим синдромом, который часто является единственным клиническим признаком даже при тяжелой степени анемии.
Диагностика анемии основана на анамнезе, клинической картине, морфологическом исследовании клеток крови и костного мозга, анализа крови на содержание цианокобаламина и фолиевой кислоты.
Диагностика B12-дефицитной анемии
При B12-дефицитной анемии происходят характерные изменения гемограммы, включающие лейкопению, макроцитарную анемию, тромбоцитопению, а также гиперсегментированные нейтрофилы в мазке крови.
Мегалобластные анемии характеризуются преимущественным снижением уровня эритроцитов и в меньшей степени гемоглобина. Гиперхромия в этом случае проявляется повышением величины гемоглобина > 35 пг или цветового показателя > 1,1. Также увеличивается средний объем эритроцитов (> 100 фл и даже > 120 фл). В случаях, когда B12-дефицитная анемия сочетается с железодефицитной анемией или анемией хронического воспаления, средний объем эритроцитов может оставаться в пределах нормы. Выраженное повышение уровня ретикулоцитов (200-300% и выше) развивается на 5-8 день лечение витамином B12 – это повышение является подтверждением диагноза. Кроме этого, у многих пациентов наблюдается лейкопения (выраженность лейкопении часто коррелирует со степенью тяжести анемии). В некоторых случаях может наблюдаться снижение уровня тромбоцитов.
Большое диагностическое значение среди биохимических анализов крови имеет исследование уровня цианокобаламина. В миелограмме при нормальном или повышенном уровне миелокариоцитов обнаруживается выраженная гиперплазия эритроидного ростка и мегалобластический тип кроветворения (см рис. 1-7).
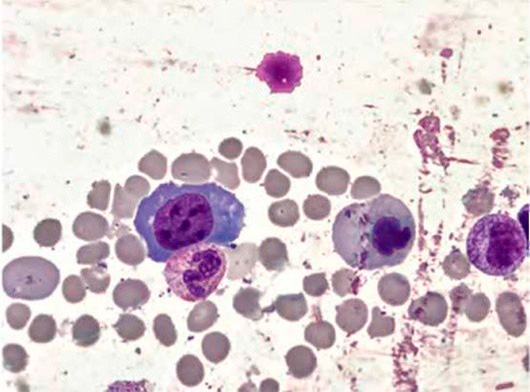
Рисунок 1. B12-дефицитная анемия. Костный мозг. Мегалобласты (окр. по Романовскому-Гимзе; ув. ×100)
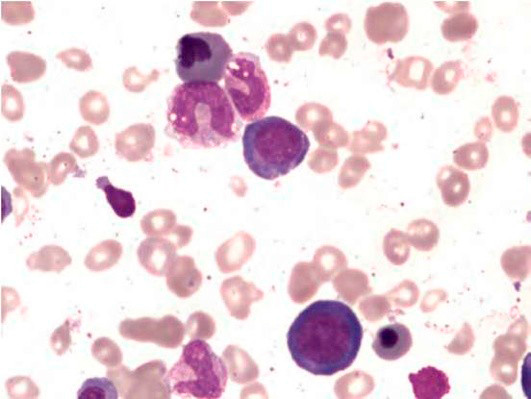
Рисунок 2. B12-дефицитная анемия. Костный мозг. Мегалобласты. Гигантские палочкоядерные нейтрофилы (окр. по Романовскому-Гимзе; ув. ×100)
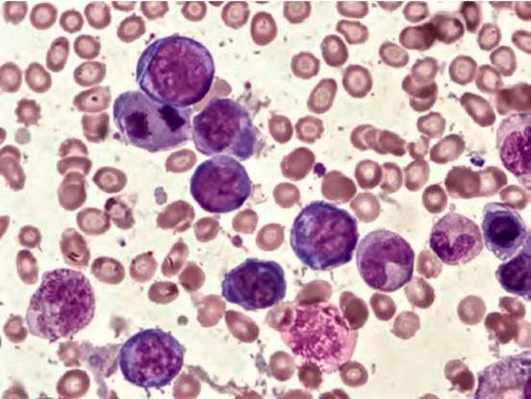
Рисунок 3. B12-дефицитная анемия. Костный мозг. Множественные базофильные мегалобласты – «синий костный мозг» (окр. по Романовскому-Гимзе; ув. ×100)
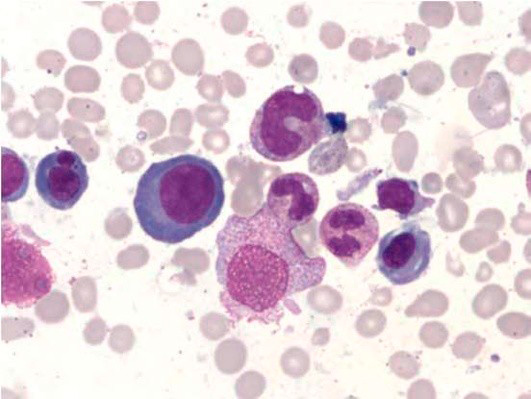
Рисунок 4. B12-дефицитная анемия. Препарат костного мозга. Мегалобластный тип кроветворения (окр. по Романовскому-Гимзе; ув. ×100)
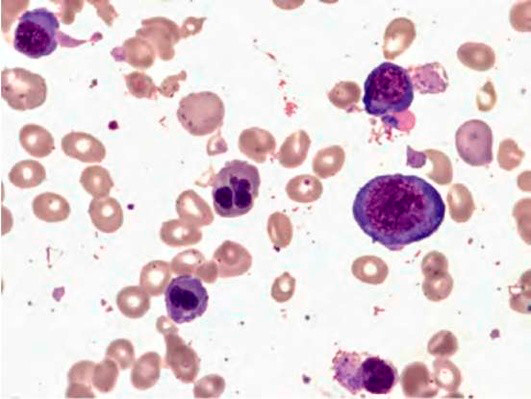
Рисунок 5. B12-дефицитная анемия. Препарат костного мозга. Множественные базофильные мегалобласты – «синий костный мозг» (окр. по Романовскому-Гимзе; ув. ×100)
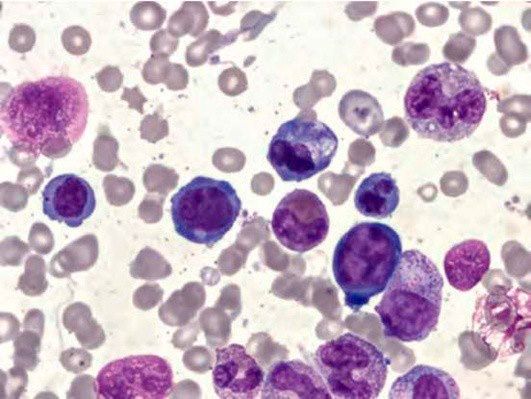
Рисунок 6. B12-дефицитная анемия. Препарат костного мозга. Мегалобласты, гигантские палочкоядерные нейтрофилы (окр. по Романовскому-Гимзе; ув. ×100)
Такие изменения миелограммы можно наблюдать только до начала терапии витамином B12. В аспирате костного мозга, полученного даже после однократной инъекции препарата, мегалобласты исчезают, а мегалобластический тип кроветворения сменяется нормобластическим. Отметим, что очень важным диагностическим критерием является высокий уровень лактатдегидрогеназы в крови.
Основа диагностики B12-дефицитной анемии в гематологии – анализ костного мозга на предмет наличия мегалобластов и миелоцитов с метамиелоцитами (гигантских клеток-предшественников гранулоцитопоэза). Но на практике эти клетки обнаруживаются не во всех случаях (даже если у больного явная форма анемии). Предположительно это происходит из-за того, что какое-то количество цианокобаламина больной все-таки как-то получил, что послужило причиной временного изменения гемопоэза, но не позволило полностью улучшить состояние. Но точные причины такого парадокса неизвестны. Поэтому с целью диагностики типичного случая B12-дефицитной анемии достаточно провести анализ периферической крови, с помощью которого можно определить гиперхромную макроцитарную анемию (при дифференциальной диагностике только патологий из группы миелодиспластических синдромов!). При этом могут обнаруживаться гиперсегментированные нейтрофилы (см рис. 7, 8), иногда метамиелоциты.
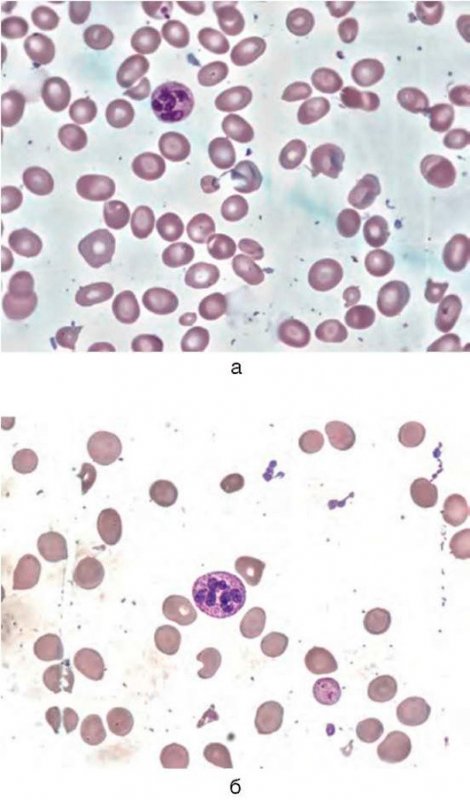 B12-дефицитная анемия
B12-дефицитная анемия
Рисунок 7. B12-дефицитная анемия. Препарат костного мозга. Множественные мегалобласты (окр. по Романовскому-Гимзе; ув. ×100) (а, б)

Рисунок 8. B12-дефицитная анемия. Костный мозг. (окр. по Романовскому-Гимзе; ув. ×100)
Если лабораторные исследования демонстрируют умеренную тромбоцитопению, незначительное повышение уровня непрямого билирубина и значительное повышение концентрации лактатдегидрогеназы, диагноз можно считать подтвержденным (в этом случае проведение дополнительных пункций – лишняя процедура).
При диагностике B12-дефицитной анемии важное значение играет фиброгастроскопия, с помощью которой можно подтвердить диагноз «атрофический гастрит» – главная причина дефицита цианокобаламина. Кроме этого, гастроскопия позволяет исключить злокачественную патологию желудка.
После назначения лечения витаминами B9 и B12 наблюдается следующая динамика изменения показателей лабораторных исследований:
– значительное повышение уровня эритроцитов и гемоглобина в течение 14 дней, показатель которых, в зависимости от выраженности дефицита, нормализуется через 8-12 недель с момента начала лечения; отметим, что уровень гемоглобина повышается медленнее, поэтому его показатель в периферической крови возвращается в норму через 1-2 месяца лечения;
– на 2-4-й день терапии начинает увеличиваться уровень ретикулоцитов, достигает максимума на 8-9-й день, и нормализуется к 14-му дню лечения; при этом повышается уровень тромбоцитов и лейкоцитов;
– на 10-14-й день терапии гиперсегментация ядер нейтрофилов сохраняется;
– в течение 24-48 часов после первого введения препарата в костном мозге исчезают мегалобласты; изменения морфологии ядер гранулоцитов сохраняется еще несколько суток;
– биохимический анализ крови показывает повышение уровня мочевой кислоты и холестерина (максимум достигается на пике ретикулоцитоза); концентрация лактатдегидрогеназы, щелочной фосфотазы и билирубина возвращаются в норму; может наблюдаться незначительное снижение концентрации калия в крови.
Лечение
Пока врачи не могли использовать в терапии препараты цианокобаламина, B12-дефицитная анемия считалось фатальным заболеванием. В те времена ремиссию можно было получить с помощью эмпирического подбора рациона питания, трансфузионной терапии или спленэктомии, но после этого следовал очередные рецидивы, которые приводили к смерти пациента (как правило это происходило через 1-3 года с момента диагностирования патологии).
С целью профилактики развития B12-дефицитной анемии рацион питания должен содержать животный белок (печень, сердце, мясо, рыба, молочные продукты и др). Во время манифестации патологии нужно назначать цианокобаламин. Если у больного диагностированы глистные инвазии, дополнительно назначается противогельминтная терапия.
Сегодня для лечения B12-дефицитной анемии широко применяются два препарата: Цианокобаламин и Оксикобаламин. В нашей стране принято назначать Цианокобаламин: подкожно или внутримышечно 200-400 мкг 1 раз в день на протяжении 4-5 недель. В тяжелых случаях и при развитии фуникулярного миелоза суточная дозировка цианокобаламина повышают до 1000 мкг.
При условии назначения адекватного лечения явное улучшение состояния пациента и нормализацию картины костного мозга можно наблюдать уже на 3-4-е сутки лечения. Повышение уровня ретикулоцитов в периферической крови в среднем на 20-30% (ретикулоцитарный криз) развивается через 1-2 недели. Концентрация билирубина в крови возвращается в норму на протяжении 3-4 недель, лактатдегидрогеназы – через 7-14 дней.
При назначении цианокобаламина ремиссия наступает у всех больных B12-дефицитной анемией.
При отсутствии эффекта от терапии на протяжении нескольких недель, следует предполагать неверную трактовку генеза анемии. В этом случае пациенту необходимо провести дополнительную диагностику, чтобы уточнить причину анемического синдрома.
ФОЛИЕВО-ДЕФИЦИТНАЯ АНЕМИЯ
Эта патология относится к группе мегалобластных анемий. Дефицит фолиевой кислоты приводит к нарушению влияния цианокобаламина на процесс синтеза ДНК, что приводит к развитию мегалобластного типа кроветворения.
Дефицит витамина B9 может возникать из-за недостаточного поступления в организм фолиевой кислоты с пищей, патологий желудочно-кишечного тракта (нарушений усвоения фолиевой кислоты), а также при повышенной потребности организма в этом витамине.
Характерные жалобы пациентов с фолиево-дефицитной анемией – общая слабость и головокружения. Глоссит у таких больных, в отличие от больных B12-дефицитной анемией, развивается очень редко. Также при B9-дефицитной анемии не обнаруживаются признаки фуникулярного миелоза.
Как и при дефиците цианокобалавина, при дефиците фолиевой кислоты в периферической крови обнаруживается макроцитоз, повышается среднее содержание гемоглобина в эритроците и средний объем эритроцитов. В костном мозге появляются мегалобласты. Повышается уровень непрямого билирубина в крови, увеличивается активность лактатдегидрогеназы.
Дефицит фолиевой кислоты в организме приводит к повышению уровня гомоцистеина, что является фактором риска для образования венозных тромбов
