Кооперативные изменения конформации протомеров гемоглобина
О2 связывается с протомерами гемоглобина через Fe2+ , который соединён с четырьмя атомами азота пиррольных колец тема и атомом азота
Рис. 1-32. Строение гемоглобина.
Гис F8 белковой части протомера. Связывание О2 с оставшейся свободной координационной связью Fe2+ происходит по другую сторону от плоскости гема в области Гис Е7 (аналогично тому, как это происходит у миоглобина). Гис Е7 не взаимодействует с О2, но обеспечивает оптимальные условия для его связывания (рис. 1-33).
В дезоксигемоглобине благодаря ковалентной связи с белковой частью атом Fe2+ выступает из плоскости гема в направлении Гис F8. Присоединение О2 к атому Fe2+ одного протомера вызывает его перемещение в плоскость гема, за ним перемещаются остаток Гис F8 и полипептидная цепь, в состав которой он входит. Так как протомер связан с остальными протомерами, а белки обладают конформационной лабильностью, происходит изменение конформации всего белка. Конформационные изменения, произошедшие в других протомерах, облегчают присоединение следующей молекулы О2, что вызывает новые конформационные изменения в белке и ускорение связывания следующей молекулы О2. Четвёртая молекула О2 присоединяется к гемоглобину в 300 раз легче, чем первая молекула (рис. 1-34).
Рис. 1-33. Изменение прложения Fe2+ и белковой части гемоглобина при присоединении О2.
Рис. 1-34. Кооперативные изменения конформации протомеров гемоглобина при присоединении О2.
Изменение конформации (а следовательно и функциональных свойств) всех протомеров олигомерного белка при присоединении лиганда только к одному из них носит название кооперативных изменений конформации протомеров.
Аналогичным образом в тканях диссоциация каждой молекулы О2 изменяет конформацию всех протомеров и облегчает отщепление последующих молекул О2.
Кривые диссоциации О2 для миоглобина и гемоглобина
Кооперативность в работе протомеров гемоглобина можно наблюдать и на кривых диссоциации О2 для миоглобина и гемоглобина (рис. 1-35).
Отношение занятых О2 участков связывания белка к общему числу таких участков, способных к связыванию, называется степенью насыщения этих белков кислородом. Кривые диссоциации показывают, насколько насыщены данные белки О2 при различных значениях парциального давления кислорода.
Кривая диссоциации О2 для миоглобинаимеет вид простой гиперболы. Это указывает на то, что миоглобин обратимо связывается с лигандом, и на это не оказывают влияние никакие посторонние факторы (схема ниже).
Схема
Рис. 1-35. Кривые диссоциации кислорода для миоглобина и гемоглобина в зависимости от парциального давления кислорода.
Процессы образования и распада оксимиоглобина находятся в равновесии, и это равновесие смещается влево или вправо в зависимости от того, добавляется или удаляется кислород из системы. Миоглобин связывает кислород, который в капиллярах тканей высвобождает гемоглобин, и сам миоглобин может освобождать О2 в ответ на возрастание потребностей в нём мышечной ткани и при интенсивном использовании О2 в результате физической нагрузки.
Миоглобин имеет очень высокое сродство к О2. Даже при парциальном давлении О2, равном 1-2 мм рт. ст., миоглобин остаётся связанным с О2 на 50%.
Кривая диссоциации О2 для гемоглобина.Из графика на рис. 1-35 видно, что гемоглобин имеет значительно более низкое сродство к О2; полунасыщение гемоглобина О2 наступает при более высоком давлении О2 (около 26 мм рт. ст.).
Кривая диссоциации для гемоглобина имеет сигмоидную форму (S-образную). Это указывает на то, что протомеры гемоглобина работают кооперативно: чем больше О2 отдают протомеры, тем легче идёт отщепление последующих молекул О2.
В капиллярах покоящихся мышц, где давление О2 составляет около 40 мм рт. ст., большая часть кислорода возвращается в составе оксигемоглобина обратно в лёгкие. При физической работе давление О2 в капиллярах мышц падает до 10-20 мм рт. ст. Именно в этой области (от 10 до 40 мм рт. ст.) располагается “крутая часть” S-образной кривой, где в наибольшей степени проявляется свойство кооперативной работы протомеров.
Следовательно, благодаря уникальной структуре каждый из рассмотренных белков приспособлен выполнять свою функцию: миоглобин – присоединять О2, высвобождаемый гемоглобином, накапливать в клетке и отдавать в случае крайней необходимости; гемоглобин – присоединять О2 в лёгких, где его насыщение доходит до 100%, и отдавать О2 в капиллярах тканей в зависимости от изменения в них давления О2
4. Перенос Н+ и С02 из тканей в лёгкие
с помощью гемоглобина. Эффект Бора
Окисление органических веществ с целью получения энергии происходит в митохондриях клеток с использованием О2, доставляемого гемоглобином из лёгких. В результате окисления веществ образуются конечные продукты распада – СО2 и Н2О, количество которых пропорционально интенсивности процессов окисления. СО2, образовавшийся в тканях, транспортируется в эритроциты. Там под действием фермента карбангидразы происходит увеличение скорости образования Н2СО3. Слабая угольная кислота может диссоциировать на Н+ и НСО3-
СО2 + Н2О – H2CO 3 – H+ + HCO3-.
Равновесие реакции в эритроцитах, находящихся в капиллярах тканей, смещается вправо, так как образующиеся в результате диссоциации угольной кислоты протоны могут присоединяться к специфическим участкам молекулы гемоглобина: к радикалам Гис146 двух ?-цепей, радикалам Гис122 и концевым ?-аминогруппам двух ?-цепей. Все эти 6 участков при переходе гемоглобина от окси- к дезоксиформе приобретают большее сродство к Н+ в результате локального изменения аминокислотного окружения вокруг этих участков (приближения к ним отрицательно заряженных карбоксильных групп аминокислот).
Присоединение 3 пар протонов к гемоглобину уменьшает его сродство к О2 и усиливает транспорт О2 в ткани, нуждающиеся в нём (рис. 1-36, А). Увеличение освобождения О2 гемоглобином в зависимости от концентрации Н+ называют эффектом Бора (по имени датского физиолога Христиана Бора, впервые открывшего этот эффект).
В капиллярах лёгких высокое парциальное давление О2 приводит к оксигенированию гемоглобина и удалению 6 протонов. Реакция СО2 + Н2О – Н2СО3 – Н+ + НСО3- сдвигается влево и образующийся СО2 выделяется в альвеолярное пространство и удаляется с выдыхаемым воздухом (рис. 1-36, Б). Следовательно, молекула гемоглобина в ходе эволюции приобрела способность воспринимать и реагировать на информацию, получаемую из окружающей среды. Увеличение концентрации протонов в среде снижает сродство О2 к гемоглобину и усиливает его транспорт в ткани (рис. 1-37).
Большая часть СО2 транспортируется кровью в виде бикарбоната НСО3-. Небольшое количество
Рис. 1-36. Перенос Н+ и СО2 с кровью. Эффект Бора. А – влияние концентрации СО2 и Н+ на высвобождение О2 из комплекса с гемоглобином в тканях (эффект Бора); Б – оксигенирование дезоксигемоглобина в лёгких, образование и выделение СО2.
Рис. 1-37. Влияние рН на кривую диссоциации О2 для гемоглобина.
СО2 (около 15-20%) может переноситься в лёгкие, обратимо присоединяясь к неионизированным концевым ?-аминогруппам. R-NH2+ СО2 = R-NH-COO + Н+, в результате образуется карбогемоглобин, где R – полипептидная цепь гемоглобина. Присоединение СО2 к гемоглобину также снижает его сродство к О2.
5. 2,3-Бифосфоглицерат – аллостертеский регулятор сродства гемоглобина к О2
2,3-Бифосфоглицерат (БФГ) – вещество, синтезируемое в эритроцитах из промежуточного продукта окисления глюкозы 1,3-бифосфоглицерата.
Кооперативными изменениями конформации протомеров называются изменения конформации всего олигомерного белка после присоединения лиганда к одному из протомеров, приводящее к изменению функциональных свойств белка в целом. Для гемоглобина это означает, что кооперативные изменения конформации его протомеров ускоряют присоединение кислорода в легких и облегчают отщепление кислорода в тканях: – присоединение кислорода через Fe2+ к одному протомеру (оксигенация гемоглобина) вызывает перемещение Fe2+ в плоскость гема; одновременно перемещается и остаток Гис F8, связанный с ним. Это влечет изменение конформации данного протомера, а также остальных субъединиц гемоглобина и их активных центров, то есть вследствии конформационной лабильности изменяется конформация и свойства всего белка;
– измененная конформация белка облегчает связывание второй молекулы кислорода со следующим протомером, что вызывает дополнительные кооперативные изменения конформации протомеров и еще более облегчает связывание со следующей молекулой 02. Четвертая молекула кислорода присоединяется к оставшемуся протомеру в 300 раз легче, чем первая.
– последовательное отщепление кислорода (дезоксигенация) в тканях изменяет на каждом этапе конформацию всех протомеров и облегчает диссоциацию последующих молекул 02.
Кривая диссоциации оксигемоглобина имеет выраженный S-образный характер и отражает положительный кооперативный эффект взаимодействия протомеров (субъединиц) в тетрамер-ной молекуле гемоглобина при его оксигенации.
Гемоглобин имеет S-образную кривую насыщения, которая показывает, что субъединицы белка работают кооперативно, и чем больше кислорода они отдают, тем легче идет диссоциация остальных молекул 02; этот процесс зависит от изменения парциального давления 02 в тканях.
Кривая насыщения (диссоциации) миоглобина – простая гипербола, отражает функции миоглобина – обратимое связывание с кислородом, высвобождаемым гемоглобином, депонирование его и освобождение в случае интенсивной физической нагрузки; не зависит от посторонних факторов
Возможность адаптивной регуляции биологической функции олигомерных белков с помощью аллостерических лигандов
Если белок при взаимодействии с лигандом повышает или понижает актив- ность вследствии конформационных изменений, то имеет место аллостериче-ская регуляция, а лиганд называется аллостерическим. Данное свойство проявляется, как правило, у олигомерных белков, т.е. для проявления аллостериче-ского эффекта необходимо взаимодействие субъединиц. При воздействии аллостерических лигандов белки адаптируют свою конформацию (в том числе и активного центра) и функцию к изменившимся условиям окружающей среды.
Для гемоглобина аллостерическими лигандами являются Н+, С02 и 2,3-бифосфоглицерат (БФГ). Эти лиганды присоединяются к участкам (аллостерическим центрам), пространственно удаленным друг от друга. Концентрация аллостерических лигандов влияет на сродство гемоглобина к кислороду (миог-лобин и разделенные субъединицы гемоглобина нечувствительны к изменениям концентрации Н+, СО2 и БФГ, т. е. аллостерические свойства гемоглобина возникают только в результате взаимодействия субъединиц).
В центре молекулы гемоглобина аминокислотными остатками четырех субъединиц образована полость, величина ее увеличивается в дезоксигемогло-бине и уменьшается в оксигемоглобине. БФГ, синтезируемый в эритроцитах при гликолизе, может поместиться только в большой полости дезоксигемоглобина, избирательно связывается с дезоксигемоглобином, снижая его сродство к О2 в 26 раз. В результате повышается высвобождение кислорода в капиллярах ткани при постоянном парциальном давлении О2.
Исследование роли БФГ в транспорте крови прояснило адаптивные механизмы, включающиеся при гипоксии – нарушении снабжения тканей кислородом. У больных с тяжелой обструктивной энфиземой легких затруднено поступление воздуха в легкие, парциальное давление кислорода в артериальной крови (50 мм рт. ст.) вдвое ниже нормы (100 мм рт. ст.). При этом происходит усиление синтеза БФГ в эритроцитах (его концентрация повышается с 4,5 мМ/л до 8 мМ/л), что приводит к увеличению доставки кислорода в ткани. На рис. это отражается компенсаторным сдвигом кривой насыщения гемоглобина кислородом вправо.
Механизм адаптивной регуляции к высоте – также результат изменения концентрации БФГ в эритроцитах крови. На высоте 4,5 км над уровнем моря насыщение крови кислородом снижается из-за снижения парциального давления О2, но уже через два дня возрастает концентрация БФГ в крови с 4,5 мМ/л до 7,0 мМ/л. Сродство к кислороду снижается, и количество высвобождаемого кислорода в капиллярах тканей возрастает. При спуске на уровень моря концентрация БФГ возвращается к исходному уровню.
Date: 2016-05-24; view: 4442; Нарушение авторских прав
Кооперативное взаимодействие
Взаимовлияние протомеров олигомерного белка друг на друга называется кооперативное взаимодействие.
В легких такое взаимодействие субъединиц гемоглобина повышает его сродство к кислороду и ускоряет присоединение кислорода в 300 раз. В тканях идет обратный процесс, сродство снижается и ускорение отдачи кислорода также 300-кратное.
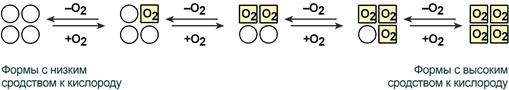
Схема кооперативного взаимодействия субъединиц гемоглобина
Объясняется такой феномен тем, что в легких при присоединении первой молекулы кислорода к железу (за счет 6-й координационной связи) атом железа втягивается в плоскость гема, кислород остается вне плоскости. Это вызывает перемещение участка белковой цепи и изменение конформации первого протомера. Такой измененный протомер влияет на другие субъединицы и облегчает связывание кислорода со второй субъединицей. Это меняет конформацию второй субъединицы, облегчая присоединение последующих молекул кислорода и изменение других протомеров.
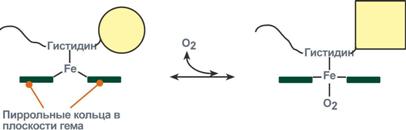
Изменение формы субъединиц гемоглобина
при присоединении и отщеплении кислорода
Дезоксиформа гемоглобина обозначается как Т-форма, напряженная (англ. tense), она обладает существенно более низким сродством к кислороду. Оксигенированная форма, или R-форма (англ. relaxed), обладает высоким сродством к кислороду.
Изменение рН среды
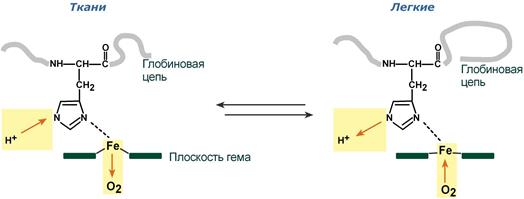
Влияние рН на сродство гемоглобина к кислороду носит название эффекта Бора. При закислении среды сродство снижается, при защелачивании – повышается.
При повышении концентрации протонов (закисление среды) в тканях возрастает освобождение кислорода из оксигемоглобина. В легких после удаления угольной кислоты (в виде СО2) из крови и одновременном увеличении концентрации кислорода высвобождаются ионы Н+ из гемоглобина.
Реакция взаимодействия кислорода с гемоглобином упрощенно имеет вид:

Изменение сродства гемоглобина к кислороду в тканях и в легких при изменении концентрации ионов H+ и О2 обусловлено конформационными перестройками глобиновой части молекулы. В тканях молекула О2 отрывается от железа и ионы водорода присоединяются к остаткам гистидина (глобиновой части), образуя восстановленный гемоглобин (H-Hb) с низким сродством к кислороду. В легких поступающий в больших количествах кислород “вытесняет” ион водорода из связи с остатком гистидина гемоглобиновой молекулы.

Механизм эффекта Бора
Роль 2,3-дифосфоглицерата
2,3-Дифосфоглицерат образуется в эритроцитах из 1,3-дифосфоглицерата, промежуточного метаболита гликолиза, в реакциях, получивших название шунт Раппопорта.
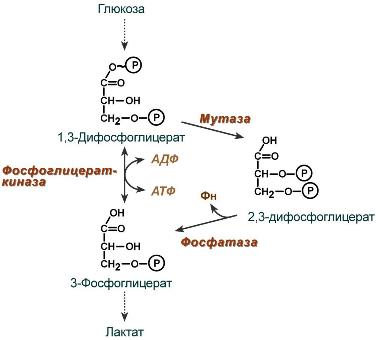
Реакции шунта Раппопорта
2,3-Дифосфоглицерат располагается в центральной полости тетрамера дезоксигемоглобина и связывается с β-цепями, образуя поперечный солевой мостик между атомами кислорода 2,3-дифосфоглицерата и аминогруппами концевого валина обеих β-цепей, также аминогруппами радикалов лизина и гистидина.
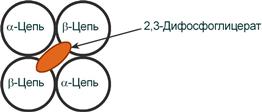
Расположение 2,3-дифосфоглицерата в гемоглобине
Функция 2,3-дифосфоглицерата заключается в снижении сродства гемоглобина к кислороду, что имеет особенное значение при подъеме на высоту и при нехватке кислорода во вдыхаемом воздухе. В этих условиях связывание кислорода с гемоглобином в легких не нарушается, так как концентрация его относительно высока. Однако в тканях за счет 2,3-дифосфоглицерата отдача кислорода возрастает в 2 раза.
Четвертичная структура – это и количество, и способ укладки полипептидных цепей (протомеров) в пространстве. Если белки состоят из двух и более полипептидных цепей, связанных между собой нековалентными (не пептидными и не дисульфидными) связями, то говорят, что они обладают четвертичной структурой.Такие агрегаты стабилизируются водородными связями, ионными связями и электростатическими взаимодействиями между остатками аминокислот, находящимися на поверхности глобулы. Подобные белки называются олигомерами, а их индивидуальные цепи протомерами (мономерами, субъединицами). Если белки содержат 2 протомера, то они называются димерами, если 4, то тетрамерами и т.д.
Протомеры связаны друг с другом посредством лишь нековалентных связей (ионных, водородных, гидрофобных). Причем протомеры взаимодействуют друг с другом только определенными участками своей поверхности (контактные участки). Взаимное «узнавание» контактных участков происходит по принципу комплементарности. Каждый протомер взаимодействует с другим во многих точках. Следовательно, ошибочные комплексы в олигомере практически невозможны. Так как субъединицы в олигомерах очень тесно взаимодействуют между собой, то любое изменение конформации какой-либо одной субъединицы обязательно влечет за собой изменение других субъединиц. Этот эффект называется кооперативное взаимодействие. Например, у гемоглобина такое взаимодействие субъединиц в легких ускоряет в 300 раз присоединение О2 к гемоглобину. В тканях отдача О2 также ускоряется в 300 раз. Присоединение в легких первой молекулы кислорода к одной из субъединиц гемоглобина изменяет ее конформацию. В результате она начинает влиять на следующую убъединицу, облегчая присоединение к ней кислорода. После этого они вдвоем влияют на третью субъединицу и так далее. В тканях первая молекула кислорода отделяется от своей субъединицы не очень легко, вторая уже быстрее и т.д. Олигомерные белки способны взаимодействовать с несколькими лигандами в центрах, удаленных друг от друга. Связывание одного протомера с лигандом изменяет конформацию этого протомера, а также всего олигомера и, кроме того, сродство к другим лигандам. Таким образом, функциональная активность олигомерных белков может регулироваться аллостерическими лигандами.
Аллостерическими ферментами называют ферменты, активность которых регулируется не только количеством молекул субстрата, но и другими веществами, называемыми эффекторами (обычно это олигомерные белки, состоящие из нескольких протомеров или имеющие доменное строение; они имеют аллостерический центр, пространственно удалённый от каталитического активного центра; эффекторы присоединяются к ферменту нековалентно в аллостерических (регуляторных) центрах; аллостерические ферменты обладают свойством кооперативности: регуляция аллостерических ферментов обратима). Участвующие в аллостерической регуляции эффекторы – клеточные метаболиты часто именно того пути, регуляцию которого они осуществляют. Связь между структурой белка и его функцией можно рассмотреть на примере двух родственных белков: миоглобина и гемоглобина:
Миоглобин – мономер (состоит из одной полипептидной цепи), основная его функция – запасание кислорода в тканях. Имея высокое сродство к кислороду, миоглобин легко присоединяет его и отдает кислород только при интенсивной мышечной работе, когда парциальное давление кислорода падает ниже 10 мм рт. ст.
Гемоглобин – тетрамер (состоит из 4х протомеров). Основная функция гемоглобина – обратимое связывание с кислородом в легких, где парциальное давление кислорода высокое и гемоглобин взаимодействует с четырьмя молекулами кислорода.
В тканях СО2 и Н2О, образующиеся при катаболизме пищевых веществ, взаимодействуют с гемоглобином и уменьшают его сродство к кислороду, что облегчает поступление кислорода в ткани.
В эритроцитах имеется также аллостерический лиганд 2,3-дифосфоглицерат, способный взаимодействовать с дезоксигемоглобином. Это препятствует обратному связыванию освободившегося О2 с гемоглобином.
Таким образом, связывание гемоглобина с аллостерическими лигандами в тканях, при относительно высоком парциальном давлении, обеспечивает поступление кислорода в ткани.
Из рассмотренных примеров следует заключить, что аллостерический эффект является результатом связывания лиганда со специфическим участком белка. Это вызывает значительное изменение в белковой молекуле, которая в свою очередь влияет на активность другого, пространственно удаленного участка. Кооперативные изменения конформации олигомерных белков составляют основу механизма регуляции функциональной активности не только гемоглобина, но и многих других белков.
