Наибольшее сродство к гемоглобину
Оглавление темы “Вентиляция легких. Перфузия легких кровью.”: Сродство гемоглобина к кислороду. Изменение сродства гемоглобина к кислороду. Эффект Бора.Молекула гемоглобина может находиться в двух формах — напряженной и расслабленной. Расслабленная форма гемоглобина имеет свойство насыщаться кислородом в 70 раз быстрее, чем напряженная. Изменение фракций напряженной и расслабленной формы в общем количестве гемоглобина в крови обусловливает S-образный вид кривой диссоциации оксигемоглобина, а следовательно, так называемое сродство гемоглобина к кислороду. Если вероятность перехода от напряженной формы гемоглобина к расслабленной больше, то возрастает сродство гемоглобина к кислороду, и наоборот. Вероятность образования указанных фракций гемоглобина изменяется в большую или меньшую сторону под влиянием нескольких факторов. Основной фактор — это связывание кислорода с геминовой фуппой молекулы гемоглобина. При этом чем больше геминовых фупп гемоглобина связывают кислород в эритроцитах, тем более легким становится переход молекулы гемоглобина к расслабленной форме и тем выше их сродство к кислороду. Поэтому при низком Р02, что имеет место в метаболически активных тканях, сродство гемоглобина к кислороду ниже, а при высоком Р02 — выше. Как только гемоглобин захватывает кислород, повышается его сродство к кислороду и молекула гемоглобина становится насыщенной при связывании с четырьмя молекулами кислорода.
Когда эритроциты, содержащие гемоглобин, достигают тканей, то кислород из эритроцитов диффундирует в клетки. В мышцах он поступает в своеобразного депо кислорода — в молекулы миоглобина, из которого кислород используется в биологическом окислении мышц. Диффузия кислорода из гемоглобина эритроцитов в ткани обусловлена низким Р02 в тканях — 35 мм рт. ст. Внутри клеток тканей напряжение кислорода, необходимое для поддержания нормального метаболизма, составляет еще меньшую величину — не более 1 кПа. Поэтому кислород путем диффузии из капилляров достигает метаболически активных клеток. Некоторые ткани приспособлены к низкому содержанию Р02 в капиллярах крови, что компенсируется высокой плотностью капилляров на единицу объема тканей. Например, в скелетной и сердечной мышцах Р02 в капиллярах может снизиться чрезвычайно быстро во время сокращения. В мышечных клетках содержится белок миоглобин, который имеет более высокое сродство к кислороду, чем гемоглобин. Миоглобин интенсивно насыщается кислородом и способствует его диффузии из крови в скелетную и сердечную мышцы, где он обусловливает процессы биологического окисления. Эти ткани способны экстрагировать до 70 % кислорода из крови, проходящей через них, что обусловлено снижением сродства гемоглобина к кислороду под влиянием температуры тканей и рН. Эффект рН и температуры на сродство гемоглобина к кислороду. Молекулы гемоглобина способны реагировать с ионами водорода, в результате этой реакции происходит снижение сродства гемоглобина к кислороду. При насыщении гемоглобина менее 100 % низкое рН понижает связывание кислорода с гемоглобином — кривая диссоциации оксигемоглобина смещается вправо по оси х. Это изменение свойства гемоглобина под влиянием ионов водорода называется эффектом Бора. Метаболически активные ткани продуцируют кислоты, такую как молочная, и С02. Если рН плазмы крови снижается от 7,4 в норме до 7,2, что имеет место при сокращении мыщц, то концентрация кислорода в ней будет возрастать вследствие эффекта Бора. Например, при постоянном рН 7,4 кровь отдавала бы порядка 45 % кислорода, т. е. насыщение гемоглобина кислородом снижалось до 55 %. Однако когда рН снижается до 7,2, кривая диссоциации смещается по оси х вправо. В результате насыщение гемоглобина кислородом падает до 40 %, т. е. кровь может отдавать в тканях до 60 % кислорода, что на 1/з больше, чем при постоянном рН.
Метаболически активные ткани повышают продукцию тепла. Повышение температуры тканей при физической работе изменяет соотношение фракций гемоглобина в эритроцитах и вызывает смещение кривой диссоциации оксигемоглобина вправо вдоль оси х. В результате большее количество кислорода будет освобождаться из гемоглобина эритроцитов и поступать в ткани. Эффект 2,3-дифосфоглицерата (2,3-ДФГ) на сродство гемоглобина к кислороду. При некоторых физиологических состояниях, например при понижении Р02 в крови ниже нормы (гипоксия) в результате пребывания человека на большой высоте над уровнем моря, снабжение тканей кислородом становится недостаточным. При гипоксии может понижаться сродство гемоглобина к кислороду вследствие увеличения содержания в эритроцитах 2,3-ДФГ. В отличие от эффекта Бора, уменьшение сродства гемоглобина к кислороду под влиянием 2,3-ДФГ не является обратимым в капиллярах легких. Однако при движении крови через капилляры легких эффект 2,3-ДФГ на снижение образования оксигемоглобина в эритроцитах (плоская часть кривой диссоциации оксигемоглобина) выражен в меньшей степени, чем отдача кислорода под влиянием 2,3-ДФГ в тканях (наклонная часть кривой), что обусловливает нормальное кислородное снабжение тканей. – Также рекомендуем “Углекислый газ. Транспорт углекислого газа.” |
Молекула гемоглобина: 4 субъединицы окрашены в разные цвета
Структура гемоглобина человека. Железосодержащие гем-группы показаны зелёным. Красным и синим показаны альфа- и бета- субъединицы.
Гемоглоби́н (от др.-греч. αἷμα «кровь» + лат. globus «шар») (Hb или Hgb) — сложный железосодержащий белок животных, обладающих кровообращением, способный обратимо связываться с кислородом, обеспечивая его перенос в ткани. У позвоночных животных содержится в эритроцитах, у большинства беспозвоночных растворён в плазме крови (эритрокруорин) и может присутствовать в других тканях[1]. Молекулярная масса гемоглобина человека — около 66,8 кДа. Молекула гемоглобина может нести до четырёх молекул кислорода. Один грамм гемоглобина может переносить до 1.34 мл. O2
Гемоглобин появился более чем 400 миллионов лет назад у последнего общего предка человека и акул в результате 2 мутаций, приведших к формированию четырёхкомпонентного комплекса гемоглобина, сродство которого к кислороду достаточно для связывания кислорода в насыщенной им среде, но недостаточно, чтобы удерживать его в других тканях организма.[2][3]
Большой вклад в исследование структуры и функционирования гемоглобина внёс Макс Фердинанд Перуц, получивший за это в 1962 году Нобелевскую премию[4].
Нормальным содержанием гемоглобина в крови человека считается: у мужчин — 130—160 г/л (нижний предел — 120, верхний предел — 180 г/л), у женщин — 120—160 г/л; у детей нормальный уровень гемоглобина зависит от возраста и подвержен значительным колебаниям. Так, у детей через 1—3 дня после рождения нормальный уровень гемоглобина максимален и составляет 145—225 г/л, а к 3—6 месяцам снижается до минимального уровня — 95—135 г/л, затем с 1 года до 18 лет отмечается постепенное увеличение нормального уровня гемоглобина в крови[5].
Во время беременности в организме женщины происходит задержка и накопление жидкости, что является причиной гемодилюции — физиологического разведения крови. В результате наблюдается относительное снижение концентрации гемоглобина (при беременности уровень гемоглобина в норме составляет 110—155 г/л). Кроме этого, в связи с внутриутробным ростом ребёнка происходит быстрое расходование запасов железа и фолиевой кислоты. Если до беременности у женщины был дефицит этих веществ, проблемы, связанные со снижением гемоглобина, могут возникнуть уже на ранних сроках беременности[6].
Главные функции гемоглобина: перенос кислорода и буферная функция. У человека в капиллярах лёгких в условиях избытка кислорода последний соединяется с гемоглобином. Потоком крови эритроциты, содержащие молекулы гемоглобина со связанным кислородом, доставляются к органам и тканям, где кислорода мало; здесь необходимый для протекания окислительных процессов кислород освобождается от связи с гемоглобином. Кроме того, гемоглобин способен связывать в тканях небольшое количество диоксида углерода (CO2) и освобождать его в лёгких.
Монооксид углерода (CO) связывается с гемоглобином крови намного сильнее (в 250 раз[7]), чем кислород, образуя карбоксигемоглобин (HbCO). Впрочем, монооксид углерода может быть частично вытеснен из гема при повышении парциального давления кислорода в лёгких. Некоторые процессы приводят к окислению иона железа в гемоглобине до степени окисления +3. В результате образуется форма гемоглобина, известная как метгемоглобин (HbOH) (metHb, от «мета-» и «гемоглобин», иначе гемиглобин или ферригемоглобин, см. Метгемоглобинемия). В обоих случаях блокируются процессы транспортировки кислорода.
Строение[править | править код]
Гемоглобин является сложным белком класса гемопротеинов, то есть в качестве простетической группы здесь выступает гем — порфириновое ядро, содержащее железо. Гемоглобин человека является тетрамером, то есть состоит из 4 протомеров. У взрослого человека они представлены полипептидными цепями α1, α2, β1 и β2. Субъединицы соединены друг с другом по принципу изологического тетраэдра. Основной вклад во взаимодействие субъединиц вносят гидрофобные взаимодействия. И α-, и β-цепи относятся к α-спиральному структурному классу, так как содержат исключительно α-спирали. Каждая цепь содержит восемь спиральных участков, обозначаемых буквами от A до H (от N-конца к C-концу).
Гем представляет собой комплекс протопорфирина IX, относящегося к классу порфириновых соединений, с атомом железа(II). Этот кофактор нековалентно связан с гидрофобной впадиной молекул гемоглобина и миоглобина.
Железо(II) характеризуется октаэдрической координацией, то есть связывается с шестью лигандами. Четыре из них представлены атомами азота порфиринового кольца, лежащими в одной плоскости. Две другие координационные позиции лежат на оси, перпендикулярной плоскости порфирина. Одна из них занята азотом остатка гистидина в 93-м положении полипептидной цепи (участок F). Связываемая гемоглобином молекула кислорода координируется к железу с обратной стороны и оказывается заключённой между атомом железа и азотом ещё одного остатка гистидина, располагающегося в 64-м положении цепи (участок E).
Всего в гемоглобине человека четыре участка связывания кислорода (по одному гему на каждую субъединицу), то есть одновременно может связываться четыре молекулы. Гемоглобин в лёгких при высоком парциальном давлении кислорода соединяется с ним, образуя оксигемоглобин. При этом кислород соединяется с гемом, присоединяясь к железу гема на 6-ю координационную связь. На эту же связь присоединяется и монооксид углерода, вступая с кислородом в «конкурентную борьбу» за связь с гемоглобином, образуя карбоксигемоглобин.
Связь гемоглобина с монооксидом углерода более прочная, чем с кислородом. Поэтому часть гемоглобина, образующая комплекс с монооксидом углерода, не участвует в транспорте кислорода. В норме у человека образуется 1,2 % карбоксигемоглобина. Повышение его уровня характерно для гемолитических процессов, в связи с этим уровень карбоксигемоглобина является показателем гемолиза.
Физиология[править | править код]
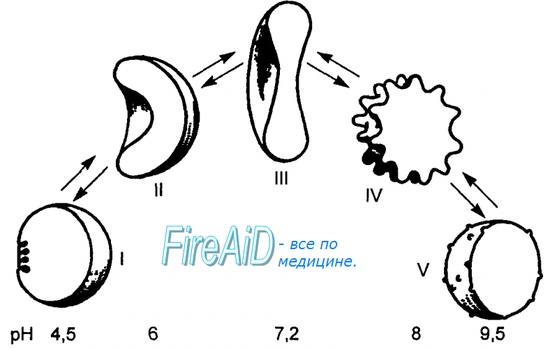
Изменение состояний окси- и дезоксигемоглобина
В отличие от миоглобина гемоглобин имеет четвертичную структуру, которая придаёт ему способность регулировать присоединение и отщепление кислорода и характерную кооперативность: после присоединения первой молекулы кислорода связывание последующих облегчается. Структура может находиться в двух устойчивых состояниях (конформациях): оксигемоглобин (содержит 4 молекулы кислорода; напряжённая конформация) и дезоксигемоглобин (кислорода не содержит; расслабленная конформация).
Устойчивое состояние структуры дезоксигемоглобина усложняет присоединение к нему кислорода. Поэтому для начала реакции необходимо достаточное парциальное давление кислорода, что возможно в альвеолах лёгких. Изменения в одной из 4-х субъединиц влияет на оставшиеся, и после присоединения первой молекулы кислорода связывание последующих облегчается.
Отдав кислород тканям, гемоглобин присоединяет к себе ионы водорода и углекислый газ, перенося их в лёгкие[8].
Гемоглобин является одним из основных белков, которыми питаются малярийные плазмодии — возбудители малярии, и в эндемичных по малярии районах земного шара весьма распространены наследственные аномалии строения гемоглобина, затрудняющие малярийным плазмодиям питание этим белком и проникновение в эритроцит. В частности, к таким имеющим эволюционно-приспособительное значение мутациям относится аномалия гемоглобина, приводящая к серповидноклеточной анемии. Однако, к несчастью, эти аномалии (как и аномалии строения гемоглобина, не имеющие явно приспособительного значения) сопровождаются нарушением кислород-транспортирующей функции гемоглобина, снижением устойчивости эритроцитов к разрушению, анемией и другими негативными последствиями. Аномалии строения гемоглобина называются гемоглобинопатиями.
Гемоглобин высокотоксичен при попадании значительного его количества из эритроцитов в плазму крови (что происходит при массивном внутрисосудистом гемолизе, геморрагическом шоке, гемолитических анемиях, переливании несовместимой крови и других патологических состояниях). Токсичность гемоглобина, находящегося вне эритроцитов, в свободном состоянии в плазме крови, проявляется тканевой гипоксией — ухудшением кислородного снабжения тканей, перегрузкой организма продуктами разрушения гемоглобина — железом, билирубином, порфиринами с развитием желтухи или острой порфирии, закупоркой почечных канальцев крупными молекулами гемоглобина с развитием некроза почечных канальцев и острой почечной недостаточности.
Ввиду высокой токсичности свободного гемоглобина в организме существуют специальные системы для его связывания и обезвреживания. В частности, одним из компонентов системы обезвреживания гемоглобина является особый плазменный белок гаптоглобин, специфически связывающий свободный глобин и глобин в составе гемоглобина. Комплекс гаптоглобина и глобина (или гемоглобина) затем захватывается селезёнкой и макрофагами тканевой ретикуло-эндотелиальной системы и обезвреживается.
Другой частью гемоглобинообезвреживающей системы является белок гемопексин[en], специфически связывающий свободный гем и гем в составе гемоглобина. Комплекс гема (или гемоглобина) и гемопексина затем захватывается печенью, гем отщепляется и используется для синтеза билирубина и других жёлчных пигментов, или выпускается в рециркуляцию в комплексе с трансферринами для повторного использования костным мозгом в процессе эритропоэза.
Экспрессия генов гемоглобина до и после рождения.
Также указаны типы клеток и органы, в которых происходит экспрессия гена (данные по Wood W. G., (1976). Br. Med. Bull. 32, 282.).[9]
Гемоглобин при заболеваниях крови[править | править код]
Дефицит гемоглобина может быть вызван, во-первых, уменьшением количества молекул самого гемоглобина (см. анемия), во-вторых, из-за уменьшенной способности каждой молекулы связать кислород при том же самом парциальном давлении кислорода.
Гипоксемия — это уменьшение парциального давления кислорода в крови, её следует отличать от дефицита гемоглобина. Хотя и гипоксемия, и дефицит гемоглобина являются причинами гипоксии.
Если дефицит кислорода в организме в общем называют гипоксией, то местные нарушения кислородоснабжения называют ишемией.
Прочие причины низкого гемоглобина разнообразны: кровопотеря, пищевой дефицит, болезни костного мозга, химиотерапия, отказ почек, атипичный гемоглобин.
Повышенное содержание гемоглобина в крови связано с увеличением количества или размеров эритроцитов, что наблюдается также при истинной полицитемии. Это повышение может быть вызвано: врождённой болезнью сердца, лёгочным фиброзом, слишком большим количеством эритропоэтина.
См. также[править | править код]
- Гемоглобин А
- Гемоглобин С (мутантная форма)
- Эмбриональный Гемоглобин (эмбриональный)
- Гемоглобин S (мутантная форма)
- Гемоглобин F (фетальный)
- Кобоглобин
- Нейроглобин
- Анемия
- Порфирия
- Талассемия
- Эффект Вериго — Бора
Примечания[править | править код]
- ↑ Haemoglobins of invertebrate tissues. Nerve haemoglobins of Aphrodite, Aplysia and Halosydna
- ↑ Ученые выяснили происхождение гемоглобина. РИА Новостей, 20.05.2020, 18:59
- ↑ Michael Berenbrink. Evolution of a molecular machine/Nature, NEWS AND VIEWS, 20 MAY 2020
- ↑ Лауреаты нобелевской премии. Макс Перуц.
- ↑ Назаренко Г. И., Кишкун А. А. Клиническая оценка результатов лабораторных исследований. — 2005.
- ↑ Общий анализ крови и беременность Архивная копия от 10 марта 2014 на Wayback Machine
- ↑ Hall, John E. Guyton and Hall textbook of medical physiology (англ.). — 12th ed.. — Philadelphia, Pa.: Saunders/Elsevier, 2010. — P. 1120. — ISBN 978-1416045748.
- ↑ Степанов В. М. Структура и функции белков : Учебник. — М. : Высшая школа, 1996. — С. 167—175. — 335 с. — 5000 экз. — ISBN 5-06-002573-X.
- ↑ Айала Ф., . Современная генетика: В 3-х т = Modern Genetics / Пер. А. Г. Имашевой, А. Л. Остермана, . Под ред. Е. В. Ананьева. — М.: Мир, 1987. — Т. 2. — 368 с. — 15 000 экз. — ISBN 5-03-000495-5.
Литература[править | править код]
- Mathews, CK; KE van Holde & KG Ahern (2000), Biochemistry (3rd ed.), Addison Wesley Longman, ISBN 0-8053-3066-6
- Levitt, M & C Chothia (1976), “Structural patterns in globular proteins”, Nature
Ссылки[править | править код]
- Eshaghian, S; Horwich, TB; Fonarow, GC (2006). “An unexpected inverse relationship between HbA1c levels and mortality in patients with diabetes and advanced systolic heart failure”. Am Heart J. 151 (1): 91.e1—91.e6. DOI:10.1016/j.ahj.2005.10.008. PMID 16368297.
- Kneipp J, Balakrishnan G, Chen R, Shen TJ, Sahu SC, Ho NT, Giovannelli JL, Simplaceanu V, Ho C, Spiro T (2005). “Dynamics of allostery in hemoglobin: roles of the penultimate tyrosine H bonds”. J Mol Biol. 356 (2): 335—53. DOI:10.1016/j.jmb.2005.11.006. PMID 16368110.
- Hardison, Ross C. (2012). “Evolution of Hemoglobin and Its Genes”. Cold Spring Harbor Perspectives in Medicine. 2 (12): a011627. DOI:10.1101/cshperspect.a011627. ISSN 2157-1422. PMC 3543078. PMID 23209182.
Органические фосфаты, особенно 2,3-дифосфоглицерат (ДФГ), также оказывают влияние на сродство гемоглобина к кислороду. [c.171]
Численно сродство гемоглобина к кислороду принято выражать величиной Р д-парциальное напряжение кислорода, при котором 50% гемоглобина связано с кислородом (pH 7,4 температура 37°С). Нормальная величина Рз около 34,67 гПа (см. рис. 17.6). Смещение кривой насыщения гемоглобина кислородом вправо означает уменьшение способности гемоглобина связывать кислород и, следовательно, сопровождается повышением Рз . Напротив, смещение кривой влево свидетельствует о повышенном сродстве гемоглобина к кислороду, величина Рз снижена. [c.594]
РЕГУЛЯЦИЯ СРОДСТВА ГЕМОГЛОБИНА К КИСЛОРОДУ [c.364]
Возрастание интенсивности окислительных процессов в тканях, например при усиленной мышечной работе всегда связано с более полным извлечением кислорода из крови. Кроме того, при физической работе резко увеличивается скорость кровотока. Зависимость между степенью насыщения гемоглобина кислородом и Р ,, можно выразить в виде кривой насыщения гемоглобина кислородом, или кривой диссоциации оксигемоглобина, которая имеет 8-образную форму и характеризует сродство гемоглобина к кислороду (рис. 17.6). [c.593]
Ход кривой насыщения гемоглобина кислородом или диссоциации оксигемоглобина зависит от ряда факторов. Сродство гемоглобина к кислороду в первую очередь связано с pH. Чем ниже pH, тем меньше способность гемоглобина связывать кислород и тем выше Рз . В тканевых капиллярах pH ниже (поступает большое количество СО,), в связи с чем гемоглобин [c.594]
Способность гемоглобина связывать кислород зависит также от температуры. Чем выше температура (в тканях температура выше, чем в легких), тем меньше сродство гемоглобина к кислороду. Напротив, снижение температуры вызывает обратные явления. [c.595]
Сродство гемоглобина к кислороду зависит от величины pH и содержания СОг. [c.171]
Влияние СОг, Н+ и ДФГ на сродство гемоглобина к кислороду и на кооперативность функционирования ассоциированных гемоглобиновых субъединиц описаны в гл. 5 (разд. 5.5.2). [c.406]
TOB промежуточного обмена, зависимых от АТФ. Они также угнетают активность некоторых ферментов, участвующих в гликолизе эритроцитов, и снижают содержание 2,3 – дифосфоглицерата красных кровяных клеток. В результате увеличивается сродство гемоглобина и кислорода, что может уменьшить поступление кислорода к тканям. [c.521]
Способность гемоглобина связывать кислород зависит от ряда факторов. Было обнаружено, в частности, что на связывание гемоглобином кислорода большое влияние оказывает pH среды и содержание СО . В тканях, где значение pH несколько меньшее по сравнению с легкими, а концентрация Oj достаточно высока, сродство гемоглобина к кислороду снижается, кислород отделяется, а Oj и протон водорода присоединяются к гемоглобину. Напротив, в альвеолах легких при освобождении Oj происходит повышение pH и сродство гемоглобина к кислороду увеличивается (рис. 3.18). Этот феномен называется эффектом Бора в честь ученого, впервые открывшего это явление. В реализации данного эффекта кроме гемоглобина и кислорода участвуют СО2 и протон водорода. Дезоксигемоглобин представляет собой прото-нированную форму пигмента. Реакцию оксигенации можно записать следующим образом [c.51]
Окись углерода является одним из самых опасных ядов. Она имеет в 300 раз большее сродство с гемоглобином, чем кислород. Попав через легкие в кровь, она очень легко соединяется с гемоглобином крови, вытесняя кислород. Кровь теряет способность доставлять тканям необ одимый для жизни кислород, вследствие чего наступает кислородное голодание. Кроме того, окись углерода оказывает непосредственное отравляющее действие на центральную нервную систему. [c.729]
Уже давно известно, что 2,3-дифосфоглицерат (рис. 1) присутствует в эритроцитах в довольно высоких концентрациях, однако функция этого соединения оставалась загадкой до тех пор, пока не было обнаружено, что он оказывает сильное влияние на сродство гемоглобина к кислороду. При добавлении 2,3-дифосфоглицерата (ДФГ) к раствору [c.211]
Другим физиологически важным свойством гемоглобина является увеличение его кислотности при насыщении кислородом. Обратный процесс — уменьшение сродства гемоглобина к кислороду при его окислении в среде с физиологическим pH — [c.422]
Например, из данных рис. 156 ясно видно, что в реакции гемоглобина с кислородом принимают участие четыре участка. Их легко идентифицировать как четыре атома железа в этой макромолекуле, так как известно много металлосодержащих комплексных соединений, способных связывать молекулярный кислород. Большинство из них—комплексы Со ” , однако известен также ряд комплексов Ре ” , обладающих этим же свойством. Вместе с тем неизвестен ни один комплекс Ре-” , сродство которого к О2 было бы равно сродству Ре , содержащегося в гемоглобине. [c.617]
Водородные ионы могут вызывать еще один отрицательный эффект, опять-таки сходный с механизмом воздействия некоторых отрицательных модуляторов на ферментативный катализ. Снижение pH может уменьшать и максимальную способность гемоглобина связывать кислород, т. е, ион водорода понижает не только сродство гемоглобина к О2, но и характеристику, аналогичную l max- для ферментов (рис. 115,5). Это влияние pH на кислородную емкость гемоглобина называют эффектом Рута. Сильно выраженный эффект Рута часто сопутствует большому эффекту Бора. [c.364]
В регуляции сродства гемоглобина к кислороду могут также участвовать низкомолскулярные вещества, образующиеся внутри эритроцитов. Например, в эритроцитах млекопитающих сродство НЬ к О2 уменьшается с увеличением концентрации [c.364]
Это наблюдается в подвергнутых электродиализу бессолевых растворах белка [20, 53]. Соединение двуокиси углерода с гемоглобином имеет большое значение в физико-химическом равновесии крови, поскольку в присутствии углекислоты сродство гемоглобина к кислороду снижается — явление, хорошо известное в физиологии. Влияние углекислоты на сродство гемоглобина к кислороду обусловлено тем, что двуокись углерода соединяется с основными аминогруппами или имидазольными группами, расположенными в непосредственной близости к атому железа, к которому присоединяется кислород [52, 54]. [c.88]
Синтезированная недавно модель кобальтзамещенного гемоглобина приведена на схеме 6.1 [245]. Длинная боковая цепь обеспечивает координацию пиридинового кольца с центральным атомом кобальта. Комплекс Со(П) и этого так называемого петлеобразного порфирина обратимо реагирует с молекулярны.м кислородом при низких температурах (от —30 до — G0° ), но боковая цепь лишь в незначительной степени увеличивает сродство кислорода к таким модельным соединениям по сравнению с жслсзопорфириновыми системами. [c.371]
НОМ очень сильное влияние оказывает pH и концентрация СО2 связывание СО2 и ионов Н снижает способность гемоглобина связывать О2. В периферических тканях с относительно низким значением pH и высокой концентрацией СО2 сродство гемоглобина к кислороду падает по мере связывания СО2 и ионов Н . И наоборот, в легочных капиллярах выделение СО2 и сопутствующее ему повышение pH крови приводит к увеличению сродства гемоглобина к кислороду. Это влияние величины pH и концентрации СО2 на связывание и освобождение кислорода гемоглобином назьшают эффектом Бора в честь датского физиолога Христиана Бора, впервые открьшшего этот эффект. [c.209]
В тетрамерном гемоглобине сродство гема к Оа контролируется концентрациями О2, СО2, и 2,3-дифосфоглицерата. Что же было достигнуто в результате эволюции мономерного гемоглобина типа миоглобина в сложный гемоглобин млекопитающих Основное преимущество заключается в возросшей физиологической приспособляемости тетрамерного белка, которая достигнута за счет постепенного перевода сродства к кислороду, свойственного центру связывания, под контроль внеии1их влияний [276, 549, 667] (рис. 10.4). [c.257]
Дана зависимость насыщения гемоглобина (НЬ) кислородом при pH 7,2 от концентрации свободного кислорода. Концентрации 0 в капиллярах легких (125 мкМ) н в капиллярах тканей, потребляющих (50 мкМ), зафиксированы в узких пределах. Кривая а в отсутствие дифосфоглицерата (ДФГ) гемоглобин насыщается О в легких, но не может доставлять его к тканям. Кривая б прн физиологическом уровне ДФГ (4.5 мМ. приблизительно 30% Оа. поглощенного легкими, высвобождается в тканях (стрелка 1). Кривые бив поскольку гемоглобин плода (кривая в) имеет более низкое сродство к ДФГ. чем материнский гемоглобин, освобожденный из материнской крови молекулярный кислород может захватываться гемоглобином плода (стрелка [[I). Кривая г высокая концентрация ДФГ (8 мМ) приводит к повышенному снабжению тканей кислородом (стре.жи I и [[). Кривая д при отсутствии кооператнвиостн между субъединицами гемоглобина от легких к тканям транспортировалось бы меньше Оз. При построении гипотетической кривой связывания (5) для комплекса НЬОз принята константа диссоциации 38 мкМ. [c.258]
Физиологический смысл S-образности кривой У(р) для НЬ состоит в падении сродства гемоглобина к кислороду по мере отщепления его молекул. Изменения парциального давления О2 в тканях должны быть невелики. Если бы для гемоглобина была характерна гиперболическая кривая Y(p), подобная кривой Y(р) для миоглобина, то лищь малая доля переносимого О2 отщеплялась бы в тканях. [c.425]
Важной особенностью гемоглобина, которая обусловлена наличием нескольких гем-групп, является форма кривой связывания кислорода не простая гиперболическая кривая насыщения, как для миоглобина, а S-образная. Сродство гемоглобина к кислороду возрастает с давлением. Поэтому при умеренных давлениях гемоглобин эффективно связывает кислород в легких, но отдает его миоглобину при низких давлениях в тканях. При потере кислорода образуется дезоксигемоглобин, субъединицы молекулы слегка смещаются относительно друг друга и поворачиваются так, что два р-гема удаляются друг от друга на расстояние около 6,5 А. Эта конформационная перестройка, несомненно, тесно связана с кооперативным взаимодействием гемов, которое позволяет им более прочно связывать кислород, когда молекула уже частично окислена. Однако детали этого взаимодействия еще не ясны. В концентрированных солевых растворах (например, в 4 М Na l) молекула [c.375]
Рассмотренным выще сезонным изменениям сродства гемоглобина к кислороду на эволюционном уровне соответствует генетическая адаптация эктотермных организмов к различным температурным режимам. Гемоглобины эктотермных видов способны присоединять и отдавать кислород именно при тех условиях температуры и содержания Ог в среде, которые типичны для местообитания данного вида. Это обусловлено сильным давлением отбора в пользу таких величин Р о, которые достаточно низки для того, чтобы кислород мог эффективно связываться у дыхательных поверхностей, но еще достаточно высоки, чтобы он мог легко освобождаться в более глубоких тканях. Эту эволюционную адаптацию иллюстрируют графики на рис. 118. Так же как и в случае эволюционной адаптации ферментов к температуре, где отбор благоприятствует ферментам с подходящими величинами Км. или 5о,5, выработка хорощо адаптированных гемоглобинов, по-видимому, требует изменений в первичной структуре их полипептидных цепей. Попутно следует заметить, что гем оказался одним и тем же во всех исследованных гемоглобинах. Таким образом, гем, который мы могли бы назвать почетным коферментом гемоглобина, аналогичен настоящим коферментам вроде, например, НАД или НАДФ, которые тоже обнаруживают одни и те же химические и функциональные свойства независимо от того, какие изменения происходят в связанной с ними белковой цепи (или цепях). [c.374]
Но теперь снова возникает ряд вопросов. В чем состоит особенность структуры гемоглобина, обеспечивающая эти выгодные для организма изменения сродства гемоглобина к кислороду, находящиеся в обратной зависимости от его сродства к СО2 и ионам Н Как информация о связывании лиганда передается от одной полипептвдной субъединицы гемоглобина к другой Почему гемоглобин обладает такими свойствами, а миоглобин нет [c.210]
ЧИСТОГО гемоглобша сродство гемоглобина к кислороду значительно снижается. Этот эффект обусловлен тем, что ДФГ сам связывается с дезоксигемоглобином. Следовательно, можно написать уравнение еще одной (четвертой по счету) реакции связьшания гемоглобина с лигандом [c.212]
Регулирующее влияние ДФГ на сродство гемоглобина к кислороду в эритроцитах зависит от величины парциального давления кислорода в легких. После того как здоровый человек поднимется, скажем, на высоту 4000 м над уровнем моря, в течение первых нескольких часов концентрация ДФГ в его эритроцитах будет возрастать при этом число молекул ДФГ, связанных с >гемоглобином, увеличится, а сродство гемоглобина к кислороду снизится. На большой высоте парциальное давление кислорода значительно ниже, чем на уровне моря. Поэтому и в тканях парциальное давление кислорода снижается. Увеличение содержания ДФГ в эритроцитах при восхождении на большую высоту облегчает освобождение кислорода из гемоглобина в тканях. Изменения противоположного характера наблюдаются у людей, акклиматизировавшихся к условиям высокогорья, например у жителей Гималаев или Андов, когда они спускаются в долины. Повьш1ение концентрации [c.212]
При обычном вьзделении гемоглобина из крови он содержит довольно большое количество ДФГ, от которого трудно освободиться полностью. При полном удалении ДФГ из гемоглобина кривая связывания его с кислородом в значительной степени утрачивает свою сигмоидную форму и гемоглобин приобретает намного более высокое сродство к кислороду. После добавления избытка ДФГ к гемоглобину способность последнего к связыванию кислорода понижается (рис. 2). Таким образом, присутствие ДФГ весьма существенно для нормального освобождения кислорода из гемоглобина в тканях. В эритроцитах некоторых птиц содержится не ДФГ, а другое фосфатсодержащее со-единенш-инозитолгексафосфат, который даже еще более эффективно, чем ДФГ, снижает сродство гемоглобина к кислороду. [c.213]
Р тщательно удалить весь 2,3-дифосфоглицерат (ДФГ), кривые их насыщения кислородом сместятся влево (т.е. сродство гемоглобинов к кислороду повысится). Однако у гемоглобина А сродство к кислороду при этом становится выше, чем у гемоглобина Р. Если в препараты гемоглобина вновь добавить ДФГ, то кривые насьпцения кислородом примут прежний вид, показанный на рисунке. Какое влияние оказывает ДФГ на сродство гемоглобина к кислороду Как на основе приведенной вьппе информации можно объяснить различие в сродстве к кислороду у гемоглобинов матери и плода [c.225]
Важным регулятором степени оксигенирования гемоглобина служит 2,3-бис-фосфоглицерат (БФГ). Чем выше концентрация БФГ в клетке, тем ниже сродство гемоглобина к кислороду. В случаях когда доставка кислорода в ткани оказывается хронически недостаточной, как это бывает у людей с пониженным содержанием эритроцитов в крови или у обитателей высокогорья, концентрация БФГ в эритроцитах оказывается выше, чем у здоровых людей, живуцщх на уровне моря. Этот биохимический сдвиг способствует тому, что гемоглобин легче отдает тканям связанный кислород, и тем самым компенсируется снижение количества кислорода, связываемого гемоглобином в легких. [c.769]
Физиологический смысл 5-сбразной формы кривой на рис. 31 состоит в том, чтобы помочь гемоглобину освободиться от кислорода в процессе переноса его в клетки ткани там и тогда, где и когда кислород более необходим, а именно там, где парциальное давление кислорода минимально. Большинство типичных гемоглобйнов обнаруживает и другие необычные вариации Р1/2, которые также выполняют определенную физиологическую функцию. На рис. 32 показано, как меняется lg l/2 в зависимости от pH. Это так называемый эффект Бора. Выше pH

