Резервная щелочность крови норма
25 07 2016
Виктор Боченков
Пока нет комментариев
Здравствуйте постоянные читатели и гости блога. Сегодня продолжаем разговор о сбалансированном кормлении в молочном скотоводстве. Вновь затронем тему о биохимических показателях крови у КРС, а в частности поговорим более подробно о таком показатели, как резервная щелочность в крови у коров.
В начале марта на блоге была опубликована общая статья о биохимии крови у коров. Кто не читал, заходим по ссылке.
И как обещал, делюсь с вами своими результатами. Тем более что прошло 3 месяца и можно уже о чем то говорить по существу. Так как показателей в крови довольно много я решил сконцентрироваться на одном – это резервная щелочность.
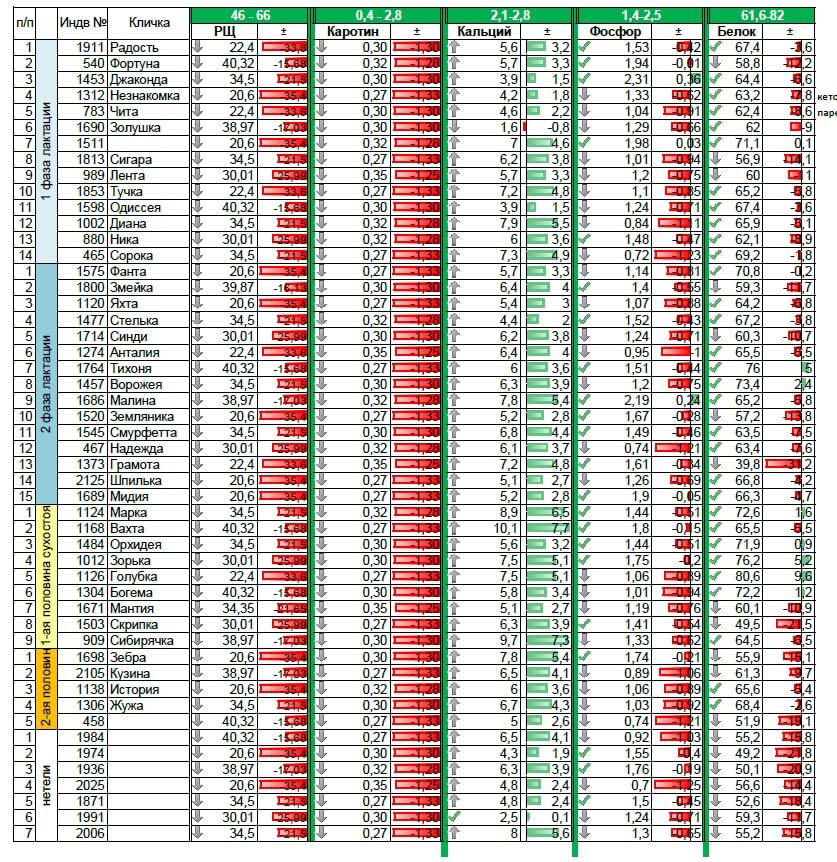
Напомню, что этот показатель отвечает за кислотно-щелочное равновесие в организме ваших коров. В моем случае этот показатель был явно ниже нормы и равен 30% (норма 46-66%).

биохимия в марте. нажми чтобы увеличить
А вот результат исследования крови через три месяца:
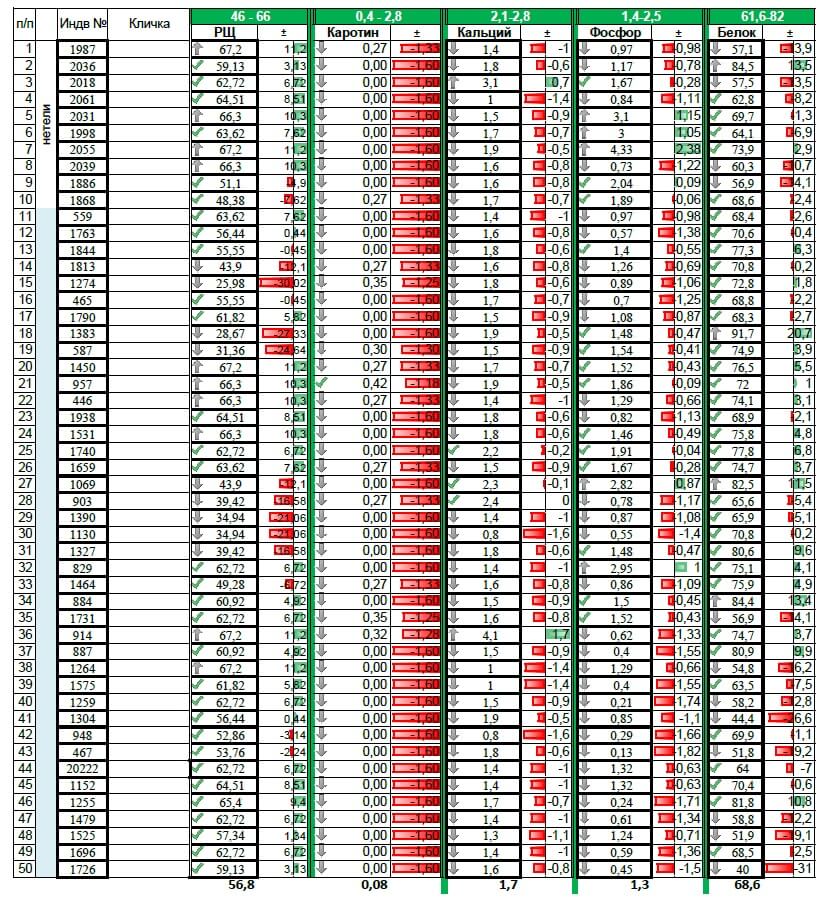
биохимия в июне, нажми чтобы увеличить
Как видно из таблицы 36 проб из 50 в пределах нормы (72%), 9 проб – ниже нормы(18%) и 5 проб явно выше нормы (10%).
Перейти с 0% на 72% я считаю достойным результатом. И вы конечно спросите меня «Как этого добиться?». Довольно просто!
Пути снижения резервной щелочности в организме у коров
В этом деле вам поможет пищевая сода, он же карбонат натрия (Na2CO3), который в пищевой промышленности носит название пищевая добавка E200. Пищевая сода способна нейтрализовать кислоты в силосе.
Кто не знает, силос в своем составе содержит несколько групп кислот: муравьиная, уксусная и масляная. Собственно они и влияют на pH корма. Если pH силоса равен 3,8-3,99, то он считается кислым, если 3,6-3,8 – очень кислым, при pH равном 4-4,2 умеренно кислым.
В моем случае средняя pH силоса составляет 4,4.
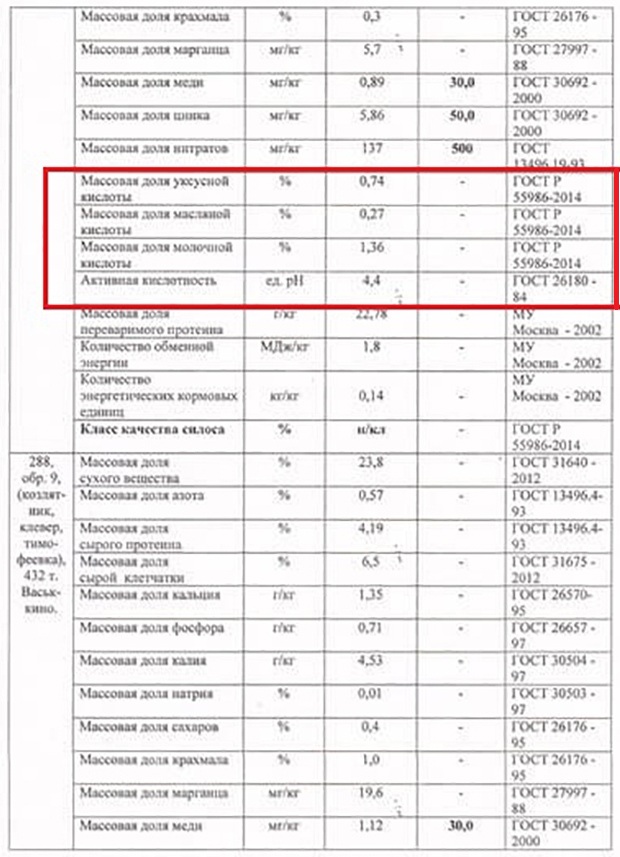 А теперь представьте, что корова все эти кислоты пропускает через свой организм. Для наибольшей наглядности средняя сумма активных кислот в моем силосе составляет 2,37%. (нужно сложить долю масляной, уксусной и муравьиной кислот).
А теперь представьте, что корова все эти кислоты пропускает через свой организм. Для наибольшей наглядности средняя сумма активных кислот в моем силосе составляет 2,37%. (нужно сложить долю масляной, уксусной и муравьиной кислот).
Возьмем, к примеру, что корова потребляет 25 кг силоса в сутки. 25 кг * 2,37%/100% = 0,592.
592 грамма органических кислот поступает в организм коровы каждый день!!!
Добавим к этому нагрузку печени из-за концентратов. Так как комбикорма и зерно содержат в своем составе крахмал, который в процессе ферментации в пищеварительном тракте так же образует кислоты.
В результате получаем предрасположенность коров к ацидозу.
 Полистав каталог своего поставщика примексов и минеральных добавок для коров («АгроБалт Трейд» Ленинградская область), я наткнулся на буферную смесь, которая содержит в своем составе соду, минералы и ароматизаторы. Норма ввода 100-300 грамм в сутки. Подача в составе кормосмеси или дробная с первыми утренними порциями концентратов, по силосу.
Полистав каталог своего поставщика примексов и минеральных добавок для коров («АгроБалт Трейд» Ленинградская область), я наткнулся на буферную смесь, которая содержит в своем составе соду, минералы и ароматизаторы. Норма ввода 100-300 грамм в сутки. Подача в составе кормосмеси или дробная с первыми утренними порциями концентратов, по силосу.
Но после первой поставки мне подсказали, что можно использовать и пищевую соду в кормлении коров. Собственно с поставкой и этого продукта помогли те же самые партнеры.
В сутки одной корове скармливают по 100–150 г соды, а животным, имеющим склонность к ожирению, — до 250 г. Стельным сухостойным коровам за три недели до отела, а также новотельным в первую неделю после отела соду из рациона исключают, т. к. избыток натрия способствует отекам вымени.
Свойства пищевой соды:
— создание оптимальных условий для микрофлоры рубца, увеличивается переваримость клетчатки и органических веществ
— быстрая адаптация коров к высокоэнергетическому корму
— снижение отрицательного влияния корма, повышающих кислотность
Особой разницы в поедаемости буферной смеси и соды я не увидел. А вопрос цены незначительный, но все же есть.
Буферная смесь стоит 28,80 рублей за 1 кг, сода – 25,50 рублей.
 Должен так же отметить, что рационы коровы должны содержать минимум 2 кг сена, его наличие нормализует жвачку и стимулирует образование слюны, что является профилактикой ацидоза.
Должен так же отметить, что рационы коровы должны содержать минимум 2 кг сена, его наличие нормализует жвачку и стимулирует образование слюны, что является профилактикой ацидоза.
Что помимо от хорошего самочувствия коров получило хозяйство?
Напомню, что балансировать рацион по резервной щелочности и другим элементам я начал с марта 2016 года.
Но давайте посмотрим на процент плодотворного осеменения коров с этого момента:

нажми, чтобы увеличить
Как видим — он вырос. Может быть, этому способствовали и другие факторы, но кормление я не стал бы сбрасывать со щитов.
На данном этапе я не собираюсь останавливаться, и теперь все мое внимание нацелено на выравнивание соотношения кальция и фосфора в рационе коров. Оба показателя пока ниже нормы.
Как я это буду делать вы сможете узнать из новых статей, поэтому подписывайтесь на обновления блога и будете в курсе всех новостей.
На этом у меня все, берегите своих коров и будьте здоровы!
© 2020 Молочный фермер · Копирование материалов сайта без разрешения запрещено
Дизайн и поддержка: GoodwinPress.ru
Что нужно знать для балансировки рациона коровам? Это не только химический анализ кормов, но биохимические показатели крови крс. В ходе исследований можно увидеть реальную картину обмена веществ у животных.
Если вы не знаете, что такое биохимические исследования проб сыворотки крови, обратитесь к своему ветеринарному врачу. У него наверняка есть похожий документ, который я выложил здесь ниже. Если нет, срочно с ветеринарной службой исследуйте кровь стада. Это даст ответы на многие вопросы.
Биохимический анализ крови – это метод лабораторный диагностики, который позволяет определить работу внутренних органов, получить информацию о метаболизме (обмене веществ) и выяснить потребность в макроэлементах.
Если вам сложно уловить суть, то попробуйте перевести данную проблему на самого себя.
Вы заболели, пошли в поликлинику, записались к врачу на прием. Что первым делом он просит вас сделать? Правильно! Сдать анализы.
Вот и в животноводстве все аналогично. Только необходимо работать на опережение. Увидев картину биохимии, зоотехник может подкорректировать рацион под потребность животного.
А за этим следует улучшение здоровья и, как правило, увеличение продуктивности.
Хочу отметить, что пробы крови, представленные в документе, взяты от проблемных коров. К примеру, у коровы по кличке Аура был кетоз. Данное заболевание подтвердило наличие кетоновых тел в сыворотки крови.
Правильнее будет взять пробы крови у нескольких физиологических групп:
- нетели
- коровы в фазу раздоя
- коровы второй половины лактации
- сухостой первой половины
- сухостой второй половины
Кальций – является основным элементом в строении костной ткани, крови, нервной и мышечной ткани.
Фосфор, так же как и кальций, основа костной ткани. Участвует в обмене жиров и углеводов. Данный элемент необходим для нормального развития микроорганизмов в рубце коровы.
«Недостаток кальция и фосфора в организме животных может привести к рахиту, остеомаляции, остеопорозу, остеофиброзу».
Белок (он же протеин) – главная составляющая всех живых клеток. Протеин участвует во всех жизненно важных процессах: размножении, росте, развитии, продуктивности, а так же является основным компонентом ферментов, гормонов и иммунных тел.
Как видите, роль белка в организме значима, более подробно о роли протеина и других элементов, мы еще поговорим в отдельных статьях на блоге.
Резервная щелочность – по сути это показатель кислотно-щелочного соотношения в организме.
«Количество двуокиси углерода (мл), которое может связать100 мл плазмы крови»
Снижение данного параметра говорит о сдвиге кислотно-щелочного равновесия в сторону ацидоза, повышение — в сторону алкалоза.
Каротин – является провитамином (биохимическим предшественником витамина А). Витамин А участвует в развитии и росте клеток, обеспечивает нормальное состояние слизистых оболочек, поддерживает зрительные функции.
Кетоновые тела – промежуточные продукты обмена веществ белков, жиров и углеводов, которые образуются в печени. Это бета-оксимасляная кислота, ацетоуксусная кислота, ацетон. Повышенный уровень таких веществ говорит о нарушении обмена веществ.
НОРМЫ БИОХИМИЧЕСКИХ ПОКАЗАТЕЛЕЙ КРОВИ У КОРОВ
- кальций 2,5 – 3,13 ммоль/л
- фосфор 1,45 – 1,94 ммоль/л
- белок 72- 86 г/л
- каротин 0,4 – 1,0 мг%
- резервная щелочность 46 -66%
Отлично. У нас есть результаты анализов. Мы знаем, на что влияет каждый показатель. Осталось только решить – что с этим делать?
На мой взгляд, есть три варианта развития событий.
1. Постараться сбалансировать рацион, что на практике, практически нереально. Улучшать кормовую базу при заготовке силоса, сенажа, сена. Обратить внимание видовой состав трав (отдать предпочтение сахару или протеину).
2. Включить в рацион животных кормовые добавки, которыми заполнен наш рынок. Здесь только вопрос цены и качества. К примеру, поставщик примексов в мое хозяйство, разработал минеральную добавку, чтобы восполнить пробелы в рационе.
3. Попробуйте найти медикаментозный выход. К примеру, существует множество препаратов, которые содержат витамин А (карток, карсел, элеовит, карофертин, каролин и др). Почему бы вам таким способом не восполнить дефицит данного витамина?
Надеюсь, что данная статья будет для вас полезной. Занимайтесь профилактикой заболеваний в стаде и надои ваших буренок обязательно вырастут!
Поддержите статью лайком и подписывайтесь на канал, чтобы не пропустить новые публикации!
Оригинальная статья на milkfermer.ru
Приглашаем посетить сайт
РЕЗЕРВНАЯ ЩЕЛОЧНОСТЬ
РЕЗЕРВНАЯ ЩЕЛОЧНОСТЬ, по Ван-Слайку (см. Ван-Слайка методы)-объем углекислоты, к-рый может быть выделен из 100 смг венозной крови или кровяной плазмы, предварительно насыщенной при комнатной t° альвеолярным воздухом или углекислотой при напряжении в 40 мм Hg.-Понятие о Р. щ. было впервые введено в 1892 г. Жаке (Jaquet) и в 1917 г. снова применено Ван-Слайком. В 1877 г. Вальтером (Walter) была показана на собаках зависимость между кислотной интоксикацией и содержанием бикарбонатов в крови; он нашел, что содержание углекислоты в крови пропорционально количеству несвязанных оснований и что оно уменьшается соответственно коли-«=*
честву введенной к-ты. Позднее /jf S
в 1905 г. Бор (Bohr) и в 1908- /И* 1)
1909 году Гендерсон (Henderson) показали, что углекислота, находящаяся в крови в виде бикарбонатов (ВНС03), в норме составляет около 95% всей углекислоты крови. В 1883 г. Штадель-ман (Stadelmann) применил наблюдение Вальтера в клинике- он отметил сходство между картиной диабетич. комы и кислотной интоксикацией и нашел увеличенное выделение организмом к-т при коме и в прекоматозном состоянии. Им же была предложена в качестве леч. средства NaHC03. Ряд авторов в 1920 году наблюдал сильное повышение содержания бикарбонатов в крови собак, у к-рых привратник был закрыт и к-рым производилось в течение нескольких дней промывание желудка, обусловливающее большую потерю НС1. Выражения «бикарбонаты крови», «способность связывать углекислоту» применяются для определения того же, что теперь понимают под термином резервная щелочность. Р. щ. представляет количество оснований, оставшихся после нейтрализации их нелетучими кислотами, и представляет показатель того резерва щелочей, который может быть связан добавочно углекислотой. Нормальные колебания Р. щ., по Ван-Слайку, 55-70% (эквивалентно 23-32 миллимолям ВНС03 на 1 л); для детей нормальные количества несколько ниже. По Шлоссу, у детей грудного возраста Р. щ. выражается в 46-63%. Постоянные цифры держатся приблизительно до 4-5 лет. Дальше отмечается прогрессивное повышение до цифр взрослого. При определении СО 2 плазмы получаемый результат до известной степени зависит от того, как получена плазма, под парафином или путем отделения эритроцитов и последовательным насыщением ее углекислотой.- Содержание С02 в крови может быть определено при помощи аппарата Баркрофта или Ван-Слайка методом (см.). При насыщении плазмы углекислотой при 40 мм давления и 38° содержание Н2С03 * соответствует 2,75 объемн. %, или 1,23 миллимоля Н2С03 на 1 л .Общее количество С02 эквивалентно ВНС03+Н2С03; вычитая из этой величины

1,23 миллимоля Н2С03>, получают содержание ВНС03 (см. Бикарбонаты), Помимо определения Р. щ. объемным путем за последнее время часто пользуются манометрическим методом: Извлеченные газы приводятся к определенному объему, и количество их определяют по давлению, отсчитываемому по манометру. Это делает определение более точным, не зависящим от барометрического давления. Преимущество этого метода в том, что исследователь может подбирать измеряемые объем и давление так, чтобы ошибки определения объема и давления были равны. Точность определения делается т. о. независимой от содержания С02.
Аппарат (см. рисунок). Пипетка А имеет две отметки для установки на а в 0,5 см? и а’ в 2 cms. Определение производится следующим образом: г/2–1 см3 крови или плазмы впускают через кран В, смывают остаток крови водой, прибавляют 0,2 смг n-раствора молочной к-ты, свободной от С02. Путем опускания уравнительной груши С образуется Торичеллиева пустота и путем двухминутного встряхивания извлекаются газы. Объем газа приводится к а или а’; давление рх отсчитывается на манометре D. В пипетку вводится для поглощения выделенной С02 0,2 ем3 5п-раствора NaOH и давление рг отсчитывается после приведения газов до прежнего объема. Давление Р для углекислоты т. о. равно pcot = Pi- Ра-Определение бикарбонатов плазмыможет быть произведено титрованием (Van Slyke, Still-man, Cullen). Принцип основан на определении количества НС1, необходимого для переведения NaHC03 плазмы в NaCl; pH должно быть в конце титрования тем же, как и в первоначальной плазме, чтобы предотвратить участие в реакции других буферов кроме ВНС03. К плазме добавляют избыток n/100 HC1, удаляют свободную СО 2 и титруют n/100 NaOH до первоначального рН=7,4. Индикатор фенолсуль-фофталеин. Титрование не дает таких точных результатов, как газиметрический метод, особенно при применении манометрического аппарата, однако расхождение редко больше, чем на 0,3 миллимоля ВНС03на .1 л (=0,7 об. % С02). Простое титрование плазмы или крови не определяет истинной (активной) реакции (см. Активная реакция), т. к. им определяется не только количество свободных, диссоциированных ионов, но также и потенциальные ионы, т. е. освобождающиеся при протекании титрования (см. Буферные свойства).-Уменьшение Р. щ. одно время рассматривалось как достаточный признак для диагноза ацидоза, но хотя это в большинстве случаев и справедливо, оно может иногда привести к неправильному заключению, т. к. уменьшение Р. щ. указывает лишь на падение связанной С02, но не указывает на взаимоотношения ВНС03 и свободной угольной к-ты, которые лишь совокупно определяют состояние ще л очно-кислотно го соотношения и влияют на активную реакцию (см. Ацидоз- ацидоз крови, и Кровь-физ.-хим. свойства крови). Названия ацидоз_ и алкалез применяются к состояниям, связанным с изменением 1) содержания бикарбонатов (резервная щелочность), 2) активной реакции крови (понижения или повышения концентрации Н-ионов). Для характеристики ацидоза в отношении крови необходимы двоякого рода данные: 1) определение Р. щ., 2) определение свободной Н2С03. Табл. 1. Обусловлен. Резервная щелочность Напряжение СОа ими концентр. Н-ионов Определение Примеры | Норм. Норм. Нормацидемия – эйгид-рия Норм.-эйкапния < Повыш. Повыш. Ацидемия (ацидоз) -ги- При начале вдыхания пергидрия воздуха, богатого СОа Пониж. Пониж. Алкалемия (алкалез)-гипергидрия При начале искусств. гипервентиляции Норм, или пониж. или Пониж. Алкалемия-гипогидрия При вливании соды несоответств. повыш. (алкалез) Соотв. повыш. Норм. Нормацидемия – эйгид- Некоторое время пос- Повыш.-гиперкапния J рия ле вливания соды. Со- (алкалез) < стояние с длительной перегрузкой СОа (эмфизема) Больше, чем соотв. по- Повыш. Ацидемия-гипергидрия В течение дальнейшего вышение (ацидоз) вдыхания СО2 i Норм, или повыш. или Повыш. Ацидемия-гипергидрия При начале вливания несоотв. пониж. (ацидоз) кислоты Соотв. пониж. Норм. Нормацидемия – эйгид-рия Некоторое время после вливания кислоты. Со- Пониж.-гипокапния J (ацидоз) 1 стояние с длительным пониж. напряж. СО2. Гипер вентиляция на | высотах. Апетонемия Больше, чем соотв. по- Пониж. Алкалемия-гипогидрия В течение дальнейшей нижение (алкалез) энергичной гипервентиляции Табл. 2. Рез. ще- Тип расстройства лочи. или содерж. общ. С02 Примеры Ацидоз 1) Вследствие дефицита бикарб. (не газов) а) компенсиров. гр. 8 б) некомпенсир. гр. 9 . Понижен Диабетич. кома, период. рвота, детск. гастро-энтерит. дизентерия, уремия, отравление салици-латами 2) Вследствие избытка СО 2 (газов) а) компенсиров. гр. 5 б) некомпенсир. гр. 4 Повышен Отравление морфием, эмфизема Алкалез 1) Вследствие избытка бикарб. (не газов) а) компенсиров. гр. 5 б) некомпенсир. гр. 6 Повышен Вливание двууглекислой соды. Высокая закупорка кишечника 2) Вследствие дефицита СО 2 (газов) а) компенсиров. гр. 8 б) некомпенсир. гр. 7 Понижен Условия аноксемии, на высотах гипервентиляции Между тем как в крови сдвига активной реакции почти не наблюдается (см.: Ацидоз-ацидоз крови), активная реакция тканей является величиной гораздо менее постоянной, и сдвиг рН “может достигать значительной величины. Путем комбинации изменений ВНС03 и Н2С03 могут получиться восемь различных видов нарушения кислотно-щелочного соотношения (Ван-Слайк) (табл.1). Таким образом одно и то же состояние может быть определено одним автором как ацидоз, другим как алкалез, поэтому нужно точнее указать, к какому признаку отнести это обозначение. Голден (Haldane) предлагает клас- сификацию, дающую в отдельных случаях указания на процессы, вызывающие соответственное изменение (табл. 2).
Лит.: Г е ф т е р Ю., Резервная щелочность, Моск. мед. ж., 1925, № 37; К а п л а н с к и й СГ, Кислотно-щелочное равновесие в организме, М., 1932; Скворцов В., Ацидоз и алкалоз в медицине, М., 1928; Eli as H., Zur Bedeutung des Saurebasenhaushaltes, Erg. d. inn. Med., B. XXV, 1924 (лит.); L a b b e M. u. NepveuxE., Acidose et alcalose, P., 1928 (рус. изд.- M.-Л., 1930); Peters J. a. Van Slyke D., Quantitative clinical chemistry, Baltimore, 1931; S t r a -u b H., Storung d. pnys.-chem. Atmungsregulation, Erg. d. inn. Med., B. XXV, 1924 (лит.); Van SlykeD., Bestimmung d. Alkalireserve des Blutes (Hndb. d. biol. Arbeitsmethoden. hrsg. v. Abderbalden, Abt.IV, T. 4, Heft 4, В.-Wien, 1927).
Ю. Гефтер.
© 2000- NIV
Под резервной щелочностью понимают запас бикарбонатов крови, определенный по общему СО2. Известно, что углекислый газ содержится в основном в составе бикарбонатов крови и только ‘/20 его находится в растворенном и свободном состоянии. Такая малая доля не оказывает существенного влияния на оценку состояния бикарбонатной системы по общему СО2.
Принцип метода. В одной половине колбы плазму крови обрабатывают серной кислотой, благодаря чему выделяется углекислый газ, находящийся в составе бикарбонатов. Выделившийся углекислый газ поглощается раствором натрия гидроокиси (едкий натр), который находится в другой половине колбы. Избыток натрия гидроокиси, не вошедший в реакцию с углекислым* газом, и половину натрия углекислого (Na2CO3), образовавшегося в процессе поглощения СО2, оттитровывают раствором серной кислоты. По количеству связанного первоначально натрия* гидроокиси определяют количество выделенного из плазмы углекислого газа, которое эквивалентно содержанию бикарбонатов.
Реактивы:
- 0,1 н. (0,05 моль/л) раствор серной кислоты (готовят и& фиксанала);
- 0,02 н. (0,01 моль/л) (точно) раствор серной кислоты (готовят из 0,1 н. раствора серной кислоты);
- 0,1 н. (0,1 моль/л) раствор натрия гидроокиси;
- 0,02 н. (0,02 моль/л) раствор натрия гидроокиси (готовят из 0,1 н. раствора натрия гидроокиси). Титр этого раствора проверяют перед анализом и доводят до нужной величины;
- 5%-ный раствор серной кислоты;
- 1 %-ный спиртовой раствор фенолфталеина.
Оборудование. Сдвоенные колбы с резиновыми пробками (30 шт. и более). Микробюретки на 2 и 5 мл. Центрифужные-пробирки из толстого стекла.
Ход определения. Предварительно готовят плазму (сыворотку крови). По количеству проб крови с учетом параллельных исследований подбирают одинаковые колбы и не менее-3 сдвоенных колб оставляют для контроля. Точность результатов всей серии исследований зависит от точности титрование эаствора натрия гидроокиси в контрольных колбах. Все колбы закрывают резиновыми пробками.
Анализы проводят серийно. В одну из каждой пары сдвоен-чых колб, поочередно открывая, вносят с помощью бюретки или липетки (не выдувая) по 2 мл 0,02 н. раствора натрия гидроокиси и плотно закрывают пробкой. В смежную колбу, кроме контрольных (опять поочередно открывая и закрывая), вносят аз пипетки (не выдувая) 0,5 мл плазмы крови, находящейся под вазелиновым маслом. После этого в колбы с плазмой (контрольные без плазмы), также поочередно открывая, вносят из пипетки (не выдувая) по 1 мл 5%-ного раствора серной кислоты и быстро плотно закрывают пробкой. Проверяют, хорошо ли закрыты колбы, осторожно вращательными движениями перемешивают плазму крови с кислотой и оставляют стоять в течение 1 – 2 ч (можно и больше). Плазму с кислотой перемешивают не менее 3 раз.
Через 1 – 2 ч приступают к титрованию. Для этого поочередно открывают колбы, где находится раствор натрия гидроокиси, вносят туда 1 – 2 капли раствора фенолфталеина и титруют из микробюретки на 2 мл 0,02 н. раствором серной кислоты до полного обесцвечивания. Опытные и контрольные пробы титруют с одинаковой скоростью.
Расчет. По разнице результатов титрования в контрольных ч опытных образцах устанавливают количество мл 0,02 н. раствора натрия гидроокиси, связанного с углекислым газом, вытесненным из бикарбонатов плазмы. Расчет ведут по формуле (об % С02):
X=(Vk-Vn)*89,6
где Vk – количество 0,02 н. раствора серной кислоты, мл, пошедшей на титрование контроля; Vn – количество 0,02 н. раствора серной кислоты, мл, пошедшего на титрование исследуемого образца; 89,6 – коэффициент для пересчета раствора натрия гидроокиси на СО2 в 100 мл плазмы крови в условиях чанной реакции. Для перевода полученной величины в миллимоль на литр ее умножают на 0,413.
Клиническое значение.
Снижение резервной щелочности крови свидетельствует о сдвиге кислотно-щелочного равновесия в сторону ацидоза, повышение – алкалоза. Метаболический ацидоз отмечают при однотипном высококонцентратном или силосно-жомовом кормлении, кетозе, вторичной остеодистрофии, ацидозе рубца, сахарном диабете, расстройствах желудочно-кишечного тракта, особенно при диарее молодняка, нефрите, нефрозе, септических процессах. и т. д.
Газовый ацидоз бывает вследствие замедления процесса отдачи углекислоты легкими. Такое явление наблюдается при расстройстве сердечной деятельности, эмфиземе легких, при нахождении животных в среде с высокой концентрацией в воздухе гглекислоты.
Состояние метаболического алкалоза у животных бывает при алкалозе рубца, введении в организм больших доз пищевой соды. Газовый алкалоз наблюдается при усиленной гипервентиляции легких вследствие выведения из организма большого количества углекислого газа, а также при содержании животных на большой высоте над уровнем моря.
