Сидеробластная анемия гемолитическая анемия

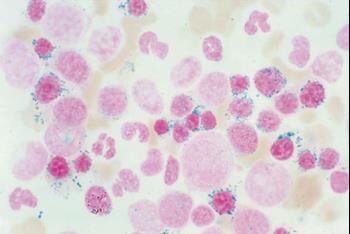
Что такое сидеробластная анемия

Кольцевидные сидеробласты в мазке крови
Сидеробластная анемия — одна из редких форм анемии, которая возникает при нормальном или повышенном содержании в крови железа. Общеизвестно, что для нормального образования гемоглобина нужно, чтобы с пищей поступало достаточное количество железа и некоторых других полезных веществ. Но в случае сидеробластной анемии правильное питание не работает, железо просто не усваивается главным кроветворным органом человека — красным костным мозгом. Железо в свободном виде остается в крови и начинает отравлять организм при повышенных концентрациях.
Часто можно встретить термин «сидеробластные анемии», что подчеркивает множественность причин и вариантов течения этого заболевания у разных людей. Существуют как легкие формы, годами не беспокоящие пациентов (их выявляют чаще всего случайно на медосмотрах), так и тяжелые, когда красный костный мозг практически полностью перестает производить нормальные эритроциты, содержащие гемоглобин. В крови в таком случае обнаруживаются бледные «пустышки» вместо обычных красных эритроцитов, а железо, которое должно было пойти на их производство, растворено в жидкой среде организма и может плохо сказываться на работе внутренних органов.
Иногда сидеробластная анемия носит преходящий характер: быстро проявляется на фоне неблагоприятных условий (приема алкоголя, отравления) и так же скоро и без следа проходит.
Симптомы и признаки сидеробластной анемии

Непереносимость физических нагрузок — тревожный симптом
Из-за того, что здоровых, способных выполнять свои функции эритроцитов в крови недостаточно, сидеробластная анемия имеет общие признаки со всеми остальными анемиями:
- головокружения,
- беспричинные обмороки,
- быстрая утомляемость,
- непереносимость душных, слабо проветриваемых помещений,
- невозможность обычной физической работы,
- одышка,
- тусклые, ломкие ногти, секущиеся волосы.
Есть и ряд характерных именно для сидеробластной анемии симптомов, которые связаны с циркуляцией в крови свободного железа, которое накапливается в различных внутренних органах и коже. Наиболее частые из них:
- изменение цвета кожи на «загорелый» без воздействия солнечных лучей;
- геморрагические высыпания на коже (красноватая постоянная сыпь);
- увеличение и болезненность печени;
- увеличение селезенки;
- проблемы с перевариванием пищи (из-за нарушения печеночных функций).
При очень больших концентрациях в крови железа выходить из строя могут любые внутренние органы, на первый взгляд совсем не связанные с анемией (легкие, селезенка).
Причины

Прием ряда препаратов может вызвать сидеробластную анемию
Все причины сидеробластной анемии можно разделить на врожденные и приобретенные. В случае, если есть врожденные причины, болезнь проявляется в раннем детском возрасте или в период полового созревания. Приобретенные причины могут спровоцировать появление болезни в любом возрасте.
Главные причины сидеробластной анемии:
- Наследственная предрасположенность (чаще встречается у мужчин) — к ней относятся митохондриальные цитопатии и наследственная Х-хромосомная форма болезни.
- Отравления вредными химическими веществами (тяжелые металлы, ртуть и свинец) — может возникать при частом контакте с этими веществами на работе, а также в быту при отравлении выхлопными газами автомобилей, использование старых свинцовых белил и красок.
- Острое отравление алкоголем (проще говоря, похмелье), а также постоянное его чрезмерное употребление.
- Химиотерапия онкологических болезней, прием цитостатиков и противоопухолевых препаратов.
- Тяжелая нехватка витамина В₆.
- Прием некоторых лекарств (особенно у пациентов, имеющих генетическую предрасположенность к анемии):
- антибиотиков (левомицетина, метронидазола, некоторых сульфаниламидов),
- противоревматических препаратов (бутадиона, оксифенбутазона),
- противосудорожных препаратов (гидантоина, дифенина, карбамазепина),
- антидепрессантов (миансерина, флуоксетина).
Диагностика заболевания

Лабораторные тесты — неотъемлемый этап диагностики
Врачу позволяет заподозрить сидеробластную анемию простой общий анализ крови, а также специфические симптомы у пациента. Диагностировать болезнь может как терапевт или педиатр, так и врач-гематолог.
Исследования, которые необходимо будет пройти, назначает в каждом конкретном случае лечащий врач, однако чаще всего нужны:
- Общий анализ крови с лейкоцитарной формулой («кровь из пальца»);
- Биохимический анализ крови (железо, прямой и непрямой билирубин);
- УЗИ органов брюшной полости (печени и селезенки).
Иногда для постановки диагноза нужна биопсия красного костного мозга, генетические исследования.
Лечение

Воздействие на причину приводит к выздоровлению пациента
Основу лечения приобретенной сидеробластной анемии составляет устранение повреждающего организм фактора, если это возможно. В случаях, когда болезнь была вызвана применением лекарственных средств, врач отменяет их прием и находит замену среди нетоксичных для крови препаратов. Если сидеробластная анемия вызвана поступлением в организм отравляющих веществ или алкоголя, то необходимо будет исключить контакт с ними по крайней мере на период восстановления после болезни.
Наследственные формы сидеробластной анемии не подлежат радикальному лечению. Терапия основана на поддержании кроветворной функции красного костного мозга.
При тяжелой, угрожающей жизни пациента форме анемии проводится переливание крови либо ее компонентов (эритроцитарной массы). При выраженном поражении органа свободным железом проводят удаление селезенки.
Практически во всех случаях проводят следующие виды терапии:
- назначение инъекций витамина В₆ (раствор пиридоксина гидрохлорида) или его прием в форме таблеток;
- прием препарата, связывающего свободное железо (дефероксамин, препарат «Десферал»);
- курс лечения гепатопротекторами для восстановления функции печени (фосфолипиды, препараты природного происхождения).
Важно знать, что прием препаратов железа в случае сидеробластной анемии не только не приводит к улучшению состояния, но и может значительно усугубить болезнь. Именно поэтому самостоятельная диагностика и назначение себе препаратов против анемии крайне опасны.
Прогноз и профилактика

Хроническая интоксикация имеет неблагоприятный прогноз
Прогноз течения болезни зависит от причин, которые ее вызвали. В случаях острых отравлений токсическими веществами или алкоголем сидеробластная анемия зачастую проходит без особенных последствий для здоровья.
При хронических интоксикациях на работе прогноз не так благоприятен, потому что при постоянном воздействии повреждающего здоровье фактора защитные резервы организма истощаются. Работник может перестать контактировать с вредными веществами, но красный костный мозг к тому моменту иногда бывает серьезно поврежден, потому болезнь продолжается.
Если же причиной является наследственная аномалия кроветворения, то сидеробластная анемия будет сопровождать человека на протяжении всей жизни, возможны только изменения по форме тяжести заболевания. При своевременном лечении пациенты с наследственной сидеробластной анемией имеют легкую форму болезни, которая не мешает их нормальной жизни.
В случаях сильного витаминного дефицита достаточно устранить его и улучшить питание, и болезнь оказывается навсегда устранена, однако такая причина сидеробластной анемии встречается крайне редко.

Бесконтрольный прием препаратов железа недопустим!
К основным направлениям профилактики сидеробластной анемии относятся:
- Недопущение самолечения антибиотиками и другими сильнодействующими препаратами. Лекарства, которые могут повлиять на функции красного костного мозга, должны использоваться под контролем показателей крови.
- Контроль над количеством потребляемого алкоголя. При наличии наследственной предрасположенности алкогольные напитки не должны употребляться вовсе.
- Использование индивидуальных средств защиты на работе, если она предполагает контакт с опасными химическими веществами, соблюдение правил безопасности.
- Регулярное прохождение медицинских осмотров (по общему анализу крови врач легко заподозрит сидеробластную анемию и вовремя назначит лечение).
- Отдых в экологически чистых местностях. Особенно это важно при жизни в крупных городах с большим количеством автомобилей, отравляющих воздух.
- Недопущение приема лечебных доз препаратов железа без назначения врача. Железо часто содержится в составе поливитаминных комплексов, их самостоятельный прием более безопасен из-за того, что там оно будет в поддерживающих здоровье дозах.

Благоприятное влияние оказывает диета
Рекомендовано сбалансированное питание, богатое источниками витамина В₆:
- фисташки, семечки подсолнечника;
- отруби, хлеб из цельнозерновой муки;
- чеснок;
- орехи (фундук, грецкие);
- горбуша, семга;
- гречневая крупа, фасоль;
Сидеробластная анемия встречается значительно реже обычной железодефицитной, но является более тяжелой, так как может наносить здоровью серьезный вред из-за повреждения внутренних органов. Нужно помнить, что самостоятельно отличить разные виды анемий невозможно, потому необходимо обратиться к врачу при появлении первых симптомов болезни.
Что такое сидеробластная анемия?
Сидеробластная анемия представляют собой группу заболеваний крови, при которых в организме достаточно железа, однако организм не может использовать его для выработки гемоглобина, который переносит кислород в крови. В результате железо накапливается в митохондриях эритроцитов, придавая ядру кольцевой вид.
Существует три типа сидеробластной анемии: наследственные, приобретенные и идиопатические (неизвестного происхождения).
Признаки и симптомы данной анемии могут варьироваться от легких до тяжелых и включают усталость, затрудненное дыхание и слабость. Может также произойти увеличение селезенки или печени. В тяжелых случаях повышение уровня железа в крови может привести к сердечным заболеваниям, повреждению печени и почечной недостаточности.
Признаки и симптомы

Сидеробластные анемии характеризуются усталостью, затрудненным дыханием и ощущением слабости. При физической нагрузке люди с этим расстройством могут чувствовать боли в груди, похожие на стенокардию.
Более распространенные формы анемии вызваны дефицитом железа в крови. Люди с сидеробластными анемиями имеют аномально высокий уровень железа и железосодержащих веществ в сыворотке крови. В некоторых случаях слизистые оболочки, кожа рук и лица при сидеробластной анемии могут выглядеть бледными, часто лимонно-желтого цвета. Редко может появиться коричневато-красное изменение цвета, вызванное кровотечением под кожей.
Увеличение селезенки (спленомегалия) или печени (гепатомегалия) являются другими симптомами этого нарушения. Острый лейкоз развивается менее чем в 10% случаев как осложнение прогрессирующих сидеробластных анемий.
Причины
Наследственная сидеробластная анемия является результатом дефекта в X-сцепленном рецессивном гене. Ген, известный как ALAS2, производит фермент, который необходим для производства «гема», кислородсодержащей части молекулы гемоглобина. Дефектный ген находится на Х-хромосоме (Xp11.21).
Х-сцепленная сидеробластная анемия обычно проявляется в определенный момент в течение первых трех десятилетий жизни.
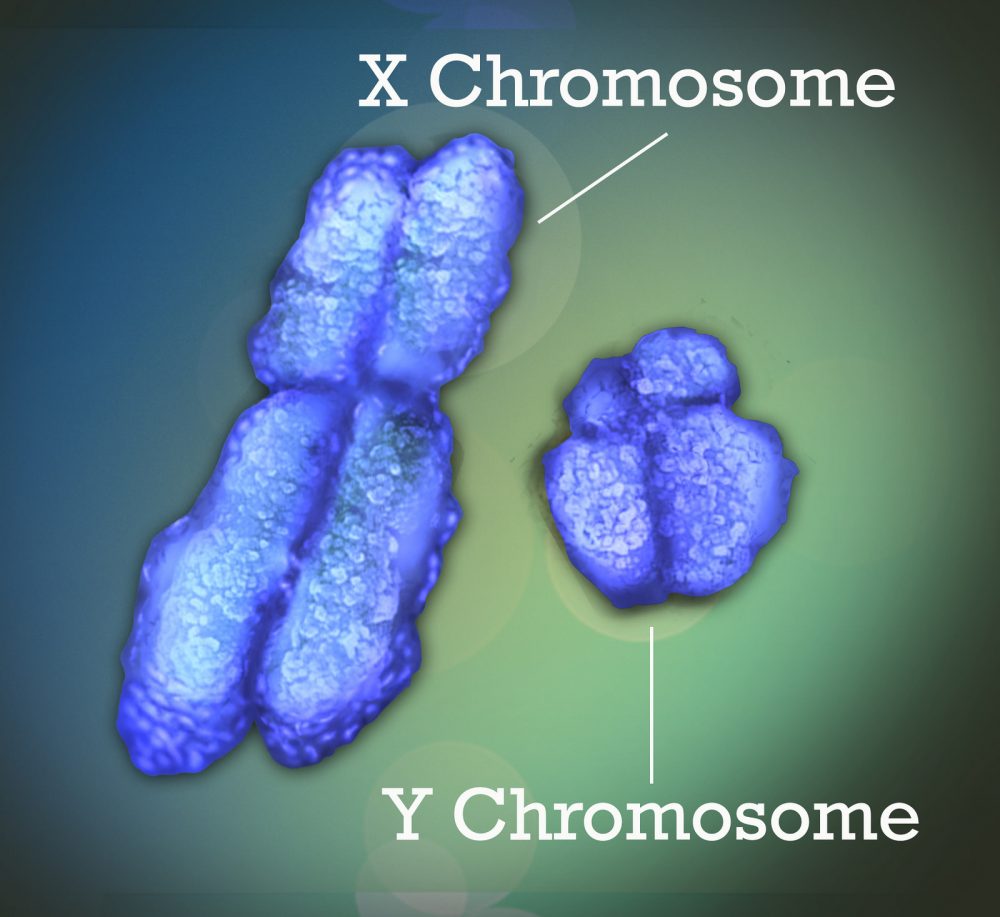
Хромосомы, которые присутствуют в ядре клеток человека, несут генетическую информацию каждого человека. Клетки человеческого тела обычно имеют 46 хромосом. Пары человеческих хромосом пронумерованы от 1 до 22, а половые хромосомы обозначены X и Y. У мужчин есть одна X и одна Y-хромосома, а у женщин две X-хромосомы.
Каждая хромосома имеет короткое плечо, обозначенное «p», и длинное плечо, обозначенное «q». Хромосомы далее подразделяются на множество полос, которые пронумерованы. Например, «хромосома Xp11.21» относится к полосе 11.21 на коротком плече Х-хромосомы. Пронумерованные полосы указывают на местоположение тысяч генов, присутствующих в каждой хромосоме.
Х-сцепленные рецессивные генетические нарушения представляют собой состояния, вызванные ненормальным геном в Х-хромосоме. У самок две Х-хромосомы, но одна из Х-хромосом выключена, и все гены этой хромосомы инактивированы.

Женщины, у которых есть ген заболевания, присутствующий в одной из их Х-хромосом, являются носителями этого расстройства. Женщины-носители обычно не проявляют симптомов расстройства, потому что обычно это Х-хромосома с ненормальным геном, который «выключен».
У мужчины есть одна Х-хромосома, и если он унаследует Х-хромосому, содержащую ген болезни, у него возникнет эта болезнь. Мужчины с Х-связанными нарушениями передают ген болезни всем своим дочерям, которые будут носителями. Мужчина не может передать X-связанный ген своим сыновьям, потому что мужчины всегда передают свою Y-хромосому вместо своей X-хромосомы потомству мужского пола.
Приобретенная сидеробластная анемия является результатом длительного воздействия определенных токсических веществ и лекарств или неприятного эффекта других расстройств, таких как иммунные расстройства, гранулематозные заболевания, опухоли или метаболические расстройства.
Как следует из названия, причина идиопатической сидеробластной анемии неизвестна.
Затронутые группы населения
Наследственная сидеробластная анемия поражает как мужчин, так и женщин, но чаще встречается у мужчин. Начало этой формы расстройства обычно происходит до 30 лет, хотя были случаи диагностирования расстройства у пациентов старше 70 лет.
Приобретенная сидеробластная анемия чаще наблюдается у пожилых пациентов любого пола, обычно в возрасте 65 лет и старше. Тем не менее, были случаи диагностирования болезни у пациентов в середине 50 лет.
Связанные расстройства
В дополнение к формам сидеробластной анемии, описанным выше, существует несколько дополнительных типов или подтипов, которые встречаются крайне редко.
- Малая и большая (крупная) талассемия — две наследственные анемии. Малая талассемия — более легкая форма из двух. Крупная талассемия (анемия Кули) относится к группе хронических семейных гемолитических анемий. Он характеризуется заметным увеличением F-гемоглобина и снижением синтеза бета-полипептидных цепей в молекуле гемоглобина. Симптомы включают уменьшение количества эритроцитов, генерализованную слабость, смутное чувство недомогания, расстройство желудка и сердцебиения.
- Идиопатический гемохроматоз — наследственное нарушение обмена железа, характеризующееся избыточными отложениями железа в тканях, особенно в печени, поджелудочной железе и сердце, а также пигментацией кожи в бронзовый цвет. Также могут возникнуть цирроз печени, сахарный диабет и связанные с ними изменения в костях и суставах.
Для получения дополнительной информации о вышеупомянутых расстройствах перейдите на страницу «Талассемия» и «Гемохроматоз».
Диагностика
Подозрение на возникновение сидеробластной анемии приведет к заказу врачом анализов крови, включая окрашивание эритроцитов, чтобы определить, присутствуют ли характерные кольцевые сидеробласты в митохондриях. Биохимические анализы могут проводиться для определения уровня фермента, необходимого для гемоглобина, дельта-аминолевулиновой синтетазы.
Стандартные методы лечения
Лечение зависит от причины сидеробластной анемии. Если расстройство приобретено, ответственный агент должен быть идентифицирован и вылечен.
Терапия витамином B6 (Пиридоксин) может быть полезна в некоторых случаях.
Чтобы удалить избыток железа из организма человека с сидеробластной анемией, под кожу (подкожно) или в мышцу (внутримышечно) вводят препарат Дефероксамин — это часто дает положительный ответный результат. Дефероксамин связывает избыток железа и способствует его выведению из организма.
В крайних случаях прибегают к переливании крови.
Прогноз
Прогноз развития сидеробластной анемии варьируется в зависимости от основной причины. В приобретенных случаях, например, связанных с употреблением алкоголя и наркотиков, долгосрочные симптомы могут отсутствовать.
Пациенты, нуждающиеся в переливании крови, пациенты с заболеваниями, не реагирующими на пиридоксин и другие методы лечения, а также пациенты с миелодиспластическим синдромом, который перерастает в острый лейкоз, имеют более низкий прогноз. Основными причинами смерти при данной анемии являются вторичный гемохроматоз при переливании крови и лейкемия.
Тромбоцитоз является относительно хорошим прогностическим признаком. Пациенты, которым переливание крови не требуется, скорее всего, останутся в живых в течение длительного времени, в то время как те, кто станет зависимым от переливания крови, рискуют в дальнейшем умереть от осложнений вторичного гемохроматоза.
Содержание
- Гемолитическая анемия
- Классификация гемолитических анемий
- Причины гемолитических анемий
- Симптомы гемолитических анемий
- Наследственные мембранопатии, ферментопении и гемоглобинопатии
- Приобретенные гемолитические анемии
- Диагностика гемолитических анемий
- Лечение гемолитических анемий
Гемолитическая анемия – патология эритроцитов, отличительным признаком которой является ускоренное разрушение красных кровяных телец с высвобождением повышенного количества непрямого билирубина. Для гемолитических анемий типично сочетание анемического синдрома, желтухи и увеличения размеров селезенки. В процессе диагностики исследуется общий анализ крови, уровень билирубина, анализ кала и мочи, УЗИ органов брюшной полости; проводится биопсия костного мозга, иммунологические исследования. В качестве методов лечения гемолитической анемии используется медикаментозная, гемотрансфузионная терапия; при гиперспленизме показана спленэктомия.
Гемолитическая анемия
Гемолитическая анемия — анемия, обусловленная нарушением жизненного цикла эритроцитов, а именно преобладанием процессов их разрушения (эритроцитолиза) над образованием и созреванием (эритропоэзом). Группа гемолитических анемий очень обширна. Их распространенность неодинакова в различных географических широтах и возрастных группах; в среднем патология встречается у 1% населения. Среди прочих видов анемий на долю гемолитических приходится 11%. При гемолитической анемии жизненный цикл эритроцитов укорочен и их распад (гемолиз) происходит раньше времени (через 14-21 день вместо 100-120 суток в норме). При этом разрушение эритроцитов может происходить непосредственно в сосудистом русле (внутрисосудистый гемолиз) или в селезенке, печени, костном мозге (внесосудистый гемолиз).
Классификация гемолитических анемий
В гематологии гемолитические анемии подразделяются на две большие группы: врожденные (наследственные) и приобретенные.
Наследственные гемолитические анемии включают следующие формы:
- эритроцитарные мембранопатии (микросфероцитоз – болезнь Минковского-Шоффара, овалоцитоз, акантоцитоз) – гемолитические анемии, обусловлены структурными аномалиями мембран эритроцитов
- ферментопении (энзимопении) – гемолитические анемии, вызванные дефицитом тех или иных ферментов (глюкозо-6-фосфатдегидрогеназы, пируваткиназы и др.)
- гемоглобинопатии — гемолитические анемии, связанные с качественными нарушениями структуры гемоглобина или изменением соотношения его нормальных форм (талассемия, серповидно-клеточная анемия).
Приобретенные гемолитические анемии подразделяются на:
- мембранопатии приобретенные (пароксизмальная ночная гемоглобинурия – б-нь Маркиафавы-Микели, шпороклеточная анемия)
- иммунные (ауто- и изоиммунные анемии) – обусловлены воздействием антител
- токсические – гемолитические анемии, обусловленные воздействием химических веществ, биологических ядов, бактериальных токсинов
- гемолитические анемии, вызванные механическим повреждением структуры эритроцитов (тромбоцитопеническая пурпура, маршевая гемоглобинурия)
Причины гемолитических анемий
Патогенетическую основу наследственных гемолитических анемий составляют генетические дефекты мембран эритроцитов, их ферментных систем либо структуры гемоглобина. Данные предпосылки обусловливают морфо-функциональную неполноценность эритроцитов и их повышенное разрушение. Гемолиз эритроцитов при приобретенных анемиях наступает под влиянием внутренних факторов или факторов окружающей среды.
Развитию иммунных гемолитических анемий могут способствовать посттрансфузионные реакции, профилактическая вакцинация, гемолитическая болезнь плода, прием определенных лекарств (противомалярийных препаратов, сульфаниламидов, производных нитрофуранового ряда, анальгетиков). Аутоиммунные реакции с образованием антител, агглютинирующих эритроциты, возможны при гемобластозах (остром лейкозе, хроническом лимфолейкозе, лимфогранулематозе, миеломной болезни), аутоиммунной патологии (СКВ, неспецифическом язвенном колите), инфекционных заболеваниях (инфекционном мононуклеозе, токсоплазмозе, сифилисе, вирусной пневмонии).
В ряде случаев острому внутрисосудистому гемолизу предшествует отравление мышьяковистыми соединениями, тяжелыми металлами, уксусной кислотой, грибными ядами, алкоголем и др. Механическое повреждение и гемолиз эритроцитов может наблюдаться при тяжелых физических нагрузках (длительной ходьбе, беге, лыжном переходе), при ДВС-синдроме, малярии, злокачественной артериальной гипертензии, протезировании клапанов сердца и сосудов, проведении гипербарической оксигенации, сепсисе, обширных ожогах. В этих случаях под действием тех или иных факторов происходит травматизация и разрыв мембран изначально полноценных эритроцитов.
Центральным звеном патогенеза гемолитических анемий является повышенное разрушение эритроцитов в органах ретикулоэндотелиальной системы (селезенке, печени, костном мозге, лимфатических узлах) или непосредственно в сосудистом русле. Эти процессы сопровождаются развитием анемического и желтушного синдромов (так называемой «бледной желтухой»). Возможно интенсивное окрашивание кала и мочи, увеличение селезенки и печени.
Симптомы гемолитических анемий
Наследственные мембранопатии, ферментопении и гемоглобинопатии
Наиболее распространенной формой данной группы гемолитических анемий является микросфероцитоз, или болезнь Минковского-Шоффара. Наследуется по аутосомно-доминантному типу; обычно прослеживается у нескольких представителей семьи. Дефектность эритроцитов обусловлена дефицитом в мембране актомиозиноподобного белка и липидов, что приводит к изменению формы и диаметра эритроцитов, их массивному и преждевременному гемолизу в селезенке.
Манифестация микросфероцитарной гемолитической анемии возможна в любом возрасте (в младенчестве, юношестве, старости), однако обычно проявления возникают у детей старшего возраста и подростков. Тяжесть заболевания варьирует от субклинического течения до тяжелых форм, характеризующихся часто повторяющимися гемолитическими кризами. В момент криза нарастает температура тела, головокружение, слабость; возникают боли в животе и рвота.
Основным признаком микросфероцитарной гемолитической анемии служит желтуха различной степени интенсивности. Вследствие высокого содержания стеркобилина кал становится интенсивно окрашенным в темно-коричневый цвет. У пациентов с болезнь Минковского-Шоффара наблюдается склонность к образованию камней в желчном пузыре, поэтому часто развиваются признаки обострения калькулезного холецистита, возникают приступы желчной колики, а при закупорке холедоха конкрементом — обтурационная желтуха. При микросфероцитарной гемолитической анемии во всех случаях увеличена селезенка, а у половины пациентов – еще и печень.
Кроме наследственной микросфероцитарной гемолитической анемии, у детей часто встречаются другие врожденные дисплазии: башенный череп, косоглазие, седловидная деформация носа, аномалии прикуса, готическое нёбо, полидактилия или брадидактилия и пр. Пациенты среднего и пожилого возраста страдают трофическими язвами голени, которые возникают в результате гемолиза эритроцитов в капиллярах конечностей и плохо поддаются лечению.
Энзимопенические гемолитические анемии связаны с недостатком определенных ферментов эритроцитов (чаще — Г-6-ФД, глутатион-зависимых ферментов, пируваткиназы и др). Гемолитическая анемия может впервые заявлять о себе после перенесенного интеркуррентного заболевания или приема медикаментов (салицилатов, сульфаниламидов, нитрофуранов). Обычно заболевание имеет ровное течение; типична «бледная желтуха», умеренная гепатоспленомегалия, сердечные шумы. В тяжелых случаях развивается ярко выраженная картина гемолитического криза (слабость, рвота, одышка, сердцебиение, коллаптоидное состояние). В связи с внутрисосудистым гемолизом эритроцитов и выделением гемосидерина с мочой последняя приобретает темный (иногда черный) цвет.
Особенностям клинического течения гемоглобинопатий — талассемии и серповидно-клеточной анемии посвящены самостоятельные обзоры.
Приобретенные гемолитические анемии
Среди различных вариантов приобретенных гемолитических анемий чаще других встречаются аутоиммунные анемии. Для них общим пусковым фактором выступает образование антител к антигенам собственных эритроцитов. Гемолиз эритроцитов может носить как внутрисосудистый, так и внутриклеточный характер.
Гемолитический криз при аутоиммунной анемии развивается остро и внезапно. Он протекает с лихорадкой, резкой слабостью, головокружением, сердцебиением, одышкой, болями в эпигастрии и пояснице. Иногда острым проявлениям предшествуют предвестники в виде субфебрилитета и артралгий. В период криза стремительно нарастает желтуха, не сопровождающаяся кожным зудом, увеличивается печень и селезенка.
При некоторых формах аутоиммунных гемолитических анемий больные плохо переносят холод; в условиях низких температур у них может развиваться синдром Рейно, крапивница, гемоглобинурия. Вследствие недостаточности кровообращения в мелких сосудах возможны осложнения в виде гангрены пальцев ног и рук.
Токсические гемолитические анемии протекают с прогрессирующей слабостью, болями в правом подреберье и поясничной области, рвотой, гемоглобинурией, высокой температурой тела. Со 2-3 суток присоединяется желтуха и билирубинемия; на 3-5 сутки возникает печеночная и почечная недостаточность, признаками которых служат гепатомегалия, ферментемия, азотемия, анурия.
Отдельные виды приобретенных гемолитических анемий рассмотрены в соответствующих статьях: «Гемоглобинурия» и «Тромбоцитопеническая пурпура», «Гемолитическая болезнь плода».
Диагностика гемолитических анемий
Определение формы гемолитической анемии на основе анализа причин, симптоматики и объективных данных относится к компетенции гематолога. При первичной беседе выясняется семейный анамнез, частота и тяжесть протекания гемолитических кризов. В процессе осмотра оценивается окраска кожных покровов, склер и видимых слизистых, производится пальпация живота для оценки величины печени и селезенки. Сплено- и гепатомегалия подтверждается при проведении УЗИ печени и селезенки.
Изменения в гемограмме характеризуются нормо- или гипохромной анемией, лейкопенией, тромбоцитопенией, ретикулоцитозом, ускорением СОЭ. При аутоиммунных гемолитических анемиях большое диагностическое значение имеет положительная проба Кумбса. В биохимических пробах крови определяется гипербилирубинемия (увеличение фракции непрямого билирубина), увеличение активности лактатдегидрогеназы. Исследование мочи выявляет протеинурию, уробилинурию, гемосидеринурию, гемоглобинурию. В копрограмме повышено содержание стеркобилина. Исследование пунктата костного мозга обнаруживает гиперплазию эритроидного ростка.
В процессе дифференциальной диагностики исключаются гепатиты, цирроз печени, портальная гипертензия, гепатолиенальный синдром, гемобластозы.
Лечение гемолитических анемий
Различные формы гемолитической анемии имеют свои особенности и подходы к лечению. При всех формах приобретенной гемолитической анемии необходимо позаботиться об устранении влияния гемолизирующих факторов. Во время гемолитических кризов больным необходимы инфузии растворов, плазмы крови; витаминотерапия, по необходимости – гормоно- и антибиотикотерапия. При микросфероцитозе единственно эффективным методом, приводящим к 100 % прекращению гемолиза, является спленэктомия.
При аутоиммунной гемолитической анемии показана терапия глюкокортикоидными гормонами (преднизолоном), сокращающая или прекращающая гемолиз. В некоторых случаях требуемый эффект достигается назначением иммунодепрессантов (азатиоприна, 6-меркаптопурина, хлорамбуцила), противомалярийных препаратов (хлорохина). При резистентных к медикаментозной терапии формах аутоиммунной гемолитической анемии выполняется спленэктомия.
Лечение гемоглобинурии предполагает переливание отмытых эритроцитов, плазмозаменителей, назначение антикоагулянтов и антиагрегантов. Развитие токсической гемолитической анемии диктует необходимость проведения интенсивной терапии: дезинтоксикации, форсированного диуреза, гемодиализа, по показаниям – введение антидотов. При развитии почечной недостаточности прогноз неблагоприятен.
