Соединение гемоглобина с углекислым газом называется ответ
Гемоглобин (Нв) – основной компонент эритроцитов, благодаря которому эритроциты выполняют дыхательную функцию и поддерживают рН крови. По химической природе он относится к хромопротеидам. У мужчин в крови содержится в среднем 130-160 г/л гемоглобина, у женщин – 120-150 г/л. Молекулярная масса гемоглобина составляет около 60000 Да. Гемоглобин состоит из белка глобина и 4 молекул гема. Гем имеет в своем составе атом железа, способный присоединять или отдавать молекулу кислорода.
Гем содержит двухвалентное железо, которое играет ключевую роль в деятельности гемоглобина, являясь его активной (простетической) группой. Гемоглобин синтезируется эритро- и нормобластами костного мозга. Для нормального синтеза гемоглобина необходимо достаточное поступление железа с пищей. При разрушении эритроцитов гемоглобин, после отщепления гема, превращается в билирубин – желчный пигмент, который поступает, в основном, в кишечник в составе желчи, где превращается в стеркобилин, выводящийся из организма с каловыми массами. Часть билирубина удаляется с мочой в виде уробилина.
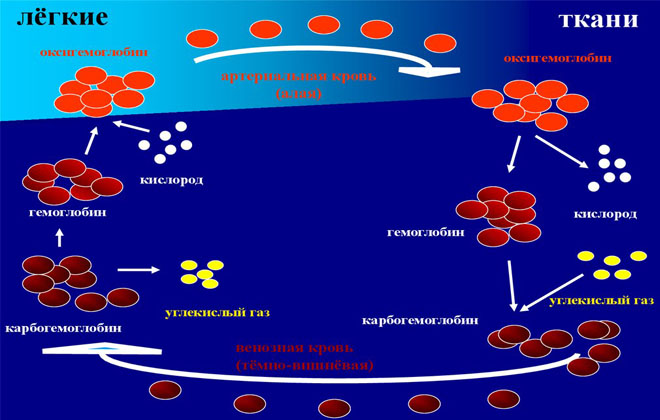
Основная функция гемоглобина – перенос кислорода и углекислого газа. Гемоглобин, присоединивший к себе кислород, превращается в оксигемоглобин. Соединение гемоглобина с кислородом происходит в капиллярах легких. Это соединение непрочное. В виде оксигемоглобина переносится большая часть кислорода. Гемоглобин, отдавший кислород, называется восстановленным, или дезоксигемоглобином. Гемоглобин, соединенный с углекислым газом носит название карбгемоглобина. Соединение гемоглобина с углекислым газом происходит в капиллярах тканей организма. Это соединение легко распадается. В виде этого соединения переносится 20 % СО2. Оксигемоглобин и карбгемоглобин являются физиологическими соединениями гемоглобина.
В скелетных и сердечной мышцах находится мышечный гемоглобин, называемый миоглобином. Он играет важную роль в снабжении кислородом работающих мышц, его можно рассматривать, как депо О2 в мышцах.
Имеется несколько форм гемоглобина, отличающихся строением белковой части – глобина. Первые 7-12 нед. внутриутробного развития зародыша его красные кровяные тельца содержат примитивный гемоглобин. У плода содержится гемоглобин F (80 %) или фетальный гемоглобин (от англ. Faetus – плод) гемоглобин. Он обладает более высокой способностью связывать кислород. Это помогает плоду не испытывать гипоксии при относительно низком парциальном напряжении кислорода в его крови. После рождения гемоглобин F практически полностью заменяется на взрослый – гемоглобин А (от англ. adult – взрослый). В эритроцитах взрослого человека содержатся гемоглобин А (95-98 % Hb A1 и 2-3 % HbA2 ).
Гемоглобин может вступать в соединение и с другими газами. Соединение гемоглобина с угарным газом (СО) называется карбоксигемоглобином – это патологическое соединение, в норме его не существует, т.к. в атмосфере отсутствует СО. Является прочным соединением. Гемоглобин блокирован в нем угарным газом и не способен осуществлять перенос кислорода. Сродство гемоглобина к угарному газу выше его сродства к кислороду, поэтому даже небольшое количество угарного газа в воздухе является опасным для жизни. При этом более критическим является не концентрация угарного газа, а длительность его вдыхания. Даже предельно низкое содержание СО в воздухе, но при длительном вдыхании, например, во время сна может оказаться летальным. Вследствие своего высокого сродства угарный газ в виде карбоксигемоглобина способен циркулировать в крови предельно долго.
Часто отравления угарным газом возникают у водителей при длительном нахождении в закрытом гараже с включенным двигателем автомобиля. Другим распространенным клинически значимым источником СО являются древесный дым, а также сырой кирпич печей изб и свежий печной лак. Поэтому при первом или после длительного перерыва протапливании таких печей необходимо тщательное проветривание помещения.
Особенностью угарного газа является то, что он не обладает запахом, поэтому отравление развивается незаметно. Часто пострадавший осознает это, когда проявляется миорелаксирующее (расслабление скелетной мускулатуры) действие угарного газа, при этом человек не может самостоятельно покинуть помещение.
Первая помощь при отравлении угарным газом. Пострадавшего следует переместить на свежий воздух. Следует учитывать, что при значительном отравлении сохранность самостоятельного дыхания не снимает необходимости проведения дальнейших действий по оказанию помощи. Наиболее оптимальным будет подача воздуха с повышенным содержание О2, например, из кислородной подушки. При отсутствии таковой – произвести искусственное дыхание. Во время искусственного дыхания в легкие потерпевшего воздух нагнетается под давлением, большим атмосферного.
При этом парциальное давление О2 в таком воздухе оказывается большим, чем в норме, что способствует его большему растворению в крови, а также лучшему вытеснению угарного газа из связи с гемоглобином. Если же пострадавший будет дышать самостоятельно, парциальное давление О2 во вдыхаемом воздухе окажется меньшим (примерно, 100 мм рт.ст.), что окажется недостаточным для вытеснения из карбоксигемоглобина угарного газа, т. к. сродство Нb к СО значительно выше, чем О2. В дальнейшем пострадавший должен быть доставлен в больницу.
При воздействии на гемоглобин экзогенных сильных окислителей происходит окисление железа гема с переходом его в 3-х валентную форму. В результате этого образуется метгемоглобин, который не способен присоединять ни О2, ни СО2. В результате окисления гемоглобин прочно удерживает кислород и теряет способность отдавать его тканям, что может привести к гибели организма.
К подобным сильным окислителем относятся нитраты и нитриты, содержащиеся, например, в химических удобрениях, также опасность представляют пероксиды, нитрокраски, анилиновые красители и ряд других веществ бытовой химии. В норме ежедневно около 0,5 % всего гемоглобина превращается в метгемоглобин, но затем она снова восстанавливается в гемоглобин специальным ферментом метгемоглобинредуктазой. Встречаются наследственные метгемоглобинемии, когда снижена активность метгемоглобинредуктазы в эритроцитах, что вызывает кислородное голодание. Метгемоглобин, также как карбоксигемоглобин, относится к группе патологических соединений гемоглобина.
91. При значительном уменьшении количества эритроцитов СОЭ:
+1) увеличивается 2) уменьшается 3) не изменяется4) может и увеличиваться, и уменьшаться 5) сначала уменьшается, потом увеличивается
92. При значительном уменьшении показателя гематокрита СОЭ:
+1) увеличивается 2) уменьшается 3) не изменяется4) может и увеличиваться, и уменьшаться5) сначала уменьшается, потом увеличивается
93. При увеличении показателя гематокрита СОЭ:
1) увеличивается +2) уменьшается 3) не изменяется 4) может и увеличиваться, и уменьшаться5) сначала уменьшается, потом увеличивается
94. Удельный вес эритроцитов по сравнению с плазмой крови:
+1) больше 2) меньше 3) одинаково4) может быть и больше, и меньше5) одинаков или больше
95. Соединение гемоглобина с кислородом называется:
+1) оксигемоглобином2) дезоксигемоглобином3) карбоксигемоглобином4) карбогемоглобином5) метгемоглобином
96. Соединение гемоглобина с двуокисью углерода называется:
1) оксигемоглобином 2) дезоксигемоглобином 3) карбоксигемоглобином +4) карбогемоглобином 5) метгемоглобином
97. Соединение гемоглобина с окисью углерода называется:
1) оксигемоглобином 2) дезоксигемоглобином +3) карбоксигемоглобином4) карбогемоглобином5) метгемоглобином
98. Форма гемоглобина, в которой он способен присоединить кислород или другие соединения, называется:
1) оксигемоглобином +2) дезоксигемоглобином 3) карбоксигемоглобином4) карбогемоглобином5) метгемоглобином
99. Соединение гемоглобина, в котором железо из двухвалентной формы переходит в трехвалентную, называется:
1) оксигемоглобином 2) дезоксигемоглобином 3) карбоксигемоглобином 4) карбогемоглобином+5) метгемоглобином
100. В методике определения количества гемоглобина в крови по методу Сали используется:
1) 3 % раствор хлорида натрия 2) 6 % раствор цитрата натрия 3) 0,5 % раствор хлорида натрия 4) 1 % раствор хлорида натрия +5) 0,1 Н раствор соляной кислоты
101. Снижение содержания гемоглобина в крови по сравнению с нормой называется:
1) нормогемоглобинемией +2) гипогемоглобинемией3) гиперглобинемией4) анизоцитозом5) пойкилоцитозом
102. Эритроциты, содержание гемоглобина в которых соответствует норме, называются:
+1) нормохромными2) гиперхромными3) гипохромными4) макроцитами5) мегалоцитами
103. Эритроциты, содержание гемоглобина в которых ниже нормы, называются:
1) нормохромными 2) гиперхромными +3) гипохромными4) макроцитами5) мегалоцитами
104. Эритроциты, содержание гемоглобина в которых выше нормы, называются:
1) нормохромными +2) гиперхромными3) гипохромными4) макроцитами5) мегалоцитами
105. У людей, длительно живущих в условиях высокогорья, содержание гемоглобина в крови:
+1) увеличивается2) уменьшается3) не изменяется4) может и увеличиваться, и уменьшаться5) сначала уменьшается, потом увеличивается
106. В колориметрической методике определения количества гемоглобина в крови используется _____ вид гемолиза эритроцитов:
1) осмотический2) биологический3) физиологический +4) химический +5) механический
107. Показатель относительного насыщения эритроцитов гемоглобином называется:
+1) цветовым2) гематокритом3) СОЭ4) Сали5) количеством гемоглобина
108. При быстром поступлении жидкости в кровяное русло наблюдается:
1) абсолютный эритроцитоз 2) относительный эритроцитоз 3) абсолютная эритропения +4) относительная эритропения5) неизменное содержание эритроцитов в 1 мл крови
109. К относительному эритроцитозу приводит
+1) интенсивное выделение пота2) быстрое увеличение жидкости в организме3) длительная кровопотеря4) длительная гипоксия5) систематическая физическая тренировка
110. При постоянном пребывании человека в зоне низкого барометрического давления наблюдается:
+1) абсолютный эритроцитоз2) относительный эритроцитоз3) абсолютная эритропения4) относительная эритропения5) неизменное содержание эритроцитов в 1 мл крови
111. После значительной кровопотери наблюдается:
1) абсолютный эритроцитоз 2) относительный эритроцитоз +3) абсолютная эритропения4) относительная эритропения5) неизменное содержание эритроцитов в 1 мл крови
112. При длительном пребывании на высокогорье количество эритропоэтинов в крови:
+1) увеличивается2) уменьшается3) не изменяется4) может и увеличиваться, и уменьшаться5) сначала уменьшается, потом увеличивается
113. При снижении парциального давления кислорода в альвеолярном воздухе количество эритропоэтинов в крови:
+1) увеличивается2) уменьшается3) не изменяется4) может и увеличиваться, и уменьшаться5) сначала уменьшается, потом увеличивается
114. При гипоксии количество эритропоэтинов:
+1) увеличивается2) уменьшается3) не изменяется4) может и увеличиваться, и уменьшаться5) сначала уменьшается, потом увеличивается
115. Интенсивность эритропоэза при гипоксемии:
+1) увеличивается2) уменьшается3) не изменяется4) может и увеличиваться, и уменьшаться5) сначала уменьшается, потом увеличивается
116. Под влиянием эстрогенов интенсивность эритропоэза:
1) увеличивается +2) уменьшается 3) не изменяется4) может и увеличиваться, и уменьшаться5) сначала уменьшается, потом увеличивается
117. Интенсивность эритропоэза становится меньше под влиянием:
1) соматотропного гормона2) тиреотропного гормона+3) эстрогенов4) АКТГ5) андрогенов
118. Под влиянием соматотропного гормона скорость эритропоэза:
+1) увеличивается2) уменьшается3) не изменяется4) может и увеличиваться, и уменьшаться5) сначала уменьшается, потом увеличивается
119. Эритропоэз при увеличении секреции тиреотропного гормона:
+1) увеличивается2) уменьшается3) не изменяется4) может и увеличиваться, и уменьшаться5) сначала уменьшается, потом увеличивается
120. Эритропоэз при увеличении секреции андрогенов:
+1) увеличивается2) уменьшается3) не изменяется4) может и увеличиваться, и уменьшаться5) сначала уменьшается, потом увеличивается
Дыхание — непременное условие жизнедеятельности клеток организма, которые поглощают кислород и выделяют двуокись углерода. Функцию транспортного средства, доставляющего О2 и выводящего СО2, выполняет кровь. Карбогемоглобин — это ее важная составляющая, участвующая в газообмене.

Что это такое
Гемоглобин (Hb) состоит из гема, соединения, содержащего железо, и белкового вещества глобина. Связываясь с О2, поступающим в кровь из легких, Hb снабжает им ткани, а соединяясь с СО2, очищает их от двуокиси углерода и доставляет ее к альвеолам, через которые этот газ удаляется в атмосферу.
Существуют 3 фракции (вида, модификации) гемоглобина, обусловленные физиологическими функциями. Соединяясь с О2, Hb превращается в оксигемоглобин НbО2. Это ярко-красное вещество преобладает в артериальной крови. Кроме того, оно содержится и в миокарде, во всех скелетных мышцах. Мышечный гемоглобин связывает около 10-14% всего О2 в организме. Миоглобин обеспечивает мышцы кислородом, когда они сокращаются, поскольку в это время кровоток приостанавливается.
НbО2, отдав тканям кислород, преобразуется в восстановленный (редуцированный) гемоглобин HНb. Эта субстанция содержится в венозной крови, обуславливая ее темно-вишневую окраску.
Соединение гемоглобина с углекислым газом называется карбогемоглобином. НbСO2 выводит двуокись углерода из клеток и транспортирует в легкие до 20% этого газа. Карбогемоглобин тоже содержится в венозной крови. Hb непрерывно преобразуется из оксигемоглобина в карбогемоглобин и обратно.
Кроме того, Hb образует стойкое соединение с глюкозой, содержащейся в крови. При диабете уровень гликированного гемоглобина HbA1c существенно возрастает. По динамике его концентрации можно судить об эффективности лечения этого заболевания.
Еще одна модификация Hb — фетальный гемоглобин, который содержится в крови новорожденных и исчезает к 1 году. Его наличие у взрослых свидетельствует о нарушениях в организме.
Однако Hb может видоизменяться, образуя и патологические модификации. Соединение гемоглобина с угарным газом называется карбоксигемоглобином. HbСО утрачивает способность транспортировать О2, поэтому клетки испытывают острое кислородное голодание. Анализ на наличие карбоксигемоглобина используется в криминалистике, поскольку позволяет выявить скрытые следы крови. Так, например, отсутствие HbСО в костной ткани трупного материала доказывает, что погибший был уже мертв до начала пожара.
От сильной гипоксии ткани также страдают, когда Hb окисляется и двухвалентное железо в геме замещается трехвалентным Fe. Образующийся при этом метгемоглобин HbMet настолько прочно связывается с О2, что практически не отдает его клеткам. Такое патологическое состояние наступает при отравлении нитратами, нитритами, анилинами, перекисью водорода, марганцовокислым калием, бертолетовой солью и другими веществами-окислителями.
Норма и отклонения
Количество гемоглобина в крови считается оптимальным в следующих пределах (г/л):
- у мужчин: 130-160, после 55-60 лет — 120-140;
- у женщин: 120-140, при беременности — 110-150;
- у детей: до 6 лет — 110-140, до 15 лет — 115-150;
- у жителей высокогорных районов: на 10-20 г/л выше.
Карбоксигемоглобин обнаруживается у некурящих в диапазоне от 0,5 до 1,5%, а у курильщиков — от 4 до 9% от всего объема Hb. О тяжелых отравлениях свидетельствуют показатели более 20%.
Норма в крови метгемоглобина — 0,04-1,52 %. При отравлениях концентрация HbMet достигает более 15%. Летальный исход наступает, если отклонения в показателях превышают 70%.
Проведение и расшифровка анализа
Результаты исследования Hb в медучреждениях нередко отличаются друг от друга, поскольку лаборатории оснащены приборами разных поколений. При проведении анализов крови нередко сказывается и субъективный фактор, зависящий от квалификации лаборанта. Кроме того, следует иметь в виду, что количество гемоглобина максимально вечером и минимально утром.
Сегодня наиболее распространен традиционный метод Сали. Содержание Hb определяют, добавляя к крови соляную кислоту. При этом гем, соединяясь с HCl, преобразуется в кристаллический гемин. Анализы биоматериалов на гемин применяются в судебной медицине для выявления следов крови.
Наиболее точные результаты дает автоматизированный метод с использованием гемометра. Такое исследование проводится гораздо быстрее. Но и при этом методе возможны незначительные расхождения показателей. Однако при расшифровке анализа следует обращать внимание на большие отклонения от нормы Hb, которые свидетельствуют о патологических процессах.
Так, избыток гемоглобина может быть следствием:
- легочной недостаточности;
- обезвоживания организма;
- химических отравлений;
- заболеваний крови, печени, кишечника;
- пороков сердца и др.
Дефицит Hb может быть признаком:
- анемий различной этиологии;
- нарушений менструального цикла;
- эрозий и изъязвлений ЖКТ;
- внутренних кровотечений;
- инфекций;
- воспалительных процессов с отечностью;
- сахарного диабета;
- заболеваний почек;
- злокачественных опухолей и других патологий.
При существенных отклонениях гемоглобина от нормы следует незамедлительно пройти углубленное обследование организма. Вовремя назначенное лечение позволит избежать развития многих опасных заболеваний.
Гемоглобин (Нв) – основной компонент эритроцитов, благодаря которому эритроциты выполняют дыхательную функцию и поддерживают рН крови. По химической природе он относится к хромопротеидам. У мужчин в крови содержится в среднем 130-160 г/л гемоглобина, у женщин – 120‑150 г/л. Молекулярная масса гемоглобина составляет около 60000 Да. Гемоглобин состоит из белка глобина и 4 молекул гема. Гем имеет в своем составе атом железа, способный присоединять или отдавать молекулу кислорода. Гем содержит двухвалентное железо, которое играет ключевую роль в деятельности гемоглобина, являясь его активной (простетической) группой. Гемоглобин синтезируется эритро- и нормобластами костного мозга. Для нормального синтеза гемоглобина необходимо достаточное поступление железа с пищей. При разрушении эритроцитов гемоглобин, после отщепления гема, превращается в билирубин – желчный пигмент, который поступает, в основном, в кишечник в составе желчи, где превращается в стеркобилин, выводящийся из организма с каловыми массами. Часть билирубина удаляется с мочой в виде уробилина.
Основная функция гемоглобина – перенос кислорода и углекислого газа. Гемоглобин, присоединивший к себе кислород, превращается в оксигемоглобин. Соединение гемоглобина с кислородом происходит в капиллярах легких. Это соединение непрочное. В виде оксигемоглобина переносится большая часть кислорода. Гемоглобин, отдавший кислород, называется восстановленным, или дезоксигемоглобином. Гемоглобин, соединенный с углекислым газом носит название карбгемоглобина. Соединение гемоглобина с углекислым газом происходит в капиллярах тканей организма. Это соединение легко распадается. В виде этого соединения переносится 20 % СО2. Оксигемоглобин и карбгемоглобин являются физиологическими соединениями гемоглобина.
В скелетных и сердечной мышцах находится мышечный гемоглобин, называемый миоглобином. Он играет важную роль в снабжении кислородом работающих мышц, его можно рассматривать, как депо О2 в мышцах.
Имеется несколько форм гемоглобина, отличающихся строением белковой части – глобина. Первые 7-12 нед. внутриутробного развития зародыша его красные кровяные тельца содержат примитивный гемоглобин. У плода содержится гемоглобин F (80 %) или фетальный гемоглобин (от англ. Faetus – плод) гемоглобин. Он обладает более высокой способностью связывать кислород. Это помогает плоду не испытывать гипоксии при относительно низком парциальном напряжении кислорода в его крови. После рождения гемоглобин F практически полностью заменяется на взрослый – гемоглобин А (от англ. adult – взрослый). В эритроцитах взрослого человека содержатся гемоглобин А (95‑98 % Hb A1 и 2-3 % HbA2 ).
Гемоглобин может вступать в соединение и с другими газами. Соединение гемоглобина с угарным газом (СО) называется карбоксигемоглобином – это патологическое соединение, в норме его не существует, т.к. в атмосфере отсутствует СО. Является прочным соединением. Гемоглобин блокирован в нем угарным газом и не способен осуществлять перенос кислорода. Сродство гемоглобина к угарному газу выше его сродства к кислороду, поэтому даже небольшое количество угарного газа в воздухе является опасным для жизни. При этом более критическим является не концентрация угарного газа, а длительность его вдыхания. Даже предельно низкое содержание СО в воздухе, но при длительном вдыхании, например, во время сна может оказаться летальным. Вследствие своего высокого сродства угарный газ в виде карбоксигемоглобина способен циркулировать в крови предельно долго.
Часто отравления угарным газом возникают у водителей при длительном нахождении в закрытом гараже с включенным двигателем автомобиля. Другим распространенным клинически значимым источником СО являются древесный дым, а также сырой кирпич печей изб и свежий печной лак. Поэтому при первом или после длительного перерыва протапливании таких печей необходимо тщательное проветривание помещения.
Особенностью угарного газа является то, что он не обладает запахом, поэтому отравление развивается незаметно. Часто пострадавший осознает это, когда проявляется миорелаксирующее (расслабление скелетной мускулатуры) действие угарного газа, при этом человек не может самостоятельно покинуть помещение.
Первая помощь при отравлении угарным газом. Пострадавшего следует переместить на свежий воздух. Следует учитывать, что при значительном отравлении сохранность самостоятельного дыхания не снимает необходимости проведения дальнейших действий по оказанию помощи. Наиболее оптимальным будет подача воздуха с повышенным содержание О2, например, из кислородной подушки. При отсутствии таковой – произвести искусственное дыхание. Во время искусственного дыхания в легкие потерпевшего воздух нагнетается под давлением, большим атмосферного. При этом парциальное давление О2 в таком воздухе оказывается большим, чем в норме, что способствует его большему растворению в крови, а также лучшему вытеснению угарного газа из связи с гемоглобином. Если же пострадавший будет дышать самостоятельно, парциальное давление О2 во вдыхаемом воздухе окажется меньшим (примерно, 100 мм рт.ст.), что окажется недостаточным для вытеснения из карбоксигемоглобина угарного газа, т. к. сродство Нb к СО значительно выше, чем О2. В дальнейшем пострадавший должен быть доставлен в больницу.
При воздействии на гемоглобин экзогенных сильных окислителей происходит окисление железа гема с переходом его в 3-х валентную форму. В результате этого образуется метгемоглобин, который не способен присоединять ни О2, ни СО2. В результате окисления гемоглобин прочно удерживает кислород и теряет способность отдавать его тканям, что может привести к гибели организма. К подобным сильным окислителем относятся нитраты и нитриты, содержащиеся, например, в химических удобрениях, также опасность представляют пероксиды, нитрокраски, анилиновые красители и ряд других веществ бытовой химии. В норме ежедневно около 0,5 % всего гемоглобина превращается в метгемоглобин, но затем она снова восстанавливается в гемоглобин специальным ферментом метгемоглобинредуктазой. Встречаются наследственные метгемоглобинемии, когда снижена активность метгемоглобинредуктазы в эритроцитах, что вызывает кислородное голодание.
Метгемоглобин, также как карбоксигемоглобин, относится к группе патологических соединений гемоглобина.
