Соединение окиси углерода с гемоглобином
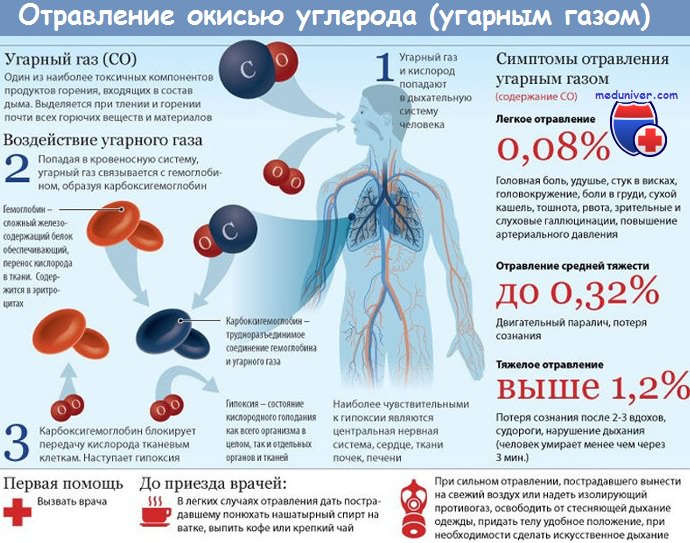
Отравление угарным газом. КарбоксигемоглобинемияКлассическим примером повреждающего действия на кровь с нарушением ее дыхательной функции, обусловленным инактивацией кровяного пигмента — гемоглобина, служит образование карбоксигемоглобина (НbСО) под влиянием оксида углерода. Превращение гемоглобина в НbСО приводит к изменению спектральных характеристик крови, что легло в основу количественного определения его в крови. НbСО образуется в результате взаимодействия оксида углерода (СО) с железом гемоглобина, что лишает его способности к оксигенации, приводит к нарушению транспортной функции и как результат вызывает развитие гемической гипоксии. Появление НbСО служит следствием поступления СО в легкие с вдыхаемым воздухом. Образование НbСО начинается с периферии эритроцитов уже в легочных капиллярах. В дальнейшем с увеличением содержания СО во вдыхаемом воздухе НbСО образуется не только в периферических отделах эритроцита, но и в центральных его отделах. Причем скорость образования НbСО прямо пропорциональна величине концентрации СО во вдыхаемом воздухе, а максимум его в крови определяется временем контакта. Способность гемоглобина связывать 02 и СО одинакова при условии, что 1 г гемоглобина может связывать 1,33—1,34 мл 02. Эта зависимость носит название константы Хюфнера. Вместе с тем сродство гемоглобина к СО в 250—300 раз больше, чем к 02. Примечательно, что оболочка эритроцитов служит своего рода защитным барьером при образовании НbСО, так как во взвеси эритроцитов этого деривата гемоглобина образуется на 20 % меньше, чем в растворе гемоглобина. Валентность железа в НbСО остается неизмененной, происходит лишь перестройка связей Fe2+. Все непарные электроны участвуют в образовании НbСО. Параллельно с образованием связей между СО и Fe2+ изменяется характер связи железа с глобином и порфирином. Она теряет свой ионный характер и превращается в ковалентную. Взаимодействие СО с Нb02 выражается взаимно сопряженными реакциями. нbо2 + со -> нbсо + о2
Скорость этих реакций и образование НЬСО определяются парциальным давлением СО и О2 в воздухе. При этом количество образовавшегося НbCO мо пропорционально давлению СО в окружающей среде и обратно пропорционально давлению 02. Несмотря на высокое, как указывалось выше, сродство СО к гемоглобину, ассоциация его с гемоглобином происходит в 10 раз медленнее, чем таковая с 02. Однако при этом диссоциация HbСО протекает в 3600 раз медленнее, чем диссоциация Нb02. По этой причине HbCO очень быстро накапливается в крови даже при сравнительно небольшом содержании СО во вдыхаемом воздухе. Таким образом, помимо выключения части гемоглобина из транспорта кислорода, еще одним патогенетически важным звеном в нарушении дыхательной функции крови на фоне карбоксигемоглобинемии служит замедление диссоциации оксигемоглобина под влиянием НЬСО, что известно под названием эффекта Холдена. Так в физиологических условиях повышение концентрации С02 в крови способствует ускоренному отщеплению 02 от НЬ02, при наличии НЬСО этот сбалансированный процесс нарушается. Принято считать, что суть эффекта Холдена заключается в том, что при взаимодействии СО с гемоглобином поступивший в кровь СО соединяется только с 3 из 4 атомов железа в молекуле гемоглобина, тогда как с 4-м атомом железа соединяется 02, сродство которого к этому атому железа резко возрастает, что, естественно, затрудняет диссоциацию оксигемоглобина. Еще одним причинным фактором угнетения диссоциации Нb02 под влиянием СО служит снижение уровня промежуточного метаболита 2,3-дифосфоглицерата, который образуется в процессе реакции гликолиза. 2,3-Дифосфоглицерат обладает способностью усиливать процесс диссоциации НbСО за счет вызываемых им конформационных изменений гемоглобина, поэтому естественно, что дефицит этого метаболита косвенно тормозит высвобождение 02 из Нb02. Итак, основным пусковым механизмом развития специфической гемической гипоксии при отравлении СО является образование НbСО, который утрачивает способность переносить кислород в сочетании с угнетающим влиянием на процесс диссоциации Нb02. Неопровержимое доказательство того, что первопричиной развития СО-интоксикации является карбоксиге-моглобинемия, — прямая зависимость между уровнем НbСО в крови и тяжестью интоксикации. Так, по данным V.E.Henderson, при содержании НbСО в крови, равном 10 %, отмечена лишь одышка при физическом напряжении, при 40—50 % НbСО появляются явные признаки интоксикации: головная боль, помрачение сознания вплоть до его потери, концентрация НbСО в крови свыше 60 % ведет к летальному исходу. Во всяком случае у людей, впадающих в коматозное состояние или погибающих от острого отравления СО, содержание НbСО, как правило, не менее 50 %. Однако не всегда прослеживается прямая связь между содержанием в крови НbСО и тяжестью отравления. Известны случаи, когда тяжелая форма отравления развивалась уже при 20 % НbСО и, наоборот, при 60 % НbСО встречаются легкие формы отравления. Во многом это объясняется достаточно большой индивидуальной чувствительностью к СО, которую связывают с генетическим фактором. – Также рекомендуем “Диагностика карбоксигемоглобинемии. Изменения красной крови при карбоксигемоглобинемии” Оглавление темы “Алкилирующие яды. Отравление угарным газом”: |
Оксид углерода (угарный газ, СО) обладает гораздо большим сродством к гемоглобину, чем кислород. Даже при крайне низких парциальных давлениях СО гемоглобин превращается в карбоксигемоглобин: Нb+СО Þ НbСО. Равновесие этой реакции значительно смещено вправо, поэтому кривая диссоциации карбоксигемоглобина имеет очень крутой наклон. Высокое сродство оксида углерода к гемоглобину обусловлено тем, что СО диссоциирует от НЬ гораздо медленнее, чем О2. Максимально эффективная концентрация для СО составляет 30 частей на миллион, что соответствует 0,003 объемных %. В артериальной крови человека, пребывающего достаточно долго в среде с таким содержанием СО, на долю НЬСО приходится около 5% общего содержания гемоглобина. Парциальные давления СО и О2, при которых содержание соответственно НbСО и НbО2 составляет по 5%, соотносятся как 1:350. Иными словами, в данных пределах парциальных давлений сродство Нb к СО примерно в 35O раз выше, чем к О2.
Токсичность оксида углерода обусловлена именно высоким сродством этого соединения к гемоглобину. СО представляет собой газ без цвета и запаха, образующийся при неполном сгорании органических веществ. Иногда он входит в состав бытового газа; кроме того, он выделяется при работе двигателей внутреннего сгорания. Даже при низких концентрациях СО вытесняет кислород из соединения с гемоглобином, при этом последний теряет способность к переносу О2. В норме на долю НbСО приходится лишь 1% общего количества гемоглобина в крови; у курильщиков же к вечеру она достигает 20%. Об опасности, которую угарный газ представляет для автомобилистов, говорит тот факт, что на дорогах с особенно интенсивным движением содержание СО в воздухе достигает 3-10 ч. При такой концентрации СО шахтерам положено надевать дыхательные аппараты.
Токсичность угарного газа обусловлена не только блокированием гемоглобина, но и другим эффектом. Когда часть гемоглобина превращается в НbСО, кривая диссоциации оксигемоглобина (для гемоглобина, еще не блокированного СО) сдвигается влево и может в итоге приобретать форму гиперболы. В результате происходит еще большее снижение напряжения О2 в тканевых капиллярах.
При тяжелом отравлении угарным газом, отличительным признаком которого служит вишнево-красная окраска крови, жизнь пострадавшего можно спасти путем немедленного применения искусственного дыхания, по возможности с чистым кислородом. При этом напряжение кислорода в крови увеличивается, и О2 частично вытесняет СО из связи с гемоглобином. Рекомендуется также переливание большого количества крови, так как при этом в кровь пострадавшего поступает гемоглобин, способный переносить кислород.
Перенос СО2 кровью. Формы транспорта СО2.
Диоксид углерода (СО2, углекислый газ) ― конечный продукт окислительного метаболизма в клетках ― переносится с кровью к легким и удаляется через них во внешнюю среду. Подобно кислороду, диоксид углерода может переноситься как в физически растворенном виде, так и в составе химических соединений. Химическое связывание СО2 ―более сложный процесс по сравнению со связыванием кислорода. Это обусловлено тем, что механизм, отвечающий за транспорт СО2, должен одновременно обеспечивать поддержание постоянства кислотно-щелочного равновесия крови и тем самым внутренней среды организма в целом.
Связывание СО2. Напряжение СО2 в артериальной крови, поступающей в тканевые капилляры, составляет 40 мм рт.ст. (5,3 кПа). В клетках же, расположенных около этих капилляров, напряжение СО2 значительно выше, так как углекислый газ постоянно образуется в процессе метаболизма. В связи с этим физически растворенный СО2 диффундирует по градиенту напряжения из тканей в капилляры. Здесь некоторое количество углекислого газа остается в растворенном состоянии, но большая часть СО2 претерпевает ряд химических превращений. Прежде всего, происходит гидратация молекул СО2 с образованием угольной кислоты, сразу же диссоциирующей на ион бикарбоната и протон:
В плазме крови эта реакция протекает очень медленно; в эритроците же она ускорена примерно в 10 тыс. раз. Это связано с действием фермента карбоангидразы. Поскольку этот фермент присутствует только в эритроцитах, практически все молекулы СО2, участвующие в реакции гидратации, должны сначала проникнуть в эритроциты.
Роль разных форм СО2 в газообмене. В крови, поступающей к тканям, напряжение СО2 составляет 40 мм рт.ст. Проходя через них, кровь насыщается углекислым газом, и напряжение его в оттекающей из тканей крови достигает в среднем 46 мм рт.ст. При этом 1 л крови поглощает примерно 1,8 ммоль СО2. Около 12% этого количества остается в физически растворенном виде или в форме недиссоциированной угольной кислоты, 11% образует карбаминовое соединение с гемоглобином, 27% транспортируется в виде бикарбоната в эритроцитах, а остальное количество ― около 50% ― растворено в виде НСО3¯ в плазме. При прохождении крови через легкие СО2 высвобождается из этих четырех форм в таком же соотношении.
Сатурационные кривые СО2
Зависимость содержания СО2 от его напряжения. Общее содержание диоксида углерода в крови складывается из концентраций физически растворенного и форм химически связанного СО2 ― угольной кислоты, карбамата и бикарбоната. Большая часть СО2 присутствует внутри и вне эритроцитов в форме бикарбоната. При повышении РСО2 содержание всех этих форм СО2 увеличивается.
Связь между концентрацией в крови и парциальным давлением СО2 описывается сатурационной кривой, сходной с кривой диссоциации оксигемоглобина. Зависимость связывания СО2 от степени оксигенации гемоглобина называют эффектом Христиансена-Дугласа-Холдена «или кратко эффектом Холдена.
Существует принципиальная разница между сатурационными кривыми связывания СО2 и кривыми диссоциации оксигемоглобина. Кривые диссоциации НbО2 асимптотически приближаются к максимуму, а связывание СО2 не достигает насыщения. По мере увеличения парциального давления СО2 количество связанного СО2 постоянно возрастает, так как образование бикарбоната в крови практически не лимитировано.
Физиологическое значение эффекта Христиансена-Дугласа-Холдена. При рассмотрении процессов поступления СО2 в кровь из тканей и его высвобождения в легких следует помнить о том, что эти процессы происходят одновременно с обменом О2. Изменения в насыщении гемоглобина кислородом влияют на связывание СО2 кровью и тем самым на его обмен.
К тканевым капиллярам обычно притекает полностью оксигенированная кровь. По мере того как кровь проходит через капилляры и кислород выходит из нее в ткани, способность крови поглощать СО2 увеличивается. Таким образом, эффект Христиансена-Дугласа-Холдена способствует поглощению СО2 кровью в тканях. В легких происходят обратные процессы. В результате того, что в кровь поступает кислород, ее сродство к углекислому газу снижается, и тем самым облегчается диффузия СО2 в альвеолы. Итак, мы убедились в том, что как при поступлении СО2 в кровь из тканей, так и при выделении его в легких эффект Христиансена-Дугласа-Холдена способствует диффузионному обмену этого газа.
Гемоглобин (Нв) – основной компонент эритроцитов, благодаря которому эритроциты выполняют дыхательную функцию и поддерживают рН крови. По химической природе он относится к хромопротеидам. У мужчин в крови содержится в среднем 130-160 г/л гемоглобина, у женщин – 120-150 г/л. Молекулярная масса гемоглобина составляет около 60000 Да. Гемоглобин состоит из белка глобина и 4 молекул гема. Гем имеет в своем составе атом железа, способный присоединять или отдавать молекулу кислорода.
Гем содержит двухвалентное железо, которое играет ключевую роль в деятельности гемоглобина, являясь его активной (простетической) группой. Гемоглобин синтезируется эритро- и нормобластами костного мозга. Для нормального синтеза гемоглобина необходимо достаточное поступление железа с пищей. При разрушении эритроцитов гемоглобин, после отщепления гема, превращается в билирубин – желчный пигмент, который поступает, в основном, в кишечник в составе желчи, где превращается в стеркобилин, выводящийся из организма с каловыми массами. Часть билирубина удаляется с мочой в виде уробилина.
Основная функция гемоглобина – перенос кислорода и углекислого газа. Гемоглобин, присоединивший к себе кислород, превращается в оксигемоглобин. Соединение гемоглобина с кислородом происходит в капиллярах легких. Это соединение непрочное. В виде оксигемоглобина переносится большая часть кислорода. Гемоглобин, отдавший кислород, называется восстановленным, или дезоксигемоглобином. Гемоглобин, соединенный с углекислым газом носит название карбгемоглобина. Соединение гемоглобина с углекислым газом происходит в капиллярах тканей организма. Это соединение легко распадается. В виде этого соединения переносится 20 % СО2. Оксигемоглобин и карбгемоглобин являются физиологическими соединениями гемоглобина.
В скелетных и сердечной мышцах находится мышечный гемоглобин, называемый миоглобином. Он играет важную роль в снабжении кислородом работающих мышц, его можно рассматривать, как депо О2 в мышцах.
Имеется несколько форм гемоглобина, отличающихся строением белковой части – глобина. Первые 7-12 нед. внутриутробного развития зародыша его красные кровяные тельца содержат примитивный гемоглобин. У плода содержится гемоглобин F (80 %) или фетальный гемоглобин (от англ. Faetus – плод) гемоглобин. Он обладает более высокой способностью связывать кислород. Это помогает плоду не испытывать гипоксии при относительно низком парциальном напряжении кислорода в его крови. После рождения гемоглобин F практически полностью заменяется на взрослый – гемоглобин А (от англ. adult – взрослый). В эритроцитах взрослого человека содержатся гемоглобин А (95-98 % Hb A1 и 2-3 % HbA2 ).
Гемоглобин может вступать в соединение и с другими газами. Соединение гемоглобина с угарным газом (СО) называется карбоксигемоглобином – это патологическое соединение, в норме его не существует, т.к. в атмосфере отсутствует СО. Является прочным соединением. Гемоглобин блокирован в нем угарным газом и не способен осуществлять перенос кислорода. Сродство гемоглобина к угарному газу выше его сродства к кислороду, поэтому даже небольшое количество угарного газа в воздухе является опасным для жизни. При этом более критическим является не концентрация угарного газа, а длительность его вдыхания. Даже предельно низкое содержание СО в воздухе, но при длительном вдыхании, например, во время сна может оказаться летальным. Вследствие своего высокого сродства угарный газ в виде карбоксигемоглобина способен циркулировать в крови предельно долго.
Часто отравления угарным газом возникают у водителей при длительном нахождении в закрытом гараже с включенным двигателем автомобиля. Другим распространенным клинически значимым источником СО являются древесный дым, а также сырой кирпич печей изб и свежий печной лак. Поэтому при первом или после длительного перерыва протапливании таких печей необходимо тщательное проветривание помещения.
Особенностью угарного газа является то, что он не обладает запахом, поэтому отравление развивается незаметно. Часто пострадавший осознает это, когда проявляется миорелаксирующее (расслабление скелетной мускулатуры) действие угарного газа, при этом человек не может самостоятельно покинуть помещение.
Первая помощь при отравлении угарным газом. Пострадавшего следует переместить на свежий воздух. Следует учитывать, что при значительном отравлении сохранность самостоятельного дыхания не снимает необходимости проведения дальнейших действий по оказанию помощи. Наиболее оптимальным будет подача воздуха с повышенным содержание О2, например, из кислородной подушки. При отсутствии таковой – произвести искусственное дыхание. Во время искусственного дыхания в легкие потерпевшего воздух нагнетается под давлением, большим атмосферного.
При этом парциальное давление О2 в таком воздухе оказывается большим, чем в норме, что способствует его большему растворению в крови, а также лучшему вытеснению угарного газа из связи с гемоглобином. Если же пострадавший будет дышать самостоятельно, парциальное давление О2 во вдыхаемом воздухе окажется меньшим (примерно, 100 мм рт.ст.), что окажется недостаточным для вытеснения из карбоксигемоглобина угарного газа, т. к. сродство Нb к СО значительно выше, чем О2. В дальнейшем пострадавший должен быть доставлен в больницу.
При воздействии на гемоглобин экзогенных сильных окислителей происходит окисление железа гема с переходом его в 3-х валентную форму. В результате этого образуется метгемоглобин, который не способен присоединять ни О2, ни СО2. В результате окисления гемоглобин прочно удерживает кислород и теряет способность отдавать его тканям, что может привести к гибели организма.
К подобным сильным окислителем относятся нитраты и нитриты, содержащиеся, например, в химических удобрениях, также опасность представляют пероксиды, нитрокраски, анилиновые красители и ряд других веществ бытовой химии. В норме ежедневно около 0,5 % всего гемоглобина превращается в метгемоглобин, но затем она снова восстанавливается в гемоглобин специальным ферментом метгемоглобинредуктазой. Встречаются наследственные метгемоглобинемии, когда снижена активность метгемоглобинредуктазы в эритроцитах, что вызывает кислородное голодание. Метгемоглобин, также как карбоксигемоглобин, относится к группе патологических соединений гемоглобина.
