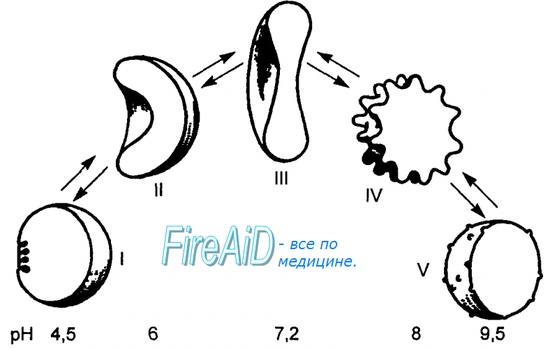
Сродство гемоглобина к кислороду при гиперкапнии
Оглавление темы “Вентиляция легких. Перфузия легких кровью.”: Сродство гемоглобина к кислороду. Изменение сродства гемоглобина к кислороду. Эффект Бора.Молекула гемоглобина может находиться в двух формах — напряженной и расслабленной. Расслабленная форма гемоглобина имеет свойство насыщаться кислородом в 70 раз быстрее, чем напряженная. Изменение фракций напряженной и расслабленной формы в общем количестве гемоглобина в крови обусловливает S-образный вид кривой диссоциации оксигемоглобина, а следовательно, так называемое сродство гемоглобина к кислороду. Если вероятность перехода от напряженной формы гемоглобина к расслабленной больше, то возрастает сродство гемоглобина к кислороду, и наоборот. Вероятность образования указанных фракций гемоглобина изменяется в большую или меньшую сторону под влиянием нескольких факторов. Основной фактор — это связывание кислорода с геминовой фуппой молекулы гемоглобина. При этом чем больше геминовых фупп гемоглобина связывают кислород в эритроцитах, тем более легким становится переход молекулы гемоглобина к расслабленной форме и тем выше их сродство к кислороду. Поэтому при низком Р02, что имеет место в метаболически активных тканях, сродство гемоглобина к кислороду ниже, а при высоком Р02 — выше. Как только гемоглобин захватывает кислород, повышается его сродство к кислороду и молекула гемоглобина становится насыщенной при связывании с четырьмя молекулами кислорода.
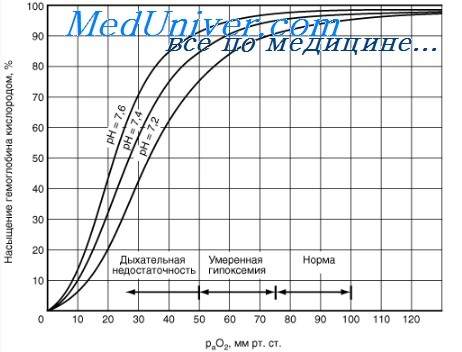
Когда эритроциты, содержащие гемоглобин, достигают тканей, то кислород из эритроцитов диффундирует в клетки. В мышцах он поступает в своеобразного депо кислорода — в молекулы миоглобина, из которого кислород используется в биологическом окислении мышц. Диффузия кислорода из гемоглобина эритроцитов в ткани обусловлена низким Р02 в тканях — 35 мм рт. ст. Внутри клеток тканей напряжение кислорода, необходимое для поддержания нормального метаболизма, составляет еще меньшую величину — не более 1 кПа. Поэтому кислород путем диффузии из капилляров достигает метаболически активных клеток. Некоторые ткани приспособлены к низкому содержанию Р02 в капиллярах крови, что компенсируется высокой плотностью капилляров на единицу объема тканей. Например, в скелетной и сердечной мышцах Р02 в капиллярах может снизиться чрезвычайно быстро во время сокращения. В мышечных клетках содержится белок миоглобин, который имеет более высокое сродство к кислороду, чем гемоглобин. Миоглобин интенсивно насыщается кислородом и способствует его диффузии из крови в скелетную и сердечную мышцы, где он обусловливает процессы биологического окисления. Эти ткани способны экстрагировать до 70 % кислорода из крови, проходящей через них, что обусловлено снижением сродства гемоглобина к кислороду под влиянием температуры тканей и рН. Эффект рН и температуры на сродство гемоглобина к кислороду. Молекулы гемоглобина способны реагировать с ионами водорода, в результате этой реакции происходит снижение сродства гемоглобина к кислороду. При насыщении гемоглобина менее 100 % низкое рН понижает связывание кислорода с гемоглобином — кривая диссоциации оксигемоглобина смещается вправо по оси х. Это изменение свойства гемоглобина под влиянием ионов водорода называется эффектом Бора. Метаболически активные ткани продуцируют кислоты, такую как молочная, и С02. Если рН плазмы крови снижается от 7,4 в норме до 7,2, что имеет место при сокращении мыщц, то концентрация кислорода в ней будет возрастать вследствие эффекта Бора. Например, при постоянном рН 7,4 кровь отдавала бы порядка 45 % кислорода, т. е. насыщение гемоглобина кислородом снижалось до 55 %. Однако когда рН снижается до 7,2, кривая диссоциации смещается по оси х вправо. В результате насыщение гемоглобина кислородом падает до 40 %, т. е. кровь может отдавать в тканях до 60 % кислорода, что на 1/з больше, чем при постоянном рН.
Метаболически активные ткани повышают продукцию тепла. Повышение температуры тканей при физической работе изменяет соотношение фракций гемоглобина в эритроцитах и вызывает смещение кривой диссоциации оксигемоглобина вправо вдоль оси х. В результате большее количество кислорода будет освобождаться из гемоглобина эритроцитов и поступать в ткани. Эффект 2,3-дифосфоглицерата (2,3-ДФГ) на сродство гемоглобина к кислороду. При некоторых физиологических состояниях, например при понижении Р02 в крови ниже нормы (гипоксия) в результате пребывания человека на большой высоте над уровнем моря, снабжение тканей кислородом становится недостаточным. При гипоксии может понижаться сродство гемоглобина к кислороду вследствие увеличения содержания в эритроцитах 2,3-ДФГ. В отличие от эффекта Бора, уменьшение сродства гемоглобина к кислороду под влиянием 2,3-ДФГ не является обратимым в капиллярах легких. Однако при движении крови через капилляры легких эффект 2,3-ДФГ на снижение образования оксигемоглобина в эритроцитах (плоская часть кривой диссоциации оксигемоглобина) выражен в меньшей степени, чем отдача кислорода под влиянием 2,3-ДФГ в тканях (наклонная часть кривой), что обусловливает нормальное кислородное снабжение тканей. – Также рекомендуем “Углекислый газ. Транспорт углекислого газа.” |
Факторы влияющие на КДО. Влияние температуры на кривую диссоциации оксигемоглобина (КДО)
Обсуждению этого вопроса посвящена обширная литература. Считается, что наибольшее влияние на положение КДО оказывает кислотность среды (эффект Бора). Было установлено, что при Ph больше 6,0 в крови преобладает оксигемоглобин, при Ph менее 6,0 — восстановленный гемоглобин.
Было установлено также, что на величину Р50 влияет находящееся в эритроците фосфорное соединение 2,3 дифосфоглицерат (2,3-ДФГ) и что концентрация этого вещества увеличивается по мере снижения Ph. Высказывалось даже предположение, что на положение кривой диссоциации оксигемоглобина Ph влияет через 2,3-ДФГ. Это предположение в дальнейшем частично подтвердилось, что позволило окончательно прояснить роль Ph в изменениях положения КДО.
Ph, изменяя структуры групп гемоглобина, связанных с кислородом, непосредственно влияет на аффинитет гемоглобина с кислородом. Кроме того, Ph оказывает на положение КДО опосредованное влияние через содержание в эритроците 2,3-ДФГ, поскольку кислая среда активирует образование этого фосфата, а щелочная среда его ингибирует.
Однако 2,3-ДФГ и сам может непосредственно влиять на положение КДО. Воздействуя на атомы железа в молекулах гемоглобина, 2,3-ДФГ снижает сродство гемоглобина к кислороду и способствует ускорению диссоциации оксигемоглобина. Установлено, что увеличение 2,3-ДФГ на 1 ммоль/л повышает Р50 на 1,23 мм Нд. На содержание в эритроците 2,3-ДФГ оказывают непосредственное влияние неорганические фосфаты, тиреоидные и некоторые гипофизарные гормоны.
Основная роль напряжения углекислоты в регуляции положения КДО реализуется через влияние ее на кислотность среды. При гиперкапнии Ph снижается, при гипокапнии — повышается.

Температура крови оказывает серьезное влияние на положение кривой диссоциации оксигемоглобина. Установлено, что при гипертермии КДО смещается вправо, при гипотермии — влево.
Этот феномен имеет серьезный физиологический смысл. В альвеоле притекающая кровь контактирует с охлажденным альвеолярным воздухом, что способствует смещению КДО влево и повышению аффинитета гемоглобина с кислородом. Ускоряется оксигенация крови.
В тканях, особенно в функционирующей мышечной ткани, температура всегда повышена. Это способствует смещению КДО вправо и снижению сродства гемоглобина к кислороду, что облегчает переход кислорода в клетки.
Воздействие температуры на положение КДО усиливается под влиянием 2,3-ДФГ. При низком содержании этого фосфата в эритроците, при прочих равных условиях, влияние гипотермии на увеличение аффинитета гемоглобина к кислороду существенно повышается и способствует большему смещению кривой влево.
Данный феномен создает серьезные проблемы для реаниматолога в случаях переохлаждения организма пострадавшего (длительное нахождение в холодной воде, замерзание при отрицательной температуре воздуха, особенно в состоянии алкогольного опьянения). В этой ситуации сродство гемоглобина к кислороду может быть столь высоким, что на тканевом уровне практически прекращается газообмен.
Противоположная ситуация возникает при гипертермии, при которой на фоне резкого увеличения потребности в кислороде в силу низкого аффинитета гемоглобина к кислороду (смещение КДО вправо) возникают сложности в оксигенации крови в легких.
– Также рекомендуем “Значение положения кривой диссоциации оксигемоглобина (КДО). Механизм формирования КДО”
Оглавление темы “Параметры потребления кислорода и гемодинамики”:
1. Кривая диссоциации оксигемоглобина (КДО). Физиологический смысл КДО
2. Кислородтранспортная функция крови. Нормальная кривая диссоциации оксигемоглобина (КДО)
3. Факторы влияющие на КДО. Влияние температуры на кривую диссоциации оксигемоглобина (КДО)
4. Значение положения кривой диссоциации оксигемоглобина (КДО). Механизм формирования КДО
5. Гемодинамические параметры. Кислородный поток и потребление кислорода
6. Факторы влияющие на потребление кислорода. Предупреждение критической тканевой гипоксии
7. Законы Старлинга. Сердечный выброс по Старлингу
8. Регуляция сердечного выброса по кислороду. Влияние венозного притока на сократимость миокарда
9. Современный взгляд на сердечный выброс. Взаимоотношение факторов влияющих на сократимость миокарда
10. Неконтролируемая внутривенная инфузия. Кривая венозного притока
факторы.
Под действием перечисленных факторов изменяется степень сродства гемоглобина к
кислороду, что оказывает влияние на скорость взаимодействия между ними, прочность
связи и быстроту диссоциации НbО2 в капиллярах тканей, а это очень важно, так как в
клетки тканей проникает только физически растворенный
Рис. 16-7.
Кривая диссоциации оксигемоглобина: раО2 – рО2 в артериальной крови; SаО2 – насыщение
гемоглобина артериальной крови кислородом; СаО2 – содержание кислорода в
артериальной крови
Рис. 16-8.
Влияние различных факторов на кривую диссоциации оксигемоглобина: А – температуры, Б – рН, В – раСО2
в плазме крови кислород. В зависимости от изменения степени сродства гемоглобина к
кислороду происходят сдвиги кривой диссоциации оксигемоглобина. Если в норме
превращение 50% гемоглобина в НbО2 происходит при раО2, равном 26,6 мм рт.ст., то при
снижении сродства между гемоглобином и кислородом это имеет место при 30-32 мм
рт.ст. В результате кривая смещается вправо. Сдвиг кривой диссоциации НbО2 вправо
происходит при метаболическом и газовом (гиперкапния) ацидозе, при повышении
температуры тела (лихорадка, перегревание, лихорадоподобные состояния), при
увеличении содержания АТФ и 2,3-ДФГ в эритроцитах;
накопление последнего имеет место при гипоксемии, различных видах анемий (особенно
при серповидно-клеточной). При всех указанных состояниях увеличивается быстрота
отщепления кислорода от НbО2 в капиллярах тканей, и вместе с тем замедляется скорость
оксигенации гемоглобина в капиллярах легких, что ведет к снижению содержания
кислорода в артериальной крови.
Сдвиг кривой диссоциации НbО2 влево происходит при увеличении сродства
гемоглобина к кислороду и наблюдается при метаболическом и газовом (гипокапния) алкалозе, при общей гипотермии и в участках местного охлаждения тканей, при
понижении содержания в эритроцитах 2,3-ДФГ (например, при сахарном диабете), при
отравлении окисью углерода и при метгемоглобинемии, при наличии в эритроцитах
больших количеств фетального гемоглобина, что имеет место у недоношенных детей. При
сдвиге влево (вследствие повышения сродства гемоглобина к кислороду) ускоряется
процесс оксигенации гемоглобина в легких, и вместе с тем замедляется процесс
дезоксигенации НbО2 в капиллярах тканей, что ухудшает снабжение клеток кислородом, в том
числе клеток ЦНС. Это может вызвать ощущение тяжести в голове, головную боль и тремор.
Снижение транспорта кислорода к тканям будет наблюдаться при уменьшении
кислородной емкости крови вследствие анемии, гемодилюции, образования карбокси- и
метгемоглобина, не участвующих в транспорте кислорода, а также при понижении
сродства гемоглобина к кислороду. Снижение содержания НbО2 в артериальной крови
происходит при усиленном ее шунтировании в легких, при пневмонии, отеке, эмболии a.
pulmonalis. Доставка кислорода тканям уменьшается при снижении объемной скорости
кровотока в связи с сердечной недостаточностью, гипотонией, снижением объема
циркулирующей крови, расстройством микроциркуляции вследствие уменьшения
количества функционирующих микрососудов из-за нарушения их проходимости или
централизации кровообращения. Доставка кислорода становится недостаточной при
увеличении расстояния между находящейся в капиллярах кровью и клетками тканей в
связи с развитием интерстициального отека и гипертрофией клеток. При всех указанных
нарушениях может развиться гипоксия.
Важным показателем, позволяющим определить количество кислорода, поглощенное
тканями, является индекс утилизации кислорода, который представляет собой
умноженное на 100 отноше-
ние артериовенозной разницы по содержанию кислорода к объему его в артериальной
крови. В норме при прохождении крови через тканевые капилляры используется клетками
в среднем 25% поступающего кислорода. У здорового человека индекс утилизации
кислорода существенно возрастает при физической работе. Повышение этого индекса
происходит также при пониженном содержании кислорода в артериальной крови и при
уменьшении объемной скорости кровотока; индекс будет снижаться при уменьшении
способности тканей утилизировать кислород.
16.2.2. Транспорт углекислого газа и его нарушения
Парциальное давление СО2 (рСО2) в артериальной крови такое же, как в альвеолах, и
соответствует 4,7-6,0 кПа (35-45 мм рт.ст., в среднем 40 мм рт.ст.). В венозной крови рСО2
равно 6,3 кПа (47 мм рт.ст.). Количество транспортируемого СО2 в артериальной крови
равняется 50 об.%, а в венозной – 55 об.%. Примерно 10% этого объема физически
растворено в плазме крови, и именно эта часть углекислоты определяет напряжение газа в
плазме; еще 10-11% объема СО2 транспортируется в виде карбгемоглобина, при этом
восстановленный гемоглобин более активно, чем оксигемоглобин, связывает углекислоту.
Остальной объем СО2 переносится в составе молекул бикарбоната натрия и калия,
которые образуются при участии фермента карбоангидразы эритроцитов. В капиллярах
легких по причине превращения гемоглобина в оксигемоглобин связь СО2 с гемоглобином
становится менее прочной и происходит его превращение в физически растворимую
форму. Вместе с тем образующийся оксигемоглобин, являясь сильной кислотой, отнимает
калий от бикарбонатов. Образовавшаяся при этом Н2СО3 расщепляется под действием
карбоангидразы на Н2О и СО2, и последний диффундирует в альвеолы.
Транспорт СО2 нарушается: 1) при замедлении кровотока; 2) при анемиях, когда
уменьшается связывание его с гемоглобином и включение в бикарбонаты из-за недостатка
карбоангидразы (которая содержится только в эритроцитах).
На парциальное давление СО2 в крови существенное влияние оказывает понижение или
повышение вентиляции альвеол. Уже незначительное изменение парциального давления
СО2 в крови влияет на мозговое кровообращение. При гиперкапнии (вследствие
гиповентиляции) сосуды мозга расширяются, повышается
внутричерепное давление, что сопровождается головной болью и головокружением.
Уменьшение парциального давления СО2 при гипервентиляции альвеол снижает мозговой
кровоток, при этом возникает состояние сонливости, возможны обмороки.
16.2.3. Гипоксия
Гипоксия (от греч. hypo – мало и лат. oxigenium – кислород) – состояние, возникающее
при недостаточном поступлении кислорода в ткани или при нарушении его
использования клетками в процессе биологического окисления.
Гипоксия является важнейшим патогенетическим фактором, играющим ведущую роль в
развитии многих заболеваний. Этиология гипоксии отличается большим разнообразием, вместе с тем ее проявления при различных формах патологии и компенсаторные реакции, возникающие при этом, имеют много общего. На этом основании гипоксию можно
считать типическим патологическим процессом.
Виды гипоксии. В.В. Пашутин предложил различать два вида гипоксии –
физиологическую, связанную с повышенной нагрузкой, и патологическую. Д. Баркрофт
(1925) выделил три вида гипоксии: 1) аноксическую, 2) анемическую и 3) застойную.
В настоящее время используется классификация, предложенная И.Р. Петровым (1949), который разделил все виды гипоксии на: 1) экзогенную, возникающую при понижении
рО2 во вдыхаемом воздухе; она была подразделена, в свою очередь, на гипо- и
нормобарическую; 2) эндогенную, возникающую при различного рода заболеваниях и
патологических состояниях. Эндогенная гипоксия представляет собой обширную группу, и в зависимости от этиологии и патогенеза в ней выделены следующие виды: а)
Гипоксия при патологических процессах в организме (эндогенная)
Дыхательная (легочная) гипоксия развивается при различных видах дыхательной недостаточности, когда по тем или другим причинам затруднено проникновение кислорода из альвеол в кровь. Это может быть связано: 1) с плохой вентиляцией альвеол, вследствие чего в них падает парциальное давление кислорода; 2) с их спадением из-за недостатка сурфактанта; 3) с уменьшением дыхательной поверхности легких вследствие понижения количества функционирующих альвеол; 4) с затруднением диффузии кислорода через альвеолярно-капиллярную мембрану; 5) с нарушением кровоснабжения ткани легких, развитием в них отека; 6) с появлением большого количества перфузируемых, но не вентилируемых альвеол; 7) с усилением шунтирования венозной крови в артериальную на уровне легких (пневмония, отек, эмболия a. pulmo-nalis) или сердца (при незаращении боталлова протока, овального отверстия и др.). Из-за этих нарушений снижается рО9 в артериальной крови, уменьшается содержание оксигемоглобина, т.е. возникает состояние гипоксемии. Вместе с тем в крови возрастает содержание восстановленного гемоглобина, что способствует появлению цианоза. При гиповентиляции альвеол развивается гиперкапния, понижающая сродство гемоглобина к кислороду и затрудняющая еще больше процесс оксигенации гемоглобина в легких.
Скорость кровотока и кислородная емкость при дыхательном типе гипоксии нормальны или повышены.
Циркуляторная (сердечно-сосудистая) гипоксия развивается при нарушениях кровообращения и может иметь генерализованный (системный) или местный характер. Причиной раз
сии могут являться: 1) недостаточность функции сердца; 2) снижение сосудистого тонуса (шок, коллапс); 3) уменьшение общей массы крови в организме (гиповолемия) после острой кровопотери и при обезвоживании; 4) усиленное депонирование крови (например, в органах брюшной полости при портальной гипертензии и др.); 5) нарушение текучести крови в случаях сладжа эритроцитов и при ДВС-синдроме; 6) централизация кровообращения, что имеет место при различных видах шока.
Циркуляторная гипоксия местного характера, захватывающая какой-либо орган или область тела, может развиться при таких местных нарушениях кровообращения, как венозная гиперемия и ишемия. Для всех перечисленных состояний характерно уменьшение объемной скорости кровотока. Общее количество крови, притекающей к органам и участкам тела, снижается, соответственно уменьшается и объем доставляемого кислорода, хотя его напряжение в плазме крови и кислородная емкость могут быть нормальными. При этом виде гипоксии нередко обнаруживается нарастание коэффициента утилизации кислорода тканями вследствие увеличения времени контакта между ними и кровью при замедлении скорости кровотока, кроме того, замедление скорости кровотока способствует накоплению в тканях и капиллярах углекислоты, которая ускоряет процесс диссоциации оксигемог-лобина. Повышение утилизации кислорода тканями не происходит при усиленном шунтировании крови по артериоло-венулярным анастомозам вследствие спазма прекапиллярных сфинктеров или нарушения проходимости капилляров при сладже эритроцитов или развитии ДВС-син-дрома. В этих условиях содержание оксигемог-лобина в венозной крови может оказаться повышенным. То же происходит, когда транспорт кислорода замедлен на отрезке пути от капилляров до митохондрий, что имеет место при ин-терстициальном и внутриклеточном отеках, при снижении проницаемости стенок капилляров и клеточных мембран. Из этого следует, что для правильной оценки количества кислорода, потребленного тканями, большое значение имеет определение содержания оксигемоглобина в венозной крови.
Гемическая (кровяная) гипоксия развивается при уменьшении кислородной емкости крови из-за снижения-содержания гемоглобина или вследствие образования его разновидностей, не
nспособных транспортировать кислород, таких как карбоксигемоглобин и метгемоглобин. Снижение содержания гемоглобина имеет место при различных видах анемий и при гидремии, возникающей в связи с избыточной задержкой воды в организме. При этих состояниях рО2 в артериальной крови и процент оксигенации гемоглобина не отклоняются от нормы (за исключением тех случаев, когда в крови содержится карбок-си- или метгемоглобин), но снижается общее количество кислорода, связанного с гемоглобином, и поступление его в ткани является недостаточным. При этом виде гипоксии содержание оксигемоглобина и рО2 в венозной крови по сравнению с нормой понижены.
Образование карбоксигемоглобина происходит при отравлении окисью углерода (СО), которая присоединяется к молекуле гемоглобина в том же месте, что и кислород, причем сродство гемоглобина к СО в 250-350 раз (по данным различных авторов) превышает сродство к кислороду. При содержании в воздухе 0,1% окиси углерода более половины гемоглобина быстро превращается в карбоксигемоглобин. Как известно, СО образуется при неполном сгорании топлива, при работе двигателей внутреннего сгорания, может накапливаться в шахтах. Важным источником СО является курение. Содержание карбоксигемоглобина в крови курильщиков может достигать 1-15%, у некурящих оно составляет 1-3% . Отравление СО происходит также при вдыхании большого количества дыма при пожарах. Частым источником СО является метилен-хлорид – распространенный компонент растворителей красок. Он проникает в организм в виде паров и через кожу, поступает с кровью в печень, где расщепляется с образованием СО.
Карбоксигемоглобин не может участвовать в транспорте кислорода. Частичная замена гемоглобина на карбоксигемоглобин не только уменьшает его количество, способное переносить кислород, но и затрудняет диссоциацию оставшегося оксигемоглобина и отдачу кислорода тканям. Кривая диссоциации оксигемоглобина сдвигается влево. Поэтому инактивация 50% гемоглобина при превращении его в карбоксигемоглобин сопровождается более тяжелой гипоксией, чем недостаток 50 % гемоглобина при анемии. Утяжеляющим является и то обстоятельство, что при отравлении СО не происходит рефлекторной стиОбразование карбоксигемоглобина не является полностью ответственным за токсическое действие СО. Малая фракция растворенной в плазме крови окиси углерода играет очень важную роль, так как она проникает в клетки и повышает образование в них активных радикалов кислорода и перекисное окисление ненасыщенных жирных кислот, что ведет к нарушению структуры и функции клеток, в первую очередь в ЦНС, с развитием осложнений: угнетение дыхания, падение кровяного давления; в случаях тяжелых отравлений быстро возникает состояние комы и наступает смерть. Наиболее эффективными мерами помощи при отравлении СО являются нормо- и гипербарическая оксигена-ция. Сродство окиси углерода к гемоглобину снижается при повышении температуры тела и под действием света, а также при гиперкапнии, что послужило поводом для использования кар-богена при лечении людей, отравленных СО.
Метгемоглобин отличается от гемоглобина и оксигемоглобина наличием в составе тема трехвалентного железа и так же, как карбоксигемог-лобин, не способен к переносу кислорода.
Существует большое количество веществ –метгемоглобинообразователей. К их числу относятся: 1) нитросоединения (окислы азота, неорганические нитриты и нитраты, селитра, органические нитросоединения); 2) аминосоеди-нения – анилин и его производные в составе чернил, гидроксиламин, фенилгидразин и др.; 3) различные красители, например метиленовая синь; 4) окислители – бертолетова соль, перман-ганат калия, нафталин, хиноны, красная кровяная соль и др.; 5) лекарственные препараты -новокаин, аспирин, фенацитин, сульфаниламиды, ПАСК, викасол, цитрамон, анестезин и др. Вещества, вызывающие превращение гемоглобина в метгемоглобин, образуются при ряде производственных процессов: при производстве силоса, при работе с ацетиленовыми сварочно-режу-щими аппаратами, гербицидами, дефолиантами и др. Контакт с нитритами и нитратами происходит также при изготовлении взрывчатых веществ, консервировании пищевых продуктов, при сельскохозяйственных работах; нитраты часто присутствуют в питьевой воде.
Существуют наследственные формы метгемог-лобинемии, обусловленные дефицитом ферментных систем, участвующих в превращении (редукции) постоянно образующегося в малых количествах метгемоглобина в гемоглобин. Обра-
зование метгемоглобина не только снижает кислородную емкость крови, но и резко уменьшает способность оставшегося оксигемоглобина отдавать кислород тканям вследствие сдвига кривой диссоциации оксигемоглобина влево. В связи с этим уменьшается артерио-венозная разница по содержанию кислорода.
Метгемоглобинообразователи могут оказывать и непосредственное угнетающее действие на тканевое дыхание, разобщать окисление и фосфо-рилирование. Таким образом, имеется значительное сходство в механизме развития гипоксии при отравлении СО и метгемоглобинообразователя-ми. Признаки гипоксии выявляются при превращении в метгемоглобин 20-50 % гемоглобина. Превращение в метгемоглобин 75 % гемоглобина является смертельным.
При метгемоглобинемии происходит спонтанная деметгемоглобинизация благодаря активации редуктазной системы эритроцитов и накоплению недоокисленных продуктов. Этот процесс ускоряется под действием аскорбиновой кислоты и глутатиона.
При тяжелом отравлении метгемоглобинооб-разователями лечебный эффект могут оказать обменное переливание крови, гипербарическая оксигенация и вдыхание чистого кислорода.
Тканевая (гистотоксическая) гипоксия характеризуется нарушением способности тканей поглощать в нормальном объеме доставленный им кислород из-за нарушения системы клеточных ферментов в цепи транспорта электронов.
В этиологии данного вида гипоксии играют роль: 1) инактивация дыхательных ферментов: цитохромоксидазы под действием цианидов; клеточных дегидраз – под действием эфира, уре-тана, алкоголя, барбитуратов и других веществ; ингибирование дыхательных ферментов происходит также под действием ионов Си, Hg и Ag; 2) нарушение синтеза дыхательных ферментов при дефиците витаминов В]; В2, РР, пантотено-вой кислоты; 3) понижение сопряжения процессов окисления и фосфорилирования при действии разобщающих факторов (отравление нитритами, микробными токсинами, тиреоидными гормонами и др.); 4) повреждение митохондрий ионизирующей радиацией, продуктами перекисного окисления липидов, токсически действующими метаболитами при уремии, кахексии, тяжелых инфекциях. Гистотоксическая гипоксия может развиться также при отравлении эндотоксинами.муляции дыхания, так как парциальное давление кислорода в крови остается неизменным.
При тканевой гипоксии, обусловленной разобщением процессов окисления и фосфо-рилирования, потребление кислорода тканями может возрастать, однако превалирующее количество образующейся энергии рассеивается в виде тепла и не может использоваться для нужд клетки. Синтез макроэргических соединений снижен и не покрывает потребностей тканей, они находятся в таком же состоянии, как при недостатке кислорода.
Подобное состояние возникает и при отсутствии в клетках субстратов для окисления, что имеет место при тяжелой форме голодания. На этом основании выделяют субстратную гипоксию.
При гистотоксической и субстратной формах гипоксии напряжение кислорода и процент ок-сигемоглобина в артериальной крови нормальны, а в венозной крови – повышены. Артерио-венозная разница в содержании кислорода падает вследствие снижения утилизации кислорода тканями. Цианоз при данных видах гипоксии не развивается (табл. 75).
Смешанные формы гипоксии являются наиболее частыми. Они характеризуются сочетанием двух или более основных типов гипоксии: 1) при травматическом шоке наряду с циркулятор-ной может развиться дыхательная форма гипоксии в связи с нарушением микроциркуляции в
легких («шоковое легкое»); 2) при тяжелой анемии или массивном образовании карбокси- или метгемоглобина развивается гипоксия миокарда, это ведет к снижению его функции, падению кровяного давления – в результате на анемическую гипоксию наслаивается циркуляторная; 3) отравление нитратами вызывает гемическую и тканевые формы гипоксии, так как под действием этих ядов происходит не только образование метгемоглобина, но и разобщение процессов окисления и фосфолирирования. Разумеется, смешанные формы гипоксии могут оказать более выраженное повреждающее действие, чем какой-либо один вид гипоксии, так как приводят к срыву ряда компенсаторно-приспособительных реакций.
Развитию гипоксии способствуют состояния, при которых возрастает потребность в кислороде, – лихорадка, стресс, высокая физическая нагрузка и др.
Перегрузочная форма гипоксии (физиологическая) развивается у здоровых людей при тяжелой физической работе, когда поступление в ткани кислорода может стать недостаточным из-за высокой потребности в нем. При этом коэффициент потребления кислорода тканями становится очень высоким и может достигать 90% (вместо 25% в норме). Повышенной отдаче кислорода тканям способствует развивающийся притяжелой физической работе метаболический ацидоз, который снижает прочность связи гемоглобина с кислородом. Парциальное давление кислорода в артериальной крови нормально, так же как и содержание оксигемоглобина, а в венозной крови эти показатели резко снижены.