Сродство гемоглобина к оксиду углерода больше чем к кислороду в
Оглавление темы “Вентиляция легких. Перфузия легких кровью.”: Сродство гемоглобина к кислороду. Изменение сродства гемоглобина к кислороду. Эффект Бора.Молекула гемоглобина может находиться в двух формах — напряженной и расслабленной. Расслабленная форма гемоглобина имеет свойство насыщаться кислородом в 70 раз быстрее, чем напряженная. Изменение фракций напряженной и расслабленной формы в общем количестве гемоглобина в крови обусловливает S-образный вид кривой диссоциации оксигемоглобина, а следовательно, так называемое сродство гемоглобина к кислороду. Если вероятность перехода от напряженной формы гемоглобина к расслабленной больше, то возрастает сродство гемоглобина к кислороду, и наоборот. Вероятность образования указанных фракций гемоглобина изменяется в большую или меньшую сторону под влиянием нескольких факторов. Основной фактор — это связывание кислорода с геминовой фуппой молекулы гемоглобина. При этом чем больше геминовых фупп гемоглобина связывают кислород в эритроцитах, тем более легким становится переход молекулы гемоглобина к расслабленной форме и тем выше их сродство к кислороду. Поэтому при низком Р02, что имеет место в метаболически активных тканях, сродство гемоглобина к кислороду ниже, а при высоком Р02 — выше. Как только гемоглобин захватывает кислород, повышается его сродство к кислороду и молекула гемоглобина становится насыщенной при связывании с четырьмя молекулами кислорода.
Когда эритроциты, содержащие гемоглобин, достигают тканей, то кислород из эритроцитов диффундирует в клетки. В мышцах он поступает в своеобразного депо кислорода — в молекулы миоглобина, из которого кислород используется в биологическом окислении мышц. Диффузия кислорода из гемоглобина эритроцитов в ткани обусловлена низким Р02 в тканях — 35 мм рт. ст. Внутри клеток тканей напряжение кислорода, необходимое для поддержания нормального метаболизма, составляет еще меньшую величину — не более 1 кПа. Поэтому кислород путем диффузии из капилляров достигает метаболически активных клеток. Некоторые ткани приспособлены к низкому содержанию Р02 в капиллярах крови, что компенсируется высокой плотностью капилляров на единицу объема тканей. Например, в скелетной и сердечной мышцах Р02 в капиллярах может снизиться чрезвычайно быстро во время сокращения. В мышечных клетках содержится белок миоглобин, который имеет более высокое сродство к кислороду, чем гемоглобин. Миоглобин интенсивно насыщается кислородом и способствует его диффузии из крови в скелетную и сердечную мышцы, где он обусловливает процессы биологического окисления. Эти ткани способны экстрагировать до 70 % кислорода из крови, проходящей через них, что обусловлено снижением сродства гемоглобина к кислороду под влиянием температуры тканей и рН. Эффект рН и температуры на сродство гемоглобина к кислороду. Молекулы гемоглобина способны реагировать с ионами водорода, в результате этой реакции происходит снижение сродства гемоглобина к кислороду. При насыщении гемоглобина менее 100 % низкое рН понижает связывание кислорода с гемоглобином — кривая диссоциации оксигемоглобина смещается вправо по оси х. Это изменение свойства гемоглобина под влиянием ионов водорода называется эффектом Бора. Метаболически активные ткани продуцируют кислоты, такую как молочная, и С02. Если рН плазмы крови снижается от 7,4 в норме до 7,2, что имеет место при сокращении мыщц, то концентрация кислорода в ней будет возрастать вследствие эффекта Бора. Например, при постоянном рН 7,4 кровь отдавала бы порядка 45 % кислорода, т. е. насыщение гемоглобина кислородом снижалось до 55 %. Однако когда рН снижается до 7,2, кривая диссоциации смещается по оси х вправо. В результате насыщение гемоглобина кислородом падает до 40 %, т. е. кровь может отдавать в тканях до 60 % кислорода, что на 1/з больше, чем при постоянном рН.
Метаболически активные ткани повышают продукцию тепла. Повышение температуры тканей при физической работе изменяет соотношение фракций гемоглобина в эритроцитах и вызывает смещение кривой диссоциации оксигемоглобина вправо вдоль оси х. В результате большее количество кислорода будет освобождаться из гемоглобина эритроцитов и поступать в ткани. Эффект 2,3-дифосфоглицерата (2,3-ДФГ) на сродство гемоглобина к кислороду. При некоторых физиологических состояниях, например при понижении Р02 в крови ниже нормы (гипоксия) в результате пребывания человека на большой высоте над уровнем моря, снабжение тканей кислородом становится недостаточным. При гипоксии может понижаться сродство гемоглобина к кислороду вследствие увеличения содержания в эритроцитах 2,3-ДФГ. В отличие от эффекта Бора, уменьшение сродства гемоглобина к кислороду под влиянием 2,3-ДФГ не является обратимым в капиллярах легких. Однако при движении крови через капилляры легких эффект 2,3-ДФГ на снижение образования оксигемоглобина в эритроцитах (плоская часть кривой диссоциации оксигемоглобина) выражен в меньшей степени, чем отдача кислорода под влиянием 2,3-ДФГ в тканях (наклонная часть кривой), что обусловливает нормальное кислородное снабжение тканей. – Также рекомендуем “Углекислый газ. Транспорт углекислого газа.” |
Транспорт кислорода и углекислого газа кровью, формы анемии
Транспорт О2 с помощью гемоглобина
Красный пигмент гемоглобин (Нb) состоит из белковой части (глобина) и собственно пигмента (гема). Молекулы составляют четыре белковые субъединицы, каждая из которых присоединяет гем-группу с двухвалентным атомом железа, находящимся в ее центре. В легких каждый атом железа присоединяет одну молекулу кислорода. Кислород переносится в ткани, где он отделяется. Присоединение О2 называется оксигенацией (насыщением кислородом), а его отсоединение – дезоксигенацией.
Транспорт СО2

Около 10% углекислого газа (СО2), конечного продукта окислительного метаболизма в клетках тканей, переносится кровью физически растворенным п 90% — в химически связанной форме. Большая часть углекислого газа сначала диффундирует из клеток тканей в плазму, а оттуда в эритроциты. Там молекулы СО2 химически связываются и превращаются с помощью ферментов в намного более растворимые бикарбонат-ионы (НСО3-), которые переносятся в плазме крови. Образование СO2 из НСО3- значительно ускоряется с помощью фермента карбоангидразы, присутствующего в эритроцитах.
Большая часть (около 50-60%) образованных бикарбонат-ионов поступает из эритроцитов обратно в плазму в обмен на хлорид-ионы. Они переносятся в легкие и выделяются в процессе выдоха после превращения в СO2. Оба процесса — образование НСО3- и освобождение СO2, соответственно связаны с оксигенацией и дезоксигенацией гемоглобина. Дезоксигемоглобин — заметно более сильное основание, чем оксигемоглобин, и может присоединить больше ионов Н+ (буферная функция гемоглобина), таким образом способствуя образованию НСО3- в капиллярах тканей. В капиллярах легких НСО3- опять проходит из плазмы крови в эритроциты, соединяется с Н+-ионами и превращается опять в СO2. Этот процесс подтверждается тем фактом, что окисленная кровь выделяет больше протонов Н+. Намного меньшая доля СО2 (около 5-10%) связана непосредственно с гемоглобином и переносится как карбаминогемоглобин.
Гемоглобин и угарный газ
Оксид углерода (угарный газ, СО) является бесцветным газом без запаха, который образуется во время неполного сгорания и, как кислород, может обратимо связываться с гемоглобином. Однако сродство угарного газа к гемоглобину заметно больше, чем у кислорода. Таким образом, даже когда содержание СО во вдыхаемом воздухе составляет 0,3%, 80% гемоглобина связывается с угарным газом (НbСО). Так как угарный газ в 200-300 раз медленней, чем кислород, освобождается от связи с гемоглобином, его токсическое действие определяется тем, что гемоглобин больше не может переносить кислород. У тяжелых курильщиков, например, 5-10% гемоглобина присутствует как НbСО, в то время как при его содержании в 20% появляются симптомы острого отравления (головная боль, головокружение, тошнота), а 65% могут быть смертельным.
Содержание гемоглобина в крови (Нb)
Часто для оценки гемопоэза или для распознавания различных форм анемии определяют среднее содержание гемоглобина в эритроците (СГЭ). Оно вычисляется по формуле:
СГЭ = (содержание гемоглобина (г/100 мл крови) / количество эритроцитов (10ˉ6г/мкл))*10
Значение среднего содержания гемоглобина в эритроците лежит между 38 и 36 пикограммами (пг) (1 пг = 10ˉ¹² г). Эритроциты с нормальным СГЭ называются нормохромными (ортохромными). Если СГЭ низкое (например, из-за постоянной потери крови или дефицита железа), эритроциты называются гипохромными; если СГЭ высокое (например, при пернициозной анемии благодаря дефициту витамина В12), они называются гиперхромными.
Формы анемии
Анемия определяется как дефицит (снижение количества) эритроцитов или сниженное содержание гемоглобина в крови. Диагноз анемии обычно ставится по содержанию гемоглобина, нижняя граница нормы достигает 140 г/л у мужчин и 120 г/л у женщин. Почти при всех формах анемии надежным симптомом заболевания является бледный цвет кожи и слизистых оболочек. Часто во время физических нагрузок заметно увеличивается сердечный ритм (увеличивая скорость кровообращения), а уменьшение кислорода в тканях приводит к одышке. Кроме того, встречается головокружение и легкая утомляемость.
Кроме железодефицитной анемии и хронической потери крови, например, из-за кровоточащих язв или опухолей в желудочно-кишечном тракте (гипохромные анемии), анемия может возникать при дефиците витамина В12. фолиевой кислоты или эритропоэтина. Витамин В12 и фолиевая кислота участвуют в синтезе ДНК в незрелых клетках костного мозга и, таким образом, заметно влияют на деление и созревание эритроцитов (эритропоэз). При их нехватке образуется меньше эритроцитов, но они заметно увеличены из-за повышенного содержания гемоглобина (макроциты (мегалоциты), предшественники: мегалобласты), поэтому содержание гемоглобина в крови практически не изменяется (гиперхромная, мегалобластическая, макроцитарная анемия).
Дефицит витамина В12 нередко возникает из-за нарушения всасывания витамина в кишечнике, реже — вследствие недостаточного приема с пищей. Эта так называемая пернициозная анемия наиболее часто является результатом хронического воспаления в слизистой кишечника с уменьшением образования желудочного сока.
Витамин В12 всасывается в кишечнике только в связанном виде с фактором, находящимся в желудочном соке «внутренним фактором (Кастла)», который защищает его от разрушения пищеварительным соком в желудке. Так как печень может запасать большое количество витамина В12, то перед тем, как ухудшение всасывания в кишечнике повлияет на образование эритроцитов, может пройти 2-5 лет. Как и в случае дефицита витамина В12, дефицит фолиевой кислоты, другого витамина группы В, приводит к нарушению эритропоэза в костном мозге.
Есть две другие причины анемии. Одна из них — разрушение костного мозга (аплазия костного мозга) радиоактивным излучением (например, после аварии на атомной электростанции) или в результате токсичных реакций на лекарства (например, цитостатики) (апластическая анемия). Другая причина — это уменьшение продолжительности жизни эритроцитов в результате их разрушения или увеличенного распада (гемолитическая анемия). При сильной форме гемолитической анемии (например, следующей за неудачным переливанием крови), кроме бледности может наблюдаться изменение цвета кожи и слизистых оболочек на желтоватый. Эта желтуха (гемолитическая желтуха) вызвана увеличивающимся разрушением гемоглобина до билирубина (желтого желчного пигмента) в печени. Последнее приводит к увеличению уровня билирубина в плазме и его отложению в тканях.
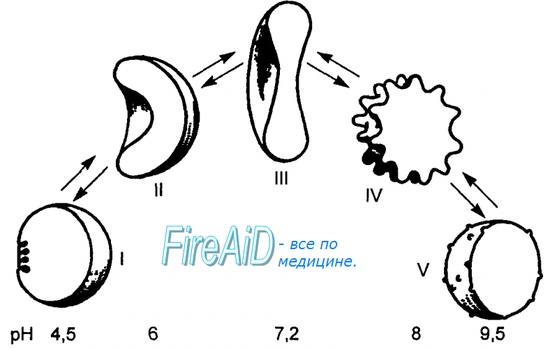
Примером анемии, возникающей в результате наследственного нарушения синтеза гемоглобина, клинически проявляющейся как гемолитическая, служит серповидноклеточная анемия. При этой болезни, которая практически встречается только у представителей негроидных популяций, имеется молекулярное нарушение, приводящее к замене нормального гемоглобина на другую форму гемоглобина (HbS). В HbS аминокислота валин заменена на глутаминовую кислоту. Эритроцит, содержащий такой неправильный гемоглобин, в дезоксигенированном состоянии принимает форму серпа. Серповидные эритроциты более жесткие и плохо проходят через капилляры.
Наследственное нарушение у гомозигот (доля HbS в суммарном гемоглобине 70-99%) приводит к закупорке небольших сосудов и, таким образом, к постоянному повреждению органов. Пораженные этой болезнью люди обычно достигают зрелости только при интенсивном лечении (например, частичной замене крови, приеме анальгетиков, избегании гипоксии (кислородного голодания) и иногда — пересадке костного мозга). В некоторых регионах тропической Африки с высоким процентом малярии 40% популяции являются гетерозиготными носителями данного гена (когда содержание HbS менее 50%), у них таких симптомов не обнаруживается. Измененный ген обусловливает устойчивость к малярийной инфекции (селективное преимущество).
Регуляция образования эритроцитов
Образование эритроцитов регулируется гормоном почек эритропоэтином. Организм обладает простой, но очень эффективной системой регуляции для поддержания содержания кислорода и вместе с тем количества эритроцитов относительно постоянным. Если содержание кислорода в крови падает ниже определенного уровня, например, после большой потери крови или во время пребывания на больших высотах, постоянно стимулируется образование эритропоэтина. В результате усиливается образование эритроцитов в костном мозге, что увеличивает способность крови к переносу кислорода. Когда дефицит кислорода преодолевается увеличением числа эритроцитов, образование эритропоэтина опять уменьшается. Пациенты, нуждающиеся в диализе (искусственном очищении крови от продуктов обмена веществ), с нарушением функционирования почек (например, с хронической почечной недостаточностью) часто испытывают явный дефицит эритропоэтина и поэтому почти всегда страдают от сопутствующей анемии.
Невероятные курсы массажа! СПб.
Оксид углерода (угарный газ, СО) обладает гораздо большим сродством к гемоглобину, чем кислород. Даже при крайне низких парциальных давлениях СО гемоглобин превращается в карбоксигемоглобин: Нb+СО Þ НbСО. Равновесие этой реакции значительно смещено вправо, поэтому кривая диссоциации карбоксигемоглобина имеет очень крутой наклон. Высокое сродство оксида углерода к гемоглобину обусловлено тем, что СО диссоциирует от НЬ гораздо медленнее, чем О2. Максимально эффективная концентрация для СО составляет 30 частей на миллион, что соответствует 0,003 объемных %. В артериальной крови человека, пребывающего достаточно долго в среде с таким содержанием СО, на долю НЬСО приходится около 5% общего содержания гемоглобина. Парциальные давления СО и О2, при которых содержание соответственно НbСО и НbО2 составляет по 5%, соотносятся как 1:350. Иными словами, в данных пределах парциальных давлений сродство Нb к СО примерно в 35O раз выше, чем к О2.
Токсичность оксида углерода обусловлена именно высоким сродством этого соединения к гемоглобину. СО представляет собой газ без цвета и запаха, образующийся при неполном сгорании органических веществ. Иногда он входит в состав бытового газа; кроме того, он выделяется при работе двигателей внутреннего сгорания. Даже при низких концентрациях СО вытесняет кислород из соединения с гемоглобином, при этом последний теряет способность к переносу О2. В норме на долю НbСО приходится лишь 1% общего количества гемоглобина в крови; у курильщиков же к вечеру она достигает 20%. Об опасности, которую угарный газ представляет для автомобилистов, говорит тот факт, что на дорогах с особенно интенсивным движением содержание СО в воздухе достигает 3-10 ч. При такой концентрации СО шахтерам положено надевать дыхательные аппараты.
Токсичность угарного газа обусловлена не только блокированием гемоглобина, но и другим эффектом. Когда часть гемоглобина превращается в НbСО, кривая диссоциации оксигемоглобина (для гемоглобина, еще не блокированного СО) сдвигается влево и может в итоге приобретать форму гиперболы. В результате происходит еще большее снижение напряжения О2 в тканевых капиллярах.
При тяжелом отравлении угарным газом, отличительным признаком которого служит вишнево-красная окраска крови, жизнь пострадавшего можно спасти путем немедленного применения искусственного дыхания, по возможности с чистым кислородом. При этом напряжение кислорода в крови увеличивается, и О2 частично вытесняет СО из связи с гемоглобином. Рекомендуется также переливание большого количества крови, так как при этом в кровь пострадавшего поступает гемоглобин, способный переносить кислород.
Перенос СО2 кровью. Формы транспорта СО2.
Диоксид углерода (СО2, углекислый газ) ― конечный продукт окислительного метаболизма в клетках ― переносится с кровью к легким и удаляется через них во внешнюю среду. Подобно кислороду, диоксид углерода может переноситься как в физически растворенном виде, так и в составе химических соединений. Химическое связывание СО2 ―более сложный процесс по сравнению со связыванием кислорода. Это обусловлено тем, что механизм, отвечающий за транспорт СО2, должен одновременно обеспечивать поддержание постоянства кислотно-щелочного равновесия крови и тем самым внутренней среды организма в целом.
Связывание СО2. Напряжение СО2 в артериальной крови, поступающей в тканевые капилляры, составляет 40 мм рт.ст. (5,3 кПа). В клетках же, расположенных около этих капилляров, напряжение СО2 значительно выше, так как углекислый газ постоянно образуется в процессе метаболизма. В связи с этим физически растворенный СО2 диффундирует по градиенту напряжения из тканей в капилляры. Здесь некоторое количество углекислого газа остается в растворенном состоянии, но большая часть СО2 претерпевает ряд химических превращений. Прежде всего, происходит гидратация молекул СО2 с образованием угольной кислоты, сразу же диссоциирующей на ион бикарбоната и протон:
В плазме крови эта реакция протекает очень медленно; в эритроците же она ускорена примерно в 10 тыс. раз. Это связано с действием фермента карбоангидразы. Поскольку этот фермент присутствует только в эритроцитах, практически все молекулы СО2, участвующие в реакции гидратации, должны сначала проникнуть в эритроциты.
Роль разных форм СО2 в газообмене. В крови, поступающей к тканям, напряжение СО2 составляет 40 мм рт.ст. Проходя через них, кровь насыщается углекислым газом, и напряжение его в оттекающей из тканей крови достигает в среднем 46 мм рт.ст. При этом 1 л крови поглощает примерно 1,8 ммоль СО2. Около 12% этого количества остается в физически растворенном виде или в форме недиссоциированной угольной кислоты, 11% образует карбаминовое соединение с гемоглобином, 27% транспортируется в виде бикарбоната в эритроцитах, а остальное количество ― около 50% ― растворено в виде НСО3¯ в плазме. При прохождении крови через легкие СО2 высвобождается из этих четырех форм в таком же соотношении.
Сатурационные кривые СО2
Зависимость содержания СО2 от его напряжения. Общее содержание диоксида углерода в крови складывается из концентраций физически растворенного и форм химически связанного СО2 ― угольной кислоты, карбамата и бикарбоната. Большая часть СО2 присутствует внутри и вне эритроцитов в форме бикарбоната. При повышении РСО2 содержание всех этих форм СО2 увеличивается.
Связь между концентрацией в крови и парциальным давлением СО2 описывается сатурационной кривой, сходной с кривой диссоциации оксигемоглобина. Зависимость связывания СО2 от степени оксигенации гемоглобина называют эффектом Христиансена-Дугласа-Холдена «или кратко эффектом Холдена.
Существует принципиальная разница между сатурационными кривыми связывания СО2 и кривыми диссоциации оксигемоглобина. Кривые диссоциации НbО2 асимптотически приближаются к максимуму, а связывание СО2 не достигает насыщения. По мере увеличения парциального давления СО2 количество связанного СО2 постоянно возрастает, так как образование бикарбоната в крови практически не лимитировано.
Физиологическое значение эффекта Христиансена-Дугласа-Холдена. При рассмотрении процессов поступления СО2 в кровь из тканей и его высвобождения в легких следует помнить о том, что эти процессы происходят одновременно с обменом О2. Изменения в насыщении гемоглобина кислородом влияют на связывание СО2 кровью и тем самым на его обмен.
К тканевым капиллярам обычно притекает полностью оксигенированная кровь. По мере того как кровь проходит через капилляры и кислород выходит из нее в ткани, способность крови поглощать СО2 увеличивается. Таким образом, эффект Христиансена-Дугласа-Холдена способствует поглощению СО2 кровью в тканях. В легких происходят обратные процессы. В результате того, что в кровь поступает кислород, ее сродство к углекислому газу снижается, и тем самым облегчается диффузия СО2 в альвеолы. Итак, мы убедились в том, что как при поступлении СО2 в кровь из тканей, так и при выделении его в легких эффект Христиансена-Дугласа-Холдена способствует диффузионному обмену этого газа.

