Переливание эритроцитарной массы при гемолитической анемии

Онкологическая клиника в Москве ¦ ПЕРЕЛИВАНИЕ КРОВИ ОНКОБОЛЬНЫМ ¦ Переливание эритроцитарной массы
Переливание компонентов крови в Европейской клинике
В своей практике врачам нередко приходится назначать переливание крови в тяжелых случаях, когда не остается других эффективных способов быстро нормализовать состояние больного.
Цельную кровь переливают не всегда, поскольку, например, у раковых пациентов она может стимулировать метастазирование. Негативное свойство цельной крови заключается в большом разнообразии антигенных раздражителей, которые в ней содержатся.
После получения ее от донора и хранения в течение определенного времени часть клеток разрушается и теряет свои функциональные свойства, а кроме того, появление значительного количества таких «обломков» чревато большой нагрузкой на почки и иммунную систему реципиента.
По этой причине обычно используют отдельные фракции крови строго по показаниям. В них спектр возможных антигенов намного меньше, и они не содержат клеток и компонентов, в которых нет необходимости.
В Европейской клинике хирургии и онкологии нередко приходится прибегать к переливанию крови и ее компонентов, так как здесь проводится лечение пациентов с тяжелой раковой и соматической патологией.
Благодаря многолетнему опыту работы и высокому уровню подготовки врачей, количество осложнений от переливания крови и ее фракций сведено к минимуму.
Четкое следование предписанным протоколам и постоянный мониторинг состояния пациентов позволяет вовремя диагностировать и предотвращать любые негативные побочные эффекты проводимой терапии.
Получение эритромассы
Если целью лечения данного конкретного пациента является устранение анемии, то нет необходимости переливать цельную кровь, поскольку перечень осложнений для такой процедуры гораздо обширней, чем, например, при переливании эритромассы.
Существует много способов ее заготовки, но основной смысл заключается в отстаивании и центрифугировании крови, удалении плазмы и аппаратном фракционировании форменных элементов. При этом иногда эритроциты отмывают в растворе, что позволяет снизить антигенную нагрузку.
В ряде случаев их погружают в крио-протекторный раствор, который дает возможность осуществлять замораживание без разрушения клеток. Также готовят эритроцитарную взвесь, в которой помимо отмытых (от остатков плазмы и других форменных элементов) эритроцитов содержится физиологический раствор.
Такая взвесь не содержит антигенов, ассоциированных с лейкоцитами, тромбоцитами, и сывороточных белков. Отмытую эритроцитарную взвесь используют для тех больных, у которых в анамнезе были аллергические реакции при трансфузии крови и ее компонентов.
Показания к переливанию эритромассы
Общим показанием к переливанию эритроцитарной массы является падение гемоглобина ниже 70 г/л и гематокрита ниже 25%. Такая ситуация может быть при острых кровотечениях, когда человек потерял треть объема циркулирующей крови.
Хронические кровопотери также могут быть показанием для переливания крови. При заболеваниях желудочно-кишечного тракта происходит нарушение всасывания железа и витаминов, в частности В12 и фолиевой кислоты, что приводит к развитию анемии.
При онкологической патологии из-за синдрома интоксикации подавляется красный росток кроветворения, что приводит к развитию апластической анемии.
При лейкозах и лимфомах избыточное производство лейкоцитов приводит к инфильтрации костного мозга раковыми клетками, в результате чего активность кроветворной системы, не имеющей отношение к производству пула мутировавших клеток, сильно снижается и развивается анемия.
Различные болезни пищеварительной системы, которые сопровождаются образованием эрозий и язв, часто приводят к хронической кровоточивости и возникновению выраженной анемии, которая нуждается в соответствующей терапии.
У женщин патология репродуктивной системы нередко провоцирует анемию: это могут быть не только новообразования, но и предраковые состояния, а также полипы полости и шейки матки, которые в результате механической травматизации кровоточат, приводя к потере гемоглобина.
Противопоказания к переливанию крови
Противопоказания к переливанию крови при тяжелых кровопотерях и анемиях носят относительный характер и не могут быть препятствием для этой процедуры.
В случае выраженной сердечной недостаточности введение в кровеносное русло избыточного объема жидкости может вызвать дополнительную нагрузку на сердечную мышцу и тогда приходится вводить пациенту мочегонные и вазодилататоры.
Следует также проявлять осторожность при выраженной почечной недостаточности.
Эритромасса содержит некоторое количество разрушенных клеток и свободного гемоглобина, которые могут засорять почечные канальцы и усиливать дисфункцию.
Кроме того, возможно разрушение части эритроцитов из-за возможного присутствия антиэритроцитарных антител и развитие гемолиза.
Процедуры переливания стараются избегать при острых инсультах, печеночной недостаточности, эндокардите, который сопровождается уменьшением сердечного выброса.
Процедура переливания эритромассы
Эритроциты необходимо человеку, поскольку основная их функция – это перенос кислорода в молекулах гемоглобина. При их снижении организм испытывает кислородное голодание, что проявляется в общей слабости, бледности, снижении умственной и физической выносливости.
Критическая потеря крови с форменными элементами приводит к гиповолемическому шоку и смерти. По этой причине необходимо замещать как утраченный объем, так и клетки крови для быстрого улучшения состояния пациента.
Перед переливанием донорский материал тестируют на антигены системы AB0, резус-фактор и Келл-антигены. Это позволяет минимизировать риски иммунного конфликта между кровью донора и реципиента.
Кроме того, после того, как эритромасса доставлена в отделение проводят пробу на совместимость. Для этого берут две капли сыворотки крови пациента в пробирке, добавляют одну каплю эритромассы и две капли полиглюкина – все тщательно перемешивают.
Затем доливают 3 мл физиологического раствора. Если материал пациента и донорских эритроцитов не совместимы, то образуются мелкие агглютинаты, которые выглядят, как мелкий красный песок в растворе и на стенках пробирки.
В этом случае переливать такой материал нельзя и подыскивают другую эритромассу. Если испытание на совместимость пройдено благополучно, то проводят биологическую пробу.
Для этого в вену пациента вводят 10 мл эритромассы и выжидают 3-5 минут: при отсутствии неблагоприятных симптомов, испытание повторяют еще два раза. Если пациент хорошо отреагировал на биологическую пробу, то вводят основной объем эритромассы.
Вводимый раствор предварительно прогревают до 38ºС. Соблюдение всех необходимых правил позволяет максимально сократить риски осложнений.
Перед самой трансфузией врач осматривает пациента и заносит в историю болезни данные о его текущем состоянии. В процессе непосредственно переливания производится мониторинг самочувствия больного, измеряется пульс, давление.
После процедуры документально оформляется протокол переливания крови. Весь процесс введения эритромассы занимает 30-40 минут и происходит со скоростью 40-60 капель в минуту.
Чаще всего осложнением от такой манипуляции бывает кожная сыпь, вызванная освобождением гистамина, лихорадка, озноб.
После окончания переливания эритромассы человек проводит в постели 2-3 часа, и медсестра отслеживает его состояние: измеряет температуру, пульс и давление.
На следующий день собирают анализ мочи и крови для мониторинга функции почек и общей реакции организма.
Как правило, при соблюдении всех установленных протоколов побочных эффектов почти не бывает, зато самочувствие пациента быстро улучшается за счет устранения кислородного голодания и активации метаболизма.
+7(925)191-50-55 – европейские протоколы лечения в Москве
ЗАПРОС в КЛИНИКУ

Гемолитическая анемия – патология эритроцитов, отличительным признаком которой является ускоренное разрушение красных кровяных телец с высвобождением повышенного количества непрямого билирубина. Для данной группы заболеваний типично сочетание анемического синдрома, желтухи и увеличения размеров селезенки. В процессе диагностики исследуется общий анализ крови, уровень билирубина, анализ кала и мочи, УЗИ органов брюшной полости; проводится биопсия костного мозга, иммунологические исследования. В качестве методов лечения используется медикаментозная, гемотрансфузионная терапия; при гиперспленизме показана спленэктомия.
Общие сведения
Гемолитическая анемия (ГА) – малокровие, обусловленное нарушением жизненного цикла эритроцитов, а именно преобладанием процессов их разрушения (эритроцитолиза) над образованием и созреванием (эритропоэзом). Данная группа анемий очень обширна. Их распространенность неодинакова в различных географических широтах и возрастных когортах; в среднем патология встречается у 1% населения. Среди прочих видов анемий на долю гемолитических приходится 11%. Патология характеризуется укорочением жизненного цикла эритроцитов и их распадом (гемолизом) раньше времени (через 14-21 день вместо 100-120 суток в норме). При этом разрушение эритроцитов может происходить непосредственно в сосудистом русле (внутрисосудистый гемолиз) или в селезенке, печени, костном мозге (внесосудистый гемолиз).
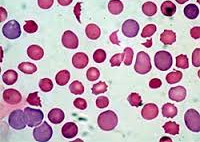
Гемолитическая анемия
Причины
Этиопатогенетическую основу наследственных гемолитических синдромов составляют генетические дефекты мембран эритроцитов, их ферментных систем либо структуры гемоглобина. Данные предпосылки обусловливают морфофункциональную неполноценность эритроцитов и их повышенное разрушение. Гемолиз эритроцитов при приобретенных анемиях наступает под влиянием внутренних факторов или факторов окружающей среды, среди которых:
- Аутоиммунные процессы. Образование антител, агглютинирующих эритроциты, возможно при гемобластозах (остром лейкозе, хроническом лимфолейкозе, лимфогранулематозе), аутоиммунной патологии (СКВ, неспецифическом язвенном колите), инфекционных заболеваниях (инфекционном мононуклеозе, токсоплазмозе, сифилисе, вирусной пневмонии). Развитию иммунных гемолитических анемий могут способствовать посттрансфузионные реакции, профилактическая вакцинация, гемолитическая болезнь плода.
- Токсическое действие на эритроциты. В ряде случаев острому внутрисосудистому гемолизу предшествует отравление мышьяковистыми соединениями, тяжелыми металлами, уксусной кислотой, грибными ядами, алкоголем и др. Вызывать разрушение клеток крови может прием определенных лекарств (противомалярийных препаратов, сульфаниламидов, производных нитрофуранового ряда, анальгетиков).
- Механическое повреждение эритроцитов. Гемолиз эритроцитов может наблюдаться при тяжелых физических нагрузках (длительной ходьбе, беге, лыжном переходе), при ДВС-синдроме, малярии, злокачественной артериальной гипертензии, протезировании клапанов сердца и сосудов, проведении гипербарической оксигенации, сепсисе, обширных ожогах. В этих случаях под действием тех или иных факторов происходит травматизация и разрыв мембран изначально полноценных эритроцитов.
Патогенез
Центральным звеном патогенеза ГА является повышенное разрушение эритроцитов в органах ретикулоэндотелиальной системы (селезенке, печени, костном мозге, лимфатических узлах) или непосредственно в сосудистом русле. При аутоиммунном механизме анемии происходит образование антиэритроцитарных АТ (тепловых, холодовых), которые вызывают ферментативный лизис мембраны эритроцитов. Токсические вещества, являясь сильнейшими окислителями, разрушают эритроцит за счет развития метаболических, функциональных и морфологических изменений оболочки и стромы красных кровяных телец. Механические факторы оказывают прямое воздействие на клеточную мембрану. Под влиянием этих механизмов из эритроцитов выходят ионы калия и фосфора, а внутрь поступают ионы натрия. Клетка разбухает, при критическом увеличении ее объема наступает гемолиз. Распад эритроцитов сопровождаются развитием анемического и желтушного синдромов (так называемой «бледной желтухой»). Возможно интенсивное окрашивание кала и мочи, увеличение селезенки и печени.
Классификация
В гематологии гемолитические анемии подразделяются на две большие группы: врожденные (наследственные) и приобретенные. Наследственные ГА включают следующие формы:
- эритроцитарные мембранопатии (микросфероцитоз – болезнь Минковского-Шоффара, овалоцитоз, акантоцитоз) – анемии, обусловлены структурными аномалиями мембран эритроцитов
- ферментопении (энзимопении) – анемии, вызванные дефицитом тех или иных ферментов (глюкозо-6-фосфатдегидрогеназы, пируваткиназы и др.)
- гемоглобинопатии – анемии, связанные с качественными нарушениями структуры гемоглобина или изменением соотношения его нормальных форм (талассемия, серповидно-клеточная анемия).
Приобретенные ГА подразделяются на:
- мембранопатии приобретенные (пароксизмальная ночная гемоглобинурия – б-нь Маркиафавы-Микели, шпороклеточная анемия)
- иммунные (ауто- и изоиммунные) – обусловлены воздействием антител
- токсические – анемии, обусловленные воздействием химических веществ, биологических ядов, бактериальных токсинов
- механические – анемии, вызванные механическим повреждением структуры эритроцитов (тромбоцитопеническая пурпура, маршевая гемоглобинурия)
Симптомы
Наследственные мембранопатии, ферментопении и гемоглобинопатии
Наиболее распространенной формой данной группы анемий является микросфероцитоз, или болезнь Минковского-Шоффара. Наследуется по аутосомно-доминантному типу; обычно прослеживается у нескольких представителей семьи. Дефектность эритроцитов обусловлена дефицитом в мембране актомиозиноподобного белка и липидов, что приводит к изменению формы и диаметра эритроцитов, их массивному и преждевременному гемолизу в селезенке. Манифестация микросфероцитарной ГА возможна в любом возрасте (в младенчестве, юношестве, старости), однако обычно проявления возникают у детей старшего возраста и подростков. Тяжесть заболевания варьирует от субклинического течения до тяжелых форм, характеризующихся часто повторяющимися гемолитическими кризами. В момент криза нарастает температура тела, головокружение, слабость; возникают боли в животе и рвота.
Основным признаком микросфероцитарной гемолитической анемии служит желтуха различной степени интенсивности. Вследствие высокого содержания стеркобилина кал становится интенсивно окрашенным в темно-коричневый цвет. У пациентов с болезнь Минковского-Шоффара наблюдается склонность к образованию камней в желчном пузыре, поэтому часто развиваются признаки обострения калькулезного холецистита, возникают приступы желчной колики, а при закупорке холедоха конкрементом – обтурационная желтуха. При микросфероцитозе во всех случаях увеличена селезенка, а у половины пациентов – еще и печень. Кроме наследственной микросфероцитарной анемии, у детей часто встречаются другие врожденные дисплазии: башенный череп, косоглазие, седловидная деформация носа, аномалии прикуса, готическое нёбо, полидактилия или брадидактилия и пр. Пациенты среднего и пожилого возраста страдают трофическими язвами голени, которые возникают в результате гемолиза эритроцитов в капиллярах конечностей и плохо поддаются лечению.
Энзимопенические анемии связаны с недостатком определенных ферментов эритроцитов (чаще – Г-6-ФД, глутатион-зависимых ферментов, пируваткиназы и др). Гемолитическая анемия может впервые заявлять о себе после перенесенного интеркуррентного заболевания или приема медикаментов (салицилатов, сульфаниламидов, нитрофуранов). Обычно заболевание имеет ровное течение; типична «бледная желтуха», умеренная гепатоспленомегалия, сердечные шумы. В тяжелых случаях развивается ярко выраженная картина гемолитического криза (слабость, рвота, одышка, сердцебиение, коллаптоидное состояние). В связи с внутрисосудистым гемолизом эритроцитов и выделением гемосидерина с мочой последняя приобретает темный (иногда черный) цвет. Особенностям клинического течения гемоглобинопатий – талассемии и серповидно-клеточной анемии посвящены самостоятельные обзоры.
Приобретенные гемолитические анемии
Среди различных приобретенных вариантов чаще других встречаются аутоиммунные анемии. Для них общим пусковым фактором выступает образование антител к антигенам собственных эритроцитов. Гемолиз эритроцитов может носить как внутрисосудистый, так и внутриклеточный характер. Гемолитический криз при аутоиммунной анемии развивается остро и внезапно. Он протекает с лихорадкой, резкой слабостью, головокружением, сердцебиением, одышкой, болями в эпигастрии и пояснице. Иногда острым проявлениям предшествуют предвестники в виде субфебрилитета и артралгий. В период криза стремительно нарастает желтуха, не сопровождающаяся кожным зудом, увеличивается печень и селезенка. При некоторых формах аутоиммунных анемий больные плохо переносят холод; в условиях низких температур у них может развиваться синдром Рейно, крапивница, гемоглобинурия. Вследствие недостаточности кровообращения в мелких сосудах возможны осложнения в виде гангрены пальцев ног и рук.
Токсические анемии протекают с прогрессирующей слабостью, болями в правом подреберье и поясничной области, рвотой, гемоглобинурией, высокой температурой тела. Со 2-3 суток присоединяется желтуха и билирубинемия; на 3-5 сутки возникает печеночная и почечная недостаточность, признаками которых служат гепатомегалия, ферментемия, азотемия, анурия. Отдельные виды приобретенных гемолитических анемий рассмотрены в соответствующих статьях: «Гемоглобинурия» и «Тромбоцитопеническая пурпура», «Гемолитическая болезнь плода».
Осложнения
Каждый вид ГА имеет свои специфические осложнения: например, ЖКБ – при микросфероцитозе, печеночная недостаточность – при токсических формах и т.д. К числу общих осложнений относятся гемолитические кризы, которые могут провоцироваться инфекциями, стрессами, родами у женщин. При остром массивном гемолизе возможно развитие гемолитической комы, характеризующейся коллапсом, спутанным сознанием, олигурией, усилением желтухи. Угрозу жизни больного несут ДВС-синдром, инфаркт селезенки или спонтанный разрыв органа. Неотложной медицинской помощи требуют острая сердечно-сосудистая и почечная недостаточность.
Диагностика
Определение формы ГА на основе анализа причин, симптоматики и объективных данных относится к компетенции гематолога. При первичной беседе выясняется семейный анамнез, частота и тяжесть протекания гемолитических кризов. В процессе осмотра оценивается окраска кожных покровов, склер и видимых слизистых, производится пальпация живота для оценки величины печени и селезенки. Сплено- и гепатомегалия подтверждается при проведении УЗИ печени и селезенки. Лабораторный диагностический комплекс включает:
- Исследование крови. Изменения в гемограмме характеризуются нормо- или гипохромной анемией, лейкопенией, тромбоцитопенией, ретикулоцитозом, ускорением СОЭ. В биохимических пробах крови определяется гипербилирубинемия (увеличение фракции непрямого билирубина), увеличение активности лактатдегидрогеназы. При аутоиммунных анемиях большое диагностическое значение имеет положительная проба Кумбса.
- Анализы мочи и кала. Исследование мочи выявляет протеинурию, уробилинурию, гемосидеринурию, гемоглобинурию. В копрограмме повышено содержание стеркобилина.
- Миелограмму. Для цитологического подтверждения выполняется стернальная пункция. Исследование пунктата костного мозга обнаруживает гиперплазию эритроидного ростка.
В процессе дифференциальной диагностики исключаются гепатиты, цирроз печени, портальная гипертензия, гепатолиенальный синдром, порфирии, гемобластозы. Пациента консультируют гастроэнтеролог, клинический фармаколог, инфекционист и другие специалисты.

Аутоиммунная гемолитическая анемия
Лечение
Различные формы ГА имеют свои особенности и подходы к лечению. При всех вариантах приобретенной гемолитической анемии необходимо позаботиться об устранении влияния гемолизирующих факторов. Во время гемолитических кризов больным необходимы инфузии растворов, плазмы крови; витаминотерапия, по необходимости – гормоно- и антибиотикотерапия. При микросфероцитозе единственно эффективным методом, приводящим к 100 % прекращению гемолиза, является спленэктомия.
При аутоиммунной анемии показана терапия глюкокортикоидными гормонами (преднизолоном), сокращающая или прекращающая гемолиз. В некоторых случаях требуемый эффект достигается назначением иммунодепрессантов (азатиоприна, 6-меркаптопурина, хлорамбуцила), противомалярийных препаратов (хлорохина). При резистентных к медикаментозной терапии формах аутоиммунной анемии выполняется спленэктомия. Лечение гемоглобинурии предполагает переливание отмытых эритроцитов, плазмозаменителей, назначение антикоагулянтов и антиагрегантов. Развитие токсической гемолитической анемии диктует необходимость проведения интенсивной терапии: дезинтоксикации, форсированного диуреза, гемодиализа, по показаниям – введение антидотов.
Прогноз и профилактика
Течение и исход зависят от вида анемии, тяжести протекания кризов, полноты патогенетической терапии. При многих приобретенных вариантах устранение причин и полноценное лечение приводит к полному выздоровлению. Излечения врожденных анемий добиться нельзя, однако возможно достижение длительной ремиссии. При развитии почечной недостаточности и других фатальных осложнений прогноз неблагоприятен. Предупредить развитие ГА позволяет профилактика острых инфекционных заболеваний, интоксикаций, отравлений. Запрещается бесконтрольное самостоятельное использование лекарственных препаратов. Необходимо тщательная подготовка пациентов к гемотрансфузиям, вакцинации с проведением всего комплекса необходимых обследований.
