При какой опухоли чаще развивается железодефицитная анемия
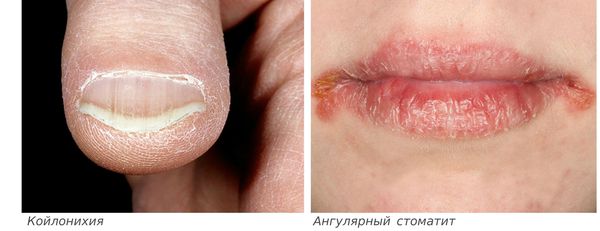

Анемия представляет собой патологическое состояние, для которого характерно снижение эритроцитов и/или концентрации гемоглобина в единице объема крови. Анемия не является самостоятельным заболеванием, это симптом, который характерен для самых разнообразных заболеваний, в том числе и для злокачественных опухолей.
Согласно статистике, данное состояние выявляется у каждого третьего онкологического пациента, а при прохождении химиотерапии — более чем в 90% случаев. Опасность анемии в онкологии заключается в том, что вместе с уменьшением уровня гемоглобина и эритроцитов, уменьшается и кислородная емкость крови. Этот фактор неблагоприятно сказывается на течении ракового процесса, снижает эффективность лечения и ухудшает дальнейший прогноз.
Основные причины развития анемии у онкологических пациентов
Снижение уровня эритроцитов и гемоглобина может развиваться вследствие снижения их образования, ускоренного разрушения или в результате потери. Каждой из этих причин способствуют собственные факторы, которые рассмотрим подробнее:
- Недостаточная выработка форменных элементов крови и гемоглобина может развиваться при поражении костного мозга, недостатке железа в организме или некоторых витаминов (фолиевая кислота, витамин В12). Данные состояния могут быть напрямую связаны с напрямую с онкологическим заболеванием. Например, потеря железа может развиваться в результате постоянной рвоты, отсутствия аппетита и нарушения его всасывания в кишечнике, который поражен опухолевым процессом. Некоторые виды препаратов, которые назначают при злокачественных опухолях, подавляют рост не только раковых клеток, но и клеток крови, которые активно делятся. Также анемия может развиваться при непосредственном поражении костного мозга опухолевым процессом.
- Ускоренное разрушение эритроцитов отмечается при воздействии различных лекарственных препаратов и при аномальной активности иммунной системы. Разрушение эритроцитов непосредственно в сосудах называется внутрисосудистым гемолизом. Этот процесс протекает в норме после завершения жизненного цикла эритроцитов, который составляет 120 дней. Однако при воздействии различных факторов (прием антибиотиков, цитостатиков, присоединение вторичной инфекции и др.), этот срок значительно уменьшается, что и приводит к развитию анемии.
- Кровопотеря у онкологических пациентов может быть как острой, так и хронической. Первый вариант встречается при проведении хирургического лечения рака, а также при развитии внутренних кровотечений, которые являются частым осложнением основного заболевания. Развитие анемии при хронической кровопотере отмечается в тех случаях, когда имеется скрытый источник незначительного кровотечения. Например, при колоректальном раке кровь может выделяться с калом незаметно для пациента.
Установление точной причины анемии играет решающее значение при выборе метода лечения. Кроме того, врач учитывает степень тяжести, тип анемии, общее состояние пациента и другие параметры. Получить эту информацию можно на диагностическом этапе.
Как выявить анемию
Обследование традиционно начинается с опроса пациента и сбора анамнеза. Врач должен помнить, что не всегда анемия развивается вследствие основного заболевания. Возможны наследственные или любые другие причины, которые не связаны с опухолевым процессом. Также необходимо установить вид предшествующего противоопухолевого лечения, продолжительность и количество курсов, наименование препаратов, которые применялись. На следующем этапе врач проводит общий осмотр. Анемия может проявляться бледностью кожных покровов, слабостью, потерей аппетита, головокружением и другими симптомами. Очень часто эти проявления отмечаются при различных видах рака, который протекает без анемии, поэтому поставить диагноз исходя только из жалоб пациента невозможно.
Объективную информацию можно получить только при помощи лабораторных исследований. Анемия диагностируется по следующим анализам:
- Количество ретикулоцитов.
- Уровень железа сыворотки крови.
- Уровень белка трансферрина и ферритина.
- Уровень витамина В12 и фолиевой кислоты.
Отдельное внимание уделяется общему анализу крови. В нем определяется уровень гемоглобина, количество эритроцитов и гематокрит (отношение форменных элементов к жидкой составляющей крови). Также определяют средний объем эритроцита, среднее содержание гемоглобина в эритроците и среднее содержание гемоглобина во всей эритроцитарной массе.
При необходимости в программу комплексного обследования при анемии могут включаться и другие лабораторные анализы или специальные методы.
Как классифицируется анемия
В зависимости от значения цветового показателя, степени тяжести и механизма развития, анемия разделяется на несколько категорий. Цветовой показатель крови отражает степень насыщения эритроцитов гемоглобином. Его значение в норме колеблется от 0,85 до 1,05 единиц. Снижение показателя отмечается при гипохромной анемии, а повышение — при гиперхромной. Если цветовой показатель в норме, но уровень гемоглобина все равно низкий, то говорят о нормохромной анемии.
По степени тяжести, анемия разделяется на три группы, в зависимости от концентрации гемоглобина:
- При легкой степени анемии уровень гемоглобина не опускается ниже отметки в 90 г/л.
- При средней степени анемии показатель колеблется в пределах 90-70 г/л.
- Тяжелая анемия характеризуется падением гемоглобина ниже 70 г/л.
Классификация анемии по механизму развития наиболее обширна. Среди распространенных форм отмечаются:
- Железодефицитная анемия. Развивается в результате нарушения всасывания, усиленной потери или недостаточного поступления железа в организм.
- Гемолитическая анемия. Характеризуется разрушением эритроцитов в сосудистом русле или за его пределами. Наиболее частые причины — недостаточность специфических ферментов, аутоиммунные заболевания, воздействие лекарственных препаратов.
- Постгеморрагическая анемия. Данное состояние характерно для острой или хронической кровопотери
- Апластическая анемия. Характеризуется снижением уровня клеток-предшественников эритроцитов в костном мозге. Обычно отмечается снижение и других форменных элементов — тромбоцитов и лейкоцитов.
- В12-дефицитная анемия. При недостатке витамина В12 нарушается процесс образования эритроцитов, снижается их продолжительность жизни. Дефицит витамина может быть связан как с нарушением его всасывания в кишечнике, так и с недостаточным поступлением в организм.
В большинстве случаев определить точный вид анемии можно после нескольких лабораторных тестов, но иногда приходится применять более сложные методы диагностики, например, генетическое исследование. Понимание механизма развития анемии и получение максимально полной информации об изменениях в показателях крови являются важным компонентом эффективной терапии данного симптома.
Методы лечения анемии
Устранить анемию у онкологических пациентов можно тремя способами: переливание эритроцитарной массы, введение эритропоэтина, назначение препаратов, содержащих железо. В отдельных случаях может применяться комбинация этих методов.
Переливание эритроцитарной массы при анемии
Переливание эритроцитарной массы является самым действенным методом, при помощи которого можно быстро восполнить дефицит эритроцитов, восстановить уровень гемоглобина и гематокрита. Однако без устранения причины анемии, этот способ даст лишь временный эффект. Поэтому переливание эритроцитарной массы не является альтернативой другим методикам и применяется только при наличии показаний. Одним из них является снижение уровня гемоглобина ниже 90 г/л. Переливание проводят при развитии у пациента характерных признаков анемии, среди которых отмечаются:
- Головокружение.
- Потеря сознания.
- Тахикардия.
- Быстрая утомляемость.
- Боль в груди.
- Одышка.
Данный метод лечения анемии также может применяться у пациентов, которые прошли курс химиотерапии или лучевой терапии и у которых отмечается быстрое снижение уровня гемоглобина или эритроцитов.
Применение стимуляторов эритропоэза
Стимуляторы эритропоэза при анемии увеличивают концентрацию гемоглобина и эритроцитов за счет усиления их образования в костном мозге. При сочетании с гемотрансфузиями, данный метод показывает очень хорошие результаты, но при этом имеет и ряд недостатков, которые касаются осложнений. В частности, применение стимуляторов эритропоэза для лечения анемии повышает риск развития тромботических осложнений, который и так является высоким у онкологических пациентов. По данным, полученным в ходе нескольких научных исследований, этот риск увеличивается в 1.4-1.7 раз.
В последнее время обсуждается вопрос о влиянии стимуляторов эритропоэза на выживаемость онкологических пациентов. В частности, специалисты установили, что применение препаратов данной группы при лечении анемии у пациентов с распространенным опухолевым процессом головы и шеи, шейки матки, молочной железы и других диагнозах снижает продолжительность жизни на 10-17%. В связи с этим специалисты предлагают придерживаться следующих правил:
- Если уровень гемоглобина составляет менее 100 г/л и пациент при этом проходит лечение химиопрепаратами, то стимуляторы эритропоэза могут назначаться с целью коррекции анемии и профилактики дальнейшего снижения показателей.
- Если уровень гемоглобина падает до 100 г/л и ниже, но химиотерапия при этом не проводится, то применять стимуляторы эритропоэза не рекомендуется ввиду повышенного риска развития осложнений и снижения продолжительности жизни.
- Во всех остальных случаях применять стимуляторы эритропоэза для лечения анемии у онкологических пациентов следует с осторожностью.
Также на протяжении всего времени лечения важно контролировать динамику лабораторных показателей и при увеличении уровня гемоглобина постепенно снижать дозировку стимуляторов эритропоэза.
Препараты железа при лечении анемии
Препараты железа применяются с целью лечения железодефицитных анемий, которые выявляются у 30-60% онкологический больных. При этом снижение уровня железа может быть связано как с самим опухолевым процессом или проводимым лечением, так и с другими факторами. Например, при назначении стимуляторов эритропоэза, существующего запаса железа в организме становится недостаточно для того, чтобы покрыть потребность, которая возникает в результате активного синтеза гемоглобина в костном мозге.

Для лечения анемии могут применяться как внутривенные, так и пероральные препараты. Второй вариант более удобен для пациента, так как таблетки проще принимать, но при этом данная форма действует медленнее и чаще приводит к осложнениям со стороны ЖКТ. Внутривенное введение позволяет добиться быстрого эффекта, что актуально при проведении химиотерапии.
Таким образом, для лечения анемии современная онкология может предложить различные методы, которые воздействуют на механизмы развития данного симптома. Точный план терапии подбирается индивидуально для каждого пациента, с учетом лабораторных показателей крови, особенностей лечения основного заболевания и других параметров.
Лечение анемии народными способами
Некоторые пациенты по разным причинам отказываются от приема описанных выше препаратов и обращаются к народной медицине. Безусловно, некоторые растения или продукты могут оказывать стимулирующее действие на систему кроветворения. Однако, учитывая основной диагноз и тяжесть анемии, этого действия крайне недостаточно для восстановления уровня гемоглобина и кислородной функции крови. В результате снижается эффективность противоопухолевого лечения, ухудшается прогноз и существенно повышается риск неблагоприятного исхода. Устранить выраженную анемию в домашних условиях при помощи народных методов невозможно. Этим должны заниматься врачи соответствующего профиля, в распоряжении которых имеются современные лекарственные препараты.
Дата публикации 18 июля 2020Обновлено 18 июля 2020
Определение болезни. Причины заболевания
Железодефицитная анемия (ЖДА) — состояние, при котором недостаток железа в организме приводит к снижению количества эритроцитов. При анемии возникают нарушения со стороны кожи и слизистых оболочек, быстрая утомляемость, головокружения и обмороки. Дефицит железа связан с нарушением его поступления, усвоения или повышенными потерями крови [1].
По данным Всемирной организации здравоохранения, в мире более двух миллиардов людей страдают ЖДА, в основном это женщины и дети [5]. Из всех анемий ЖДА составляют 80 % [2]. Эта проблема актуальна и для России, с ней сталкиваются врачи почти всех специальностей.
Основные причины развития ЖДА:
- Несбалансированное питание с нехваткой железа и преобладанием мучных и молочных продуктов (дефицит красного мяса и белка в пище, голодание, недоедание, однообразная пища, вегетарианство, искусственное вскармливание у детей, нервная анорексия) [1].
- Повышенная потребность в железе (беременность, лактация, период интенсивного роста и полового созревания, тяжёлая физическая работа, интенсивные занятия спортом, паразитарные инвазии кишечника) [1].
- Повышенные хронические потери железа (наружные или внутренние):
- частые кровотечения из дёсен;
- носовые кровотечения;
- эрозивный эзофагит;
- желудочные кровопотери — эрозии и язвы желудка, грыжи пищеводного отверстия диафрагмы, опухоли желудка;
- кишечные кровопотери — эрозии и язвы двенадцатиперстной кишки, язвенный колит, опухоли кишечника, полипы и дивертикулы кишечника (выпячивание кишечной стенки), геморроидальные кровотечения;
- маточные кровопотери — обильные и/или длительные менструации, аномальные маточные кровотечения, миома матки, эндометриоз, рак матки;
- почечные кровопотери — гематурическая форма хронического гломерулонефрита, рак мочевого пузыря, почек и мочевыводящих путей;
- геморрагические диатезы — коагулопатии (нарушение свёртываемости крови), тромбоцитопении (снижение количества тромбоцитов), тромбоцитопатии (дефект тромбоцитов), васкулиты (воспаление кровеносных сосудов) и коллагенозы (поражение соединительной ткани);
- донорство при регулярной сдаче крови пять и более раз в год [2][8].
- Нарушение ионизации железа в желудке — атрофический гастрит, гиповитаминоз С, резекция желудка (операция по удалению значительной части желудка).
- Нарушение всасывания железа в кишечнике — дуоденит (воспаление двенадцатиперстной кишки), хронические энтериты (воспаление тонкого кишечника), целиакия, резекция кишечника [2][8].
- Нарушение транспорта железа вследствие уменьшения количества трансферрина — белка, связывающегося с железом для переноса его в молекулу гемоглобина (при циррозах, инфекционных заболеваниях, уремии, туберкулёзе).
- Недостаточный исходный уровень железа в организме у детей, рождённых от матерей с низким уровнем гемоглобина крови.
Группы риска по ЖДА:
- дети (недоношенные, дети от 6 месяцев до 3 лет, подростки старше 12 лет);
- менструирующие женщины;
- женщины в период беременности и лактации;
- доноры;
- люди старше 60 лет.
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением – это опасно для вашего здоровья!
Симптомы железодефицитной анемии
Недостаток железа в организме проявляется двумя синдромами — сидеропеническим и анемическим [2][8].
Сидеропенический синдром связан с недостатком железа в тканях и проявляется нарушениями со стороны кожи и слизистых оболочек:
- сухость, дряблость, шелушение и трещины на коже;
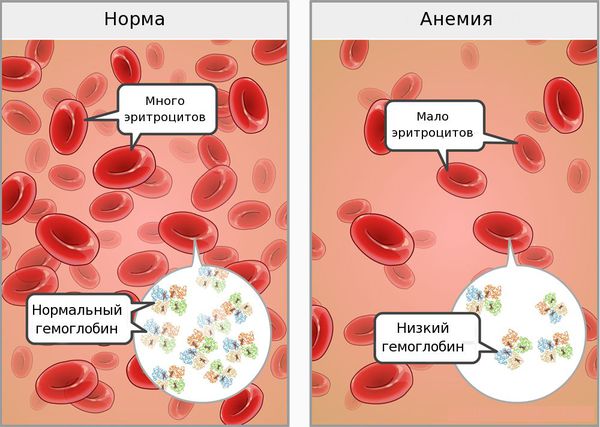
- ломкость и слоистость ногтей, их поперечная исчерченность, койлонихия (ногти становятся плоскими, иногда принимают вогнутую “ложкообразную” форму);
- ангулярный стоматит (изъязвления и трещины в уголках рта);

- ломкость и выпадение волос (волосы теряют блеск, истончаются, секутся, редеют и рано седеют);
- извращение вкуса и пристрастие к непищевым продуктам — к мелу, извести, глине, углю, краскам, земле и т. д.; причина этого симптома неизвестна, но он часто встречается при ЖДА;
- изменение обоняния и тяга к токсическим веществами — к бензину, керосину, мазуту, ацетону, лакам, краскам, гуталину, выхлопным газам, т. е. токсикомания; данный симптом необъясним, но тоже достаточно специфичен для ЖДА и полностью проходит на фоне приёма препаратов железа;
- дистрофические процессы в желудочно-кишечном тракте — глоссит (болезненность и жжение языка), гингивит, кариес, склонность к пародонтозу, атрофический гастрит и энтерит, сидеропеническая дисфагия или синдром Пламмера — Винсона (затруднённое глотание сухой и твёрдой пищи и даже слюны) [8];
- недостаточность мышечных сфинктеров (недержание мочи при кашле, смехе, непреодолимые позывы к мочеиспусканию, возможно ночное недержание мочи).
При осмотре обращает на себя внимание бледность кожных покровов, часто с зеленоватым оттенком (“хлороз”) и симптом голубых склер — дистрофические изменения роговицы глаза, через которые просвечивают сосудистые сплетения, создающие “синеву” [2][8].
Анемический синдром проявляется слабостью, быстрой утомляемостью, сонливостью днём и плохим засыпанием ночью, головокружениями, обмороками, частыми головными болями, шумом в ушах, мельканием “мушек” перед глазами, одышкой при физической нагрузке, увеличением частоты сердечных сокращений, неприятными ощущениями в области сердца, пониженным артериальным давлением.
При ЖДА может наблюдаться умеренное повышение температуры тела (до 37,5 °С), которое исчезает после лечения железосодержащими препаратами.
Зачастую снижение содержания гемоглобина происходит постепенно, при этом многие органы адаптируются к анемии. В связи с этим жалобы больных не всегда соответствуют показателям содержания гемоглобина. Многие пациенты, особенно женщины, свыкаются с неважным самочувствием, приписывая его переутомлению, психическим и физическим перегрузкам.
Патогенез железодефицитной анемии
Железо — жизненно важный для человека микроэлемент, который входит в состав гемоглобина крови, миоглобина мышц, отвечает за транспорт кислорода в организме и протекание многих биохимических реакций.
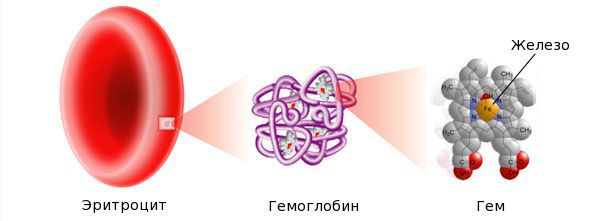
Железо поступает в организм в виде двухвалентного (мясная пища) и трёхвалентного (растительная пища) ионов. Первый всасывается легко, второй под действием соляной кислоты в желудке должен превратиться в двухвалентный. Далее он поступает в двенадцатиперстную кишку и начальные отделы тощей кишки, затем двухвалентное железо вновь переводится в трёхвалентное. В дальнейшем часть этого железа поступает в депо слизистой оболочки тонкой кишки, а другая всасывается в кровь, где соединяется с трансферрином (белком-переносчиком железа, синтезируемым в печени). Если содержание железа в организме избыточно, то оно задерживается в клетках кишечника и в дальнейшем удаляется из организма вместе со слущивающимся эпителием.
При недостатке железо поступает в кровоток и соединяется, как уже упоминалось, с трансферрином. Далее через систему воротной вены железо направляется в печень, где запасается в составе белка ферритина. Другая часть железа в составе трансферрина транспортируется к клеткам красного костного мозга и используется для образования гемоглобина, а также участвует в тканевых окислительно-восстановительных реакциях [5][9].
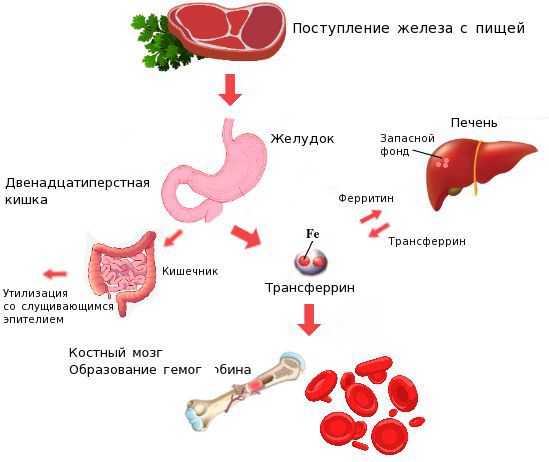
При снижении кислотности в желудке (атрофический гастрит, резекция желудка, приём препаратов, снижающих кислотность, гиповитаминоз С) нарушается ионизация железа в желудке, что ведёт к дальнейшему нарушению всасывания железа и развитию ЖДА. При резекции и хронических заболеваниях кишечника (дуоденит, хронический энтерит, целиакия) нарушается всасывание железа, что опять же приводит к развитию ЖДА.
Если нарушается включение железа в трансферрин, то оно не доходит до органов депо и клеток красного костного мозга. При этом нарушается образование гемоглобина, а также белков, содержащих железо (миоглобин, железосодержащие тканевые ферменты), что также ведёт к развитию анемии [9].
Ферменты, содержащие железо, принимают участие в синтезе гормонов щитовидной железы и поддержании иммунитета, поэтому при дефиците железа нарушаются защитные и адаптационные силы организма и весь обмен веществ.
Классификация и стадии развития железодефицитной анемии
Выделяют три стадии железодефицитных состояний: прелатентный дефицит железа, латентный дефицит и железодефицитную анемию (ЖДА).
Для прелатентного дефицита железа характерно снижение запасов железа в костном мозге:
- снижение железа в депо (снижение ферритина);
- нормальный уровень сывороточного железа;
- нормальный уровень гемоглобина и эритроцитов;
- отсутствие тканевых проявлений (нет сидеропенического синдрома) [4][6].
На этой стадии симптомов может не быть.
Латентный (скрытый) дефицит железа влияет на тканевой обмен. На этой стадии запасы железа начинают истощаться, но организм ещё не успел отреагировать снижением гемоглобина. Возникают первые проявления заболевания — человека может беспокоить повышенная утомляемость, слабость, одышка при физической нагрузке, ломкость ногтей, сухость кожи, выпадение волос. Но эти симптомы пока выражены незначительно.
Латентный дефицит железа характеризуется:
- снижением железа в депо (снижение ферритина);
- снижением уровня сывороточного железа;
- нормальным уровнем гемоглобина и эритроцитов;
- повышением общей железосвязывающей способности сыворотки (ОЖСС);
- отсутствием гемосидерина (пигмента, состоящего из оксида железа, он образуется при распаде гемоглобина) в макрофагах костного мозга;
- наличием тканевых проявлений (сидеропенический синдром) [4][6].
На третьей стадии (собственно ЖДА) снижается уровень гемоглобина и эритроцитов.
Для железодефицитной анемии характерно:
- снижение железа в депо (снижение ферритина);
- снижение уровня сывороточного железа;
- снижение уровня гемоглобина и эритроцитов;
- повышение общей железосвязывающей способности сыворотки (ОЖСС);
- отсутствие гемосидерина в макрофагах костного мозга;
- наличие тканевых проявлений (сидеропенический синдром);
- повышение растворимых трансферриновых рецепторов (рТФР);
- снижение коэффициента насыщения трансферрина железом (НТЖ);
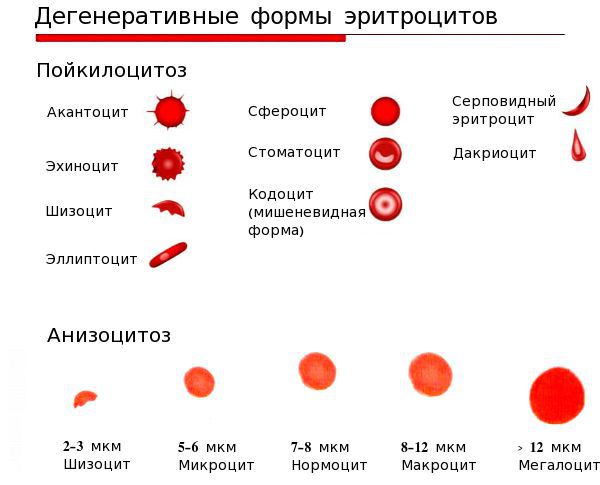
- анизоцитоз — изменение размеров эритроцитов;
- пойкилоцитоз — изменение формы эритроцитов [4][6].
Для этой стадии характерна ярко выраженная клиническая симптоматика, хотя зачастую люди списывают эти проявления на переутомление.
В норме уровень гемоглобина в крови: у женщин — 120-140 г/л, у мужчин — 130-160 г/л.
Степени тяжести ЖДА (на основании снижения уровня гемоглобина Hb):
- I — лёгкая степень: Hb от 90 до 120 г/л;
- II — средняя степень: Hb от 70 до 89 г/л;
- III — тяжёлая степень: Hb менее 70 г/л.
Осложнения железодефицитной анемии
Осложнения возникают при анемии, нелеченной более 5 лет. Тяжёлая ЖДА может привести к развитию миокардиодистрофии — поражению мышечного слоя сердца, снижению его сократительной функции и развитию сердечной недостаточности.
При ЖДА возникают сбои в работе иммунной системы, а это приводит к частым бактериальным и вирусным инфекциям (ОРВИ, гриппу, обострениям тонзиллита, бронхита, гайморита) [2][8].
У беременных с ЖДА повышается риск преждевременных родов и задержки роста плода. У детей недостаток железа приводит к задержке роста и интеллектуального развития.
Также при длительном и тяжёлом течении ЖДА нарушаются функции печени и происходят/> изменения со стороны репродуктивной сферы (нарушается менструальный цикл) [2][8].
Нередко встречаются проблемы и со стороны нервной системы — повышенная раздражительность, нервозность, плаксивость, снижение памяти, внимания, мышления и др./> С длительным дефицитом железа связывают развитие болезней Паркинсона и Альцгеймера, так как железо участвует в процессах миелинизации нервных волокон центральной нервной системы [6]. Конечно, сама по себе ЖДА не может привести к развитию этих заболеваний, но в пожилом возрасте в совокупности с хроническим воспалением в ЖКТ, повышенным уровнем холестерина в крови и сахарным диабетом анемия ускоряет развитие болезней Альцгеймера и Паркинсона.
Редким и тяжёлым осложнением ЖДА является гипоксическая кома. Ей предшествует резкое побледнение кожных покровов и видимых слизистых, судороги, а затем потеря сознания. Гипоксия из-за недостатка железа осложняет течение уже имеющихся сердечно-лёгочных заболеваний, таких как ишемическая болезнь сердца, бронхиальная астма, хроническая ишемия головного мозга и способствует развитию неотложных состояний — острому или повторному инфаркту миокарда и острому нарушению мозгового кровообращения (инсульту).
Диагностика железодефицитной анемии
Минимальный объём исследований:
- клинический анализ крови с лейкоцитарной формулой;
- биохимический анализ крови (ферритин, сывороточное железо, общая железосвязывающая способность сыворотки, коэффициент насыщения трансферрина железом, растворимые трансферриновые рецепторы).
Клинический анализ крови с лейкоцитарной формулой показывает снижение уровня гемоглобина и эритроцитов, цветового показателя крови, среднего объём эритроцита (MCV), среднего содержания гемоглобина в эритроците (МСН), средней концентрации гемоглобина в эритроците (MCHC), повышение степени анизоцитоза эритроцитов (RDW), иногда может быть увеличена скорость оседания эритроцитов (СОЭ) [1].
Биохимический анализ крови покажет снижение уровня сывороточного железа и ферритина, увеличение общей железосвязывающей способности сыворотки и растворимых трансферриновых рецепторов, снижение коэффициента насыщения трансферрина железом (НТЖ).
Лечение железодефицитной анемии
Лечение проводится железосодержащими препаратами, в основном для приёма внутрь и значительно реже для внутримышечного или внутривенного введения. Препараты нельзя принимать без назначения врача, так как переизбыток железа опасен своими последствиями — поражением зубов, развитием гепатита, цирроза печени, сахарного диабета и сердечно-сосудистых заболеваний. Также возможны тяжёлые аллергические реакции.
При анемии следует изменить рацион питания и включить в него продукты, содержащие железо в наиболее усвояемой форме — телятину, говядину, баранину, мясо кролика, печень, язык. Важно помнить, что из мяса усваивается до 30 % железа, из рыбы — 10 %, а из растительной пищи — всего лишь 3-5 %.
При анемии коррекция дефицита железа не может быть достигнута только изменением питания. Причина этого в том, что усвоение железа из пищи ограничено, а в препаратах оно содержится в большей концентрации.

При лечение больных с ЖДА необходимо учитывать характер основного заболевания и наличие сопутствующей патологии, возраст больных (дети, старики), степень выраженности анемического синдрома и дефицита железа, переносимость препаратов железа и т. д [3].
При анемии лёгкой и средней степени тяжести препараты железа лучше принимать внутрь вместе с аскорбиновой или фолиевой кислотой, так как они улучшают всасываемость железа.
В течение двух часов до или после приёма препаратов железа не рекомендуется употреблять кофе и кофеин-содержащие напитки (какао, шоколад, чай), крупы (рожь, ячмень, овес, пшеница), орехи, бобовые, молоко, яйца и молочные продукты, жирные и мучные продукты, а также некоторые лекарственные препараты и витамины, содержащие кальций, магний, цинк, селен, йод, хром. Это поможет избежать ухудшения усвоения железа. Все препараты железа назначаются врачом индивидуально. Курс лечения составляет не менее 1,5-2 месяцев, возможно, и дольше. Кроме восстановления уровня железа в крови, нужно создать его запас в организме, то есть повысить уровень ферритина. Об успехе лечения говорит нормализация уровня гемоглобина через 1-2 месяца [9][10].
Если препараты железа невозможно применять внутрь (например, при непереносимости или нарушении всасывания железа в кишечнике), то их вводят внутримышечно или внутривенно. Инъекционные препараты железа используют только в стационаре, так как они могут вызывать шоковые реакции. Их нельзя применять во время беременности и лактации.
При тяжёлой анемии (гемоглобин менее 70 г/л) и по жизненным показаниям в условиях стационара проводят переливание эритроцитарной массы.
В качестве лечебно-профилактического средства пациентам, у которых нет сахарного диабета, можно использовать гематоген. В его состав входят железо, связывающее белки, получаемые из крови крупного рогатого скота, а также аскорбиновая кислота и необходимый комплекс белков. Однако это достаточно калорийный продукт — в 100 г гематогена содержится 350–500 килокалорий, об этом следует помнить, включая его в рацион.
Прогноз. Профилактика
Прогноз при ЖДА благоприятный. В большинстве случаев заболевание успешно лечится амбулаторно. Но если не анемию не лечить, то она может прогрессировать, ухудшая общее самочувствие. ЖДА сложно скорректировать в следующих случаях:
- при сопутствующих проблемах с ЖКТ (обострение хронического гастрита, язвенной болезни желудка и двенадцатиперстной кишки, воспалительных заболеваниях кишечника, синдроме мальабсорбции — нарушенного всасывания в кишечнике, резекции желудка и/или кишечника);
- одновременном приёме препаратов, снижающих всасывание железа;
- хронических кровопотерях;
- нелеченных системных и онкологических заболеваниях;
- нерегулярном приёме препаратов железа, несоблюдении дозировки, кратности и продолжительности приёма препарата или самостоятельной его замене.
Для профилактики ЖДА следует:
- ежегодно сдавать клинический анализ крови и контролировать его параметры;
- полноценно питаться, получая с пищей достаточное количество белка и железа;
- своевременно устранять источники кровопотери в организме;
- лицам из групп риска (донорам, детям, из спортивных школ, беременным и кормящим, а также женщинам, страдающим обильными и длительными менструациями) принимать небольшие дозы препаратов железа.
Все больные ЖДА, а также люди, у которых высока вероятность развития этой патологии, должны наблюдаться у терапевта [5][7].
