Виды гемоглобина его соединения их физиологическое значение

Оглавление темы “Функции клеток крови. Эритроциты. Нейтрофилы. Базофилы.”: Гемоглобин. Типы ( виды ) гемоглобина. Синтез гемоглобина. Функция гемоглобина. Строение гемоглобина.Гемоглобин — это гемопротеин, с молекулярной массой около 60 тыс., окрашивающий эритроцит в красный цвет после связывания молекулы O2 с ионом железа (Fe++). У мужчин в 1 л крови содержится 157 (140—175) г гемоглобина, у женщин — 138 (123—153) г. Молекула гемоглобина состоит из четырех субъединиц гема, связанных с белковой частью молекулы — глобином, сформированной из полипептидных цепей.
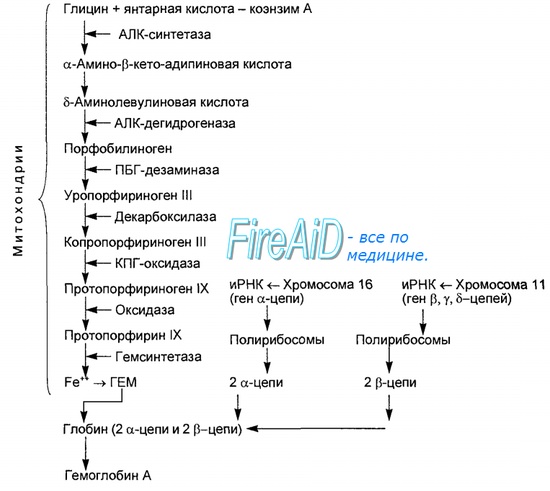
Синтез гема протекает в митохондриях эритробластов. Синтез цепей глобина осуществляется на полирибосомах и контролируется генами 11-й и 16-й хромосом. Схема синтеза гемоглобина у человека представлена на рис. 7.2. Гемоглобин, содержащий две а- и две В-цепи, называется А-тип (от adult — взрослый). 1 г гемоглобина А-типа связывает 1,34 мл O2. В первые три месяца жизни плода человека в крови содержатся эмбриональные гемоглобины типа Gower I (4 эпсилон цепи) и Gower II (2а и 25 цепи). Затем формируется гемоглобин F (от faetus — плод). Его глобин представлен двумя цепями а и двумя В. Гемоглобин F обладает на 20—30 % большим сродством к O2, чем гемоглобин А, что способствует лучшему снабжению плода кислородом. При рождении ребенка до 50—80 % гемоглобина у него представлены гемоглобином F и 15—40 % — типом А, а к 3 годам уровень гемоглобина F снижается до 2 %. Соединение гемоглобина с молекулой 02 называется оксигемоглобином. Сродство гемоглобина к кислороду и диссоциация оксигемоглобина (отсоединения молекул кислорода от оксигемоглобина) зависят от напряжения кислорода (Р02), углекислого газа (РС02) в крови, рН крови, ее температуры и концентрации 2,3-ДФГ в эритроцитах. Так, сродство повышают увеличение Р02 или снижение РС02 в крови, нарушение образования 2,3-ДФГ в эритроцитах. Напротив, повышение концентрации 2,3-ДФГ, снижение Р02 крови, сдвиг рН в кислую сторону, повышение РС02 и температуры крови — уменьшают сродство гемоглобина к кислороду, тем самым облегчая ее отдачу тканям. 2,3-ДФГ связывается с р-цепями гемоглобина, облегчая отсоединение 02 от молекулы гемоглобина. Увеличение концентрации 2,3-ДФГ наблюдается у людей, тренированных к длительной физической работе, адаптированных к длительному пребыванию в горах. Оксигемоглобин, отдавший кислород, называется восстановленным, или дезоксигемоглобином. В состоянии физиологического покоя у человека гемоглобин в артериальной крови на 97 % насыщен кислородом, в венозной — на 70 %. Чем выраженней потребление кислорода тканями, тем ниже насыщение венозной крови кислородом. Например, при интенсивной физической работе потребление кислорода мышечной тканью увеличивается в несколько десятков раз и насыщение кислородом оттекающей от мышц венозной крови снижается до 15 %. Содержание гемоглобина в отдельном эритроците составляет 27,5—33,2 пикограмма. Снижение этой величины свидетельствует о гипохромном (т. е. пониженном), увеличение — о гиперхромном (т. е. повышенном) содержании гемоглобина в эритроцитах. Этот показатель имеет диагностическое значение. Например, гиперхромия эритроцитов характерна для В|2-дефицитной анемии, гипохромия — для железодефицитной анемии. – Также рекомендуем “Старение эритроцитов. Разрушение эритроцитов. Длительность жизни эритроцита. Эхиноцит. Эхиноциты.” |

Виды гемоглобина.
Различают три вида гемоглобина; первоначально эмбрион имеет примитивный гемоглобин (HbP) – до 4-5 мес. внутриутробной жизни, затем начинает появляться фетальный гемоглобин (HbF), количество которого увеличивается до 6–7 мес. внутриутробной жизни. С этого срока происходит увеличение гемоглобина А (взрослого) максимальная величина которого достигает к 9 мес. внутриутробной жизни (90%). Количество фетального гемоглобина при рождении является одним из признаков доношенности: чем больше HbF, тем менее доношенный ребенок. Следует отметить, что HbF в присутствии 2,3 дифосфоглицерата (ДФГ – продукт метаболизма оболочки эритроцита при недостатки кислорода) не меняет своего сродства к кислороду в отличии от HbA, сродство которого к кислороду снижается.
Виды Нв отличаются друг от друга по степени химического сродства к О2. Так, НвF в физиологических условиях имеет более высокое сродство к О2, чем НвА. Эта важнейшая особенность НвF создает оптимальные условия для транспорта О2 кровью плода.
Гемоглобин представляет собой кровяной пигмент, роль которого заключается в транспорте кислорода к органам и тканям, транспорте двуокиси углерода от тканей к легким, кроме этого он является внутриклеточным буфером, который поддерживает оптимальную для метаболизма pH. Гемоглобин содержится в эритроцитах и составляет 90% их сухой массы. Вне эритроцитов гемоглобин практически не обнаруживается.
Химически гемоглобин относится к группе хромопротеидов. Его простетическая группа, включающая железо, называется гемом, белковый компонент – глобином. Молекула гемоглобина содержит 4 гема и 1 глобин.
К физиологическим гемоглобинам относятся НЬА (гемоглобин взрослого) и HbF (фетальный гемоглобин, составляющий основную массу гемоглобина плода и исчезающий почти полностью ко 2-му году жизни ребенка). Современными электрофоретическими исследованиями доказано существование по крайней мере двух разновидностей нормального гемоглобина А: А1 (главный) и А2 (медленный). Основную массу гемоглобина взрослого (96-99%) составляет HbAl, содержание других фракций (А2 F) не превышает 1 – 4%. Каждый вид гемоглобина, вернее его глобиновая часть, характеризуется своей «полипептидной формулой». Так, HbAl обозначается как ά2 β2, то есть он состоит из двух ά-цепей и двух β-цепей (всего 574 аминокислотных остатка, расположенных в строго определенном порядке). Другие виды нормальных гемоглобинов – F, A2 обладают общей с HbAl β-пептидной цепью, но отличаются структурой второй полипептидной цепи (например, структурная формула HbF – ά2γ2).
Помимо физиологических гемоглобинов, существуют еще несколько патологических разновидностей гемоглобина. Патологические гемоглобины возникают в результате врожденного, передаваемого по наследству дефекта образования гемоглобина.
В эритроцитах циркулирующей крови гемоглобин находится в состоянии беспрерывной обратимой реакции. Он то
присоединяет молекулу кислорода (в легочных капиллярах), то отдает ее (в тканевых капиллярах).
К основным соединениям гемоглобина относятся: ННв – восстановленный гемоглобин и НвСО2 – соединение с углекислым газом (карбогемоглобин). Они в основном находятся в венозной крови и придают ей темно-вишневый цвет.
НвО2 – оксигемоглобин– находится, в основном, в артериальной крови, придавая ей алый цвет. НвО2 – чрезвычайно нестойкое соединение, его концентрация определяется парциальным давлением О2 (рО2): чем больше рО2, тем больше образуется НвО2 и наоборот. Все вышеперечисленные соединения гемоглобина относятся к физиологическим.
Гемоглобин в венозной крови с низким парциальным давлением кислорода связан с 1 молекулой воды. Такой гемоглобин называется редуцированным (восстановленным) гемоглобином. В артериальной крови с высоким парциальным давлением кислорода гемоглобин соединен с 1 молекулой кислорода и имеет название – оксигемоглобин. Путем непрерывного превращения оксигемоглобина в редуцированный гемоглобин и обратно осуществляется перенос кислорода из легких к тканям. Восприятие углекислоты в тканевых капиллярах и доставка ее в легкие также является функцией гемоглобина. В тканях оксигемоглобин, отдавая кислород, превращается в редуцированный гемоглобин. Кислотные свойства редуцированного гемоглобина в 70 раз слабее свойств оксигемоглобина, поэтому свободные валентности его связывают углекислоту. Таким образом, углекислота доставляется из тканей в легкие с помощью гемоглобина. В легких образующийся оксигемоглобин в силу своих высоких кислотных свойств вступает в связь с щелочными валентностями карбогемоглобина, вытесняя углекислоту. Так как основной функцией гемоглобина является обеспечение тканей кислородом, то при всех состояниях, сопровождающихся снижением концентрации гемоглобина в крови, или при качественных его изменениях развивается гипоксия тканей.
Однако есть и патологические формы гемоглобина.
Гемоглобин обладает способностью вступать в диссоциирующие соединения не только с кислородом и углекислый газом, но и с другими газами. В результате образуются карбоксигемоглобин, оксиазотистый гемоглобинисульфгемоглобин.
Карбоксигемоглобин (оксиуглеродный) диссоциирует в несколько сотен раз медленнее, чем оксигемоглобин, поэтому даже незначительная концентрация (0,07%) в воздухе угарного газа (СО), связывая около 50% имеющегося в организме гемоглобина и лишая его способности переносить кислород, является смертельным. Карбоксигемоглобин (НвСО) – очень прочное соединение с угарным газом, обусловленное химическими свойствами угарного газа по отношению к Нв. Оказалось, что его родство к Нв в 400-500 раз больше, чем сродство О2 к Нв. Поэтому при незначительном повышении концентрации СО в окружающей среде образуется очень большое количество НвСО. Если в организме находится много НвСО, то возникает кислородное голодание. Фактически О2 в крови очень много, а клетки тканей его не получают, т.к. НвСО – прочное соединение с О2.
Метгемоглобин представляет собой более стойкое, чем оксигемоглобин, соединение гемоглобина с кислородом, получающееся при отравлениях некоторыми лекарственными препаратами – фенацетином, антипирином, сульфаниламидами. При этом двухвалентное железо простетической группы, окисляясь, превращается в трехвалентное. Метгемоглобин (MetНв) – окисленная форма Нв, крови придает коричневую окраску. Образуется MetНв при действии на Нв любым окислителями: нитраты, перекиси, перманганат калия, красная кровяная соль и т.д. Это стойкое соединение, потому что железо из ферроформы (Fe++) переходит в ферриформу (Fe+++), необратимо связывающую О2. При образовании в организме больших количеств MetНв также возникает кислородная недостаточность (гипоксия).
Сульфгемоглобин обнаруживается в крови иногда при применении лекарственных веществ (сульфаниламидов). Содержание сульфгемоглобина редко превышает 10%. Сульфгемоглобинемия – необратимый процесс. Так как пораженные эритроциты
разрушаются в те же сроки, что и нормальные, явлений гемолиза не наблюдается и сульфгемоглобин может находиться в крови в течение нескольких месяцев. На этом свойстве сульфгемоглобина основан метод определения сроков пребывания нормальных эритроцитов в периферической крови.
Дата добавления: 2015-11-05; просмотров: 4527 | Нарушение авторских прав | Изречения для студентов
Читайте также:
Рекомендуемый контект:
Поиск на сайте:
© 2015-2020 lektsii.org – Контакты – Последнее добавление
Гемоглобин – хромопротеид, окрашенный в красный цвет после присоединения к Fe++ кислорода. Состоит из белка глобина и простетической группы гема. В молекуле гемоглобина содержится одна молекула глобина и четыре молекулы гема. Гем имеет в своем составе атом двухвалентного железа, способный присоединить и отдать молекулу кислорода. Одна молекула гемоглобина присоединяет четыре молекулы кислорода. 1 гр гемоглобина присоединяет 1,34 мл кислорода. Содержание гемоглобина у мужчин 16,6 г в 100 мл крови (166 г/л), у женщин – 130 г/л.
Значение гемоглобина:
1) Выполняет роль переносчика О2 от лёгких к тканям.
2) Участвует в транспорте СО2 от клеток к лёгким.
3) Составляет гемоглобинную буферную систему и регулирует кислотно-основное состояние крови.
1. Эмбриональный вид гемоглобина — производится, уже начиная с первой недели развития эмбриона, но в завершении второго месяца вынашивания ребенка заменяется следующим видом.
2. Фетальный вид гемоглобина — это белок крови у плода. Он активно соединяет и затем переносит кислород по сравнению с аналогичным веществом в организме взрослого человека. В связи с этим ребенок в утробе матери и ещё некоторое время после появления на свет может переносить периоды недостатка кислорода намного лучше по сравнению со старшими родственниками. Фетальный вид активно производится в завершение трех месяцев беременности, но с течением времени заменяется следующей формой белка уже на протяжении первого года жизнедеятельности. У взрослого человека этот тип гемоглобина порой составляет от 1% до 1,5% от общего объема гемоглобина.
3. Нормальный вид гемоглобина — это белок, который преобладает у людей уже с четвертого года жизни.
4. Колориметрические способы — они активно реализуются на практике по причине их доступности и простоты.
5. Газометрические способы — происходит насыщение гемоглобина газом — окисью углерода или кислородом. По объему поглощаемого газа и можно рассуждать об объеме гемоглобина в крови.
6. Способы диагностики, которые основываются на выявлении содержания железа в молекуле гемоглобина. В связи с тем, что в состав гемоглобина входит определенный объем железа, то по его концентрации выявляется и объем гемоглобина.
Снижение уровня гемоглобина в крови происходит при малокровии разного происхождения — кровопотери, недостаток витамина В12, железа, фолиевой кислоты.
В эритроцитах взрослого человека гемоглобин составляет около 32 % от веса форменных элементов и в среднем 14 % от веса цельной крови (14 г на 100 г крови). Это количество гемоглобина приравнивается к 100 %. Содержание гемоглобина в эритроцитах новорожденных достигает 14,5 % нормы взрослого человека, что составляет 17–25 г гемоглобина на 100 г крови. В первые два года количество гемоглобина падает до 80–90 %, а затем снова возрастает до нормы. Относительное содержание гемоглобина с возрастом увеличивается и к 14–15 годам доходит до нормы взрослого. Оно равно (в граммах на 1 кг веса тела):
в 7–9 лет – 7,5;
10–11 лет – 7,4;
12–13 лет – 8,4;
14–15 лет – 10,4.
Роль белой крови в организме. Лейкоциты и их характеристика. Лейкопоэз и его регуляция . Возрастные изменения количества лейкоцитов
Лейкоциты – это клетки белой крови, основная задача которых – защита организма, лейкоциты – это основа иммунитета. Общее количество лейкоцитов в крови в среднем 4000 – 9000 в 1 мкл крови (4-9х109/л). Лейкоциты делятся на зернистые или гранулоциты (их ядро имеет зернистую структуру) и незернистые агранулоциты, ядро которых имеет незернистую структуру, эти виды лейкоцитов выполняют разные задачи.
1.Защитная. Благодаря движению клеток они могут проходить (мигрировать) через эндотелий капилляров (этот процесс называется диапедеза) и двигаться в направлении микробов, инородных тел, клеток на разных стадиях разрушения, комплексов антиген – антитело. По отношению к ним лейкоциты имеют положительный хемотаксис. Лейкоциты способны захватить чужеродные тела и с помощью специальных ферментов травить их. Этот процесс называется фагоцитозом. Один лейкоцит может захватить до 15-20 бактерий. Кроме того лейкоциты выделяют ряд важных для защиты организма веществ. К ним прежде всего относятся антитела, которые обладают антибактериальными и антитоксическим свойствами, вещества фагоцитарной активности.
2.Транспортная. В лейкоцитах есть целый ряд ферментов (протеазы, пептидазы, диастазы, липазы, дезоксирибонуклеазы), которые есть в лизосомальных мешочках и физиологически активных веществ (серотонин, гистамин, гепарин), которые есть в гранулах. Лейкоциты могут адсорбировать некоторые вещества и переносить их на своей поверхности.
3.Метаболическая. Лейкоциты способны синтезировать белки, гликоген, фосфолипиды.
4.Регенераторная. Лейкоциты выделяют Трофоний, которые способствуют образованию новых клеток.
Зернистые лейкоциты (гранулоциты) делятся на нейтрофилы, эозинофилы и базофилы. Нейтрофилы выполняют в организме функцию фагоцитоза – при проникновении в организм бактерий и вирусов они «проглатывают» их и растворяют – это так называемый клеточный иммунитет. Процессу фагоцитоза помогает выработка нейтрофилами фермента лизоцима и противовирусного вещества интерферона. В свою очередь нейтрофилы разделяются на зрелые формы (сегментоядерные нейтрофилы), не полностью зрелые (палочкоядерные) и совсем незрелые (юные). В общем анализе крови их принято писать по порядку, слева направо: юные – палочкоядерные – сегментоядерные. Поэтому и увеличение нейтрофилов может быть со сдвигом (увеличением той или иной их части) влево или вправо.
Эозинофилы выполняют функцию защиты от аллергии, они поглощают медиаторы – активные вещества, которые выделяются во время аллергической реакции, например, гистамин.
Основная функция базофилов – участие в иммунологических реакциях (в том числе и неадекватных, аллергических) замедленного типа.
Все лейкоциты образуются в красном костном мозге из единой стволовой клетки, однако родоначальницей миелопоэза является бипотенциальная колониеобразующая единица гранулоцитарно-моноцитарная (КОЕ-ГМ) или клетка-предшественница. Для ее роста и дифференцировки необходим особый колониестимулирующий фактор (КСФ), вырабатываемый у человека моноцитарно-макрофагальными клетками, костным мозгом и лимфоцитами.
КСФ является гликопротеидом и состоит из двух частей — стимулятора продукции эозинофилов (Эо-КСФ) и стимулятора продукции нейтрофилов и моноцитов (ГМ-КСФ), относящихся к ранним гемопоэтическим ростовым факторам. Выработка ГМ-КСФ стимулируется Т-хелперами и подавляется Т-супрессорами. На более поздних этапах на лейкопоэз влияют гранулоцитарный колониестимулирующий фактор — Г-КСФ (способствует развитию нейтрофилов) и макрофагальный колониестимулирующий фактор — М-КСФ (приводит к образованию моноцитов), являющиеся позднодействующими специфическими ростовыми факторами.
Установлено, что T-лимфоциты стимулируют дифференцировку клеток в гранулоцитарном направлении. В регуляции размножения ранних поли- и унипотентных клеток имеет важное значение их взаимодействие с Т-лимфоцитами и макрофагами. Эти клетки влияют на клетки-предшественницы с помощью лимфокинов и монокинов, содержащихся в мембране и отделяющихся от нее в виде «пузырьков» при тесном контакте с клетками-мишенями.
Из костного мозга и отдельных видов лейкоцитов (гранулоцитов и агранулоцитов) выделен комплекс полипептидных факторов, выполняющих функции специфических лейкопоэтинов.
Важная роль в регуляции лейкопоэза отводится интерлейкинам. В частности, ИЛ-3 не только стимулирует гемопоэз, но и является фактором роста и развития базофилов. ИЛ-5 необходим для роста и развития эозинофилов. Многие интерлейкины (ИЛ-2, ИЛ-4, ИЛ-6, ИЛ-7 и др.) являются факторами роста и дифференцировки Т- и В-лимфоцитов.
Выделяют следующие нарушения лейкопоэза:
1. усиление или угнетение образования лейкоцитов в гемопоэтической ткани.
2. нарушение созревания лейкоцитов в кроветворных органах.
3. продукция патологически изменённых лейкоцитов.
Нарушение лейкопоэза возникает при действии
· биологических (бактерии, вирусы),
· физических (УФ лучи, радиация)
· химических факторов.
К эндогенным факторам нарушения лейкопоэза относятся генетические дефекты образования и дифференцирования лейкоцитов.
Лейкоциты появляются в конце 3-го месяца внутриутробного развития, а на последней неделе беременности их число у плода выше, чем у взрослого человека. У новорожденного в первые часы после рождения их количество колеблется от 10 до 30 ×109/л. В течение 1-го, иногда 2-го дня жизни их число несколько увеличивается – это физиологический лейкоцитоз. Он обусловлен быстрой мобилизацией нейтрофилов из запасных пулов костного мозга в ответ на стресс при рождении. Состояние лейкоцитоза могут вызвать и внешние антигенные стимулы, с которыми сталкивается новорожденный. Это реактивный лейкоцитоз. В этих условиях поступают в циркуляцию молодые формы нейтрофилов. После этого число лейкоцитов снижается в 1-й год до 9-10 ×109/л и в 14-17 лет достигает уровня взрослых.
У недоношенных детей как при рождении, так и в последующие периоды число лейкоцитов несколько меньше, чем у доношенных.