Зависимость насыщения гемоглобина кислородом от парциального давления
Несмотря на то, что исследование кислотно-основного состояния, строго говоря, подразумевает исследование только величины pH (концентрации ионов H+), в реальности в него также включается исследование физиологически важных газов, присутствующих в крови – O2 и CO2. Анализ газов показывает эффективность газообмена по величинам парциальных давлений – pO2 и pCO2.
Через альвеолярную мембрану молекулы любых газов перемещаются диффузно по градиенту концентрации. Молекулы O2 атмосферного воздуха поступают из альвеол в кровь, а молекулы CO2 из крови в альвеолы до тех пор пока их парциальные давления не выровняются.
Величина парциального давления – это процентная доля газа в общем объеме.
Углекислый газ
Концентрация СО2 в альволярном воздухе столь низка, а в крови столь высока, что диффузия этого газа в альвеолы чрезвычайно эффективна и скорость его удаления зависит только от альвеолярной вентиляции – общего объема воздуха, транспортируемого в минуту между альвеолами и атмосферой (“скорости выдувания”).
Следовательно,
- при усиленной вентиляции легких углекислый газ быстро выводится, и показатель pCO2в крови снижается. Это означает потерю организмом угольной кислоты (ионов H+), что является причиной защелачивания крови – алкалоза, называемого дыхательным или респираторным.
- при недостаточной альвеолярной вентиляции величина рСО2 повышается, что свидетельствует о недостаточном его удалении и накоплении H2CO3. Иными словами, повышение в крови показателя рСО2 является причиной дыхательного ацидоза.
Увеличенное pCO2 (гиперкапния) всегда свидетельствует о снижении альвеолярной вентиляции.
Кислород
Вопросы, связанные с оксигенацией крови и транспортом кислорода более сложны. Связано это с тем, что в виде свободных (растворенных) молекул O2 находится лишь небольшая доля общего кислорода крови. Основная часть кислорода связана с гемоглобином (оксигемоглобин) и истинное содержание кислорода зависит от двух дополнительных параметров – концентрации Hb и насыщения (сатурации) гемоглобина кислородом.
Оксигемоглобин
Оксигемоглобин (HbО2) – процентное содержание в крови, является отношением фракции оксигемоглобина (HbО2) к сумме всех фракций (общему гемоглобину).
Насыщение гемоглобина кислородом
Насыщение гемоглобина кислородом (HbOSAT, SО2), представляет собой отношение фракции оксигенированного гемоглобина к тому количеству гемоглобина в крови, который способен транспортировать О2.
Отличия между двумя показателями HbО2 и HbOSAT заключаются в том, что у пациентов возможно наличие в крови такой формы гемоглобина, которая не способна акцептировать О2 (Hb‑CO, metHb, сульфоHb). Но так как большинство больных не имеют в крови повышенного содержания этих форм гемоглобина, значения HbО2 и SО2 обычно очень близки.
Например, если при отравлении нитритами количество metHb составляет 15%, тогда величина HbО2 никогда не сможет превысить 85%, но насыщение (HbOsat) может быть различно – от максимума (HbOsat=95-98%) при полном насыщении до низких величин при отсутствии кислорода.
Показатель насыщения кислородом показывает процент доступных мест связывания на гемоглобине.
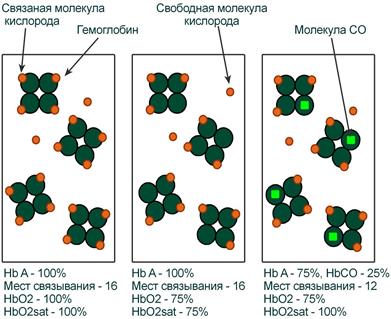
Иллюстрация понятий оксигемоглобина (HbO2) и насыщения гемоглобина (HbO2sat)
Парциальное давление кислорода (pO2)
Парциальное давление O2 выступает как движущая сила, приводящая к насыщению гемоглобина кислородом. И хотя, как правило, чем выше pO2 тем выше HbOsat, эта зависимость не является линейной.

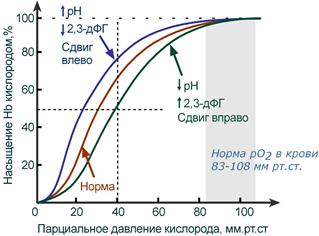
Кривая диссоциации гемоглобина в норме и
при изменении pH и концентрации 2,3-дифосфоглицерата
В центральной части кривой насыщения (или кривой диссоциации) гемоглобина малейшие сдвиги pO2 приводят к резким изменениям насыщения гемоглобина. И наоборот, при высоком pO2 (80-90-100 мм рт.ст) кривая становится плоской, насыщение гемоглобина мало зависит от колебаний кислорода в плазме.
Сдвиг влево происходит при защелачивании и снижении концентрации 2,3-дифосфоглицерата и сигнализирует об увеличении сродства кислорода к гемоглобину (в легких). Сдвиг вправо – это снижение сродства кислорода к гемоглобину (в тканях), обеспечивается закислением среды и накоплением 2,3-дифосфоглицерата.
Показатель pO2 не отражает содержание кислорода в цельной крови! Но хотя pO2 и не показывает общее количество кислорода в крови, но это общее количество зависит от pO2 через показатель сатурации гемоглобина.
В свою очередь имеются факторы, влияющие на величину pO2:
1. Альвеолярная вентиляция. Хотя она влияет как на pO2 так и на pCO2, но доля кислорода в альвеолах при гипервентиляции может лишь слегка увеличиться, приближаясь к pO2 атмосферного воздуха, при гиповентиляции – стремительно падает, вытесняясь поступающим из крови CO2. В то же время доля CO2 в альвеолах быстро снижается при усиленной вентиляции.
2. Вентиляционно-перфузионное соотношение, определяется тем, что
- не вся кровь, притекающая к легким, соприкасается с хорошо вентилируемыми альвеолами (спадение альвеол, уплотнение стенки).
- не все хорошо вентилируемые альвеолы получают достаточно крови (правожелудочковая сердечная недостаточность).
3. Концентрация кислорода во вдыхаемом воздухе (FiO2, fraction of inspired oxygen).
В таблице приведены сравнительные величины концентрации кислорода и углекислого газа в воздухе, крови и тканях.
Необходимо обратить внимание на перепады концентраций кислорода и углекислого газа в крови и альвеолярном воздухе. Важной особенностью является то, что pO2 в альвеолярном воздухе и артериальной крови очень близки, т.е. в обычных условиях глубоким и/или частым дыханием невозможно повысить потребление кислорода и насыщение им гемоглобина. В то же время разность концентраций pCO2 в венозной крови и альвеолярном воздухе позволяет эффективно его удалять при частом дыхании.
| pO2, мм рт.ст. | pCO2, мм рт.ст | |
| Вдыхаемый воздух | 159 | 0,23 |
| Альвеолярный воздух | 105-110 | 40 |
| Артериальная кровь | 83-108 | 35-45 |
| Ткани | 10-20 | 50-60 |
| Венозная кровь | 35-49 | 46-51 |
| Выдыхаемый воздух | 116 | 32 |
Эффект Бора
Аллостерическая регуляция насыщения гемоглобина кислородом
Кривая диссоциации кислорода для гемоглобина
Механизм насыщения гемоглобина кислородом
Гемоглобин присоединяет О2 последовательно, по одной молекуле на каждый гем.
В апогемоглобине, благодаря координационной связи с белковой частью, атом железа выступает из плоскости гема в направлении гистидина F8.
Присоединение О2 к шестой координационной связи железа вызывает его перемещение в плоскость гема, за ним перемещаются гистидин F8 и полипептидная цепь, в состав которой он входит.
Происходит изменение конформации текущего протомера и связанных с ним оставшихся протомеров. При этом у протомеров возрастает сродство к кислороду, в результате каждый следующий кислород присоединяется к гемоглобину лучше предыдущего. Четвертая молекула кислорода присоединяется к гемоглобину в 300 раз легче, чем первая молекула. Обратный процесс аналогичен, чем больше О2 отдают протомеры, тем легче идет отщепление последующих молекул О2.
Кооперативность в работе протомеров гемоглобина формирует сигмовидный характер кривой насыщения его кислородом в зависимости от парциального давления кислорода.
S–образная кривая насыщения гемоглобина кислородом имеет важное биологическое значение.
Во-первых, пологий участок S–образной кривой (выше 60 мм.рт.ст.) обеспечивает максимальное насыщение гемоглобина кислородом в легких, даже если концентрация кислорода в альвеолярном воздухе заметно снижена. Например, в альвеолярной крови при РО2=95 мм.рт.ст. гемоглобин насыщается кислородом на 97%, а при РО2=60 мм.рт.ст. — на 90%.
Во-вторых, Крутой наклон среднего участка S–образной кривой (от 10 до 40 мм.рт.ст.) обеспечивает максимальный переход кислорода от гемоглобина к тканям.
В области венозного конца капилляра при РО2 = 40 мм.рт.ст. гемоглобин насыщен кислородом на 73%. При снижении РО2 на 5 мм.рт.ст. насыщение гемоглобина кислородом уменьшается на 7%.
Кроме РО2 на насыщение гемоглобина кислородом влияют и другие факторы, например, рН, температура, давление, концентрация 2,3-ДФГ, РСО2.
Увеличение температуры, присоединение к гемоглобину Н + , 2,3-ДФГ, СО2 уменьшает сродство гемоглобина к кислороду, при этом кривая диссоциации оксигемоглобина сдвигается вправо и гемоглобин легче отдает кислород тканям.
Влияние рН на характер кривой диссоциации оксигемоглобина называется эффектом Бора (по имени датского физиолога Христиана Бора, впервые открывшего этот эффект).
Гемоглобин в дезоксигенерированном состоянии имеет более высокое сродство к протонам, чем оксигемоглобин. Другими словами R – форма (оксигенерированная) является более сильной кислотой, чем Т-форма (дезоксигенерированная). Поэтому когда дезоксигемоглобин в легких присоединяет кислород, происходит переход в R – форму и разрыв некоторых связей, в результате чего и высвобождаются протоны, ответственные за эффект Бора. Наоборот, при высвобождении кислорода образуется Т-структура и разорванные связи между субъединицами должны быть восстановлены, и протоны вновь присоединяются к остаткам гистидина в b — цепях. Таким образом, протонирование гемоглобина снижает его сродство к О2 и увеличивает потребление О2 в ткани.
Эффект Бора имеет важное физиологическое значение. Образующийся в тканях СО2 должен транспортироваться в легкие. Он поступает в эритроциты по градиенту напряжения. В них фермент карбоангидраза превращает его в Н2СО3, который диссоциирует на бикарбонат, ион и протон. Последний сдвигает равновесие влево в уравнении (1).
Где n — величина порядка 2; число зависит от целого комплекса параметров, тем самым заставляя Hb О2 отдавать свой кислород.
НСО3- пассивно продвигается через ионный канал по градиенту концентрации в сыворотку.
Продвижение НСО3- не сопровождается перемещением Н+, поскольку нет канала, позволяющего ему пройти через мембрану эритроцитов. Для сохранения ионного равновесия при выходе НСО3- из клетки, Cl- перемещаются внутрь её через тот же ионный канал. Такое двойное перемещение известно как хлоридный сдвиг (сдвиг Хамбургера).
Растворенный НСО3- движется вместе с венозной кровью обратно в легкие. Здесь высвобождение протона из гемоглобина при оксигениции приводит к образованию НСО3- (по принципу Ле-Шателье).
что позволяет карбоангидразе образовать СО2.
Разрушение НСО3- в эритроците обуславливает вхождение в него НСО3- из сыворотки, так что в легких происходит обратный хлоридный сдвиг, приводящий к выведению СО2 с выдыхаемым воздухом.
Не нашли то, что искали? Воспользуйтесь поиском:
Лучшие изречения: Сдача сессии и защита диплома — страшная бессонница, которая потом кажется страшным сном. 9100 —
| 7340 — или читать все.
источник
Газы крови влияют на pH
Несмотря на то, что исследование кислотно-основного состояния, строго говоря, подразумевает исследование только величины pH (концентрации ионов H + ), в реальности в него также включается исследование физиологически важных газов, присутствующих в крови – O 2 и CO 2. Анализ газов показывает эффективность газообмена по величинам парциальных давлений – pO2 и pCO2.
Через альвеолярную мембрану молекулы любых газов перемещаются диффузно по градиенту концентрации. Молекулы O2 атмосферного воздуха поступают из альвеол в кровь, а молекулы CO2 из крови в альвеолы до тех пор пока их парциальные давления не выровняются.
Величина парциального давления – это процентная доля газа в общем объеме.
Углекислый газ
Концентрация СО2 в альволярном воздухе столь низка, а в крови столь высока, что диффузия этого газа в альвеолы чрезвычайно эффективна и скорость его удаления зависит только от альвеолярной вентиляции – общего объема воздуха, транспортируемого в минуту между альвеолами и атмосферой («скорости выдувания»).
- при усиленной вентиляции легких углекислый газ быстро выводится, и показатель pCO2в крови снижается. Это означает потерю организмом угольной кислоты (ионов H + ), что является причиной защелачивания крови – алкалоза, называемого дыхательным или респираторным.
- при недостаточной альвеолярной вентиляции величина рСО2 повышается, что свидетельствует о недостаточном его удалении и накоплении H2CO3. Иными словами, повышение в крови показателя рСО2 является причиной дыхательного ацидоза .
Кислород
Вопросы, связанные с оксигенацией крови и транспортом кислорода более сложны. Связано это с тем, что в виде свободных (растворенных) молекул O2 находится лишь небольшая доля общего кислорода крови. Основная часть кислорода связана с гемоглобином ( оксигемоглобин ) и истинное содержание кислорода зависит от двух дополнительных параметров – концентрации Hb и насыщения (сатурации) гемоглобина кислородом.
Оксигемоглобин
Оксигемоглобин (HbО2) – процентное содержание в крови, является отношением фракции оксигемоглобина (HbО2) к сумме всех фракций (общему гемоглобину).
Насыщение гемоглобина кислородом
Насыщение гемоглобина кислородом (HbOSAT, SО2), представляет собой отношение фракции оксигенированного гемоглобина к тому количеству гемоглобина в крови, который способен транспортировать О2.
Отличия между двумя показателями HbО2 и HbOSAT заключаются в том, что у пациентов возможно наличие в крови такой формы гемоглобина, которая не способна акцептировать О2 (Hb‑CO, metHb, сульфоHb). Но так как большинство больных не имеют в крови повышенного содержания этих форм гемоглобина, значения HbО2 и SО2 обычно очень близки.
Например, если при отравлении нитритами количество metHb составляет 15%, тогда величина HbО2 никогда не сможет превысить 85%, но насыщение (HbOsat) может быть различно – от максимума (HbOsat=95-98%) при полном насыщении до низких величин при отсутствии кислорода.
Иллюстрация понятий оксигемоглобина (HbO2) и насыщения гемоглобина (HbO2sat)
Парциальное давление кислорода (pO2)
Парциальное давление O2 выступает как движущая сила , приводящая к насыщению гемоглобина кислородом. И хотя, как правило, чем выше pO2 тем выше HbOsat, эта зависимость не является линейной.
Кривая диссоциации гемоглобина в норме и
при изменении pH и концентрации 2,3-дифосфоглицерата
В центральной части кривой насыщения (или кривой диссоциации) гемоглобина малейшие сдвиги pO2 приводят к резким изменениям насыщения гемоглобина. И наоборот, при высоком pO2 (80-90-100 мм рт.ст) кривая становится плоской, насыщение гемоглобина мало зависит от колебаний кислорода в плазме.
Сдвиг влево происходит при защелачивании и снижении концентрации 2,3-дифосфоглицерата и сигнализирует об увеличении сродства кислорода к гемоглобину (в легких). Сдвиг вправо — это снижение сродства кислорода к гемоглобину (в тканях), обеспечивается закислением среды и накоплением 2,3-дифосфоглицерата.
Показатель pO2 не отражает содержание кислорода в цельной крови! Но хотя pO2 и не показывает общее количество кислорода в крови, но это общее количество зависит от pO2 через показатель сатурации гемоглобина.
В свою очередь имеются факторы, влияющие на величину pO2:
1. Альвеолярная вентиляция. Хотя она влияет как на pO2 так и на pCO2, но доля кислорода в альвеолах при гипер вентиляции может лишь слегка увеличиться, приближаясь к pO2 атмосферного воздуха, при гипо вентиляции – стремительно падает, вытесняясь поступающим из крови CO2. В то же время доля CO2 в альвеолах быстро снижается при усиленной вентиляции.
2. Вентиляционно-перфузионное соотношение, определяется тем, что
- не вся кровь, притекающая к легким, соприкасается с хорошо вентилируемыми альвеолами (спадение альвеол, уплотнение стенки).
- не все хорошо вентилируемые альвеолы получают достаточно крови (правожелудочковая сердечная недостаточность).
3. Концентрация кислорода во вдыхаемом воздухе (FiO2, fraction of inspired oxygen).
В таблице приведены сравнительные величины концентрации кислорода и углекислого газа в воздухе, крови и тканях.
Необходимо обратить внимание на перепады концентраций кислорода и углекислого газа в крови и альвеолярном воздухе. Важной особенностью является то, что pO2 в альвеолярном воздухе и артериальной крови очень близки, т.е. в обычных условиях глубоким и/или частым дыханием невозможно повысить потребление кислорода и насыщение им гемоглобина. В то же время разность концентраций pCO2 в венозной крови и альвеолярном воздухе позволяет эффективно его удалять при частом дыхании.
источник
Вопрос 8. Эффект Бора, аллостерическая регуляция насыщения гемоглобина кислородом
График зависимости насыщения миоглобина кислородом от парциального давления кислорода имеет вид гиперболы; для гемоглобина же это зависимость отражается S- образной кривой. Графики подтверждают функцию данных хромопротеинов. Функция миоглобина – присоединить кислород, доставляемый гемоглобином и его запасти. Миоглобин не может транспортировать кислород так как даже при парциальном давлении 20 мм.рт.ст., степень насыщения миоглобина кислородом будет около 85%. Однако при кислородном голодании, которым сопровождается тяжелая физическая работа, РО2 в мышечной ткани может понизиться и до 5 мм.рт.ст., при столь низком давлении миоглобин легко отдает связанный кислород, обеспечивая тем самым окислительный синтез АТФ в митохондриях мышечных клеток.
Кривая диссоциации оксигемоглобина имеет S- образную конфигурацию. Этот факт также связан с функцией гемоглобина и имеет биохимический смысл. В процессе поглощения кислорода в легких напряжение О2 в крови (РО2) приближается к таковому в альвеолах. У молодых людей РО2 артериальной крови составляет около 95 мм.рт.ст.. Насыщение гемоглобина при этом – 97%. С возрастом (или при заболеваниях легких) напряжение О2 в артериальной крови может значительно снижаться, однако, поскольку кривая диссоциации оксигемоглобина в правой её части почти горизонтальна, насыщение крови кислородом уменьшается не намного. При РО2 равное 60 мм.рт.ст. насыщение гемоглобина составляет 90%. Таким образом, горизонтальный участок кривой диссоциации предупреждает существенное снижение насыщения артериальной крови кислородом.
Крутой наклон среднего участка свидетельствует об очень благоприятных условиях для отдачи кислорода тканям. В состоянии покоя РО2 в области венозного конца капилляра равно приблизительно 40 мм.рт.ст., что соответствует примерно 73% насыщения. Если в результате увеличения потребления кислорода его напряжение в венозной крови падает лишь на 5 мм.рт.ст, то насыщение гемоглобина кислородом снижается не менее чем на 7%.
Олигомерные белки способны к аллостерической регуляции своих функций. Присоединение лигандов в участках, пространственно удаленных друг от друга (аллостерических), способно вызвать конформационные изменения во всем белке.
Результатом воздействия лигандов Н + , 2,3-ДФГ, СО2 является затруднение перехода из Т- состояния в R. Т-форма характеризуется меньшим сродством к кислороду и способна легко отдавать его тканям. Таким образом, при увеличение концентрации 2,3- ДФГ, уменьшение рН среды, а также при возрастании РСО2 и температуры кривая диссоциации оксигемоглобина сдвигается вправо.
Эффект Бора
Влияние рН на характер кривой диссоциации оксигемоглобина называется эффектом Бора (по имени датского физиолога Христиана Бора, впервые открывшего этот эффект).
Гемоглобин в дезоксигенерированном состоянии имеет более высокое сродство к протонам, чем оксигемоглобин. Другими словами R – форма (оксигенерированная) является более сильной кислотой, чем Т-форма (дезоксигенерированная). Поэтому когда дезоксигемоглобин в легких присоединяет кислород, происходит переход в R – форму и разрыв некоторых связей, в результате чего и высвобождаются протоны, ответственные за эффект Бора. Наоборот, при высвобождении кислорода образуется Т-структура и разорванные связи между субъединицами должны быть восстановлены, и протоны вновь присоединяются к остаткам гистидина в — цепях. Таким образом, протонирование гемоглобина снижает его сродство к О2 и увеличивает потребление О2 в ткани.
Эффект Бора имеет важное физиологическое значение. Образующийся в тканях СО2 должен транспортироваться в легкие. Он поступает в эритроциты по градиенту напряжения. В них фермент карбоангидраза превращает его в Н2СО3, который диссоциирует на бикарбонат, ион и протон. Последний сдвигает равновесие влево в уравнении (1).
Где n — величина порядка 2; число зависит от целого комплекса параметров, тем самым заставляя Hb О2 отдавать свой кислород.
НСО3 — пассивно продвигается через ионный канал по градиенту концентрации в сыворотку.
Продвижение НСО3 — не сопровождается перемещением Н + , поскольку нет канала, позволяющего ему пройти через мембрану эритроцитов. Для сохранения ионного равновесия при выходе НСО3 — из клетки, Cl — перемещаются внутрь её через тот же ионный канал. Такое двойное перемещение известно как хлоридный сдвиг (сдвиг Хамбургера).
Растворенный НСО3 — движется вместе с венозной кровью обратно в легкие. Здесь высвобождение протона из гемоглобина при оксигениции приводит к образованию НСО3 — (по принципу Ле-Шателье).
что позволяет карбоангидразе образовать СО2.
Разрушение НСО3 — в эритроците обуславливает вхождение в него НСО3 — из сыворотки, так что в легких происходит обратный хлоридный сдвиг, приводящий к выведению СО2 с выдыхаемым воздухом.
источник
Кислородная ёмкость крови и сатурация.
Опубликовано Curans в 17.12.2017
1 г гемоглобина способен связать 1,34 мл кислорода. Если известно содержание гемоглобина крови, можно рассчитать кислородную емкость крови — максимальное количество кислорода, которое может связать гемоглобин при его полном насыщении О2 (кислородом).
В норме гемоглобин например 140 г/л. Количество кислорода в 1 л крови составит 1,34мл х 140г = 187,6 мл; в 100 мл крови — 18,76 мл или 18,76 об. % (объемных %).
Процентное отношение количества O2, реально связанного с гемоглобином, к кислородной емкости крови называется насыщением (saturation — сатурация) гемоглобина кислородом (SO2 или HbO2).
Другими словами, SО2 — это отношение оксигемоглобина к общему количеству гемоглобина крови. В норме насыщение артериальной крови кислородом (SО2 или НbО2) составляет 96-98% .
Небольшое «недонасыщение» (2-4%) объясняется некоторой неравномерностью легочной вентиляции и незначительной примесью венозной крови, которые имеют место и у здоровых людей.
Насыщение гемоглобина кислородом зависит от напряжения О2 в крови (в соответствии с физическим законом действующих масс). Графически эту зависимость отражает кривая диссоциации оксигемоглобина, имеющая S-образную форму.
Показатель SО2 измеряется путём исследования артериальной крови. Аналогичный показатель, измеренный неинвазивным способом (с помощью пульсоксиметрии) обозначается как SpО2. в принципе оба показателя коррелируют хорошо, погрешность составляет 1-2%.
Основные моменты пульсоксиметрии:
1. Норма сатурации (SpО2)–95-98%, при дыхании атмосферным воздухом.
2. Что бы правильно понять цифры сатурации, можно их сравнить с парциальным давлением кислорода в крови (PaО2):
-сатурация (SpО2) 95-98% соответствует — 80-100 мм рт. ст.(PaО2).
-сатурация (SpО2) 90% соответствует — 60 мм рт.ст.(PaО2).
-сатурация (SpО2) 75% соответствует — 40 мм рт.ст.(PaО2).
3. Пульсоксиметрия не является показателем вентиляции, а характеризует только оксигенацию. Больной (особенно после преоксигенации) может не дышать несколько минут до того, как SpО2 начнет падать.
4. Сатурация не всегда является параметром адекватной периферической оксигенации. При анемии сатурация прекрасная, а ткани страдают от гемической гипоксии.
5. Цианоз возникает при SрО2 менее 85%, у новорожденных , уже, при SрО2— 90%.
6. При анемии, даже, при сатурации 70% может не быть цианоза (синюшность носогубного треугольника и ногтевых лож).
7. При отравлении угарным газом сатурация будет в пределах нормы (цветовой спектр такой же).
8. Если пульсоксиметр показывает 100%, при дыхании пациента атмосферным воздухом, значит, пульсоксиметр-некачественный.
9. Лак для ногтей практически не искажает показания пульсоксиметра, но лучше без лака.
10. При критических состояниях датчик установленный на ухо является более предпочтительным, чем датчик установленный на пальце.
источник
